海水资源的综合利用
- 格式:ppt
- 大小:1.55 MB
- 文档页数:20


海水资源的综合利用:浩瀚的海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还孕育着丰富的矿产,而海水本身含有大量的化学物质,又是宝贵的化学资源。
可从海水中提取大量的食盐、镁、溴、碘、钾等有用物质,海水素有“液体工业原料”之美誉。
•海水制盐:(1)海水制盐的方法:从海水中得到食盐的方法有蒸发法(盐田法)、电渗析法等。
目前,以蒸发法(盐田法)为主。
(2)海水晒盐的基本原理:水分不断蒸发,氯化钠等盐结晶析出。
(3)海水晒盐的流程氯碱工业:(1)食盐水的精制(2)电极反应阴极:阳极:总反应::(3)主要设备离子交换膜电解槽一一阳极用金属钛(表面涂有钛、钉氧化物层)制成,阴极用碳钢(覆有镍镀层)制成。
阳离子膜具有选择透过性,只允许Na+透过,而Cl-、 OH一和气体不能透过。
(4)产品及用途烧碱:可用于造纸、玻璃、肥皂等工业氯气:可用于制农药、有机合成、氯化物的合成氢气:可用于金属冶炼、有机合成、盐酸的制取海水提溴:(1)氯化氯化氧化溴离子,在pH=3.5的酸性条件下效果最好,所以在氯化之前要将海水酸化。
(2)吹出当海水中的Br一被氧化成Br2以后,用空气将其吹出。
另外,也可以用水蒸气,使溴和水蒸气一起蒸出。
(3)吸收目前比较多的是用二氧化硫作还原剂,使溴单质转化为HBr,再用氯气将其氧化得到溴产品。
化学方程式如下:海水提镁:(1)工艺流程(2)主要化学反应①制备石灰乳:②沉淀③制备从海水中提取重水:提取重水的方法:蒸馏法、电解法、化学交换法、吸附法等。
常用方法:化学交换法(硫化氢一水双温交换法)铀和重水目前是核能开发中的重要原料,从海水中提取铀和重水对一个国家来说具有战略意义,化学在开发海洋药物方面也将发挥越来越大的作用。
潮汐能、波浪能也是越来越受到重视的新型能源。





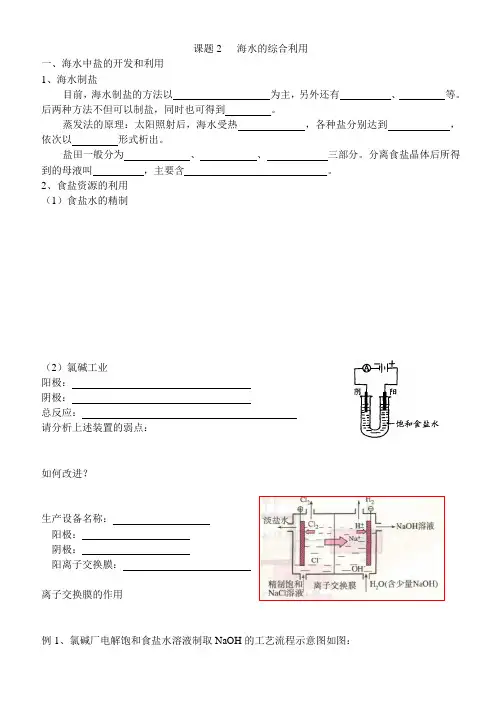
课题2 海水的综合利用一、海水中盐的开发和利用1、海水制盐目前,海水制盐的方法以为主,另外还有、等。
后两种方法不但可以制盐,同时也可得到。
蒸发法的原理:太阳照射后,海水受热,各种盐分别达到,依次以形式析出。
盐田一般分为、、三部分。
分离食盐晶体后所得到的母液叫,主要含。
2、食盐资源的利用(1)食盐水的精制(2)氯碱工业阳极:阴极:总反应:请分析上述装置的弱点:如何改进?生产设备名称:阳极:阴极:阳离子交换膜:离子交换膜的作用例1、氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如图:依据图,完成下列填空:(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和。
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是。
(3)在电解过程中,与电源正极相连的电极上所发生的反应为。
与电源负极相连的电极附近,溶液的pH .(填“升高”、“不变”、“降低”)(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是A.Ba(OH)2 B.Ba(NO3)2C.BaCl2(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为A.先加入NaOH,后加入Na2CO3,再加入钡试剂B.先加入NaOH,后加入钡试剂,再加入Na2CO3C.先加入钡试剂,后加入NaOH,再加入Na2CO3D.先加入钡试剂,后加入Na2CO3,再加入NaOH(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过(填写操作名称)、冷却、过滤除去NaCl.(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式。
※海水中提取化学物质的一般方法二、海水提溴——法基本流程:1、氯化氯化之前要将海水,原因是。
氯化反应:2、吹出用或将溴吹出。
3、吸收用还原剂使溴单质变为HBr,再用将其氧化成溴产品。

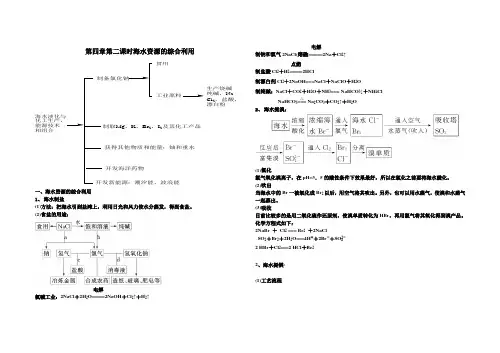
第四章第二课时海水资源的综合利用海水淡化与化工生产,能源技术相组合制备氯化钠食用工业原料生产烧碱纯碱,Na Cl 2,盐酸,漂白粉制取Mg ,K ,Br 2,I 2及其化工产品获得其他物质和能量:铀和重水开发海洋药物开发新能源:潮汐能,波浪能一、海水资源的综合利用1、 海水制盐(1)方法:把海水引到盐滩上,利用日光和风力使水分蒸发,得到食盐。
(2)食盐的用途:氯碱工业:2NaCl +2H 2O=====电解2NaOH +Cl 2↑+H 2↑制钠和氯气2NaCl(熔融)=====电解2Na +Cl 2↑ 制盐酸Cl 2+H 2=====点燃2HCl制漂白剂Cl 2+2NaOH===NaCl +NaClO +H 2O制纯碱:NaCl +CO 2+H 2O +NH 3=== NaHCO 3↓+NH 4Cl NaHCO 3=== Na 2CO 3+CO 2↑+H 2O2、 海水提溴:(1)氯化氯气氧化溴离子,在pH=3.5的酸性条件下效果最好,所以在氯化之前要将海水酸化。
(2)吹出当海水中的Br 一被氧化成Br 2以后,用空气将其吹出。
另外,也可以用水蒸气,使溴和水蒸气一起蒸出。
(3)吸收目前比较多的是用二氧化硫作还原剂,使溴单质转化为HBr ,再用氯气将其氧化得到溴产品。
化学方程式如下:2NaBr + Cl 2 === Br 2 +2NaClSO 2+Br 2+2H 2O===4H ++2Br -+SO 2-42 HBr +Cl 2===2 HCl +Br 2 2、海水提镁: (1)工艺流程△(2)主要化学反应①制备石灰乳:CaCO 3 === CaO + CO 2 ↑ ,CaO + H 2O === Ca(OH)2 ②沉淀Mg 2+: MgCl 2+Ca(OH)2===Mg(OH)2↓+CaCl 2③制备MgCl 2:Mg(OH)2+2HCl===MgCl 2+2H 2O, MgCl 2·6H 2O=====HClMgCl 2+6H 2O 制备Mg: MgCl 2(熔融)=====电解Mg +Cl 2↑3、海水提碘(1)工业海带中提碘1)流程:海带―→浸泡―→氧化―→过滤―→提纯―→碘单质 2)主要反应的原理:Cl 2+2KI===2KCl +I 2 (2)海带中含有碘元素的检验1)主要反应的原理:H ++2I -+H 2O 2===I 2+2H 2O二、侯氏制碱法NaCl +CO 2+H 2O +NH 3=== NaHCO 3↓+NH 4ClNaHCO 3=== Na 2CO 3+CO 2↑+H 2O 物质分离的几种方法:定义:物质的分离是指通过适当的方法,把混合物中的几种物质分开(要还原成原来的形式),分别得到几种比较纯净的物质。

2019-2020学年高一化学重难点探究(人教版2019必修第二册)重难点16 海水资源的综合利用方法探究一、海水的淡化1.海水淡化的方法通过从海水中提取淡水或从海水中把盐分离出去,都可以达到淡化海水的目的。
海水淡化的方法有蒸馏法(最先使用,技术成熟,但成本高)、电渗析法(成本低,但未能大量生产)、离子交换法(目前正迅速发展,但需要不断更新离子交换树脂)。
2.海水的整理(1)原理(2)注意事项①烧瓶需垫石棉网加热。
②烧瓶所盛液体不能超过烧瓶容量的23,也不能少于13。
③需向烧瓶中加几粒沸石或几片碎瓷片,以防液体暴沸。
④冷凝器里的冷却水要从冷凝器的下口进、上口出。
二、海水化学资源的开发利用1.海带中碘的提取与检验海水中碘的浓度很低,碘一般从海带或海藻等植物中提取。
使I−变成单质碘,可供选择的常见氧化剂有Cl2和H2O2。
单质碘用苯或四氯化碳萃取,分液后用蒸馏的方法将碘和有机溶剂分开。
2.海水提溴的方法3.海水提镁的方法典例剖析例1 利用海水提取溴和镁的一般过程如下,下列说法正确的是A.工业溴中含少量Cl2,可用NaOH溶液除去B.工业上常利用电解MgCl2溶液冶炼金属镁C.富集溴元素过程中,空气吹出法利用了溴易挥发的性质D.若提取1 mol Br2,至少需要44.8L的Cl2答案C解析A.由于Br2能与NaOH溶液反应,因此用NaOH溶液吸收Cl2的同时,Br2也被吸收,A错误;B.镁是活泼的金属,工业上常用电解熔融的MgCl2冶炼金属镁,惰性电极电解MgCl2溶液生成氯气、氢气和氢氧化镁,B错误;C.溴易挥发,因此在富集溴元素的过程中,可以使用空气吹出法,C正确;D.溶液酸化之后得到的滤液中Br-与氯气发生反应,生成1 mol Br2,需要1 mol Cl2,然后1 mol Br2在吹出塔富集,并在吸收塔中被SO2还原成2 mol Br-,然后在蒸馏塔中Cl2再次将2 mol Br-氧化成1 mol Br2,因此整个过程若提取1 mol Br2,至少需要2 mol氯气,标准状况下为44.8 L,D错误。