抗血小板治疗药物作用机理与实际临床应用
- 格式:ppt
- 大小:2.15 MB
- 文档页数:15
![抗血小板治疗药物的临床选择]](https://uimg.taocdn.com/e1b2b430f111f18583d05a16.webp)



阿司匹林抗板原理-概述说明以及解释1.引言1.1 概述概述部分的内容:阿司匹林作为一种常见的非处方药,被广泛应用于临床医学领域。
它具有抗炎、退热、镇痛等多种作用,但其最重要的作用之一是抗血小板聚集。
阿司匹林通过干扰血小板中的血小板激活因子的生成和释放,从而阻止血小板的凝聚,进而减少血栓形成的风险。
阿司匹林抗血小板的原理主要是通过抑制血小板中的一种酶——环氧化酶。
具体而言,阿司匹林可以通过与血小板中的环氧化酶结合,使得该酶失去活性。
环氧化酶是一种参与前列腺素生成的关键酶,而前列腺素是一类具有促血小板聚集作用的物质。
因此,通过抑制环氧化酶的活性,阿司匹林可以降低前列腺素的合成水平,从而减少血小板的活化和聚集。
阿司匹林抗血小板的机制不仅仅局限于抑制环氧化酶,它还可以干扰血小板中血小板激活因子的合成和释放。
血小板激活因子是指一类可以刺激血小板激活和凝聚的物质,如血栓素A2等。
阿司匹林可以通过不完全明确的机制干扰血小板激活因子的生成,从而减少血小板的功能性活化和凝聚。
总结起来,阿司匹林的抗血小板原理主要通过抑制环氧化酶活性和干扰血小板激活因子的合成来实现。
这一原理使得阿司匹林成为了预防和治疗心脑血管疾病的重要药物,并在临床上发挥了重要的作用。
随着对阿司匹林作用机制的深入研究,阿司匹林的应用前景也将得到进一步的扩展和优化。
1.2 文章结构文章结构本文将首先介绍阿司匹林的作用和背景,然后详细解释阿司匹林的抗血小板原理。
最后,结论部分将强调阿司匹林的重要性,并展望它在未来的应用前景。
在正文部分,我们将首先介绍阿司匹林的作用。
阿司匹林是一种非处方药,广泛用于缓解轻至中度的疼痛、降低发热和减轻炎症症状。
它也被用作预防心脏病和中风的一种药物。
阿司匹林的多种作用使其成为世界上最常用的药物之一。
接下来,我们将详细解释阿司匹林的抗血小板原理。
阿司匹林通过抑制血小板聚集来发挥抗血小板作用。
它通过抑制血小板产生血栓素A2(TXA2)的酶(TXA2合成酶)的活性,从而抑制了血小板的聚集。
常用6种抗血小板药物机制、临床应用及注意事项抗血小板聚集药物是脑梗死急性期、二级预防的主要治疗药物,它们通过作用于血栓形成的不同阶段,达到抗血小板聚集的作用。
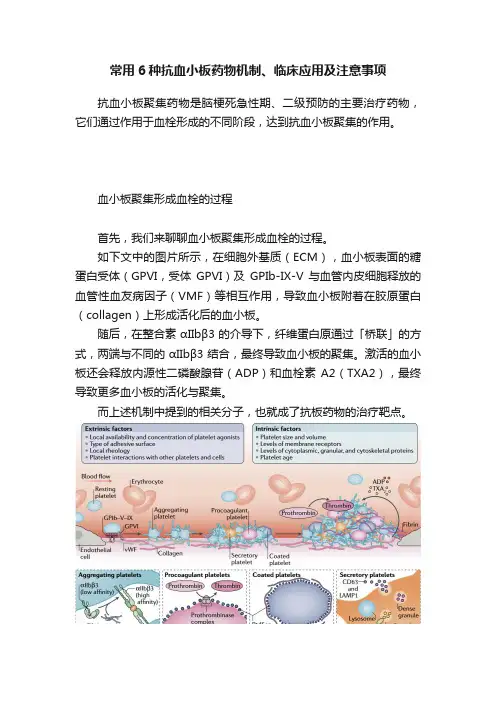
血小板聚集形成血栓的过程首先,我们来聊聊血小板聚集形成血栓的过程。
如下文中的图片所示,在细胞外基质(ECM),血小板表面的糖蛋白受体(GPVI,受体GPVI)及GPIb-IX-V 与血管内皮细胞释放的血管性血友病因子(VMF)等相互作用,导致血小板附着在胶原蛋白(collagen)上形成活化后的血小板。
随后,在整合素αIIbβ3 的介导下,纤维蛋白原通过「桥联」的方式,两端与不同的αIIbβ3 结合,最终导致血小板的聚集。
激活的血小板还会释放内源性二磷酸腺苷(ADP)和血栓素A2(TXA2),最终导致更多血小板的活化与聚集。
而上述机制中提到的相关分子,也就成了抗板药物的治疗靶点。
图 1. 血小板聚集形成血栓的过程不同抗血小板聚集药物作用机制接下来,我们看一下不同抗血小板聚集药物的作用靶点及机制。
图 2. 不同抗血小板聚集药物作用靶点及机制6 种抗血小板聚集药物作用特点1. 阿司匹林1)机制:作为最经典的抗血小板药物,阿司匹林可以不可逆的抑制血小板环氧化酶(COX-1),导致TXA2 生成减少,从而抑制血小板的聚集。
2)起效时间:阿司匹林的达峰时间约为0.3~2 小时,清除半衰期与剂量相关;肠溶片较普通片吸收时间可延长 3~6 小时。
因此,快速起效时可选择嚼服。
3)功能恢复时间:由于阿司匹林不可逆的抑制环氧化酶活性,因此,血小板功能的恢复需要等待血小板的再生,即完全停药后7~10 天。
4)代谢途径:阿司匹林经由肾脏代谢,因此,使用时需考虑肾功能情况。
禁用于合并氨甲蝶呤时,可能会减少其肾清除。
5)合并用药:同样作用于水杨酸的NSAID,如布洛芬等,合并时也需要谨慎。
此外,促进尿酸排泄的药物,如苯磺唑酮等,也可能需要谨慎。
6)注意事项:阿司匹林还可能导致支气管痉挛并引起哮喘发作,因此,也需要考虑患者是否合并哮喘。

抗血小板药物的临床应用抗血小板治疗是指通过药物抑制血小板活化从而阻止血小板参与血栓形成。
理想的抗血小板药物应具有:(1)在体外及体内均有抑制血小扳黏附、聚集和释放的作用;(2)能抑制血小板血栓形成;(3)能延长病理状态下寿命缩短的血小板的生存时间;(4)能延长出血时间但不引起过度出血;(5)口服有效,无明显副作用。
抗血小板药物可以从多步骤干扰血小板的激活,抑制血小板聚集的过程,包括附着、释放和/或聚集,在治疗和预防动脉栓塞方面的作用已很明确。
抗血小板药物种类较多,但有些药物因为其安全性、有效性和可行性等问题限止了它们的临床应用。
抗血小板药物在应用过程中的预防动脉栓塞的作用与增加出血的风险是密不可分的。
1 抗血小板药物1.1 抑制血小板A-A而阻止血小板聚集药物阿司匹林(Aspirin)又名乙酰水杨酸(acetylsalicacid,ASA)是应用和研究最多的抗血小板药物,它的抗血小扳机制包括3个方面: (1)抑制PG合成酶,从而减少PGI 2 与TXA 2 的合成;(2)抑制环氧化酶1(COX-1);(3)抗炎作用。
ASA的抑制作用是不可逆的,由于每日均有新的血小板产生,而当新的血小板占到整体的 10%时,血小板功能即可恢复正常,所以ASA需每日持续服用。
口服单剂量ASA其抗血小板作用可持续7天,接近血小板平均生存期(7~10)天。
ASA 口服生物利用度为70%左右,1~2h内血浆浓度达高峰,半衰期随剂量增加而延长。
有学者研究发现,早晨服药组的PGI 2 水平夜间高于白天,晚间服药则低于白天。
夜间为心脑血管事件高发时段,为保证夜间PGI 2 处于较高水平,ASA早晨服较晚间服有助于预防心脑血管事件的发生。
由于ASA主要是抑制COX-1而发挥作用,所以较大剂量的ASA虽然能抑制血小板的TXA 2 生成而降低血小板聚集,但同时也使血浆中PGI 2 浓度下降,然而内皮细胞的COX-1对ASA的敏感度较血小板弱50~200倍,采用小剂量ASA(50~75mg/d)就能充分抑制TXA 2 的生成,而对PGI 2 几乎无影响。

主要抗血小板药物作用机理一:环氧化酶COX抑制剂阿司匹林可促进C0X-1活性部位第529位丝氨酸乙酰化,不可逆抑制COX- 1的活性。
C0X-1在前列腺素类生物合成的初始步骤中起着关键作用,它可催化花生四烯酸转化为前列腺素H2 PGH2,而PGH2是TXA2的直接前体。
阿司匹林抑制C0X-1的结果是导致TXA2生成减少,而TXA2是强烈的血小板致聚物,TXA2生成减少终影响到血小板的聚集和释放反应。
目前,阿司匹林是动脉粥样硕化性疾病最基础的抗血小板药物。
但阿司匹林在应用过程中亦存在如下主要问题:1胃肠道损伤;2阿司匹林哮喘;3阿司匹林抵抗等。
1胃肠道损害阿司匹林所引起的胃肠道损害包括溃疡、出血甚至穿孔等。
关于阿司匹林对胃肠黏膜损伤的机制尚不完全清楚。
目前认为阿司匹林可能主耍影响了胃肠道黏膜的防御功能。
1抑制胃肠道C0X-1:胃肠黏膜C0X-1可催化花生四烯酸形成前列腺素PG, 而PG特别是PGE2具有扩张血管、增加胃肠黏膜血流、促进黏液和碳酸氢盐分泌的作用。
阿司匹林可抑制胃肠道C0X-1,干扰PG合成,进而减弱PG对胃肠黏膜的保护作用。
2 阿司匹林可穿透胃肠黏膜上皮细胞膜,破坏黏膜屏障,对胃肠黏膜产生直接损伤。
3阿司匹林可抑制血小板聚集,削弱机体的止血机制,诱发出血。
阿司匹林的抗栓作用在较宽的剂量范围内30" 1300 mg/d没有剂效关系,这是因为血小板无核,每个血小板COX-1含量趋丁-恒定,低剂量阿司匹林对血小板COX-1的抑制已经饱和。
相反,阿司匹林的消化道不良反应存在剂效关系,这是因为上消化道黏膜为有核细胞,阿司匹林对有核细胞COX-1的抑制程度与用药剂量和给药间期相关。
研究显示,服用75 mg/d 阿nJ匹林与150mg/d相比胃肠道出血可减少30%,与300 mg/d比可减少40%。
OASIS-7研究显示:服用阿司匹林300^325 mg/d较75、100 mg/d并没有减少急性冠脉综合征ACS患者的血栓性事件,反而增加了出血事件[1]。




抗血小板药的适应症及使用说明抗血小板药物是一类常用于预防和治疗血管系统疾病的药物,其作用是抑制血小板聚集及凝血过程。
正确地选择和使用抗血小板药物对于预防心血管事件的发生具有重要的意义。
本文将介绍抗血小板药物的适应症以及使用说明,帮助读者合理使用这类药物。
以下是具体内容:一、抗血小板药物的适应症1. 无症状的血小板聚集异常:某些人体内的血小板聚集异常,尽管没有任何临床症状,但可能增加心脑血管事件的风险。
对于此类患者,抗血小板药物的使用可以降低血小板聚集,预防血栓形成。
2. 心肌梗死及脑卒中患者:抗血小板药物对于已经发生心肌梗死或脑卒中的患者具有重要的临床意义。
通过抑制血小板聚集,这些药物可以预防或减轻再次心肌梗死或脑卒中的发生。
3. 控制冠心病、动脉粥样硬化和外周动脉疾病:抗血小板药物可以用于预防和治疗冠心病、动脉粥样硬化以及外周动脉疾病。
这些药物可以保持血管的通畅,减少心脑血管事件的风险。
二、常见的抗血小板药物及使用说明1. 阿司匹林:是最常用的抗血小板药物之一。
适应症包括预防心肌梗死、脑卒中、冠心病以及外周动脉疾病。
常见的剂量为75-100mg/天,需在医生的指导下使用。
2. 氯吡格雷:适应症包括急性冠脉综合征、心肌梗死、脑卒中以及外周动脉疾病。
剂量为75mg/天,需在医生的指导下使用。
3. 替格瑞洛:适应症主要是急性冠脉综合征,常见的剂量为90mg/天,需在医生的指导下使用。
4. 布洛芬:适应症主要是用于短期治疗急性冠脉综合征,剂量为300-600mg/天,需在医生的指导下使用。
5. 依克格列酮:适应症为口腔抗血小板治疗方案的一部分,常见的剂量为75-150mg/天,需在医生的指导下使用。
三、使用抗血小板药物的注意事项1. 服药时间和剂量:根据医生的指导,按照规定的时间和剂量服药,切勿擅自调整。
2. 注意副作用:某些抗血小板药物可能会引起胃溃疡、出血等副作用,特别是在使用其他药物时需特别注意。