晶体结构及氧化铝晶体特点
- 格式:ppt
- 大小:8.42 MB
- 文档页数:7
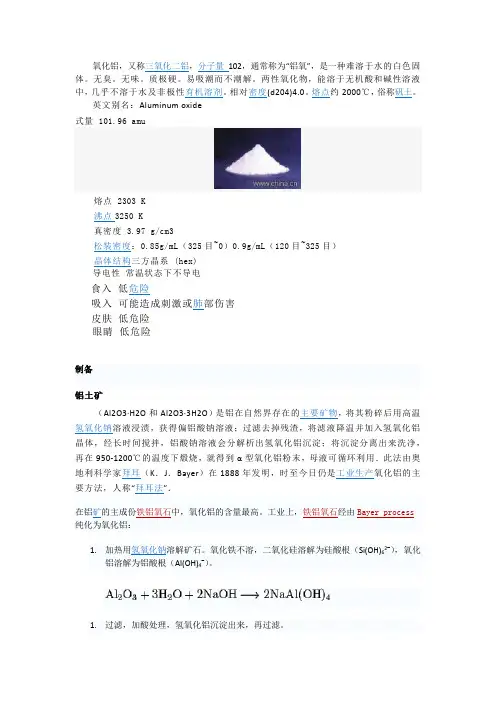
氧化铝,又称三氧化二铝,分子量102,通常称为“铝氧”,是一种难溶于水的白色固体。
无臭。
无味。
质极硬。
易吸潮而不潮解。
两性氧化物,能溶于无机酸和碱性溶液中,几乎不溶于水及非极性有机溶剂。
相对密度(d204)4.0。
熔点约2000℃,俗称矾土。
英文别名:Aluminum oxide式量 101.96 amu导电性常温状态下不导电1.加热用氢氧化钠溶解矿石。
氧化铁不溶,二氧化硅溶解为硅酸根(Si(OH)62−),氧化铝溶解为铝酸根(Al(OH)4−)。
1.过滤,加酸处理,氢氧化铝沉淀出来,再过滤。
再由Hall-Heroult法转变为铝金属。
再由Hall-Heroult法转变为铝金属。
α型氧化铝在α型氧化铝的晶格中,氧离子为六方紧密堆积,Al3+对称地分布在氧离子围成的八面体配位中心,晶格能很大,故熔点、沸点很高.α型氧化铝不溶于水和酸,工业上也称铝氧,是制金属铝的基本原料;也用于制各种耐火砖、耐火坩埚、耐火管、耐高温实验仪器;还可作研磨剂、阻燃剂、填充料等;高纯的α型氧化铝还是生产人造刚玉、人造红宝石和蓝宝石的原料;还用于生产现代大规模集成电路的板基.γ型氧化铝γ型氧化铝是氢氧化铝在140-150℃的低温环境下脱水制得,工业上也叫活性氧化铝、铝胶.其结构中氧离子近似为立方面心紧密堆积,Al3+不规则地分布在由氧离子围成的八面体和四面体空隙之中.γ型氧化铝不溶于水,能溶于强酸或强碱溶液,将它加热至1200℃就全部转化为α型氧化铝.γ型氧化铝是一种多孔性物质,每克的内表面积高达数百平方米,活性高吸附能力强.工业品常为无色或微带粉红的圆柱型颗粒,耐压性好.在石油炼制和石油化工中是常用的吸附剂、催化剂和催化剂载体;在工业上是变压器油、透平油的脱酸剂,还用于色层分析;在实验室是中性强干燥剂,其干燥能力不亚于五氧化二磷,使用后在175℃以下加热6-8h还能再生重复使用.目前世界上用拜耳法生产的氧化铝要占到总产量的90%以上,氧化铝大部分用于制金属铝,用作其它用途的不到10%.电解氧化铝工业化大规模生产电解铝的主要工艺过程是一个熔盐电化学过程,用简单的化学式可表示如下:熔盐电解主反应:Al2O3+2C ——————→ 2Al+CO2↑+CO↑ (1)阳极960~990℃阴极副反应:AlF3+C→Al+CF3 (2)Na3AlF3+C →Al+NaF+CF4+F2 (3)NaF+C → Na+CF4 (4)β型氧化铝还有一种β-Al2O3,它有离子传导能力(允许Na通过),以β-铝矾土为电解质制成钠-硫蓄电池。

氧化铝微观结构氧化铝是一种重要的陶瓷材料,具有广泛的应用领域。
了解氧化铝的微观结构对于深入理解其性质和应用具有重要意义。
从微观角度来看,氧化铝是由氧和铝元素组成的化合物。
氧化铝的晶体结构可以分为两种常见的形态,即α-Al2O3和γ-Al2O3。
其中,α-Al2O3是氧化铝的稳定相,呈现六方紧密堆积的晶体结构。
在α-Al2O3的晶体结构中,氧化铝的铝离子和氧离子按照一定的规律排列。
每个铝离子被六个氧离子包围,而每个氧离子则被三个铝离子包围。
这种紧密堆积的结构使得氧化铝具有高硬度、高熔点和良好的化学稳定性。
另一种常见的氧化铝晶体结构是γ-Al2O3。
γ-Al2O3是由α-Al2O3加热至高温后发生相变得到的。
γ-Al2O3的晶体结构为立方体,其铝离子和氧离子的排列方式与α-Al2O3有所不同。
γ-Al2O3相对于α-Al2O3具有更高的比表面积和更好的催化性能,在催化剂和吸附剂等领域有广泛的应用。
除了晶体结构外,氧化铝的微观结构中还存在着晶界、孔隙和缺陷等微观特征。
晶界是相邻晶体之间的界面,常常由于晶体生长过程中的结晶方向变化或晶体之间的位向关系不匹配而形成。
晶界对氧化铝的物理性能和化学性能有重要影响,例如可以影响材料的导电性和机械强度。
孔隙是氧化铝中的空隙或空气通道,可以分为微孔、介孔和大孔等不同尺寸的孔隙。
孔隙的存在可以影响氧化铝的比表面积、吸附性能和机械性能等。
因此,在某些应用中,需要通过控制氧化铝的制备条件来调控孔隙结构,以满足特定的需求。
氧化铝微观结构中的缺陷也是一个重要的研究对象。
缺陷包括点缺陷、线缺陷和面缺陷等。
点缺陷是晶格中原子位置的缺失或替代,线缺陷是晶格中出现的一维位错,而面缺陷则是晶体表面的不完整性。
这些缺陷对氧化铝的热稳定性、导电性和光学性质等都会产生重要影响。
氧化铝的微观结构包括晶体结构、晶界、孔隙和缺陷等。
了解氧化铝的微观结构有助于深入理解其性质和应用。
未来的研究可以进一步探索氧化铝微观结构与性能之间的关系,以提高氧化铝的性能,并拓展其在各个领域的应用。

氧化铝结构氧化铝是一种很有用的金属材料,由于其独特的物理和化学性质,在航空、航天、电气和电子等行业有广泛的应用。
它是一种金属-非金属复合材料,有独特的结构特征。
在本文中,我们将重点介绍氧化铝结构特征。
氧化铝结构由三种不同形式的晶体具有高度按照正交正方体排列,细致分为不同类型晶体。
它们是α,β和γ的氧化铝。
α氧化铝晶体是结构最简单的形式之一,最常用的形式。
它的晶胞参数接近于正方形,晶胞边长为4.14,对称性为tetrahedral。
β氧化铝的晶胞参数与α氧化铝相同,但其结构变得更加复杂,其单位晶胞为rectangular。
γ氧化铝的晶胞参数最大,达到21.1,同时结构也比其他两个形式复杂得多。
氧化铝晶体表面具有由六角形氧化铝构成的环状立方相,其中氧原子以3:1的比例平衡存在,氧原子之间存在强烈的亲和力。
氧化铝晶体还具有强烈的介电性能,其介电常数接近6.0,介电强度接近2.9 x 10-6 N/m2。
此外,氧化铝晶体表面具有由氧原子、铝原子与氢原子构成的空间结构。
氢原子以H2O形式存在,当两个氧原子靠近时,它们会靠拢形成H2O结构,形成氢结合。
在这种情况下,氢原子通过氧化铝的正交正方体晶体结构形成空间结构,这就是氧化铝的晶体结构特征。
在热处理过程中,氧化铝可以形成多种不同的相,例如α、β、γ、δ和ε等。
这些相之间存在温度和温度变化趋势的协同性,即某一种温度梯度对应某一种相的结构。
按照温度的变化,氧化铝的晶体结构也会产生一定的变化,当温度升高时,晶胞结构会变大,弹性就会增大。
总之,氧化铝晶体结构具有多种特征,其中包括按照正交正方体排列,由α、β和γ类型晶体组成,具有强烈空间结构,介电性能和温度变化对其结构影响的特点。
氧化铝由于其独特的性质,在航空、航天、电气和电子等行业有广泛的用途,将继续受到广泛关注。

氧化铝晶体结构和表面性质的化验分析摘要:氧化铝作为一种重要的材料,在诸多领域具有广泛的应用。
其晶体结构和表面性质对其性能和应用具有关键影响。
因此,对氧化铝的化验分析方法进行深入研究,以揭示其晶体结构和表面性质的信息,具有重要的科学和应用价值。
本文探讨了氧化铝晶体结构和表面性质的化验分析方法,介绍了X射线衍射、电子衍射、扫描电子显微镜、原子力显微镜、X射线光电子能谱和红外光谱等常用技术,并强调它们在研究氧化铝方面的应用。
关键词:氧化铝;晶体结构;表面性质引言:氧化铝具有多种晶体结构,如α-Al2O3、γ-Al2O3、θ-Al2O3等,其晶格常数、晶胞结构和晶体缺陷直接关联着其物理、化学和电学特性。
此外,氧化铝的表面性质,如表面形貌、组成和化学状态,对其在催化、吸附、生物相容性等方面的性能起着决定性作用。
为了深入理解氧化铝的结构和性质,采用多种化验分析方法来揭示其细节是必要的。
一、氧化铝晶体结构的化验分析(一)X射线衍射分析X射线衍射分析是一种常用的技术,用于确定物质的晶体结构和晶格参数。
该方法利用入射X射线束与晶体中的原子相互作用产生衍射现象,通过测量和分析衍射图样,可以推断出晶体中原子的排列方式和晶格的几何参数。
在X射线衍射实验中,X射线源发射的X射线束经过样品后,衍射到不同角度的探测器上形成衍射图样。
通过对衍射图样的解析和模拟,可以得到样品的晶体结构信息,如晶格常数、晶胞体积、晶胞对称性等。
X射线衍射分析在材料科学、矿物学、生物化学等领域具有广泛应用,为研究物质的晶体结构和性质提供了重要的实验手段。
(二)电子衍射技术分析电子衍射技术是一种用于研究材料的晶体结构的强大工具,它利用高能电子束与物质相互作用并产生衍射现象,通过分析衍射图样可以揭示材料的晶体结构和晶格参数[1]。
电子衍射技术可以通过透射电子衍射和选区电子衍射两种方式进行实验。
在透射电子衍射实验中,电子束穿过样品并与样品中的原子相互作用,形成衍射图样。


氧化铝氧化铝,又称三氧化二铝,俗称“矾土”。
是一种白色无定形粉状物。
与氧化铝有关的基本知识因氧化铝有不同的晶形,它可能属于不同的晶体类型:刚玉型晶体接近于原子晶体,其它晶型的基本上是离子晶体。
熔点为2050℃,沸点为3000℃,真密度为3.6g/cm。
它难溶于水,能溶解在熔融的冰晶石中。
它是铝电解生产中的主要原料,化学反应方程式为:2Al2O3=4Al+3O2。
工业上可从铝土矿中提取,化学方程式:溶解:将铝土矿溶于NaOH:Al2O3+2NaOH=2NaAlO2+H2O,过滤:除去残渣氧化铁,铝硅酸钠等酸化:向滤液中通入CO2.NaAlO2+CO2+H2O=Al(OH)3+NaHCO3.过滤,灼烧Al(OH)32Al(OH)3=Al2O3+3H2O.注释:电解时为使氧化铝融熔温度减低,在其中添加冰晶石电解:2Al2O3=4Al+3O2。
它有四种同素异构体β-氧化铝δ-氧化铝γ-氧化铝α-氧化铝,主要有α型和γ型两种变体,α型氧化铝熔点、沸点很高,不溶于水和酸,工业上也称铝氧,是制金属铝的基本原料;也用于制各种耐火砖、耐火坩埚、耐火管、耐高温实验仪器;还可作研磨剂、阻燃剂、填充料等;高纯的α型氧化铝还是生产人造刚玉、人造红宝石和蓝宝石的原料;还用于生产现代大规模集成电路的板基.γ型氧化铝是氢氧化铝在140-150℃的低温环境下脱水制得,工业上也叫活性氧化铝、铝胶.γ型氧化铝不溶于水,能溶于强酸或强碱溶液,将它加热至1200℃就全部转化为α型氧化铝.γ型氧化铝活性高吸附能力强,耐压性好.在石油炼制和石油化工中是常用的吸附剂、催化剂和催化剂载体;在工业上是变压器油、透平油的脱酸剂,还用于色层分析;在实验室是中性强干燥剂,其干燥能力不亚于五氧化二磷,使用后在175℃以下加热6-8h还能再生重复使用.我们所熟知的纯净的金属铝与空气中的氧气所生成的一层致密的氧化铝薄膜便是α型氧化铝。
我们所熟知的红宝石、蓝宝石的主成份也为氧化铝,但因为其它杂质而呈现不同的色泽。

γ-Al2O3、η-Al2O3、κ-Al2O3、χ-Al2O3、θ-Al2O3、α-Al2O3
、ρ-Al2O3和无定形相,共8种晶相。
ρ-Al2O3是结晶度最差,常温有胶结性能,500度后转变为γ-Al2O3,1000度后全变为α-Al2O3。
α-Al2O3在常温与高温都是稳定相。
即平时的刚玉材料的主晶相。
α-Al2O3也叫煅烧氧化铝,具有熔点高、硬度大、绝缘性能强、耐磨性好、化学性质稳定等特点。
广泛用于耐火材料、绝缘器材、集成电路基板、磨料磨具、陶瓷材料等许多领域。
α型氧化铝不溶于水和酸,工业上也称铝氧,是制金属铝的基本原料;也用于制各种耐火砖、耐火坩埚、耐火管、耐高温实验仪器;还可作研磨剂、阻燃剂、填充料等;。



字体大小:大- 中- 小zbgaochun发表于11-09-11 18:36 阅读(82) 评论(0)分类:氧化铝是高熔点氧化物中被研究的最成熟的一种.它的原料藏量丰富,约占地壳重量的25%,价格低廉,并且具有多方面的优良性质,因此,成为一种使用最广泛的氧化铝耐火材料。
氧化铝分子式为Al2Q3,熔点2050℃,呈白色,有许多同质异晶体,据研究报道过的有十多种,他们的结晶结构和物理性质各不相同,但常见的有3种:α- Al2Q3 β- Al2Q3 γ- Al2Q3。
γ- Al2Q3是低温形态的呈鳞片状的立方晶体结晶,其真密度为3.42-3.60g/cm3,它在1000℃以上就开始转化为高温型的α- Al2Q3结晶。
β-Al2Q3实际上并不是氧化铝的一种变体,而是一种含有碱金属或碱土金属的铝酸盐。
当,Al2Q3其化学式可写成:NA2?11-12AL2Q3,CaQ?6 Al2Q3。
这种晶体的特征呈聚片双晶发达的薄片状或板状。
其真空密度为3.30-3.60g/cm3,晶型为六方结构。
当在水蒸气中加热到1300℃或空气中1400-1500℃是就开始分解,到1600℃转化为α- Al2Q3。
α- Al2Q3是氧化铝各种变体中最稳定的结晶形态,它的稳定温度可直至熔化温度,熔点为2050℃,密度为3.96-4.01g/cm3,晶型为六方结构,相当于天然刚玉,晶体形状呈柱状、粒状或板状。
一般所知氧化铝的性质主要是指α- Al2Q3的性质。
氧化铝的莫氏硬度为9,低于金刚石和某些难溶化合物的硬度。
氧化铝制品具有很高的机械强度,常温抗折强度为250Mpa,在1000℃是仍有150Mpa,常温耐压强度可高达2000Mpa以上,某些微晶结构的制品,其耐压强度甚至可达5000Mpa.氧化铝制品的耐火度大于1900℃,0.2Mpa荷重软化开始点为1850℃左右。
它的极限使用温度为1950℃,常用温度为1800℃。
氧化铝在20-1000℃的平均线膨胀系数为8.6*10-6/℃。

铝氧化后的熔点全文共四篇示例,供读者参考第一篇示例:铝是一种常见的金属元素,它具有较轻的密度、良好的导电性和耐腐蚀性,因此被广泛用于各种领域。
在自然环境中,铝会发生氧化反应,形成氧化铝。
铝氧化后形成的氧化铝具有很高的熔点,这一特性使得氧化铝在工业生产中具有重要的应用价值。
铝氧化后的熔点取决于氧化铝的晶体结构和纯度。
氧化铝主要存在于两种晶体结构中,一种是α-Al2O3,另一种是γ-Al2O3。
其中,α-Al2O3具有较高的密度和较高的熔点,是一种石英型晶体结构;而γ-Al2O3具有较低的密度和较低的熔点,是一种立方晶体结构。
因此,氧化铝的熔点取决于其晶体结构,通常情况下,α-Al2O3的熔点约为2072°C,而γ-Al2O3的熔点约为2050°C。
在实际生产中,工业上常用的氧化铝多为α-Al2O3结构。
除了晶体结构外,氧化铝的纯度也会影响其熔点。
通常情况下,氧化铝的熔点会随着纯度的提高而增加。
由于氧化铝在高温下具有出色的耐火性和化学稳定性,因此被广泛用于制作耐火材料、陶瓷材料、电子元件等领域。
在高温工艺中,氧化铝可以作为耐火材料的重要成分,具有很好的耐高温性能和化学稳定性。
总的来说,铝氧化后形成的氧化铝具有很高的熔点,这一特性使得氧化铝在工业生产中具有广泛的应用价值。
通过对氧化铝的晶体结构和纯度进行控制,可以调节氧化铝的熔点,满足不同工艺要求。
未来,随着科学技术的不断发展,氧化铝的制备和应用领域将会进一步拓展,为人类社会的发展做出更大的贡献。
第二篇示例:铝是一种常见的金属元素,它在自然界中广泛存在于矿石中。
铝具有许多优良的性质,如轻便、坚固、具有良好的导电性和导热性等,因此被广泛应用于各种领域,如建筑、航空航天、汽车制造等。
铝的熔点相对较低,为约660摄氏度,这在一定程度上限制了其应用范围。
为了提高铝的熔点,人们常常将其与氧化物化合。
铝氧化后的熔点因其结晶结构和物理性质的改变而有所不同。
晶体结构及氧化铝晶体特点晶体结构是指晶体中原子或离子的组织方式和排列方式。
氧化铝晶体是由氧化铝分子组成的晶体,其晶体结构和特点在材料科学和固态物理领域具有重要意义。
下面将详细介绍氧化铝晶体的结构和特点。
氧化铝晶体的结构主要有两种类型,分别为α-Al2O3和γ-Al2O3α-Al2O3是一种六方最密堆积的晶体结构。
在α-Al2O3的晶体结构中,氧化铝的氧原子形成六角形的紧密堆积层,氧化铝的铝原子位于氧原子周围的空间,形成八面体的空间构型。
这种结构使得α-Al2O3具有很高的结构稳定性和硬度,使其成为一种优良的高温结构材料。
此外,α-Al2O3还具有较高的熔点和热稳定性,能够在高温下保持良好的结构稳定性。
γ-Al2O3是一种立方晶体结构。
在γ-Al2O3晶体结构中,氧化铝的氧原子形成立方堆积层,铝原子位于堆积层之间的空隙中。
此种结构能够容纳更多的氧化铝原子,使得γ-Al2O3具有较高的比表面积和较好的孔隙结构,使其在催化剂、吸附剂和分子筛等领域有广泛应用。
氧化铝晶体的特点主要体现在其物理、化学和机械性质上。
首先,氧化铝晶体具有较高的硬度。
氧化铝的晶体结构中,铝原子和氧原子之间的键强度较高,使得氧化铝具有较好的抗刮擦性和抗磨损性。
因此,氧化铝广泛应用于磨具、切削工具和机械零件等领域。
其次,氧化铝晶体具有较高的熔点和热稳定性。
氧化铝的熔点约为2072℃,使得氧化铝在高温下能够保持良好的物理和化学性质,因此被广泛应用于高温工业领域,如耐火材料、陶瓷材料和航空航天领域等。
此外,氧化铝晶体还具有较好的电绝缘性能和热传导性能,使其在电子器件和散热材料等领域有广泛应用。
总的来说,氧化铝晶体具有结构稳定性高、硬度高、热稳定性好和电绝缘性能优良等特点,使其成为一种重要的材料。
随着研究的不断深入,人们对氧化铝晶体的控制和改进也在不断进行,以满足不同领域对材料性能的要求。
蓝宝石原料:氧化铝的2种晶型蓝宝石原料纯净的氧化铝是白色无定形粉末,俗称矾土,密度3.9-4.0g/cm3,熔点2050℃、沸点2980℃,不溶于水,氧化铝主要有α型和γ型两种变体,工业上可从铝土矿中提取.铝土矿(Al2O3·H2O和Al2O3·3H2O)是铝在自然界存在的主要矿物,将其粉碎后用高温氢氧化钠溶液浸渍,获得铝酸钠溶液;过滤去掉残渣,将滤液降温并加入氢氧化铝晶体,经长时间搅拌,铝酸钠溶液会分解析出氢氧化铝沉淀;将沉淀分离出来洗净,再在950-1200℃的温度下煅烧,就得到α型氧化铝粉末,母液可循环利用.此法由奥地利科学家拜耳(K.J.Bayer)在1888年发明,时至今日仍是工业生产氧化铝的主要方法,人称“拜耳法”.在α型氧化铝的晶格中,氧离子为六方紧密堆积,Al3+对称地分布在氧离子围成的八面体配位中心,晶格能很大,故熔点、沸点很高.α型氧化铝不溶于水和酸,工业上也称铝氧,是制金属铝的基本原料;也用于制各种耐火砖、耐火坩埚、耐火管、耐高温实验仪器;还可作研磨剂、阻燃剂、填充料等;高纯的α型氧化铝还是生产人造刚玉、人造红宝石和蓝宝石的原料;还用于生产现代大规模集成电路的板基.γ型氧化铝是氢氧化铝在140-150℃的低温环境下脱水制得,工业上也叫活性氧化铝、铝胶.其结构中氧离子近似为立方面心紧密堆积,Al3+不规则地分布在由氧离子围成的八面体和四面体空隙之中.γ型氧化铝不溶于水,能溶于强酸或强碱溶液,将它加热至1200℃就全部转化为α型氧化铝.γ型氧化铝是一种多孔性物质,每克的内表面积高达数百平方米,活性高吸附能力强.工业品常为无色或微带粉红的圆柱型颗粒,耐压性好.在石油炼制和石油化工中是常用的吸附剂、催化剂和催化剂载体;在工业上是变压器油、透平油的脱酸剂,还用于色层分析;在实验室是中性强干燥剂,其干燥能力不亚于五氧化二磷,使用后在175℃以下加热6-8h还能再生重复使用.目前世界上用拜耳法生产的氧化铝要占到总产量的90%以上,氧化铝大部分用于制金属铝,用作其它用途的不到10%.6.自然界天然存在的α型氧化铝晶体叫做刚玉,常因含有不同的杂质而呈现不同的颜色.刚玉一般呈带蓝或带黄的灰色,有玻璃或金刚光泽,密度在3.9-4.1g/cm3,硬度8.8,仅次于金刚石和碳化硅,能耐高温.含有铁的氧化物的刚玉砂叫金刚砂,呈暗灰色、暗黑色,常作研磨材料,用于制各种研磨纸、砂轮、研磨石,也用于加工光学仪器和某些金属制品因天然刚玉产量供不应求,工业上常将纯α型氧化铝粉末在高温电炉中烧结制成人造刚玉,也称电熔刚玉.它能耐1800℃以上的高温,是制造高级特殊耐火材料的原料,有高温下机械强度大,抗热震性好,抗侵蚀性强,热膨胀系数小等特点,用于制火箭发动机燃烧室内衬、喷咀,雷达天线保护罩,原子能反应堆材料,高级高频绝缘陶瓷,冶炼纯金属和合金的坩埚,高温发热原件,热电偶保护管,各种高温炉的炉衬等.人造刚玉还用于制精密仪表轴承和金属丝的拉丝具.我国自1958年起就能产生人造刚玉了.7.氧化铝,化学符号:Al2O3、分子量102,纯净氧化铝是白色无定形粉末,俗称矾土,密度3.9-4.0g/cm3,熔点2050℃、沸点2980℃,不溶于水,为两性氧化物,能溶于无机酸和碱性溶液中,有四种同素异构体β-氧化铝δ-氧化铝v-氧化铝a-氧化铝,主要有α型和γ型两种变体,工业上可从铝土矿中提取。
氧化铝材料的物理化学性质氧化铝是一种广泛应用的材料,被用于制造陶瓷、玻璃、电子器件和建筑材料等领域。
它具有优良的物理化学性质,例如高温稳定性、低介电常数、高硬度和耐腐蚀性等。
在本文中,我们将探讨氧化铝材料的一些重要物理化学性质及其在不同领域中的应用。
一、晶体结构和晶格常数氧化铝的晶体结构多样,其中最常见的是以α-Al2O3为代表的三方晶系。
α-Al2O3具有六方紧密堆积结构,空位率极低,其原子结构的排列非常规则。
晶体结构中氧原子属于八面体配位,而铝原子则属于四面体配位。
在正常压力下,α-Al2O3具有较高的稳定性,能够抵抗高温、高压和复杂环境的影响。
氧化铝晶体的晶格常数与晶体结构密切相关。
α-Al2O3的晶格常数为a=4.758Å,c=12.991Å,其晶胞体积为219.52Å^3。
晶格常数与氧化铝材料的物理化学性质密切相关,并且影响着其在不同领域中的应用。
例如,在制造催化剂时,晶格常数能够影响催化活性和选择性。
二、介电性质氧化铝在常温下是绝缘体,其电阻率高达10^14Ω·cm以上。
这是因为氧化铝晶体结构中的氧原子与铝原子呈电中性分布,致使氧化铝晶体中几乎不带有自由电子。
然而,当氧化铝材料被加热至高温时,电子会被激发形成了空穴电子对。
这些电子能够在晶格中移动,导致氧化铝变成半导体。
在高场强下,氧化铝材料的电阻率降低,可以发生电击穿。
氧化铝的介电性质随温度、频率和晶体结构的变化而变化。
例如,在频率较低的情况下氧化铝材料的介电常数相对较大,通常在单晶氧化铝的范围内为9.5~12左右。
在高温下,材料的介电常数逐渐减小,这是由于加热过程中氧化铝材料的带隙变窄,导致电介质损耗增加。
三、化学性质氧化铝具有良好的耐腐蚀性,可在不同的环境下使用。
其化学惰性高,能够长期稳定的存在于强酸和弱碱性环境中。
氧化铝晶体结构中的化学键倾向于共价键,因此氧化铝材料的电子亲和能和极化能相对较小。
氧化铝的相变体积变化氧化铝是一种常见的无机化合物,具有多种晶体结构。
在不同的温度和压力条件下,氧化铝会发生相变,伴随着体积的变化。
本文将探讨氧化铝相变体积变化的相关特点和影响因素。
我们先来了解一下氧化铝的晶体结构。
氧化铝最常见的晶体结构是α-Al2O3,它是一种典型的六方最密堆积结构。
在室温下,氧化铝呈现出α-Al2O3晶体结构,具有高硬度、高熔点、良好的热稳定性和化学稳定性。
然而,在高温条件下,氧化铝会发生相变,从α-Al2O3转变为其他晶体结构。
氧化铝的相变体积变化是指在相变过程中,氧化铝晶体的体积发生变化。
一般来说,相变体积变化可以分为两种情况:正体变和负体变。
正体变是指在相变过程中,物质的体积增大。
对于氧化铝来说,从α-Al2O3晶体结构转变为其他晶体结构时,晶体的体积会增大。
这是因为在相变过程中,氧化铝晶体内部的原子或离子重新排列,晶格结构发生变化,导致晶体的体积增大。
正体变的特点是相变温度上升时,晶体的体积也随之增大。
负体变是指在相变过程中,物质的体积减小。
对于氧化铝来说,从其他晶体结构转变为α-Al2O3晶体结构时,晶体的体积会减小。
这是因为在相变过程中,晶体内部的原子或离子重新排列,晶格结构发生变化,导致晶体的体积减小。
负体变的特点是相变温度上升时,晶体的体积也随之减小。
氧化铝的相变体积变化受多种因素的影响,包括温度、压力和晶体结构等。
首先是温度的影响。
随着温度的升高,氧化铝的相变温度也会上升,从而导致相变体积变化。
在相变温度附近,晶体结构发生变化,晶体的体积也会发生明显的变化。
其次是压力的影响。
在高压条件下,氧化铝的相变温度会降低,相变体积变化也会受到压力的影响。
此外,不同的晶体结构对相变体积变化也有影响。
不同的晶体结构具有不同的晶胞体积,因此在相变过程中晶体的体积变化也会有所不同。
氧化铝的相变体积变化是一个复杂的过程,受到多种因素的影响。
正体变和负体变是晶体结构发生变化时晶体体积变化的两种情况。
α型氧化铝晶体类型Alpha(α)型氧化铝晶体是一种高品质的陶瓷材料,具有许多优良的物理、化学和机械性质,因此在各种应用领域得到了广泛的应用。
本文将从晶体结构、物理、化学和机械性质等方面介绍α型氧化铝晶体的特性。
一、晶体结构α型氧化铝晶体属于六方晶系,晶格参数为a=4.759Å、c=12.992Å,空间群为R-3C。
它的晶体结构被描述为紧密堆积的六边形氧离子,铝离子占据六边形的三分之一空间。
α型氧化铝晶体具有高度排列的晶体结构,具有高度的热稳定性,不易受到热膨胀的影响,因此在高温环境中具有广泛的应用前景。
二、物理性质α型氧化铝晶体具有优良的光学、热学和磁学等物理性质。
首先,它是一种透光性非常好的材料,透过率高达85%以上。
其次,它具有很好的耐高温性能,可以在1500℃以上的高温环境下工作。
此外,α型氧化铝晶体还具有高绝缘性、低热膨胀系数、高硬度和高抗拉强度等特性,在各种应用领域中都具有广泛的应用前景。
三、化学性质α型氧化铝晶体具有较好的耐腐蚀性能,可以耐受很强的酸、碱等化学物质的侵蚀。
此外,它的表面也具有很好的活性,可以用于吸附、催化等化学反应。
四、机械性质α型氧化铝晶体具有很好的机械性能。
它的硬度高达9级,是一种非常坚硬的材料。
此外,在高温条件下,它的强度和耐磨性能也较好。
因此,它在制备高质量研磨片和研磨材料等方面也得到了广泛的应用。
综上所述,α型氧化铝晶体是一种具有优秀物理、化学和机械性能的材料,具有很强的应用前景。
在各种场合下,它都发挥了其独特的优越性能。
因此,在今后的应用中,我们必将看到它在多个领域展示它的无限魅力。
晶体结构及氧化铝晶体特点晶体是由原子、离子或分子按照一定的规律排列而成的固体物质。
晶体结构是指晶体中原子、离子或分子的排列方式和相互间的空间关系。
氧化铝(Al2O3)是一种常见的晶体物质,具有多种不同的晶体结构。
氧化铝晶体主要有α-Al2O3和γ-Al2O3两种结构。
α-Al2O3是一种六方最密堆积结构,晶胞中有4个Al原子和8个O原子。
相邻的晶胞之间通过Al-O-Al键相连。
γ-Al2O3是一种立方晶系结构,晶胞中有2个Al原子和6个O原子。
相邻的晶胞之间通过共享O原子而相连。
氧化铝晶体的特点主要包括硬度、熔点、密度和导电性。
首先,氧化铝晶体具有很高的硬度。
α-Al2O3的硬度约为9,接近于金刚石的硬度,因此具有很好的耐磨性和耐腐蚀性。
其次,氧化铝的熔点很高。
氧化铝的熔点约为2050℃,这是因为氧化铝的晶体结构非常紧密,结构稳定性很高。
再次,氧化铝的密度较大。
α-Al2O3的密度约为3.97g/cm³,γ-Al2O3的密度约为3.6g/cm³。
这意味着氧化铝晶体具有较大的质量和较高的物质密度。
最后,氧化铝是一种绝缘体。
由于氧化铝晶体中的原子排列非常有序,缺乏自由电子,所以氧化铝没有自由电子可以运动,也就没有导电性。
氧化铝晶体在应用中有着广泛的用途。
由于其硬度高、熔点高、耐磨性好和耐腐蚀性强,氧化铝被广泛用于制造陶瓷、砂纸、磨料和抛光材料等。
此外,氧化铝晶体还可用于制备陶瓷膜、电子器件和激光材料等高科技领域。
总之,氧化铝晶体具有很高的硬度、熔点、密度和绝缘性能,这些特点赋予了它广泛的应用价值,并在多个领域发挥着重要的作用。