酸碱平衡和酸碱滴定
- 格式:pdf
- 大小:110.77 KB
- 文档页数:5





无机及分析化学06酸碱平衡与酸碱滴定法酸碱平衡是无机及分析化学中的一个重要概念,它涉及到溶液中酸和碱之间的相互作用和平衡状态。
酸碱滴定法是一种常用于测定溶液中酸碱性质和浓度的分析方法。
本文将对酸碱平衡和酸碱滴定法进行详细介绍。
首先,我们来介绍酸碱平衡的基本概念。
酸碱平衡是指溶液中酸和碱之间的反应和平衡状态。
在溶液中,酸能够释放出H+离子,而碱能够接受H+离子。
这个过程被称为质子(H+)转移反应。
在酸碱平衡中,有两个重要的概念:酸性度(pH)和酸度常数(Ka)。
pH是用来表示溶液酸碱性强弱的指标,它的定义是pH=-log[H+],其中[H+]代表溶液中的氢离子浓度。
pH值越小,表示溶液越酸;pH值越大,表示溶液越碱。
在中性水溶液中,pH值为7酸度常数Ka用来衡量酸的强弱,它的定义是Ka=[H+][A-]/[HA],其中[H+]代表酸溶液中的氢离子浓度,[A-]代表酸的共轭碱的浓度,[HA]代表未解离酸的浓度。
Ka值越大,表示酸越强。
酸碱滴定法是一种常用于测定溶液中酸碱性质和浓度的分析方法。
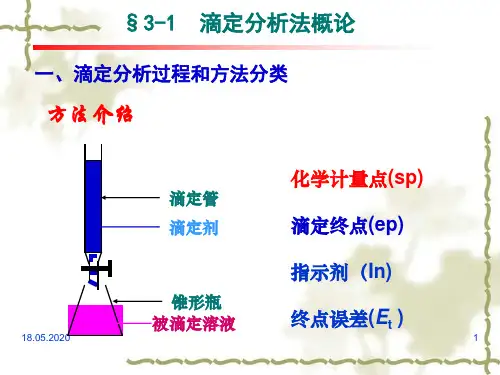
在酸碱滴定中,通常会使用滴定管、酸度计、酸碱指示剂等实验装置和试剂。
滴定过程中需要滴定剂、指示剂和滴定的原料溶液。
滴定过程中,首先准备好要分析的溶液和滴定剂。
然后,用滴定管滴入适量的滴定剂到容器中,然后再加入适当的指示剂。
当滴定剂反应完全与原料溶液中的酸或碱反应完成时,指示剂的颜色将发生明显的变化。
通过测量滴定剂用量,可以计算出原料溶液中酸或碱的浓度。
酸碱滴定法有许多不同的类型,其中最常见的有酸碱滴定、氧化还原滴定和络合滴定。
酸碱滴定是根据滴定剂对溶液中的酸或碱进行中和反应来测定其浓度。
氧化还原滴定是通过滴定剂与溶液中的氧化还原反应来测定其浓度。
络合滴定是通过滴定剂与溶液中的金属离子形成络合物来测定其浓度。
酸碱滴定法在实际应用中有广泛的用途。
例如,它可以用于测定食品和药品中的酸碱度,以确保其安全和合规性。
此外,酸碱滴定还可以用于水质分析、环境监测和药物分析等领域。



第7章酸碱平衡与酸碱滴定法7.1 溶液中酸碱平衡的处理方法 71酸碱滴定法是以酸碱反应为基础的滴定分析方法,是滴定分析中广泛应用的方法之一。
由于酸碱滴定法的基础是酸碱平衡,因此本章首先介绍溶液中酸碱平衡的基本理论,然后学习酸碱滴定法的基本原理及应用。
7.1 溶液中酸碱平衡的处理方法酸碱溶液中平衡型体之间存在三大平衡关系:①物料(质量)平衡,②电荷平衡,③质子平衡。
本章酸度的计算中,用质子平衡对酸碱平衡进行处理,最简单最常用。
因此分别介绍这些方法。
7.1.1 物料平衡平衡状态时,化学体系中某一组分的分析浓度等于该组分各种型体平衡浓度之和。
例题7-1:0.10 mol・L-1 HAc溶液,其物料平衡式为: cHAc=c(HAc) + c(Ac-)=0.10(mol・L-1)例题7-2:0.20 mol・L-1 NaHCO3溶液,其物料平衡式为:?2?c(Na+)=cNaHCO3=c(H2CO3) + c (HCO3) + c(CO3)=0.20 (mol・L-1)例题7-3:0.50 mol・L-1 NaOH溶液,其物料平衡式为: CNaOH=c(Na+ )=c(OH )=0.50 (mol・L-1)-例题7-4:0.50 mol・L-1 HCl溶液,其物料平衡式为: CHCl=c(Cl )=c(H+ )=0.50(mol・L-1 )-例题7-5:0.20 mol・L-1 NH4Cl溶液,其物料平衡式为: CNH4Cl=c(Cl )=c(NH4) + c(NH3)=0.20 (mol・L-1)-?7.1.2 电荷平衡处于平衡状态的水溶液是电中性的,即溶液中荷正电质点所带正电荷的总数与荷负电质点所带负电荷的总数相等。
例题7-6:0.10 mol・L-1 HAc溶液,其电荷平衡式为: c(H+ )=c(Ac- ) + c(OH )-对多价阳(阴)离子,平衡浓度各项中还有相应的系数,其值为相应离子的价数。


酸碱滴定曲线与酸碱平衡曲线的关系探讨酸碱滴定曲线和酸碱平衡曲线是化学中不可或缺的两种曲线类型,它们都是描述酸碱反应的动态过程,但是它们从不同的角度出发,反映的问题不同,因此有着各自的特点和意义,本文将从酸碱滴定曲线和酸碱平衡曲线的概念、实验过程、形态特征和相关理论等几个方面探讨它们之间的关系。
一、概念酸碱滴定曲线指的是在酸碱滴定过程中,酸或碱的滴加量与溶液的酸碱度之间的关系所展现出的曲线,一般是以滴加量为横坐标,PH值为纵坐标。
它揭示了酸碱滴定过程中溶液酸碱度随着滴加量的变化规律,特别是在滴加到等当点附近时,PH值发生急剧变化的现象。
酸碱平衡曲线是指在一定温度和压强下,描述酸碱解离平衡过程中,酸、碱及其离子在各种浓度下浓度以及其对应的PH之间关系的曲线。
一般是以PH值为横坐标,酸或碱的离子浓度或者浓度比值为纵坐标。
它反映了在一定条件下,溶液中酸、碱及其离子浓度以及PH值之间的关系,由于酸碱平衡的存在,曲线中有明显的极值点。
二、实验过程酸碱滴定实验是通过滴定管滴加酸或碱标准溶液到未知浓度酸或碱溶液中,并时时用PH计测定溶液的PH值,最终得到酸碱滴定曲线。
酸碱滴定常常用来测定酸、碱溶液的浓度,以及确定一些物质的酸碱性质。
酸碱平衡实验可通过在一定的条件下,即酸或碱水平、温度和浓度等条件恒定下,将不同浓度的酸或碱标溶液加入某种指示剂或直接使用PH计记录溶液的PH值,从而得到酸碱平衡曲线。
酸碱平衡实验可以反映出酸、碱及其离子或水合离子在各种浓度下所处的平衡位置,是通过测量PH值,借助酸碱计算公式得到酸、碱及其离子浓度比值,再由此得出平衡曲线。
滴定的原理是根据滴定化学反应的摩尔比的关系,已知反应物浓度以及需要达到的反应摩尔比,再测量另一物质的滴加量,从而推导出所需的另一物质的摩尔浓度。
三、形态特征酸碱滴定曲线通常表现出的特征是:曲线起点随PH值的变化而变化,呈现平稳的趋势;随着滴加剂量的增大,曲线逐渐变化,在等当点前,曲线缓慢上升或下降,到达等当点后PH值将呈现急剧变化的趋势,但变化程度较小;等当点后曲线就会开始变平缓,而且曲线对称性强。
第六章酸碱平衡与酸碱滴定【知识导航】本章是基础化学课程学习中的重点,是专升本考试必考内容,如:近年来安徽中医学院专升本考试中都有一题计算题是溶液pH值计算。
同时很多的药物是有机的弱酸弱碱,药典中近一半的药物是用酸碱滴定法测含量,故此在执业药师考试中也有相关考题出现。
学好本章内容有利于同学们备战专升本考试和执业药师考试。
【重难点】1.酸碱理论(1)酸碱电离理论要点定义:水溶液中能够电离出H+的是酸,电离出OH-的碱。
反应的实质:H+ + OH-H2O。
不足:只适用于水溶液体系优点:酸碱概念明确(2)酸碱质子理论要点定义:凡是能给出H+的是酸,能接受H+的是碱。
共轭酸碱对的关系是组成上只相差一个H。
反应的实质:Na+ + Cl- + H2O。
即:质子的传递。
反应的方向:由强向弱进行,强弱差距越大,进行的越彻底。
优点:酸碱概念明确,应用范围更广。
不足:对不含H的反应无法解释。
(3)酸碱质子电子要点(简略)定义:凡是能给出电子对的是酸,能接受电子对的是碱。
优点:应用范围最广。
不足:酸碱概念不够清楚。
2.水的离子积(1)概念定义:一定温度下,水中电离出的H+与OH-浓度的乘积,该乘积是一个常数。
K W=[H+][OH-]=10-14(2)酸碱性浓度定义:[H+]=[OH-]=10-7……中性[H+]>[OH-]……酸性由水中的离子积10-14得来[H+]<[OH-]……碱性由于浓度值往往非常小,对浓度非常小的酸碱溶液用pH表示pH定义:pH = -lg[H+]pH=7……中性pH<7……酸性由H+浓度的负对数求出来的值pH>7……碱性pH值相差1,H+浓度值相差10倍。
通常pH的范围在1~14之间。
3.共轭酸碱对K a与K b的关系(1)关系K a·K b=K W=10-14(2)值的意义K a越大,物质的酸性越强,K b越大,物质的碱性越强。
物质的酸性越强,其共轭碱的碱性就越弱。