初三化学上学期化学方程式-旧人教版
- 格式:pdf
- 大小:576.60 KB
- 文档页数:16


化学九年级上册全部化学方程式1. 镁在空气中燃烧:2Mg + O2 =点燃= 2MgO2. 铁在氧气中燃烧:3Fe + 2O2=点燃= Fe3O43. 铜在空气中受热:2Cu + O2 =加热= 2CuO4. 铝在空气中燃烧:4Al + 3O2 =点燃= 2Al2O35. 氢气中空气中燃烧:2H2 + O2 =点燃= 2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O2 =点燃= 2P2O57. 硫粉在空气中燃烧:S + O2 =点燃= SO28. 碳在氧气中充分燃烧:C + O2 =点燃= CO29. 碳在氧气中不充分燃烧:2C + O2 =点燃= 2CO10. 一氧化碳在氧气中燃烧:2CO + O2 =点燃= 2CO211. 甲烷在空气中燃烧:CH4 + 2O2 =点燃=CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 =点燃= 2CO2 + 3H2O13.玻义耳研究空气的成分实验2HgO =加热= Hg+ O2 ↑14.加热高锰酸钾:2KMnO4 =加热= K2MnO4 + MnO2 + O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应:H2O2 (MnO2催化剂)=2H2O+ O2 ↑(实验室制氧气原理2)16.水在直流电的作用下分解(研究水的组成实验):2H2O =通电= 2H2↑+ O2 ↑17.生石灰溶于水:CaO + H2O == Ca(OH)218.二氧化碳可溶于水:H2O + CO2==H2CO319.镁在空气中燃烧:2Mg + O2 =点燃= 2MgO20.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu21.氢气还原氧化铜:H2 + CuO =加热= Cu + H2O22. 镁还原氧化铜:Mg + CuO =加热= Cu + MgO23. 碳在氧气中充分燃烧:C + O2 =点燃= CO224.木炭还原氧化铜:C+ 2CuO =高温=2Cu + CO2↑25.焦炭还原氧化铁:3C+ 2Fe2O3 =高温= 4Fe + 3CO2↑26.煤炉的底层:C + O2 =点燃= CO227.煤炉的中层:CO2 + C =高温= 2CO28.煤炉的上部蓝色火焰的产生:2CO + O2 =点燃= 2CO229.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 + 2HCl == CaCl2 + H2O + CO2↑30.碳酸不稳定而分H2CO3 == H2O + CO2↑31.二氧化碳可溶于水:H2O + CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3=高温= CaO + CO2↑33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO2 === CaCO3 ↓+ H2O34.一氧化碳还原氧化铜:CO+ CuO =加热= Cu + CO235.一氧化碳的可燃性:2CO + O2 =点燃= 2CO236.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑37.甲烷在空气中燃烧:CH4 + 2O2 =点燃= CO2 + 2H2O38.酒精在空气中燃烧:C2H5OH + 3O2 =点燃= 2CO2 + 3H2O 39.氢气中空气中燃烧:2H2 + O2 =点燃= 2H2O40.镁在空气中燃烧:2Mg + O2 =点燃= 2MgO41.铁在氧气中燃烧:3Fe + 2O2 =点燃= Fe3O442. 铜在空气中受热:2Cu + O2 =加热=2CuO43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O344. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3 H2↑48. 锌和稀盐酸Zn + 2HCl == ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl == FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl == MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3 H2↑52. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 ==ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 == Cu(NO3)2 + Hg 55.3CO+ 2Fe2O3 高温4Fe + 3CO2↑56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl ==2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl ==CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 == CuSO4 + H2O60.盐酸和烧碱起反应:HCl + NaOH == NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 == CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 == AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH == Na2SO4 + 2H2O64.大理石与稀盐酸反应:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl 68.苛性钠暴露在空气中变质:2NaOH + CO2 == Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 == Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 == Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 == CaCO3 ↓+ H2O72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 == CaSO3 ↓+ H2O73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH74. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH 77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 == AgCl↓+ NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓+ 2NaCl。

九年级上册必背的化学方程式
一、化合反应(多变一)
1.二氧化碳和水反应:
2.铜在空气中加热
3.铝在氧气中燃烧
4.氧化钙和水反应
5.镁在空气中燃烧
6.碳在高温下和二氧化碳反应
7.碳在空气中燃烧 8.一氧化碳燃烧
9.硫在空气中燃烧 10.磷燃烧
11.铁在氧气中燃烧
二、分解反应(一变多)
1.高锰酸钾加热分解
2.双氧水和二氧化锰混合
3.氯酸钾和二氧化锰加热分解
4.碳酸分解
5.石灰石高温分解 (二氧化碳的工业制法)
6.水通电分解
三、置换反应:一种单质和一种化合物生成另一种单质和另一种化合物的反应。
金属氧化物和氢气或碳反应,可治炼金属
1.氢气还原氧化铜
2.碳还原四氧化三铁:
3.碳还原氧化铜
4.碳还原氧化铁:
四、复分解反应:两种化合物相互交换成分生成两种新的化合物的反应。
大理石(石灰石)和稀盐酸反应
五、不属基本反应类型的反应
1.二氧化碳与澄清石灰水反应
2.二氧化碳与氢氧化钠反应
3.一氧化碳还原氧化铜
4.一氧化碳还原氧化铁
5.一氧化碳还原氧化亚铁
6.一氧化碳还原四氧化三铁
7.甲烷(CH
天然气、沼气、瓦斯气)燃烧
4。


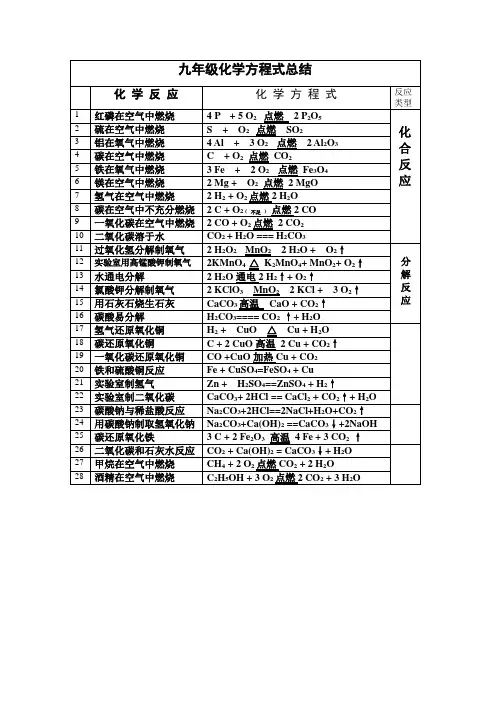
初三化学方程式总结(初三上册)初三化学方程式总结(初三上册)初三化学方程式总结(1--7单元)化合反应1、镁在空气中燃烧:2Mg+O2点燃2MgO2、铁在氧气中燃烧:3Fe+2O2点燃Fe3O43、铝在空气中燃烧:4Al+3O2点燃2Al2O34、氢气在空气中燃烧:2H2+O2点燃2H2O5、红磷在空气中燃烧:4P+5O2点燃2P2O56、硫粉在空气中燃烧:S+O2点燃SO27、碳在氧气中会充分燃烧:C+O2点燃CO28、碳在氧气中不充分燃烧:2C+O2点燃2CO9、二氧化碳通过冰凉碳层:C+CO2高温2CO10、一氧化碳在氧气中燃烧:2CO+O2点燃2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O===H2CO312、生石灰溶于水:CaO+H2O===Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O====CuSO45H2O14、钠在氯气中燃烧:2Na+Cl2点燃2NaCl分解反应15、实验室用双氧水制氧气:2H2O2MnO22H2O+O2↑16、加热高锰酸钾:2KMnO4加热K2MnO4+MnO2+O2↑17、水在直流电的积极作用下分解:2H2O通电2H2↑+O2↑18、碳酸不稳定而纯化:H2CO3===H2O+CO2↑19、高温煅烧石灰石(二氧化碳农业机械制法):CaCO3高温CaO+CO2↑置换反应20、铁和硫酸铜氢氧化钠反应:Fe+CuSO4==FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑22、镁和稀盐酸反应:Mg+2HCl===MgCl2+H2↑23、氢气还原氧化铜:H2+CuO加热Cu+H2O24、木炭还原氧化铜:C+2CuO高温2Cu+CO2↑25、甲烷在空气中会燃烧:CH4+2O2点燃CO2+2H2O26、水蒸气通过灼热碳层:H2O+C高温H2+CO27、焦炭还原氧化铁:3C+2Fe2O3高温4Fe+3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO429、甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O30、酒精在空气当中燃烧:C2H5OH+3O2点燃2CO2+3H2O31、乙炔还原氧化铜:CO+CuO加热Cu+CO232、硫化氢还原氧化铁:3CO+Fe2O3高温2Fe+3CO233、氢气通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2====CaCO3↓+H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2====Na2CO3+H2O35、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl===CaCl2+H2O+CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的电磁场):Na2CO3+2HCl===2NaCl+H2O+CO2↑一.生物体与氧气的反应:(1)单质与氧气的反应:1.镁在空气中燃烧:2Mg+O2点燃2MgO2.铁在氧气中燃烧:3Fe+2O2点燃Fe3O43.铜在空气中受热:2Cu+O2加热2CuO4.铝在空气中燃烧:4Al+3O2点燃2Al2O35.氢气中二氧化碳中燃烧:2H2+O2点燃2H2O6.红磷在空气中挥发:4P+5O2点燃2P2O57.硫粉在空气中燃烧:S+O2点燃SO28.碳在氧气中充分熔化:C+O2点燃CO29.碳在氧气中不充分燃烧:2C+O2点燃2CO(2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2CO+O2点燃2CO211.甲烷在空气之中燃烧:CH4+2O2点燃CO2+2H2O12.酒精在空气中燃点:C2H5OH+3O2点燃2CO2+3H2O二.几个分解反应:13.水在直流电的示范作用下分解:2H2O通电2H2↑+O2↑14.加热碱式碳酸铜:Cu2(OH)2CO3加热2CuO+H2O+CO2↑15.加热氯酸钾(有少量的二氧化锰):2KClO3====2KCl+3O2↑16.加热高锰酸钾:2KMnO4加热K2MnO4+MnO2+O2↑17.碳酸不稳定而分解:H2CO3===H2O+CO2↑18.高温煅烧石灰石:CaCO3高温CaO+CO2↑三.几个氧化还原成反应:19.氢气还原氧化铜:H2+CuO加热Cu+H2O20.木炭还原氧化铜:C+2CuO高温2Cu+CO2↑成才热线:8698887,8697778初三化学复习资料石灰石(或大理石)与稀盐酸反应(实验室制CO2):CaCO3+2HCl===CaCl2+H2O+CO2↑二氧化碳通过澄清石灰水(检验CO2):Ca(OH)2+CO2=CaCO3↓+H2OMnO2氯酸钾与氯二氧化锰的混合物共热:2KClO32KCl+3O2↑加热高锰酸钾:2KMnO4K2MnO4+MnO2+O2↑点燃一、燃烧反应1、木炭在氧气中会燃烧:C+O2CO2(在氧气中:产生使石灰水变浑浊的无色气体)点燃2、木炭在空气中所不充分燃烧:2C+O23、硫化氢在氧气中燃烧:2CO+O24、硫粉在氧气中所燃烧:S+O25、磷在氧气中燃烧:4P+5O26、铁在氧气中燃烧:3Fe+2O2点燃2CO2CO2(产生蓝色火焰)点燃SO2(在空气中:呈淡蓝色火焰;在氧气中:呈明亮的蓝紫色闪电,产生有刺激性气味的气体)点燃2P2O5(产生浓厚的白烟)Fe3O4(剧烈燃烧,火星四射,生成黑色固体)瓶底留少量2MgO(发出耀眼的白光,生成白色固体)2CuO(红色固体变为黑色固体)水或细沙点燃7、镁在空气中燃烧:2Mg+O28、铜在空气中加热;2Cu+O2点燃9、氢气在二氧化碳中燃烧:2H2+O2点燃2H2O(产生淡蓝色火焰,干冷烧杯壁有小水株。


九年级化学方程式总结化学反响化学方程式1 红磷在空气中焚烧4P+5O 2点燃2P 252O硫在空气中焚烧 S+ O2 点燃 SO23铝在氧气中焚烧4Al+ 3O 2点燃232AlO4 碳在空气中焚烧 C+O2 点燃CO25铁在氧气中焚烧3Fe+ 2O2点燃 3 46FeO镁在空气中焚烧 2Mg+ O2 点燃2MgO7 氢气在空气中焚烧 2H2+O 2点燃2H2O8 碳在空气中不充足焚烧 2C+O2(不足)点燃2CO9一氧化碳在空气中焚烧 2CO+O2点燃2CO210生石灰化成熟石灰CaO+H22O==Ca(OH)11CO2322二氧化碳溶于水 +HO===HCO12过氧化氢分解制氧气2H 22MnO22H 2 O+O 2↑O13 实验室用高锰酸钾制氧气2KMnO4△K242 2↑14MnO+MnO+O水通电分解 2H2通电2H 2↑+O2↑15O氧化汞受热分解 2HgO △ 2Hg+ O2↑16氯酸钾分解制氧气2KClO3MnO2 2KCl+3O2↑17 用石灰石烧生18碳酸易分解19氢气复原氧化20 碳复原氧化铜21碳复原氧化铁22铁和硫酸铜反23镁和盐酸反响24镁和硫酸反响25 锌和盐酸反响26实验室制氢气27铁和盐酸反响28铁和硫酸反响29铝和硫酸铜反30铜和硝酸银反31盐酸和氧化铜32硫酸铜和氢氧化钠反响CuSO 4+2NaOH==Cu(OH)2↓+Na 2SO 433实验室制二氧化碳CaCO 3+2HCl==CaCl 2+CO 2↑+H 2O34 铁锈溶解在盐酸中 Fe2332O+6HCl==2FeCl+3HO35 三氧化二铁与硫酸反响Fe2O3+3H2SO4==Fe2(SO4)3+3H2O36 氢氧化钠与盐酸反响NaOH+HCl==NaCl+H 2O 2氢氧化钙与盐酸反响 Ca(OH)2+2HCl==CaCl237+2HO氢氧化钙与硫酸反响Ca(OH)224423839 碳酸钠与稀盐酸反响Na232 2↑CO+2HCl==2NaCl+HO+CO反响种类化合反 应分解反 应置 换 反 应复分解反应40碳酸氢钠与稀盐酸反响41用碳酸钠制取氢氧化钠42一氧化碳复原氧化铜43二氧化碳和石灰水反响44甲烷在空气中焚烧45酒精在空气中焚烧46一氧化碳复原三氧化二铁47氢氧化钠与二氧化碳反响48氢氧化钠与二氧化硫反响49氢氧化钠与三氧化硫反响50氢氧化钙与二氧化硫反响NaHCO3+HCl==NaCl+H2O+CO2↑Na2CO3+Ca(OH)2==CaCO3↓+2NaOHCO+CuO加热Cu+CO2CO2+Ca(OH)2=CaCO3↓+H2OCH4+2O2点燃CO2+2H2OC2H5OH+3O2点燃2CO2+3H2O3CO+Fe2O3高温2Fe+3CO22NaOH+CO2==Na2CO3+H2O2NaOH+SO2==Na2SO3+H2O2NaOH+SO3==Na2SO4+H2OSO2+Ca(OH)2=CaSO3↓+H2O特殊类型。


人教版九年级化学上册化学方程式汇总化学方程式是化学学习中的重要内容,它用简洁的符号和化学式表示化学反应的过程和变化。
在人教版九年级化学上册中,我们学习了许多重要的化学方程式,下面就为大家进行汇总。
一、氧气的性质1、红磷在空气中燃烧:4P + 5O₂点燃 2P₂O₅现象:产生大量白烟,放出热量。
2、硫在空气中燃烧:S + O₂点燃 SO₂现象:发出淡蓝色火焰,生成有刺激性气味的气体,放出热量。
硫在氧气中燃烧:S + O₂点燃 SO₂现象:发出明亮的蓝紫色火焰,生成有刺激性气味的气体,放出热量。
3、木炭在氧气中充分燃烧:C + O₂点燃 CO₂现象:发出白光,放出热量,生成能使澄清石灰水变浑浊的气体。
木炭在氧气中不充分燃烧:2C + O₂点燃 2CO4、铁丝在氧气中燃烧:3Fe + 2O₂点燃 Fe₃O₄现象:剧烈燃烧,火星四射,生成黑色固体,放出热量。
5、镁在空气中燃烧:2Mg + O₂点燃 2MgO现象:发出耀眼的白光,放出热量,生成白色固体。
6、铜在空气中加热:2Cu + O₂加热 2CuO现象:红色固体变黑。
二、制取氧气1、过氧化氢分解制取氧气:2H₂O₂二氧化锰 2H₂O + O₂↑2、加热氯酸钾制取氧气:2KClO₃二氧化锰、加热 2KCl + 3O₂↑3、加热高锰酸钾制取氧气:2KMnO₄加热 K₂MnO₄+ MnO₂+ O₂↑三、水的电解2H₂O 通电 2H₂↑ + O₂↑现象:电极上有气泡产生,一段时间后,正负极产生的气体体积比约为 1:2。
四、氢气的性质1、氢气在空气中燃烧:2H₂+ O₂点燃 2H₂O现象:产生淡蓝色火焰,放出热量。
2、氢气还原氧化铜:H₂+ CuO 加热 Cu + H₂O现象:黑色粉末逐渐变红,试管口有水珠生成。
五、碳的性质1、碳在氧气中充分燃烧:C + O₂点燃 CO₂2、碳在氧气中不充分燃烧:2C + O₂点燃 2CO3、碳还原氧化铜:C + 2CuO 高温 2Cu + CO₂↑现象:黑色粉末逐渐变红,生成能使澄清石灰水变浑浊的气体。

化学方程式总汇(上册)1.碳酸钙+稀盐酸==氯化钙+水+二氧化碳2.高锰酸钾△锰酸钾+ 二氧化锰+氧气3.过氧化氢水+氧气4.二氧化碳+ 石灰水=== 碳酸钙+ 水5.甲烷+ 氧气点燃二氧化碳+ 水6.磷+ 氧气点燃五氧化二磷7.铁+ 氧气点燃四氧化三铁8.碳+ 氧气点燃二氧化碳(氧气充足)9.硫+ 氧气点燃二氧化硫10.水通电氢气+氧气11.镁+ 氧气点燃氧化镁12.二氧化碳+ 水=== 碳酸13.碳酸== 二氧化碳+ 水14.碳+氧气点燃一氧化碳(氧气不充足)15.碳+ 氧化铜高温铜+ 二氧化碳16.锌+ 稀硫酸== 硫酸锌+ 氢气17.氢气+ 氧气点燃水18.一氧化碳+ 氧气点燃二氧化碳19.一氧化碳+氧化铁高温铁+二氧化碳20.碳+ 氧化铁高温铁+ 二氧化碳21.氯酸钾MnO2△氯化钾+ 氧气22.一氧化碳+ 氧化铜△铜+ 二氧化碳23.碳酸钠+稀盐酸==氯化钠+水+二氧化碳24.碳酸钙高温氧化钙(生石灰)+二氧化碳25.酒精+ 氧气点燃二氧化碳+水26.碳+二氧化碳高温一氧化碳27.氧化钙+水==氢氧化钙(熟石灰、消石灰)28.氢气+ 氧化铜△水+ 铜29.锌+ 稀盐酸== 氯化锌+ 氢气1.CaCO3 + 2HCl == CaCl2 + H2O + CO2↑2.2KMnO4△K2MnO4 + MnO2+O2↑(分解)3.2H2O22H2O + O2↑(分解)4.CO2+ Ca(OH)2 == CaCO3↓+ H2O5.CH4 + 2 O2点燃CO2+ 2H2O6.4P + 5O2 点燃2P2O5(化合)7.3Fe + 2O2 点燃Fe3O4(化合)8. C + O2点燃CO2(化合)9.S + O2点燃SO2(化合)10.2H2O 通电2H2↑+ O2 ↑(分解)11.2Mg + O2点燃2MgO(化合)12.H2O + CO2 == H2CO3(化合)13.H2CO3 == H2O + CO2 ↑14.2C + O2点燃2CO(化合)15.C + 2CuO 高温2Cu + CO2↑(置换)16.Zn + H2SO4===ZnSO4 + H2↑(置换)17.2H2 + O2 点燃2H2O(化合)18.2CO + O2 点燃2CO2(化合)19.3CO + Fe2O3高温2Fe + 3CO220.3C + 2Fe2O3高温4Fe + 3CO2↑(置换)21.2KClO3MnO2△2KCl + 3O2↑(分解)22.CO + CuO△Cu + CO223.Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑24.CaCO3高温CaO + CO2↑(分解)25.C2H5OH + 3O2点燃2CO2+ 3H2O26.C + CO2 高温2CO(化合)27.CaO + H2O == Ca(OH)2(化合)28.H2 + CuO△H2O + Cu (置换)29.Zn + 2HCl ===ZnCl2 + H2↑(置换)备注:按重要顺序排列第 1 页,共1页。
人教版九年级化学方程式大全第一单元 走进化学世界(1) 2 NaOH + CuSO 4 ==== Na 2SO 4 + Cu(OH)2↓ (2) CaCO 3 + 2HCl ===CaCl 2 + CO 2↑ + H 2O (3) CO 2 + Ca(OH)2 ===CaCO 3↓+ H 2 (4) Na 2CO 3 + 2HCl == 2NaCl + H 2O + CO 2 ↑第二单元 我们周围的空气⑴ S + O 2SO 2 ⑵ 4 P + 5 O 22 P 2O 5 ⑶ C + O 2CO 2⑷ 3 Fe + 2 O 2Fe 3O 4⑸ 2 H 2O 2O 2↑ + 2 H 2O ⑹ 2 KClO 3 2KCl + 3O 2↑⑺ 2 KMnO 4 K 2MnO 4 + MnO 2 + O 2↑ ⑻ 2 H 2O 2 H 2 ↑+ O 2 ↑⑼ 2 H 2 + O 2 2H 2O⑽ C 2H 5OH + 3 O 22 CO 2 +3 H 2O⑾ 2 HgO 2 Hg + O 2↑⑿ CO 2 + Ca(OH)2 CaCO 3↓+ H 2OMnO 2△ MnO 2△△第三单元自然界的水⑴ 2 H2O 2 H2↑+ O2 ↑⑵ 2 HgO 2 Hg + O2↑⑶ 2 H2 + O22 H2O⑷ H2 + Cl22 HCl⑸2 KMnO4K2MnO4 + MnO2 + O2↑第四单元物质构成的奥秘⑴2 H2O 2 H2↑+ O2 ↑⑵S + O2SO2第五单元化学方程式⑴ 2 Mg + O22 MgO⑵ Fe + CuSO4 FeSO4 + Cu⑶ Na2CO3 + 2HCl == 2NaCl + H2O + CO2 ↑⑷ 2 NaOH + CuSO4Na2SO4 + Cu(OH)2↓⑸ CaCO3CaO + CO2↑⑹ H2 + CuO Cu + H2O⑺ Fe2O3 + 3 H2 2 Fe + 3 H2 O⑻ Fe2O3 + 3CO 2Fe + 3CO2⑼C2H4 + 3 O 2 2 H2O + 2 CO2△△高温高温高温△⑽ CH 4 + 2 O2 CO 2 + 2 H 2O⑾ Zn + H 2SO 4 ZnSO 4 + H 2↑ ⑿ Zn + 2HCl ZnCl 2 + H 2↑ ⒀ H 2 +Cl 22HCl第六单元 碳和碳的氧化物⑴ 2 C + O 2 (不足)2 CO⑵ 2 CuO + C2 Cu + CO 2↑⑶ 2 Fe 2O 3 + 3 C 4 Fe + 3 CO 2↑ ⑷ CaCO 3 + 2HCl CaCl 2 + CO 2↑ + H 2O ⑸ H 2CO 3 H 2O + CO 2↑ ⑹ H 2O + CO 2 H 2CO 3⑺ CO 2 + Ca(OH)2 CaCO 3↓+ H 2O ⑻ 2CO+O 22CO 2⑼ CO + CuO Cu + CO 2 ⑽ CaCO 3 CaO + CO 2↑第七单元 燃料及其利用⑴ CH 4 + 2 O2 CO 2 + 2 H 2O⑵ C 2H 5OH + 3 O22 CO 2 +3 H 2O⑶ Mg + 2HCl MgCl 2 + H 2↑高温高温△高温 高温⑷ Zn + H 2SO 4 ZnSO 4 + H 2↑ ⑸ H 2O + SO 2 H 2SO 3 ⑹ Zn + H 2SO 3 ZnSO 3 + H 2↑ ⑺ Mg + H 2SO 3 MgSO 3 + H 2↑⑻ CaCO 3 + H 2SO 3 CaSO 3↓ + H 2O + CO 2↑ ⑼ Na 2CO 3 + 2HCl == 2NaCl + H 2O + CO 2 ↑ ⑽ 2 H 2 + O 22 H 2O第八单元 金属和金属材料⑴ 4 Al + 2 O 2 2 Al 2O 3 ⑵ Zn + 2HCl ZnCl 2 + H 2↑ ⑶ Fe + 2HCl FeCl 2 + H 2↑ ⑷ Fe + H 2SO 4 Fe SO 4 + H 2↑ ⑸ 2 Al + 3 H 2SO 4 Al 2(SO 4)3 + 3 H 2↑ ⑹ 2 Cu + O 2 2 CuO⑺ Fe 2O 3 + 3CO 2 Fe +3CO 2 ⑻ Mg + H 2SO 4 MgSO 4 + H 2↑ ⑼ Zn + CuSO 4 ZnSO 4 + 3 Cu ⑽ Al + 3AgNO 3 3Ag + Al (NO 3)3 ⑾ Fe + CuCl 2 Fe Cl 2 + Cu△高温⑿ C + CO 2 2 CO⒀ Fe + CuSO 4 FeSO 4 + Cu⒁ ZnCO 3ZnO + CO 2↑ ⒂ ZnO + CO Zn + CO 2↑ ⒃ CuO +CO 2Cu + CO 2 ↑ ⒄ Mg + 2HCl MgCl 2 + H 2↑ ⒅ Zn + H 2SO 4 ZnSO 4 + H 2↑第九单元 溶液⑴ Zn + H 2SO 4 ZnSO 4 + H 2↑⑵ CaCO 3 + 2HCl CaCl 2 + CO 2↑ + H 2O第十单元 酸和碱⑴ Fe 2O 3 + 6 HCl 2 FeCl 3 + 3 H 2O⑵ Fe 2O 3 + 3 H 2SO 4 Fe 2(SO 4)3 + 3 H 2O ⑶ CaO + H 2O Ca(OH)2 ⑷ 2 NaOH + SO 3 Na 2SO 4 + H 2O ⑸ CO 2 + 2 NaOH Na 2CO 3 + 2 H 2O ⑹ HCl + NaOH NaCl + H 2O ⑺ Ca(OH)2 + 2 HCl CaCl 2 + 2 H 2O ⑻ 2 NaOH + H 2SO 4 Na 2SO 4 + 2 H 2O高温 高温 高温高温⑼ Ca(OH)2 + H 2SO 4 CaSO 4 + 2 H 2O ⑽ Mg(OH)2 + 2 HCl MgCl 2 + 2 H 2O ⑾ Al(OH)3 + 6 HCl 2 AlCl 3 + 3 H 2O ⑿ Fe + H 2SO 4 Fe SO 4 + H 2↑⒀CaCO 3 + 2HCl CaCl 2 + CO 2↑ + H 2O第十一单元 盐 化肥⑴ NaHCO 3 + HCl == NaCl + H 2O + CO 2 ↑ ⑵ Na 2CO 3 + Ca(OH)2 2 NaOH + CaCO 3↓ ⑶ K 2CO 3 + Ba(NO 3)2 2 KNO 3 + BaCO 3↓ ⑷ H 2SO 4 + Ba(NO 3)2 2 HNO 3 + BaSO 4↓ ⑸ K 2CO 3 + H 2SO 4 K 2SO 4 + H 2O + CO 2 ↑ ⑹ CaCO 3 + H 2O + CO 2 Ca(HCO 3)2⑺ Ca(HCO 3)2 CaCO 3↓ + H 2O + CO 2 ↑⑻ H 2SO 4 + BaCl 2 2HCl + BaSO 4↓⑼ 2 NH 4Cl + Ca(OH)2 CaCl 2 + 2 NH 3 ↑ + 2 H 2O ⑽ (NH 4)2SO 4 + Ca(OH)2 CaSO 4 ↓+ 2 NH 3 ↑ + 2 H 2O ⑾ K 2SO 4 + Ca(OH)2 K 2SO 4 + 2 NH 3 ↑ + 2 H 2O ⑿ (NH 4)2SO 4 + 2 NaOH Na 2SO 4 + 2 NH 3 ↑ + 2 H 2O ⒀ NH 4Cl + NaOH NaCl + NH 3 ↑ + H 2O△⒁NH4NO3 + NaOH NaNO3 + NH3↑ + H2O⒂(NH4)2SO4 + Ba(NO3)2 2 NH4NO3 + BaSO4↓⒃AgNO3 + NH4Cl == NH4NO3+ AgCl↓⒄Na2CO3 + CaCl2CaCO3↓ + 2 NaCl⒅K2CO3 + 2HCl == 2KCl + H2O + CO2 ↑⒆CuSO4 + BaCl2CuCl2 + BaSO4↓⒇HCl + NaOH NaCl + H2O(21) CaCO3 + 2HCl CaCl2 + CO2↑ + H2O(22) NH3 + CO2 + H2O +NaCl NH4Cl + NaHCO3↓第十二单元化学与生活⑴C6H12O6 +6 O26 CO2 + 6 H2O化学方程式分类汇总一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 2MgO2. 铁在氧气中燃烧:3Fe + 2O2 Fe3O43. 铜在空气中受热:2Cu + O22CuO4. 铝在空气中燃烧:4Al + 3O2 2Al2O35. 氢气中空气中燃烧:2H2 + O2 2H2O6. 红磷在空气中燃烧:4P + 5O2 2P2O5酶△7. 硫粉在空气中燃烧: S + O2SO28. 碳在氧气中充分燃烧:C + O2CO29. 碳在氧气中不充分燃烧:2C + O22CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O22CO211. 甲烷在空气中燃烧:CH4 + 2O2CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O22CO2 + 3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO32CuO + H2O + CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ====2KCl + 3O2↑16. 加热高锰酸钾:2KMnO4 === K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑18.高温煅烧石灰石:CaCO3==CaO + CO2↑三.几个氧化还原反应:19.氢气还原氧化铜:H2 + CuO ===Cu + H2O20.木炭还原氧化铜:C+ 2CuO ===2Cu + CO2↑21.焦炭还原氧化铁:3C+ 2Fe2O34Fe + 3CO2↑22.焦炭还原四氧化三铁:2C+ Fe3O4 ===3Fe + 2CO2↑高温23.一氧化碳还原氧化铜:CO+ CuO === Cu + CO224.氧化碳还原氧化铁:3CO+ Fe2O3 === 2Fe + 3CO225.一氧化碳还原四氧化三铁:4CO+ Fe3O4 ===3Fe + 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质 + 酸 -------- 盐 + 氢气(置换反应)26.锌和稀硫酸: Zn + H2SO4 = ZnSO4 + H2↑27. 铁和稀硫酸: Fe + H2SO4 = FeSO4 + H2↑28.镁和稀硫酸: Mg + H2SO4 = MgSO4 + H2↑29. 铝和稀硫酸: 2Al +3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸: Zn + 2HCl === ZnCl2 + H2↑31. 铁和稀盐酸: Fe + 2HCl === FeCl2 + H2↑32. 镁和稀盐酸: Mg+ 2HCl === MgCl2 + H2↑33. 铝和稀盐酸: 2Al + 6HCl == 2AlCl3 + 3H2↑(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐(置换反应)34. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu35. 锌和硫酸铜溶液反应:Zn + CuSO4 === ZnSO4 + Cu36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg(3)碱性氧化物 +酸 -------- 盐 + 水(复分解反应)37. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl === 2FeCl3 + 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O39. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl2 + H2O40. 氧化铜和稀硫酸反应:CuO + H2SO4 ==== CuSO4 + H2O41. 氧化镁和稀硫酸反应:MgO + H2SO4 ==== MgSO4 + H2O42. 氧化钙和稀盐酸反应:CaO + 2HCl ==== CaCl2 + H2O(4)酸性氧化物 +碱 -------- 盐 + 水(非复分解反应)43.苛性钠暴露在空气中变质:2NaOH + CO2 ==== Na2CO3 + H2O 44.苛性钠吸收二氧化硫气体:2NaOH + SO2 ==== Na2SO3 + H2O 45.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4 + H2O 46.消石灰放在空气中变质:Ca(OH)2 + CO2 ==== CaCO3↓+ H2O 47. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== CaSO3↓+ H2O(5)酸 + 碱 -------- 盐 + 水(复分解反应)48. 盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O49. 盐酸和氢氧化钾反应:HCl + KOH ==== KCl +H2O50. 盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 + 2H2O51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 + 3H2O53. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O54. 硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O55. 硫酸和氢氧化钾反应:H2SO4 + 2KOH ==== K2SO4 + 2H2O56. 硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ==== CuSO4 + 2H2O57. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸 + 盐 -------- 另一种酸 + 另一种盐(复分解反应)59.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑60.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2 + H2O + CO2↑62.盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO363.硫酸和碳酸钠反应:Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2↑64.硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ==== BaSO4↓+ 2HCl(7)碱 + 盐 -----另一种碱 + 另一种盐(复分解反应,且两种反应物均可溶)65.氢氧化钠与硫酸铜:2NaOH + CuSO4 ==== Cu(OH)2↓ + Na2SO4 66.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl67.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl68. 氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH(8)盐 + 盐 ----- 新盐1+新盐2(复分解反应,且两种反应物均可溶)70.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO3 71.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2 + H2O === H2CO373.生石灰溶于水:CaO + H2O === Ca(OH)274.氧化钠溶于水:Na2O + H2O ==== 2NaOH75.三氧化硫溶于水:SO3 + H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O ==== CuSO4 + 5H2O77.无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4·5H2O1、默写1—18号元素的符号和名称:(P59)符号:名称:2、默写常见元素的化合价:+1K、Na、Ag、H ;+2Ca、Mg、Ba、Zn、Hg ;+3 Al ;+4 Si ;+1、+2 Cu ;+2、+3 Fe ;+2、+4 C ;+4、+6 S ;-1 F、Cl ;-2 O、S ;-3 N、P 。
九上化学方程式归纳大全1、镁和稀盐酸反应:Mg + 2HCl = MgCl2 + H2↑2、镁和稀硫酸反应:Mg + H2SO4 = MgSO4 + H2↑3、铝和稀盐酸反应:2Al + 6HCl = 2AlCl3 + 3H2↑4、铝和稀硫酸反应:2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑5、锌和稀盐酸反应:Zn + 2HCl = ZnCl2 + H2↑6、锌和稀硫酸反应:Zn + H2SO4 = ZnSO4 + H2↑7、铁和稀盐酸反应:Fe + 2HCl = FeCl2 + H2↑8、铁和稀硫酸反应:Fe + H2SO4 = FeSO4 + H2↑9、氢气还原氧化铜:H2 + CuO = Cu + H2O10、碳还原氧化铜:C + 2CuO = 2Cu + CO2↑11、氢气还原氧化铁:3H2 + Fe2O3 = 2Fe + 3H2O12、一氧化碳还原氧化铁:3CO + Fe2O3 = 2Fe + 3CO213、实验室制取二氧化碳:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑14、石灰石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑15、碳酸钠与稀盐酸反应:Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑16、电解水反应:2H2O→2H2↑+O2↑17、氢氧化钠与二氧化碳反应(生成碳酸钠和水):2NaOH+CO2→Na2CO3+H2O18、氢氧化钙与二氧化碳反应(生成碳酸钙和水):Ca(OH)2+CO2→CaCO3↓+H2O19、硫酸铜与氢氧化钠反应(生成氢氧化铜沉淀和硫酸钠):CuSO4+2NaOH→Cu(OH)2↓+Na2SO420、硫酸铜与氯化钡反应(生成硫酸钡沉淀和氯化铜):CuSO4+BaCl2→BaSO4↓+CuCl221、硫酸钠与氯化钡反应(生成硫酸钡沉淀和氯化钠):Na2SO4+BaCl2→BaSO4↓+2NaCl22、碳酸钠与氢氧化钙反应(生成碳酸钙沉淀和氢氧化钠):Na2CO3+Ca(OH)2→CaCO3↓+2NaOH23、碳酸氢钠受热分解:2NaHCO3→Na2CO3+H2O+CO2↑24、甲烷燃烧:CH4+2O2→CO2+2H2O。
化学九年级上册所有方程式九上化学方程式如下:1、磷的燃烧化学方程式 4P + 5O2 ═(点燃) 2P2O5 (化合反应)。
2、硫的燃烧化学方程式 S + O2 ═(点燃) SO2 (化合反应)。
3、碳完全燃烧化学方程式 C + O2 ═(点燃) CO2 (化合反应)。
4、碳不完全燃烧化学方程式 2C + O2 ═(点燃) 2CO (化合反应)。
5、铁的燃烧化学方程式 3Fe + 2O2 ═(点燃) Fe3O4 (化合反应)。
6、镁的燃烧化学方程式 2Mg + O2 ═(点燃) 2MgO (化合反应)。
7、铝的燃烧化学方程式 4Al + 3O2 ═(点燃) 2Al2O3 (化合反应)。
8、过氧化氢溶液中加入二氧化锰化学方程式 2H2O2 ═(MnO2)2H2O+ O2↑(分解反应)。
9、加热高锰酸钾制氧气化学方程式2KMnO4 ═(加热) K2MnO4 + MnO2 + O2↑(分解反应)。
10、把氯酸钾与二氧化锰混合加热制取氧气化学方程式 2KClO3═(MnO2)2KCl+3O2 (分解反应)。
11、水中通入直流电化学方程式 2H2O ═(通电)2H2↑+ O2↑(分解反应)。
12、氢气与氯气在点燃的条件下生成氯化氢化学方程式 2H2 + Cl2 ═(点燃)2HCl (化合反应)。
13、氢气燃烧生成水化学方程式 2H2 + O2 ═(点燃) 2H2O (化合反应)。
14、镁与硫酸反应生成硫酸镁和氢气化学方程式 Mg + H2SO4 ═ MgSO4 + H2↑(置换反应)。
15、铝与硫酸反应生成硫酸铝和氢气化学方程式 2Al + 3H2SO4 ═ Al2(SO4)3 + 3H2↑(置换反应)。
16、锌与硫酸反应生成硫酸锌和氢气化学方程式 Zn + H2SO4 ═ ZnSO4 + H2↑(置换反应)。
17、铁与硫酸反应生成硫酸亚铁和氢气化学方程式 Fe + H2SO4 ═ FeSO4 + H2↑(置换反应)。
人教版初三化学全册化学方程式化学方程式是化学学习中的重要内容,它用简洁的符号和式子准确地表达了化学反应的本质。
初三化学涉及到许多化学方程式,让我们一起来梳理一下。
首先是与氧气有关的反应。
氧气是一种非常活泼的气体,能与许多物质发生反应。
红磷在空气中燃烧:4P + 5O₂点燃 2P₂O₅这个方程式表示红磷和氧气在点燃的条件下生成五氧化二磷。
现象是产生大量白烟。
木炭在氧气中充分燃烧:C + O₂点燃 CO₂木炭在氧气中燃烧发出白光,生成能使澄清石灰水变浑浊的气体。
硫在氧气中燃烧:S + O₂点燃 SO₂硫燃烧产生明亮的蓝紫色火焰,生成有刺激性气味的气体。
铁丝在氧气中燃烧:3Fe + 2O₂点燃 Fe₃O₄铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体。
接下来是实验室制取氧气的反应。
加热高锰酸钾制取氧气:2KMnO₄加热 K₂MnO₄+ MnO₂+O₂↑这是一种常见的制取氧气的方法。
过氧化氢分解制取氧气:2H₂O₂二氧化锰 2H₂O + O₂↑在这个反应中,二氧化锰起到催化作用,加快了反应的速率。
氯酸钾受热分解制取氧气:2KClO₃二氧化锰、加热 2KCl +3O₂↑水的电解:2H₂O 通电 2H₂↑ + O₂↑通过这个反应,我们可以了解到水是由氢元素和氧元素组成的。
与氢气有关的反应,氢气具有可燃性。
氢气燃烧:2H₂+ O₂点燃 2H₂O氢气在空气中燃烧产生淡蓝色火焰。
与碳有关的反应也不少。
碳在高温下还原氧化铜:C + 2CuO 高温 2Cu + CO₂↑这个反应体现了碳的还原性。
二氧化碳的相关反应也很重要。
二氧化碳与石灰水反应:CO₂+ Ca(OH)₂= CaCO₃↓ + H₂O 这个反应常用于检验二氧化碳气体。
二氧化碳与水反应:CO₂+ H₂O = H₂CO₃碳酸不稳定,容易分解:H₂CO₃= H₂O + CO₂↑一氧化碳的性质也不能忽视。
一氧化碳燃烧:2CO + O₂点燃 2CO₂一氧化碳具有还原性,比如一氧化碳还原氧化铜:CO + CuO 加热Cu + CO₂金属与酸的反应在初三化学中也经常出现。