高二必修一化学知识硅及其化合物
- 格式:doc
- 大小:25.50 KB
- 文档页数:2

非金属及其化合物一、硅及其化合物 Si硅元素在地壳中的含量排第二,在自然界中没有游离态的硅,只有以化合态存在的硅,常见的是二氧化硅、硅酸盐等。
硅的原子结构示意图为,硅元素位于元素周期表第三周期第ⅣA族,硅原子最外层有4个电子,既不易失去电子又不易得到电子,主要形成四价的化合物。
1、单质硅(Si):(1)物理性质:有金属光泽的灰黑色固体,熔点高,硬度大。
(2)化学性质:①常温下化学性质不活泼,只能跟F2、HF和NaOH溶液反应。
Si+2F2=SiF4Si+4HF=SiF4↑+2H2↑Si+2NaOH+H2O=Na2SiO3+2H2↑②在高温条件下,单质硅能与O2和Cl2等非金属单质反应。
(3)用途:太阳能电池、计算机芯片以及半导体材料等。
(4)硅的制备:工业上,用C在高温下还原SiO2可制得粗硅。
SiO2+2C=Si(粗)+2CO↑Si(粗)+2Cl2=SiCl4SiCl4+2H2=Si(纯)+4HCl2、二氧化硅(SiO2):(1)SiO2的空间结构:立体网状结构,SiO2直接由原子构成,不存在单个SiO2分子。
(2)物理性质:熔点高,硬度大,不溶于水。
(3)化学性质:SiO2常温下化学性质很不活泼,不与水、酸反应(氢氟酸除外),能与强碱溶液、氢氟酸反应,高温条件下可以与碱性氧化物反应:①与强碱反应:SiO2+2NaOH=Na2SiO3+H2O(生成的硅酸钠具有粘性,所以不能用带磨口玻璃塞试剂瓶存放NaOH溶液和Na2SiO3溶液,避免Na2SiO3将瓶塞和试剂瓶粘住,打不开,应用橡皮塞)。
②与氢氟酸反应[SiO2的特性]:SiO2+4HF=SiF4↑+2H2O(利用此反应,氢氟酸能雕刻玻璃;氢氟酸不能用玻璃试剂瓶存放,应用塑料瓶)。
③高温下与碱性氧化物反应:SiO2+CaO CaSiO3(4)用途:光导纤维、玛瑙饰物、石英坩埚、水晶镜片、石英钟、仪器轴承、玻璃和建筑材料等。
3、硅酸(H2SiO3):(1)物理性质:不溶于水的白色胶状物,能形成硅胶,吸附水分能力强。

高中化学——非金属及化合物知识点总结一、硅及其化合物(一)硅1、硅的存在和物理性质(1)存在:只以化合态存在,主要以SiO2和硅酸盐的形式存在于地壳岩层里,在地壳中含量居第二位。
(2)物理性质:晶体硅是一种灰黑色固体,具有金属光泽,硬而脆的固体,熔沸点较高,能导电,是良好的半导体材料。
2、硅的化学性质3、用途:制造半导体、计算机芯片、太阳能电池。
(二)CO2和SiO2的比较(三)硅酸及硅酸盐1、硅酸(1)物理性质:与一般的无机含氧酸不同,硅酸难溶于水。
(2)化学性质:①弱酸性:是二元弱酸,酸性比碳酸弱,与NaOH溶液反应的化学方程式为:②. 不稳定性:受热易分解,化学方程式为:(3)制备:通过可溶性硅酸盐与其他酸反应制得,如Na2SiO3溶液与盐酸反应:(4)用途:硅胶可用作干燥剂、催化剂的载体等。
2、硅酸盐定义:硅酸盐是由硅、氧、金属所组成的化合物的总称。
(1)硅酸盐结构复杂,一般不溶于水,性质很稳定。
通常用氧化物的形式来表示其组成。
例如:硅酸钠Na2SiO3(Na2O·SiO2),高岭石Al2Si2O5(OH)4(Al2O3·2SiO2·2H2O)。
书写顺序为:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水。
注意事项:① 氧化物之间以“·”隔开;②计量数配置出现分数应化为整数。
(2)硅酸钠:Na2SiO3,其水溶液俗名水玻璃,是一种无色粘稠液体,是一种矿物胶,用作黏合剂和木材防火剂。
(四)常见无极非金属材料及其主要用途(五)总结提升1、硅(1)硅的非金属性弱于碳,但碳在自然界中既有游离态又有化合态,而硅却只有化合态。
(2)硅的还原性强于碳,但碳能还原SiO2产生,但Si能跟碱溶液作用放出(3)非金属单质跟碱溶液作用一般无H2H:2(4)非金属单质一般不跟非氧化性酸反应,但硅能跟氢氟酸反应。
(5)非金属单质一般为非导体,但硅为半导体。
2、二氧化硅(1)非金属氧化物的熔沸点一般较低,但SiO2的熔点却很高。

高中化学必修一硅及其化合物复习重点1.了解C,Si元素单质及其重要化合物的主要性质及应用。
2. 了解C,Si元素单质及其重要化合物对环境质量的影响。
3.重点物质:碳、硅、CO2、SiO2。
、硅酸、硅酸盐、无机非金属材料知识梳理一、碳族元素成员:位于族在元素周期表中的位置(周期、族、原子序数)表示方法:原子结构示意图、电子式原子结构相同点:最外层电子数相同,都是个不同点:电子层数不同相似性:得失电子,易形成共价键,难形成离子键,最高正价为,最低价为。
主要性质递变性:随原子序数递增,元素金属性,非金属性;氢化物稳定性(CH4可燃,SiH4易自燃);最高价氧化物对应水化物酸性,碱性,Ge(OH)4呈两性。
碳族元素的金属性比同周期氮族元素,且自上而下由非金属性向金属性递变比氮族更为明显。
1、碳族元素的主要特征(1)C是非金属,Si貌似金属,但大多数情况下显示非金属性,Ge的金属性比非金属性强,Sn、Pb都是金属。
(2)碳族主要化合价是,除Pb的+2价化合物稳定外,其他元素的价化合物稳定。
(3)金刚石、石墨、C60互为,金刚石的硬度最大。
(4)元素是形成化合物种类最多的元素。
(5)在所有非金属元素形成的气态氢化物中,含氢量最大(25%)。
(6)硅在地壳中的含量仅次于氧,是良好的半导体材料。
2、碳族元素单质的重要性质比较二、碳及其化合物1、单质(1)同素异形体金刚石:构型、空间网状结构的晶体。
无色透明,熔沸点高,硬度大,难溶于溶剂,不导电。
用途:钻具、装饰品。
石墨:平面层状正六边形结构,层间以范德华力结合。
熔点很高,质软,有滑腻感,电的良导体。
用途:润滑剂、电极、铅笔芯、耐火材料。
C60:形似足球,俗称“足球烯”,是分子晶体。
无定形碳:木炭、活性炭(有吸附性)等,实际是石墨的微小晶体和少量杂质组成。
(2)化学性质①氧化性:②还原性:(与O2、浓H2SO4、CuO、H2O)、、2、气态氢化物——CH43、一氧化碳CO(1)物理性质:色味的气体,溶于水,有剧毒(与血红蛋白作用)(2)化学性质:高温下表现出强还原性(与O2、Fe2O3、CuO)、4、二氧化碳CO2(1)结构:电子式为,结构式为,空间构型为型。

1硅及其化合物主干知识梳理 一、 硅1、 物理性质: 晶体硅是灰黑色、有金属光泽、硬而脆的固体。
熔沸点很高,硬度也很大。
是良好的半导体材料。
2、 化学性质: 与氟气反应: Si+2F 2=SiF 4与氢氟酸反应: Si+4HF=SiF 4↑+2H 2O与强碱溶液反应: Si+2NaOH+H 2O=Na 2SiO 3+2H 2↑与氯气反应加热_: Si+2Cl 2△SiCl 4 与氧气反应加热: Si+O 2△SiO 2 2 、 制 法:高温 SiO 2+2C===Si+2CO ↑ (含杂质的粗硅)高温 Si+2Cl 2==SiCl 4高温 SiCl 4 +2H 2==Si+4HCl ↑ 这样就可得到纯度较高的多晶硅。
二、二氧化硅 1物理性质:熔点高,硬度大,不溶于水。
纯净的SiO 2晶体无色透明的固体。
2化学性质:①酸性氧化物a 、在常温下与强碱反应,生成盐和水。
例如:SiO 2+2NaOH=Na 2SiO 3+H 2Ob 、在高温下与碱性氧化物反应生成盐。
例如:SiO 2+CaO 高温CaSiO 3 ②弱氧化性:高温下被焦炭还原SiO 2+2C △Si+2CO ↑SiO 2+3C △SiC+2CO ↑(焦炭过量)③特殊反应:a 、与HF 反应 :4HF+ SiO 2= SiF 4↑+2H 2O 氢氟酸是唯一可以与的SiO 2反应的酸。
b 、与Na 2CO 3 和CaCO 3反应:Na 2CO 3+SiO 高温Na 2SiO 3+CO 2↑CaCO 3+SiO 高温CaSiO 3+CO 2↑与CO 的比较2SiO 2是由Si 原子和O 原子以原子个数比为2∶1组成的空间立体网状晶体。
SiO 2晶体与金刚石结构相似,具有高硬度、高熔沸点特征。
(说明:SiO 2晶体结构:不存在单个的SiO 2分子,是由Si 原子和O 原子以2:1组成的空间立体网状晶体。
每个Si 原子与4个O 原子相连,每个O 原子与两个Si 原子相连。

化学必修一第四章知识点归纳一、硅及其化合物。
1. 硅(Si)- 存在形式。
- 硅在地壳中的含量仅次于氧,居第二位。
硅在自然界中以化合态存在,如二氧化硅(SiO₂)和硅酸盐等。
- 物理性质。
- 晶体硅是灰黑色、有金属光泽、硬而脆的固体,熔点高(1410℃),沸点高(2355℃),是良好的半导体材料。
- 化学性质。
- 与非金属反应。
- 硅与氧气反应:Si + O₂{}SiO₂。
- 与氢氟酸反应:Si+4HF = SiF₄↑+2H₂↑,这是硅的特性反应,可用于刻蚀玻璃。
- 与强碱溶液反应:Si + 2NaOH + H₂O=Na₂SiO₃+2H₂↑。
- 工业制法。
- 用焦炭在高温下还原二氧化硅制得粗硅:SiO₂+2C{高温}Si + 2CO↑,粗硅再经过提纯得到高纯硅。
2. 二氧化硅(SiO₂)- 存在形式。
- 天然二氧化硅也叫硅石,有结晶形(如水晶、玛瑙)和无定形(如硅藻土)两种。
- 物理性质。
- 硬度大,熔点高(1710℃),不溶于水。
- 化学性质。
- 与碱性氧化物反应:SiO₂+CaO{高温}CaSiO₃。
- 与强碱反应:SiO₂ + 2NaOH=Na₂SiO₃+H₂O(盛放碱性溶液的试剂瓶不能用玻璃塞,因为生成的Na₂SiO₃有粘性,会使瓶塞与瓶口粘在一起)。
- 与氢氟酸反应:SiO₂+4HF = SiF₄↑+2H₂O。
3. 硅酸(H₂SiO₃)- 物理性质。
- 硅酸是白色胶状沉淀,不溶于水。
- 化学性质。
- 硅酸是一种弱酸,酸性比碳酸还弱。
Na₂SiO₃+CO₂+H₂O =H₂SiO₃↓+Na₂CO₃(证明酸性:碳酸>硅酸)。
- 制备。
- 通过可溶性硅酸盐(如Na₂SiO₃)与酸反应制得,如Na₂SiO₃+2HCl = H₂SiO₃↓+2NaCl。
4. 硅酸盐。
- 定义。
- 由硅、氧和金属元素组成的化合物的总称。
- 硅酸钠(Na₂SiO₃)- 硅酸钠的水溶液俗称水玻璃,是一种无色粘稠的液体,是制备硅胶和木材防火剂等的原料。


硅及其化合物知识点硅的基本概念硅是一种化学元素,化学符号为Si,原子序数为14。
它是地壳中含量第二多的元素,仅次于氧。
硅是一种非金属元素,具有半导体性质,广泛应用于电子工业。
硅的原子结构类似于碳,具有四个价电子,因此它可以形成四个共价键。
硅与氧结合形成二氧化硅(化学式SiO2),是一种常见的无机化合物,也是地壳中最主要的成分之一。
硅的化合物通常由硅原子与其他元素的化合物组成,如硅酸盐、硅烷等。
硅化合物在材料科学、电子工业、化学工业等领域具有重要的应用价值。
硅的性质和用途硅的物理性质:•硅是一种银白色晶体,具有金属光泽。
•硅是一种半导体材料,其导电性介于导体和绝缘体之间。
•硅具有较高的熔点和沸点,熔点约为1414℃,沸点约为3265℃。
硅的化学性质:•硅在常温下与大多数酸和碱不发生反应。
•硅可以与氧反应形成二氧化硅,与氟反应形成氟化硅等。
硅的应用:•电子工业:硅是半导体材料的主要成分,广泛用于制造集成电路、太阳能电池等。
•材料科学:硅的高熔点和耐高温性能使其在高温合金、陶瓷材料等方面有广泛应用。
•化学工业:硅化合物被广泛用于制造硅胶、硅橡胶、硅油等化学产品。
•建筑工业:硅酸盐是建筑材料中常见的成分,如水泥、玻璃等。
硅的化合物1. 二氧化硅(SiO2)二氧化硅是最常见的硅化合物,也是硅的主要氧化物。
它存在于自然界中的石英、石英砂、石英石等矿物中。
二氧化硅具有高熔点、高硬度和良好的绝缘性能,因此被广泛用于制造玻璃、陶瓷、光纤等。
2. 硅酸盐硅酸盐是一类含有硅酸根离子(SiO4)的化合物。
常见的硅酸盐包括长石、石英、云母等。
硅酸盐在建筑材料、陶瓷等方面有广泛应用。
3. 硅烷(SiH4)硅烷是一种由硅和氢组成的化合物,化学式为SiH4。
它是一种无色、有毒的气体,在常温下不稳定,容易分解。
硅烷被广泛用于制造光纤、半导体材料等。
4. 硅酸(H4SiO4)硅酸是一种无机酸,化学式为H4SiO4。
它是一种无色、无味的液体,具有较强的腐蚀性。

关于硅及其化合物的知识无机非金属材料的主角是——硅[知识要点]一、硅1。
物理性质晶体硅是一种具有光泽、硬度和脆性的固体。
它熔点高,能导电,是一种好材料。
在自然界中,它只能以组合状态存在。
它主要以二氧化硅和硅酸盐的形式存在。
它的元素含量在地壳中排名第一。
2.化学性质化学性质(类似于碳)——形成共价化合物,这是化学惰性的。
(1)在常温下,不能与强酸或强氧化性酸反应,只能与氟气、氢氟酸、烧碱等物质反应(方程式:),(2)在加热条件下,能与一些非金属单质(氧和氢)反应。
(3)工业准备:(焦炭在电炉中还原二氧化硅得到粗硅)粗硅提纯后,可以得到可用作半导体材料的高纯硅。
(3)目的:(1)由半导体材料制成的晶体管、集成电路、硅整流器和太阳能电池;(2)合金制造:4%的硅钢具有良好的磁导率——变压器铁芯。
含硅约15%的钢具有良好的耐酸性——耐酸设备等。
二氧化硅1。
硬度、高熔点、不导电、不溶于水的物理性质。
二氧化硅是光纤的主要成分,可用于制造光纤。
2.化学性质注意: 二氧化碳、二氧化硅与碱性氧化物和碱溶液的二氧化硅和二氧化碳反应及盐反应的比较硅酸和硅酸盐(1)硅酸1。
物理属性2。
制备方法3。
化学性质。
用途(2)硅酸盐(1)性质和特性:它性质稳定,熔点高,大部分溶于水。
(2)主要原材料:粘土(Al2O3 2SiO2 2H2O)、应时(SiO2)和长石(钾长石、Na2O Al2O3 6SiO2或钠长石、Na2O Al2O3 6SiO2)。
(3)主要产品:玻璃、水泥、陶瓷、砖瓦、水玻璃(Na2SiO3水溶液)等。
(4)水泥和玻璃生产:水泥玻璃(普通)原料石灰石,粘土纯碱,石灰石,应时设备水泥回转窑玻璃熔窑复合物理化学变化na2co 3 SiO 2 Na 2 SiO 3 CO2↓CaCO3 SiO 2 Casio 3 CO2↓主要成分3 CaO SiO 22 CaO SiO 23 CaO al2o 3 Na 2O CaO 6 SiO 2特征水力(加入石膏调节硬化速度)玻璃物质(在一定温度范围内软化)非晶关键点一.二氧化硅和硅酸[典型例子]例1。

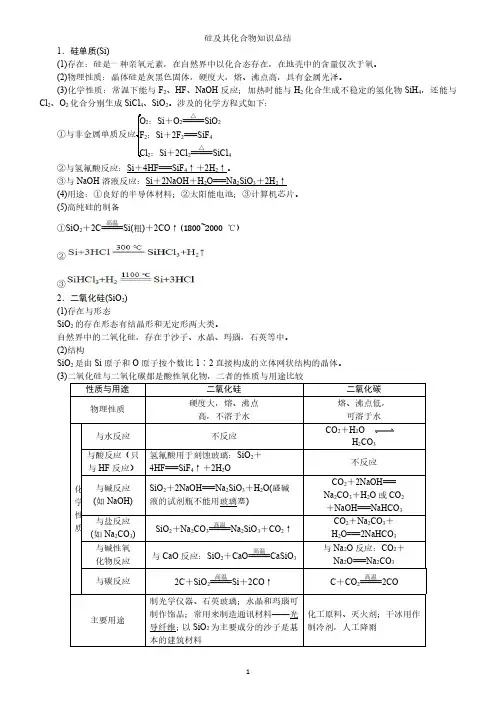
硅及其化合物知识总结1.硅单质(Si)(1)存在:硅是一种亲氧元素,在自然界中以化合态存在,在地壳中的含量仅次于氧。
(2)物理性质:晶体硅是灰黑色固体,硬度大,熔、沸点高,具有金属光泽。
(3)化学性质:常温下能与F 2、HF 、NaOH 反应;加热时能与H 2化合生成不稳定的氢化物SiH 4,还能与Cl 2、O 2化合分别生成SiCl 4、SiO 2。
涉及的化学方程式如下:2:Si +O 2=====△SiO 22:Si +2F 2===SiF 42:Si +2Cl 2=====△SiCl 4②与氢氟酸反应:Si +4HF===SiF 4↑+2H 2↑。
③与NaOH 溶液反应:Si +2NaOH +H 2O===Na 2SiO 3+2H 2↑(4)用途:①良好的半导体材料;②太阳能电池;③计算机芯片。
(5)高纯硅的制备①SiO 2+2C=====高温Si(粗)+2CO ↑(1800~2000℃)②③2.二氧化硅(SiO 2)(1)存在与形态SiO 2的存在形态有结晶形和无定形两大类。
自然界中的二氧化硅,存在于沙子、水晶、玛瑙,石英等中。
(2)结构SiO 2是由Si 原子和O 原子按个数比1∶2直接构成的立体网状结构的晶体。
(3)二氧化硅与二氧化碳都是酸性氧化物,二者的性质与用途比较性质与用途二氧化硅二氧化碳物理性质硬度大,熔、沸点高,不溶于水熔、沸点低,可溶于水化学性质与水反应不反应CO 2+H 2OH 2CO 3与酸反应(只与HF 反应)氢氟酸用于刻蚀玻璃:SiO 2+4HF===SiF 4↑+2H 2O不反应与碱反应(如NaOH)SiO 2+2NaOH===Na 2SiO 3+H 2O(盛碱液的试剂瓶不能用玻璃塞)CO 2+2NaOH===Na 2CO 3+H 2O 或CO 2+NaOH===NaHCO 3与盐反应(如Na 2CO 3)SiO 2+Na 2CO 3=====高温Na 2SiO 3+CO 2↑CO 2+Na 2CO 3+H 2O===2NaHCO 3与碱性氧化物反应与CaO 反应:SiO 2+CaO=====高温CaSiO 3与Na 2O 反应:CO 2+Na 2O===Na 2CO 3与碳反应2C +SiO 2=====高温Si +2CO ↑C +CO 2=====高温2CO 主要用途制光学仪器、石英玻璃;水晶和玛瑙可制作饰品;常用来制造通讯材料——光导纤维;以SiO 2为主要成分的沙子是基本的建筑材料化工原料、灭火剂;干冰用作制冷剂,人工降雨3.硅酸(H 2SiO 3)(1)物理性质:难溶于水的白色胶状物质。
硅元素及其化合物知识点总结
一、什么是硅
硅(Silicon)是一种无色、无臭、有较高熔点的纯净固体,是最常见的金属元素之一、它有高导电性、热电性和冶金特性,是最重要的半导体材料,可用于微电子制造、电力装置、火灾报警器、航空航天制品等。
二、硅元素的结构
硅元素是由28个阳离子和14个阴离子组成的类铁结构,由四个Si 原子构成四个一组,其中两个硅原子存在正方形的相互结合,其余两个Si原子的配对紧密相互关联,被称为类铁结构。
硅元素内部的化学性能和外部的物理性能都会受到这类铁结构的影响。
三、硅元素的物理性质
1、硅元素的密度是2.33 g/cm3,比重是大约2.4
2、硅元素的沸点是2355℃,熔点是1414℃。
3、硅元素的导热系数是159W/(m·K),具有较高的导热性,可用于制作电子器件。
4、硅元素具有高韧性,其弹性模量是约73GPa,抗拉强度约是
211MPa,抗压强度约是8.2MPa。
5、硅元素的折射率在0.5~3.6微米之间,可用作反射镜。
6、硅元素的电导率是0.6×10-(Ω·m),可用作热电力元件。
四、硅元素的化学性质
1、硅元素是一种非金属元素,属于第四周期,在元素周期表中排在14位,原子序数为14,其电子配置与硅杂质的构成相同,即[Ne]3s23p2
2、硅元素是半金属元素。
第二部分:【基本理论】替换PDF文件中的第二部分一、碳、硅及化合物的关系网络1、相互转化关系2、硅的性质和制备:物理性质:①硅在自然界中只有态,没有态。
其含量在地壳中居第位,是构成矿物和岩石的主要成分。
②晶体硅为原子晶体。
灰黑色,有金属光泽,硬而脆的固体,是半导体,具有较高的硬度和熔点。
化学性质:硅的化学性质不活泼。
①常温下,只能与氟气、氢氟酸及强碱溶液反应:Si + 2F2 = SiF4 、Si + 4HF =SiF4 + 2H2↑、Si + 2NaOH + H2O =。
②在加热条件下,能与氧气、氯气等少数非金属单质化合:Si + O2 SiO2制备:在电炉里用碳还原二氧化硅先制得粗硅:SiO2 + 2C。
将制得的粗硅,再与C12反应后,蒸馏出SiCl4,然后用H2还原SiCl4可得到纯硅。
有关的反应为:Si 十2C12 SiCl4、 SiCl4 + 2H2 Si + 4HCl应用:①高纯硅可作材料;②晶体硅还可做光电转换材料及制作生物工程芯片。
3、二氧化硅的性质和应用:①SiO2为晶体,是一种坚硬难熔的固体,硬度、熔点都很高。
②二氧化硅的化学性质很稳定,不能跟酸(氢氟酸除外)发生反应。
③二氧化硅是一种酸性氧化物,所以能跟碱性氧化物或强碱反应。
SiO2 + CaO CaSiO3 、SiO2 + 2NaOH = Na2SiO3 + H2O(碱溶液不能在使用磨口玻璃塞的试剂瓶中)④二氧化硅是一种特殊的酸性氧化物。
a.酸性氧化物大都能直接跟水化合生成酸,但二氧化硅却不能直接跟水化合,它的对应水化物(硅酸)只能用相应的可溶性硅酸盐跟盐酸作用制得。
首先,让SiO2和NaOH(或Na2CO3)在熔化条件下反应生成相应的硅酸钠:SiO2+2NaOH;然后,用酸与硅酸钠作用制得硅酸:Na2SiO3+2HCl === 。
b.酸性氧化物一般不跟酸作用,但二氧化硅却能跟氢氟酸起反应:SiO2+4HF=SiF4+2H2O④光导纤维:从高纯度的SiO2或石英玻璃熔融体中,拉出的直径约100μm的细丝,称为石英玻璃纤维,这种纤维称为光导纤维。
无机非金属材料的主角——硅【知识要点】一、硅1.物理性质晶体硅是一种色具有光泽,硬而脆的固体,熔沸点较高,能导电,是良好的材料。
在自然界中只能以化合态存在。
主要以二氧化硅和硅酸盐的形式存在。
其元素含量在地壳中居第位。
2.化学性质化学性质〔和碳相似〕——形成共价化合物,化学性质不活泼。
①常温下,不能强酸、强氧化性酸反应,只能与氟气、氢氟酸〔HF〕和烧碱等物质反应:方程式、、②加热条件下,能跟一些非金属单质〔氧气、氢气〕起反应。
〔3〕工业制法:〔焦炭在电炉中复原二氧化硅得到粗硅〕粗硅提纯后,可以得到可用作半导体材料的高纯硅。
〔3〕用途:①作半导体材料晶体管、集成电路、硅整流器和太阳能电池等;②制合金:含硅4%的钢具有良好的导磁性——变压器铁芯;含硅15%左右的钢具有良好的耐酸性——耐酸设备等。
二、二氧化硅1.物理性质硬度大,熔沸点高,不导电,不溶于水。
等的主要成分都是二氧化硅,它一般可用于制造光导纤维。
2.化学性质CO2SiO2与碱性氧化物反应与碱液反应与盐反应2Na2CO3+SiO2 CaCO3+SiO2与碳反应与H2O作用与酸反应〔一〕硅酸1. 物理性质2. 制备方法3. 化学性质4. 用途〔二〕硅酸盐〔1〕性质特征:性质稳定,熔点较高,大都溶于水。
〔2〕主要原料:黏土〔Al2O3·2SiO2·2H2O〕、石英〔SiO2〕和长石〔钾长石K2O·Al2O3·6SiO2或钠长石Na2O·Al2O3·6SiO2〕。
〔3〕主要制品:玻璃、水泥、陶瓷、砖瓦、水玻璃〔Na2SiO3的水溶液〕等。
水泥玻璃〔普通〕原料石灰石、粘土纯碱、石灰石、石英设备水泥回转窑玻璃熔炉反应复杂的物理化学变化Na2CO3+SiO2 Na2SiO3+CO2↑CaCO3+SiO2 CaSiO3+CO2↑主要成分3CaO·SiO22CaO·SiO23CaO·Al2O3Na2O·CaO·6SiO2特性水硬性〔加石膏调节硬化速度〕玻璃态物质〔在一定温度范围内软化〕非晶体要点精讲一、二氧化硅和硅酸【典型例题】例1.以下物质中,不能通过化合反应制取的是〔〕A.H2SiO3B.Fe(OH)3C.Fe(NO3)2D.CaSiO3例2.以下各组物质中不起反应的是〔〕A.SiO2与纯碱共熔B.CO2通入Na2SiO3溶液C.SiO2与大理石共熔D.SiO2和浓H2SO4共热例3.碳化硅〔SiC〕的一种晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。
2019高二必修一化学知识硅及其化合物
高中最重要的阶段,大家一定要把握好高中,多做题,多练习,为高考奋战,小编为大家整理了2019高二必修一化学知识,希望对大家有帮助。
⑧元素周期律:
从左到右:原子序数逐渐增加,原子半径逐渐减小,得电子能力逐渐增强(失电子能力逐渐减弱),非金属性逐渐增强(金属性逐渐减弱)
从上到下:原子序数逐渐增加,原子半径逐渐增大,失电子能力逐渐增强(得电子能力逐渐减弱),金属性逐渐增强(非金属性逐渐减弱)
所以在周期表中,非金属性最强的是F,金属性最强的是Fr (自然界中是Cs,因为Fr是放射性元素)
判断金属性强弱的四条依据:
a、与酸或水反应的剧烈程度以及释放出氢气的难易程度,越剧烈则越容易释放出H2,金属性越强
b、最高价氧化物对应水化物的碱性强弱,碱性越强,金属性越强
c、金属单质间的相互置换(如:Fe+CuSO4==FeSO4+Cu)
d、原电池的正负极(负极活泼性﹥正极)
判断非金属性强弱的三条依据:
a、与H2结合的难易程度以及生成气态氢化物的稳定性,越
易结合则越稳定,非金属性越强
b、最高价氧化物对应水化物的酸性强弱,酸性越强,非金属性越强
c、非金属单质间的相互置换(如:Cl2+H2S==2HCl+S)
查字典化学网小编为大家整理了2019高二必修一化学知识,希望对大家有所帮助。