医疗器械分类目录,第一类医疗器械(2015)
- 格式:doc
- 大小:79.00 KB
- 文档页数:2

医疗器械分类目录到第一类医疗器械2015医疗器械分类目录是指国家食品药品监督管理总局根据相关法律法规及标准,对医疗器械进行分类分级,并编制的一份规范性文件。
根据医疗器械分类目录的不同,医疗器械被分为一、二、三类,其中一类医疗器械是具有较高风险性、对人体有直接影响且临床应用较广泛的医疗器械。
2015年,中国的医疗器械分类目录发生了重要变化,多款医疗器械从二类被重新划分为一类。
这一调整主要是因为对不同医疗器械的功效、安全性和临床实际应用情况进行了进一步研究和评估,使得该命名有个科学的依据。
一类医疗器械主要包括具有较高风险性,并且在诊断、治疗和预防疾病过程中起关键作用的医疗器械。
这些器械在使用过程中要求严格遵循相关的法律法规和规范要求,以确保对患者的安全和有效性,同时也要求其生产、销售和使用环节的监管和管理。
将某些医疗器械由二类调整到一类,主要是为了加强对这些器械的监管和管理,提升其安全性。
这些器械包括但不限于:人工晶体、血液透析器、人工耳蜗、机械呼吸机等。
这些器械在临床上具有重要的作用,直接关系到病患的生命和健康,因此,对它们的监管要求更高。
通过将这些器械纳入一类医疗器械范畴中,可以提高其监管的严格性和透明度,进一步保障患者的利益。
此外,对这些器械的监管也提供了更多的数据和经验,使监管部门能够更好地了解其在临床实际应用中的问题和风险,并及时采取相应的措施进行调整和改进。
此次调整也对相关医疗器械的生产企业和销售商提出了更高的要求。
他们需要按照一类医疗器械的标准进行生产和销售,严格遵循技术要求和质量管理规范。
另外,不合格产品的处罚力度也将更大,以保障市场的正常秩序和消费者的权益。
总结而言,医疗器械分类目录的调整是根据科学实证和实践经验,对医疗器械风险和效用进行科学评估的结果。
将某些医疗器械从二类调整到一类,旨在加强对其的监管和管理,提高患者的安全性和治疗效果。
这对于医疗器械生产企业、销售商和监管部门都提出了更高的要求。

医疗器械分类目录全解读在我国,医疗器械按照风险程度和使用目的,分为三类。
第一类医疗器械是指风险较低的医疗器械,如棉签、纱布等;第二类医疗器械是指具有中度风险的医疗器械,如体温计、血压计等;第三类医疗器械是指具有较高风险的医疗器械,如心脏起搏器、人工关节等。
一、第一类医疗器械1. 医用敷料:如棉签、纱布、绷带等。
2. 家庭医疗用品:如体温计、血压计、血糖仪等。
3. 眼科医疗器械:如隐形眼镜、眼药水等。
4. 口腔科医疗器械:如牙刷、牙膏、假牙等。
5. 康复医疗器械:如拐杖、轮椅、按摩器等。
6. 保健医疗器械:如按摩器、足浴盆等。
二、第二类医疗器械1. 诊断器械:如心电图机、超声波仪等。
2. 治疗器械:如氧疗机、呼吸机等。
3. 监护器械:如监护仪、胎心仪等。
4. 体外诊断试剂:如血液检测试剂、尿液检测试剂等。
5. 手术器械:如刀片、钳子等。
6. 放射性医疗器械:如放射性治疗仪、放射性检测仪等。
三、第三类医疗器械1. 心脏外科器械:如心脏起搏器、人工心脏等。
2. 血管外科器械:如血管内支架、人工血管等。
3. 神经外科器械:如脑起搏器、神经导管等。
4. 骨科器械:如人工关节、骨折内固定器等。
5. 整形外科器械:如假体、脂肪填充器等。
6. 器官移植器械:如人工肾、人工肝等。
7. 血液净化器械:如血液透析机、腹膜透析器等。
8. 医疗设备:如CT、MRI、DSA等。
9. 医疗软件:如电子病历系统、医学影像处理软件等。
通过对医疗器械分类目录的全面解读,我们可以了解到医疗器械的种类、风险程度以及使用范围。
这对于我们正确选择和使用医疗器械,保障医疗安全具有重要意义。
在今后的日子里,让我们共同努力,为医疗器械行业的发展贡献力量。
第一类医疗器械。
这些医疗器械的风险较低,主要包括医用敷料、家庭医疗用品、眼科医疗器械、口腔科医疗器械、康复医疗器械和保健医疗器械等。
这些产品是我们日常生活中经常接触到的,比如棉签、纱布、体温计、血压计等。

一二三类医疗器械分类目录一、医疗器械的分类:第一类是风险程度低,实行常规管理可以保证其安全、有效的医疗器械。
第二类是具有中度风险,需要严格控制管理以保证其安全、有效的医疗器械。
第二类是具有中度风险,需要严格控制管理以保证其安全、有效的医疗器械。
二、医疗器械许可范围及生产条件:1、第一类医疗器械实行产品备案管理,第二类、第三类医疗器械实行产品注册管理。
2、医疗器械注册人、备案人应当加强医疗器械全生命周期质量管理,对研制、生产、经营、使用全过程中医疗器械的安全性、有效性依法承担责任。
3、第一类医疗器械产品备案和申请第二类、第三类医疗器械产品注册,应当提交下列资料:(一)产品风险分析资料;(二)产品技术要求;(三)产品检验报告;(四)临床评价资料;(五)产品说明书以及标签样稿;(六)与产品研制、生产有关的质量管理体系文件;(七)证明产品安全、有效所需的其他资料。
4、申请第二类医疗器械产品注册,注册申请人应当向所在地省、自治区、直辖市人民政府药品监督管理部门提交注册申请资料。
申请第三类医疗器械产品注册,注册申请人应当向国务院药品监督管理部门提交注册申请资料。
三、一类、二类、三类医疗器械目录:一类,二类和三类术语管理类别,看医疗器械监督管理条例有相关的规定。
管理由低到高。
医疗器械,是指单独或者组合使用于人体的仪器、设备、器具、材料或者其他物品,包括所需要的软件;其用于人体体表及体内的作用不是用药理学、免疫学或者代谢的手段获得,但是可能有这些手段参与并起一定的辅助作用;其使用旨在达到下列预期目的:(1)对疾病的预防、诊断、治疗、监护、缓解;(2)对损伤或者残疾的诊断、治疗、监护、缓解、补偿;(3)对解剖或者生理过程的研究、替代、调节;(4)妊娠控制。
医疗器械分为三类:第一类医疗器械有:基础外科用刀《手术刀柄和刀片、皮片刀、疣体剥离刀、柳叶刀、铲刀、剃毛刀、皮屑刮刀、挑刀、锋刀、修脚刀、修甲刀、解剖刀等》第二类医疗器械:(a) 普通诊察器械类(6820):体温计、血压计;(b) 物理治疗及康复设备类(6826):磁疗器具;(c) 临床检验分析仪器类(6840):家庭用血糖分析仪及试纸;(d) 手术室、急救室、诊疗室设备及器具类(6854):医用小型制氧机手提式氧气发生器;(e) 医用卫生材料及敷料类(6864):匡用脱脂棉、医用脱脂纱布;(f) 医用高分子材料及制品类(6866):避孕套、避孕帽等第三类医疗器械:A、一次性使用无菌医疗器械1、一次性使用无菌注射器;2、一次性使用输液器;3、一次性使用输血器;4、一次性使用麻醉穿刺包;5、一次性使用静脉输液针;6、一次性使用无菌注射针;7、一次性使用塑料血袋;8、一次性使用采血器;9、一次性使用滴定管式输液器。
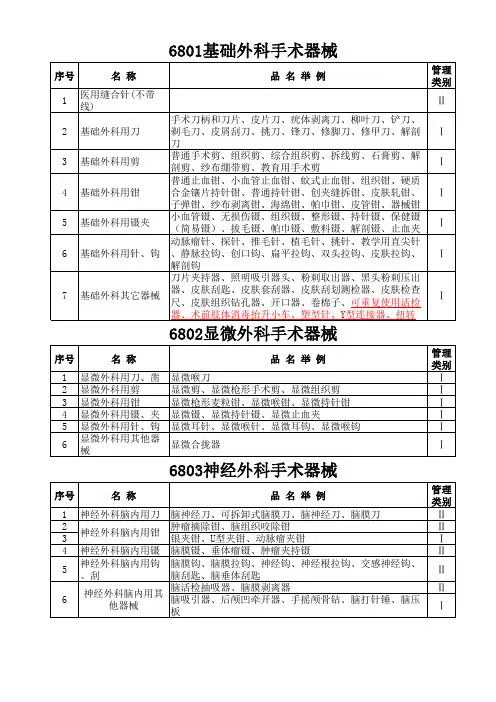
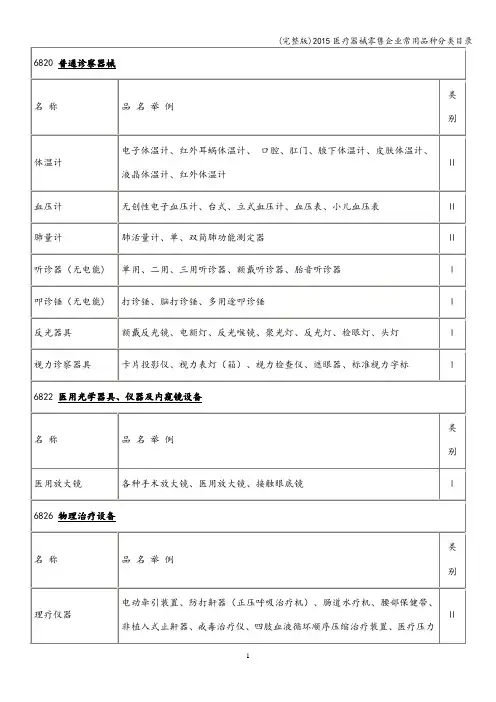
6801基础外科手术器械
6802显微外科手术器械
6803神经外科手术器械
6804眼科手术器械
6805耳鼻喉科手术器械
6806口腔科手术器械
6807胸腔心血管外科手术器械
6808腹部外科手术器械
6809泌尿肛肠外科手术器械
6810矫形外科(骨科)手术器械
6812妇产科用手术器械
6813计划生育手术器械
6815注射穿刺器械
6816烧伤(整形)科手术器械
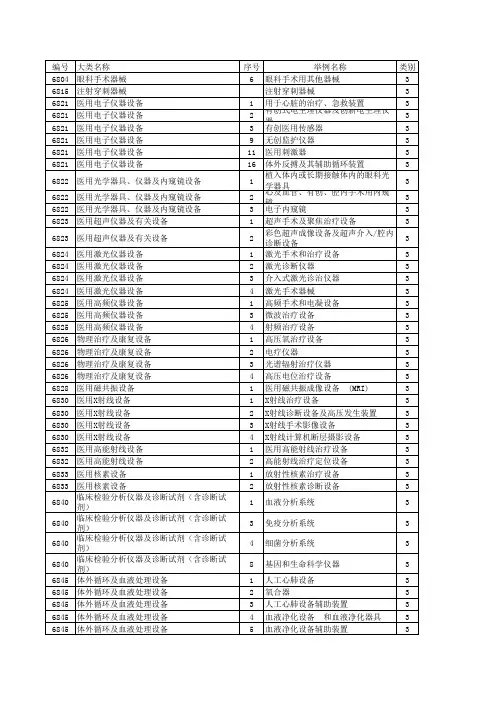
6820普通诊察器械
6821 医用电子仪器设备
6822 医用光学器具、仪器及内窥镜设备
6823医用超声仪器及有关设备
6824医用激光仪器设备
6825医用高频仪器设备
6826物理治疗设备
6827中医器械
6828医用磁共振设备
6830医用X射线设备
6831医用X射线附属设备及部件
6832医用高能射线设备
6833医用核素设备
6834医用射线防护用品、装置
6840临床检验分析仪器
6841医用化验和基础设备器具
6845体外循环及血液处理设备
6846植入材料和人工器官
6854手术室、急救室、诊疗室设备及器具
6855口腔科设备及器具
6856病房护理设备及器具
6857消毒和灭菌设备及器具
6858医用冷疗、低温、冷藏设备及器具
6863口腔科材料
6864医用卫生材料及敷料
6865医用缝合材料及粘合剂
6870 软 件
6877介入器材。

引言概述:医疗器械是指用于预防、诊断、治疗、矫正或缓解人类疾病、病理状态或身体损伤的设备、器具、材料或其他相关物品。
为了规范医疗器械管理和使用,我国制定了一类二类三类医疗器械分类目录。
本文将详细介绍一类二类三类医疗器械分类目录的内容和特点。
正文内容:一、一类医疗器械的分类目录1.手术器械类:外科刀具外科钳夹切割和缝合器械2.植入材料类:人工器官植入材料骨科植入材料心血管植入材料3.体外诊断试剂类:体外诊断试纸体外诊断试剂盒体外诊断仪器4.介入治疗器械类:血管介入器材心脏介入器械内窥镜及其附件5.康复辅助器械类:矫形器械助听器呼吸辅助器械二、二类医疗器械的分类目录1.医学影像设备类:X射线设备核磁共振设备超声波设备2.临床检验设备类:自动生化分析仪血液分析仪免疫分析仪3.医用监护设备类:呼吸机心电监护仪血压计4.临床诊断设备类:全自动生化分析仪血细胞分析仪尿常规分析仪5.系统和设备类:输液泵输血设备电刀三、三类医疗器械的分类目录1.医用缝合线类:吸收性缝线非吸收性缝线缝线夹钳2.医用材料类:医用胶带医用敷料医用冷疗贴3.医用注射器及其附件类:一次性注射器注射器针头注射器塞子4.医用输液器及其附件类:一次性输液器输液器管道输液器针头5.医用气体设备及其附件类:氧气气瓶氧气面罩大流量吸入器总结:一类二类三类医疗器械分类目录的详细内容和特点是医疗器械管理和使用的重要参考依据。
一类医疗器械对人体直接应用,在安全性方面要求极高;二类医疗器械需要临床检验确认其安全性和有效性;三类医疗器械对人体健康影响的风险较小。
通过本文的介绍,可以更好地了解一类二类三类医疗器械分类目录的内容和特点,为医疗器械的管理和使用提供指导。

医疗器械分类目录到第一类医疗器械2015医疗器械是人类现代医疗保健体系中不可或缺的重要组成部分。
医疗器械的分类和管理对保障医疗设备的安全性和有效性至关重要。
在中国,医疗器械的分类由国家食品药品监督管理局(简称CFDA)负责,并于2015年进行了最新的分类目录修订。
第一类医疗器械是医疗器械分类目录中的一个重要分类。
根据国家食品药品监督管理局发布的《医疗器械分类目录(2015年版)》,第一类医疗器械包括了人体内植入器械、体外使用器械、雷射器械、注射给药器械、体外诊断检验器械等多个细分领域的设备和工具。
作为第一类医疗器械的一种,人体内植入器械是指植入到人体内部以修复、增强或替代人体结构和生理功能的器械。
这类器械在手术中应用广泛,如人工关节、心脏起搏器等。
体外使用器械则是指在人体外部应用的医疗器械,例如血压计、听诊器等。
雷射器械则是利用激光技术进行医疗治疗或体检的器械,广泛应用于皮肤科、眼科等领域。
注射给药器械是在医疗过程中用于给药的器械,包括注射器、输液器、针头等。
这些器械对药品的安全使用起着重要的作用。
体外诊断检验器械则是用于检验人体组织或体液样本,帮助医生进行诊断和治疗的工具。
这类器械包括血液分析测定仪器、尿液分析仪器等。
第一类医疗器械的分类范围广泛,涵盖了许多不同的设备和工具。
这些器械被划分为第一类主要是因为其使用和管理的风险较低,但仍然需要严格遵守相关的技术规范和质量要求。
医疗器械的安全性和有效性对于患者的生命健康至关重要,因此,准确的分类和有效的管理是保障公众健康的重要措施。
在2015年的医疗器械分类目录修订中,第一类医疗器械的范围和具体分类都有所调整。
这次修订的目的是根据国内外科技和医疗发展的需要,对不同类别的医疗器械进行更准确的划分和管理。
其中包括对新兴技术的医疗器械进行了分类,以适应不断变化的医疗需求。
总的来说,医疗器械分类目录的修订对于保障医疗器械的安全性和有效性具有重要意义。
第一类医疗器械作为其中的一个重要分类,涵盖了多个细分领域的设备和工具。
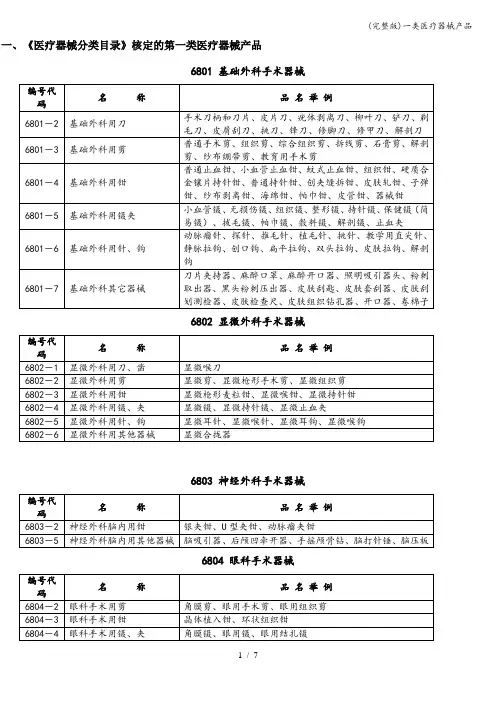
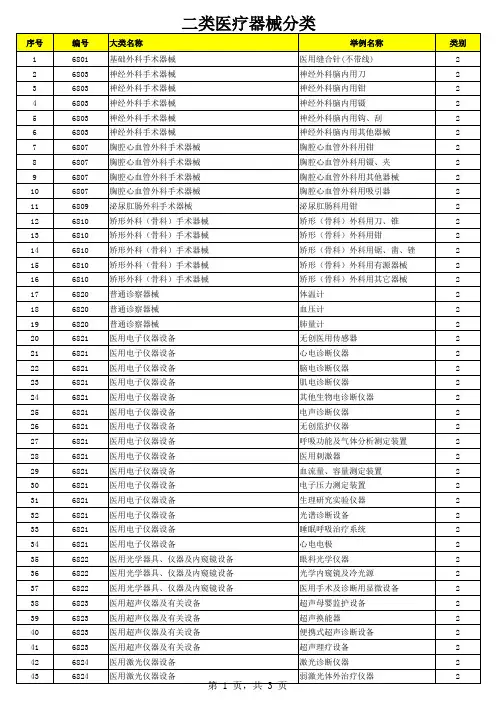
一、《医疗器械分类目录》核定的第一类医疗器械产品
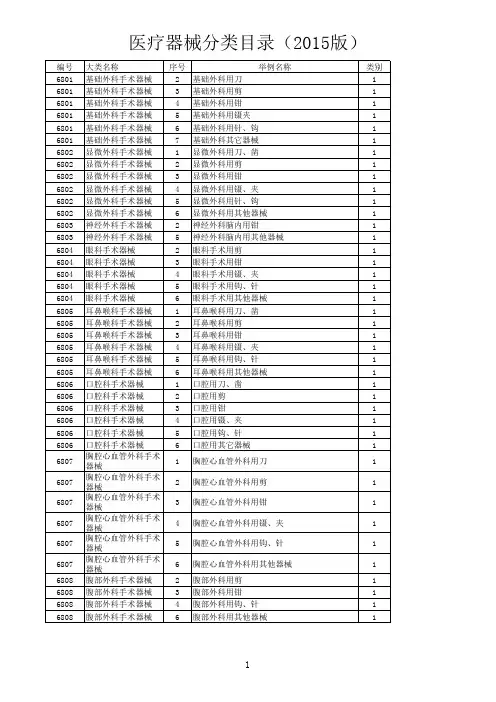
6801 基础外科手术器械
6802 显微外科手术器械
6803 神经外科手术器械
6804 眼科手术器械
6805 耳鼻喉科手术器械
6806 口腔科手术器械
6807 胸腔心血管外科手术器械
6808 腹部外科手术器械
6809 泌尿肛肠外科手术器械
6810 矫形外科(骨科)手术器械
6812 妇产科用手术器械
6813 计划生育手术器械
6816 烧伤(整形)科手术器械
6820 普通诊察器械
6821 医用电子仪器设备
6822 医用光学器具、仪器及内窥镜设备
6823 医用超声仪器及有关设备
6824 医用激光仪器设备
6826 物理治疗及康复设备
6827 中医器械个人收集整理勿做商业用途
6831 医用X射线附属设备及部件个人收集整理勿做商业用途
6834 医用射线防护用品、装置个人收集整理勿做商业用途
6840 临床检验分析仪器个人收集整理勿做商业用途
6841 医用化验和基础设备器具个人收集整理勿做商业用途
6854 手术室、急救室、诊疗室设备及器具个人收集整理勿做商业用途
6855 口腔科设备及器具个人收集整理勿做商业用途
6856 病房护理设备及器具个人收集整理勿做商业用途
6857 消毒和灭菌设备及器具个人收集整理勿做商业用途
6858 医用冷疗、低温、冷藏设备及器具个人收集整理勿做商业用途
6863 口腔科材料个人收集整理勿做商业用途
6864 医用卫生材料及敷料个人收集整理勿做商业用途
6866 医用高分子材料及制品个人收集整理勿做商业用途。
医疗器械分类目录第一类医疗器械第一类医疗器械是指适用于临床诊疗、治疗、监测和预防疾病的各类医疗器械,以及用于人体的有源和无源血修复、替代、补偿、辅助功能的医疗器械。
本文将对第一类医疗器械进行详细的分类介绍。
1.外科医疗器械:用于进行外科手术、实施切除、缝合或修复人体组织的器械,包括手术刀、剪刀、镊子、缝合针、温度探针等。
2.内科医疗器械:用于内科疾病的治疗和诊断的器械,包括心脏瓣膜、支架、造影剂、心脏起搏器、心脏除颤器、血液透析机等。
3.器官移植医疗器械:用于器官移植手术的器械,包括皮肤移植器、骨髓间充质干细胞移植器、器官保存液等。
4.呼吸和肺功能医疗器械:用于呼吸系统的诊断、治疗和监控的器械,包括氧气治疗仪、呼吸机、氧气浓缩器、肺功能检测仪等。
5.心血管医疗器械:用于心血管系统疾病的治疗和诊断的器械,包括心脏起搏器、心脏除颤器、心脏监测仪、心脏导管等。
6.消化道医疗器械:用于消化道疾病的治疗和诊断的器械,包括内窥镜、胃肠吻合器、胃肠激光刀、胃肠导管等。
7.泌尿和生殖系统医疗器械:用于泌尿系统和生殖系统疾病的治疗和诊断的器械,包括人工肾脏、输尿管导管、尿液分析仪等。
8.妇产科医疗器械:用于妇产科疾病的治疗和诊断的器械,包括超声波诊断仪、宫腔镜、剖宫钳等。
9.眼科医疗器械:用于眼科疾病的治疗和诊断的器械,包括眼科手术刀、眼科显微镜、角膜塑形片等。
10.耳鼻喉科医疗器械:用于耳鼻喉科疾病的治疗和诊断的器械,包括听力诊断仪、鼻窦镜、喉镜等。
11.口腔科医疗器械:用于口腔疾病的治疗和诊断的器械,包括牙科手术刀、口腔摄影机、牙科种植器等。
12.皮肤科医疗器械:用于皮肤疾病的治疗和诊断的器械,包括皮肤激光刀、皮肤挂针、皮肤显微镜等。
13.神经和精神科医疗器械:用于神经系统和精神系统疾病的治疗和诊断的器械,包括脑电图仪、颅脑手术器械、神经刺激器等。
14.康复和护理医疗器械:用于康复和护理的器械,包括康复治疗器、热敷器、电动轮椅、护理床等。
医疗器械分类目录第一类医疗器械医疗器械在现代医学发展中扮演着重要的角色,它们能够检测、治疗和辅助医疗工作。
为了规范医疗器械的管理和使用,各国都制定了相关的法律法规和分类标准。
在中国,医疗器械分类目录是根据医疗器械的功能和特性将其划分为不同的类别,以便于管理和监管。
本文将重点介绍医疗器械分类目录中的第一类医疗器械。
第一类医疗器械主要是指那些用于诊断、治疗、缓解疾病或者症状,但不需要经过定期检测,也没有特殊使用要求的医疗器械。
这些器械通常使用简便,安全性高,风险较低,适用于民众自用或者在非专业医疗机构中使用。
下面将分别介绍几种常见的第一类医疗器械。
一、体温计体温计是测量人体体温的仪器。
按照不同的工作原理,体温计可分为口腔体温计、耳温计、红外线额温枪等。
它们广泛应用于家庭和医疗机构,用于监测体温的变化,帮助判断患者的健康状况。
二、血压计血压计是测量人体血压的仪器。
血压计可以分为汞柱式血压计、数字式血压计等。
通过测量血压值,可以判断人体血液循环状况,帮助医生诊断和治疗心脑血管疾病。
三、拔罐器拔罐器是一种传统的中医疗法工具,用于治疗疏通经络、消除疼痛。
拔罐器一般由玻璃或者塑料制成,通过产生负压效应,将皮肤吸入罐内,刺激经络,以达到调理人体健康的目的。
四、听诊器听诊器是医生在诊断患者心肺疾病时使用的仪器。
通过听取心脏和肺部的声音,医生可以判断有无异常。
听诊器通常由听诊器头、听诊膜和听诊杆组成,形状小巧,方便携带。
五、口腔护理器具口腔护理器具包括牙刷、牙膏、牙线等。
它们用于清洁口腔、预防龋齿、滋养牙龈,是日常口腔保健的必备品。
在日常生活中,定期使用口腔护理器具能够有效预防口腔疾病的发生。
医疗器械分类目录中的第一类医疗器械涵盖了众多常见和常用的医疗器械。
它们在日常生活和医疗实践中起到了重要的作用,为人们提供了诊断、治疗和保健的便利。
在购买和使用这些器械时,我们应该遵循相关的使用说明,正确使用和维护医疗器械,以保证其有效性和安全性。