原子结构示意图大全38700教学内容
- 格式:doc
- 大小:35.50 KB
- 文档页数:2

原子结构示意图课件一、教学内容本节课主要依据教材第2章“原子结构与元素周期律”展开,详细内容为原子结构的基本组成,包括原子核、电子层、电子云等概念,重点讲解原子结构示意图的绘制方法和步骤。
二、教学目标1. 理解原子结构的基本概念,掌握原子核、电子层、电子云之间的关系。
2. 学会绘制原子结构示意图,并能正确表示原子内各部分的相对位置。
3. 能够运用原子结构示意图解释元素周期律的部分现象。
三、教学难点与重点教学难点:原子结构示意图的绘制方法,原子核与电子层之间的相互作用。
教学重点:原子结构基本概念的理解,原子结构示意图的绘制技巧。
四、教具与学具准备1. 教具:PPT课件、原子结构模型、黑板、粉笔。
五、教学过程1. 实践情景引入(5分钟)通过展示原子结构模型,引导学生思考原子的组成和结构,激发学习兴趣。
2. 理论讲解(15分钟)讲解原子结构的基本概念,包括原子核、电子层、电子云等,阐述它们之间的关系。
3. 例题讲解(10分钟)以钠原子为例,演示如何绘制原子结构示意图,讲解绘制方法和步骤。
4. 随堂练习(10分钟)学生根据所学内容,自主绘制氧原子的结构示意图,教师巡回指导。
六、板书设计1. 原子结构基本概念2. 原子结构示意图绘制方法3. 例题:钠原子结构示意图4. 课堂练习:氧原子结构示意图七、作业设计2. 答案:见附录。
八、课后反思及拓展延伸1. 反思:本节课学生对原子结构示意图的绘制掌握情况较好,但部分学生对原子核与电子层之间的相互作用理解不够深入。
2. 拓展延伸:引导学生查阅资料,了解原子结构与元素性质之间的关系,为学习元素周期律打下基础。
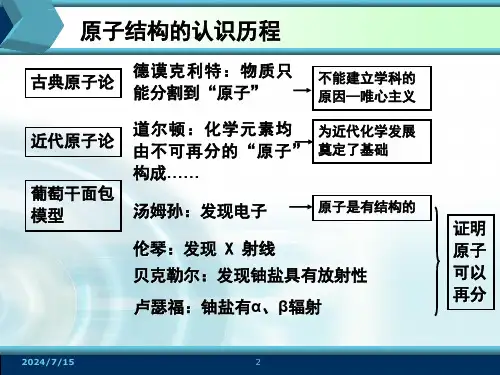
附录:碳(C)原子结构示意图:氮(N)原子结构示意图:铝(Al)原子结构示意图:重点和难点解析1. 原子结构示意图的绘制方法2. 原子核与电子层之间的相互作用3. 实践情景引入的设计4. 作业设计的具体题目和答案一、原子结构示意图的绘制方法1. 原子核位于图中心,用一个小圆圈表示,圆圈内写上原子序数(即质子数)。




+19 2 8 8 1 钾K +20 2 8 8 2 钙Ca +21 2 8 9 2 钪Sc+22 2 8 10 2 钛Ti +23 2 8 11 2 钒V +24 2 8 13 1 铬Cr+25 2 8 13 2 锰Mn +26 2 8 14 2 铁Fe +27 2 8 15 2 钴Co+28 2 8 16 2 镍Ni +29 2 8 18 1 铜Cu +30 2 8 18 2 锌Zn+31 2 8 18 3 镓Ga +32 2 8 18 4 锗Ge +33 2 8 18 5 砷As+34 2 8 18 6 硒Se +35 2 8 18 7 溴Br +36 2 8 18 8 氪Kr+37 2 8 18 8 1 铷Rb +38 2 8 18 8 2 锶Sr +39 2 8 18 9 2 钇Y+40 2 8 18 10 2 锆Zr +41 2 8 18 12 1 铌Nb +42 2 8 18 13 1 钼Mo +43 2 8 18 13 2 锝Tc +44 2 8 18 15 1 钌Ru +45 2 8 18 16 1 铑Rh +46 2 8 18 18 钯Pd +47 2 8 18 18 1 银Ag +48 2 8 18 18 2 镉Cd +49 2 8 18 18 3 铟In +50 2 8 18 18 4 锡Sn +51 2 8 18 18 5 锑Sb +52 2 8 18 18 6 碲Te +53 2 8 18 18 7 碘I +54 2 8 18 18 8 氙Xe +55 2 8 18 18 8 1 铯Cs +56 2 8 18 18 8 2 钡Ba +57 2 8 18 18 9 2 镧La +58 2 8 18 19 9 2 铈Ce +59 2 8 18 21 8 2 镨Pr +60 2 8 18 22 8 2 钕Nd +61 2 8 18 23 8 2 钷Pm +62 2 8 18 24 8 2 钐Sm +63 2 8 18 25 8 2 铕Eu +64 2 8 18 25 9 2 钆Gd +65 2 8 18 27 8 2 铽Td +66 2 8 18 28 8 2 镝Dy +67 2 8 18 29 8 2 钬Ho +68 2 8 18 30 8 2 铒Er +69 2 8 18 31 8 2 铥Tm +70 2 8 18 32 8 2 镱Yb +71 2 8 18 32 9 2 镥Lu +72 2 8 18 32 10 2 铪Hf+73 2 8 18 32 11 2 钽Ta +74 2 8 18 32 12 2 钨W +75 2 8 18 32 13 2 铼Re +76 2 8 18 32 14 2 锇Os +77 2 8 18 32 15 2 铱Ir +78 2 8 18 32 17 1 铂Pt +79 2 8 18 32 18 1 金Au +80 2 8 18 32 18 2 汞Hg +81 2 8 18 32 18 3 铊Tl +82 2 8 18 32 18 4 铅Pb +83 2 8 18 32 18 5 铋Bi +84 2 8 18 32 18 6 钋Po +85 2 8 18 32 18 7 砹At +86 2 8 18 32 18 8 氡Rn +87 2 8 18 32 18 8 1 钫Fr +88 2 8 18 32 18 8 2 镭Ra +89 2 8 18 32 18 9 2 锕Ac +90 2 8 18 32 18 10 2 钍Th +91 2 8 18 32 20 9 2 镤Pa +92 2 8 18 32 21 9 2 铀U +93 2 8 18 32 22 9 2 镎Np +94 2 8 18 32 24 8 2 钚Pu +95 2 8 18 32 25 8 2 镅Am +96 2 8 18 32 25 9 2 锔Cm +97 2 8 18 32 27 8 2 锫Bk +98 2 8 18 32 28 8 2 锎Cf +99 2 8 18 32 29 8 2 锿Es +100 2 8 18 32 30 8 2 镄Fm +101 2 8 18 32 31 8 2 钔Md(推断结构,现在科学还未确定,下同)+102 2 8 18 32 32 8 2 锘No +103 2 8 18 32 32 9 2 铹Lr +104 2 8 18 32 32 10 2 鈩Rf +105 2 8 18 32 32 11 2 钅杜Db初中常见的离子团NH4 铵根+1价SO3 亚硫酸根-2价SO4 硫酸根-2价CO3 碳酸根-2价Cl 盐酸根-1价OH 氢氧根-1价NO3 硝酸根-1价NO2 亚硝酸根-1价CIO3 氯酸根-1价ClO 次氯酸根-1价,ClO4 高氯酸根-1价,H2PO4 磷酸二氢根-1价HPO42 磷酸氢根-1价MnO4 高锰酸根-1价MnO4 锰酸根-2价SiO3 硅酸根-2价HCO3 碳酸氢根-1价HSO4 硫酸氢根-1价PO4 磷酸根-3价。




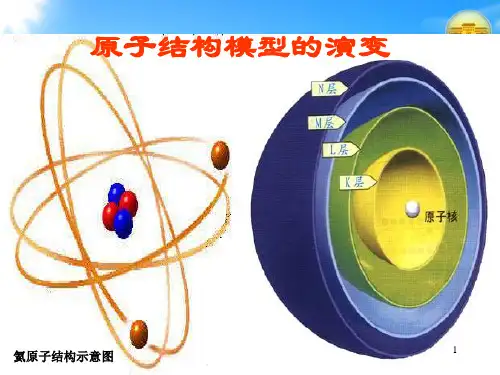
原子结构示意图第一页:原子结构的基本组成原子是由原子核和核外电子组成的。
原子核位于原子的中心,由质子和中子组成。
质子带正电荷,中子不带电荷。
核外电子围绕原子核运动,带有负电荷。
第二页:原子结构的电子排布原子中的电子按照一定的规律排布在各个能级上。
能级是电子在原子中运动的能量状态。
电子填充离原子核最近的能级,然后依次填充更远的能级。
每个能级上最多可以容纳的电子数是固定的。
第三页:原子结构的同位素同位素是指具有相同质子数但中子数不同的原子。
同位素在化学性质上基本相同,但在物理性质上可能有所不同。
例如,氢原子有三种同位素:氕、氘和氚。
第四页:原子结构的化学键原子之间的相互作用可以通过化学键来描述。
化学键是原子之间通过共享或转移电子而形成的连接。
常见的化学键有共价键、离子键和金属键等。
所有原子结构示意图第一页:原子结构的基本组成原子是构成物质的基本单位,由原子核和核外电子组成。
原子核位于原子的中心,由带正电荷的质子和不带电荷的中子组成。
质子和中子共同决定了原子的质量和稳定性。
核外电子带有负电荷,围绕原子核运动,形成电子云。
第二页:原子结构的电子排布原子中的电子按照能级分布,每个能级上最多容纳的电子数是固定的。
电子填充离原子核最近的能级,然后依次填充更远的能级。
不同原子的电子排布不同,决定了它们的化学性质和反应活性。
第三页:原子结构的同位素同位素是指具有相同质子数但中子数不同的原子。
同位素在化学性质上基本相同,但在物理性质上可能有所不同。
例如,氢原子有三种同位素:氕、氘和氚。
同位素的存在对原子的稳定性和核反应具有重要意义。
第四页:原子结构的化学键原子之间的相互作用可以通过化学键来描述。
化学键是原子之间通过共享或转移电子而形成的连接。
常见的化学键有共价键、离子键和金属键等。
化学键的形成和断裂是化学反应的基础,决定了物质的性质和反应特性。
所有原子结构示意图第一页:原子核的组成原子核是原子的中心部分,它由质子和中子组成。
+19 2 8 8 1 钾K +20 2 8 8 2 钙Ca +21 2 8 9 2 钪Sc +22 2 8 10 2 钛Ti +23 2 8 11 2 钒V +24 2 8 13 1 铬Cr +25 2 8 13 2 锰Mn +26 2 8 14 2 铁Fe +27 2 8 15 2 钴Co +28 2 8 16 2 镍Ni +29 2 8 18 1 铜Cu +30 2 8 18 2 锌Zn +31 2 8 18 3 镓Ga +32 2 8 18 4 锗Ge +33 2 8 18 5 砷As +34 2 8 18 6 硒Se +35 2 8 18 7 溴Br +36 2 8 18 8 氪Kr +37 2 8 18 8 1 铷Rb +38 2 8 18 8 2 锶Sr +39 2 8 18 9 2 钇Y +40 2 8 18 10 2 锆Zr +41 2 8 18 12 1 铌Nb +42 2 8 18 13 1 钼Mo +43 2 8 18 13 2 锝Tc +44 2 8 18 15 1 钌Ru +45 2 8 18 16 1 铑Rh +46 2 8 18 18 钯Pd +47 2 8 18 18 1 银Ag +48 2 8 18 18 2 镉Cd +49 2 8 18 18 3 铟In +50 2 8 18 18 4 锡Sn +51 2 8 18 18 5 锑Sb +52 2 8 18 18 6 碲Te +53 2 8 18 18 7 碘I +54 2 8 18 18 8 氙Xe +55 2 8 18 18 8 1 铯Cs +56 2 8 18 18 8 2 钡Ba +57 2 8 18 18 9 2 镧La +58 2 8 18 19 9 2 铈Ce +59 2 8 18 21 8 2 镨Pr +60 2 8 18 22 8 2 钕Nd +61 2 8 18 23 8 2 钷Pm +62 2 8 18 24 8 2 钐Sm +63 2 8 18 25 8 2 铕Eu +64 2 8 18 25 9 2 钆Gd +65 2 8 18 27 8 2 铽Td +66 2 8 18 28 8 2 镝Dy +67 2 8 18 29 8 2 钬Ho +68 2 8 18 30 8 2 铒Er +69 2 8 18 31 8 2 铥Tm +70 2 8 18 32 8 2 镱Yb +71 2 8 18 32 9 2 镥Lu +72 2 8 18 32 10 2 铪Hf
+73 2 8 18 32 11 2 钽Ta +74 2 8 18 32 12 2 钨W +75 2 8 18 32 13 2 铼Re +76 2 8 18 32 14 2 锇Os +77 2 8 18 32 15 2 铱Ir +78 2 8 18 32 17 1 铂Pt +79 2 8 18 32 18 1 金Au +80 2 8 18 32 18 2 汞Hg +81 2 8 18 32 18 3 铊Tl +82 2 8 18 32 18 4 铅Pb +83 2 8 18 32 18 5 铋Bi +84 2 8 18 32 18 6 钋Po +85 2 8 18 32 18 7 砹At +86 2 8 18 32 18 8 氡Rn +87 2 8 18 32 18 8 1 钫Fr +88 2 8 18 32 18 8 2 镭Ra +89 2 8 18 32 18 9 2 锕Ac +90 2 8 18 32 18 10 2 钍Th +91 2 8 18 32 20 9 2 镤Pa +92 2 8 18 32 21 9 2 铀U +93 2 8 18 32 22 9 2 镎Np +94 2 8 18 32 24 8 2 钚Pu +95 2 8 18 32 25 8 2 镅Am +96 2 8 18 32 25 9 2 锔Cm +97 2 8 18 32 27 8 2 锫Bk +98 2 8 18 32 28 8 2 锎Cf +99 2 8 18 32 29 8 2 锿Es +100 2 8 18 32 30 8 2 镄Fm +101 2 8 18 32 31 8 2 钔Md(推断结构,现在科学还未确定,下同)+102 2 8 18 32 32 8 2 锘No +103 2 8 18 32 32 9 2 铹Lr +104 2 8 18 32 32 10 2 鈩Rf +105 2 8 18 32 32 11 2 钅杜Db
初中常见的离子团
NH4 铵根+1价SO3 亚硫酸根-2价SO4 硫酸根-2价CO3 碳酸根-2价Cl 盐酸根-1价OH 氢氧根-1价NO3 硝酸根-1价NO2 亚硝酸根-1价CIO3 氯酸根-1价ClO 次氯酸根-1价,ClO4 高氯酸根-1价,H2PO4 磷酸二氢根-1价HPO42 磷酸氢根-1价MnO4 高锰酸根-1价MnO4 锰酸根-2价SiO3 硅酸根-2 HCO3 碳酸氢根-1价HSO4 硫酸氢根-1价PO4 磷酸根-3价
核外电子分层排布规律
1.从内向外依次填充,填满第一层再填第二层、第三层…
2.每层所排的电子个数最多为2n (n为电子层数)
3.最外层电子数电子不超过8。