端粒酶学说
- 格式:doc
- 大小:39.50 KB
- 文档页数:9

端粒学说线性染色体"末端复制问题"早在20世纪三十年代,科学家Barbara McClintock 和Hermann Muller就发现,区别于一般的DNA断裂,染色体末端不会发生相互融合;此外,只有包含有末端的染色体片段才能被完整复制。
因此,科学家们推测,真核生物线性染色体的末端是一种特化的结构,Muller将之命名为端粒(Telomere,在古希腊语中,telos 表示末端,而meros表示片段)。
然而在当时,人们还不知道端粒与随机产生的DNA断裂末端有什么差异。
20世纪五六十年代,当科学家们尝试解析真核生物如何实现染色体DNA的精确复制时,又一个端粒相关的难题产生了。
DNA聚合酶进行每一轮线性DNA的复制都会导致少量末端核苷酸的丢失,其结果是,真核生物线性染色体,作为基因的载体,会在细胞分裂过程中逐渐缩短。
1972年,James Watson提出了"末端复制问题",他同时推测,真核生物需要一种特殊机制来确保线性染色体末端的完整复制。
同时,Alexey Olovnikov也推测,染色体末端的逐渐缩短将导致细胞的衰老。
端粒能够稳定线性染色体七十年代后期,Blackburn在耶鲁大学Joseph Gall实验室进行博士后研究,她希望能确定真核生物染色体末端的DNA序列。
她选择了四膜虫(Tetrahymena thermophila)作为模式动物,因为相较于其他真核生物,它包含有大量的微小染色体(minichromosome),这也就意味着她能够获得大量的染色体的末端片段。
最终,她测定到四膜虫的染色体末端是(CCCCAA)的六核苷酸重复序列。
紧接着,她发现类似的序列在其它线虫中也同样存在。
但当时她们还不知道这种古怪的序列特征在其它真核生物中是否也同样存在。
1980年,Blackburn在加州大学成立了自己的实验室。
在一次研究会议上,她与酵母遗传学家Jack Szostak进行了交流,他们决定在酿酒酵母中检测四膜虫端粒的功能。

端粒学说名词解释
端粒学说是指生物学中的一种理论,认为人类细胞的寿命和衰老与端粒的长度和功能有关。
下面是相关名词的解释:
1.端粒(Telomere):位于染色体两端的一段DNA序列重复
区域,主要由TTAGGG序列组成。
端粒在细胞分裂过程中不断缩短,起到保护染色体稳定性和完整性的作用。
2.端粒酶(Telomerase):由酶蛋白和RNA分子组成的酶复
合物,具有在端粒区域添加DNA序列的功能。
正常情况下,大多数成体细胞中的端粒酶活性很低,无法有效地维持端粒长度。
3.端粒缩短(Telomere Shortening):细胞分裂过程中,每次
DNA复制时端粒会缩短一段。
随着细胞的继续分裂,端粒长度逐渐减少,当端粒变得过短时,细胞进入衰老状态或进入细胞凋亡(死亡)。
4.端粒损伤响应(Telomere Damage Response):当端粒长度
达到一定程度时,细胞会触发端粒损伤响应,导致细胞周期停滞和细胞功能下降,从而影响细胞的正常生理功能。
5.端粒理论(Telomere Theory):根据端粒理论,细胞的衰
老与端粒长度缩短及功能损失有关。
根据该理论,当端粒长度变得过短时,细胞的增殖能力受到限制,造成组织和器官功能下降,最终导致衰老和相关疾病。
该理论提供了衰老过程中基因和细胞水平的解释,并成为研究衰老和抗
衰老策略的重要基础。


端粒和端粒酶的研究及应用及如何实现反老还童端粒和端粒酶的研究及应用及如何实现反老还童生命科学焦点如何实现反老还童摘要:古往今来,“长生不老”成为人们一直追求的梦想,曾经有多少人用各种方法来延缓衰老,但终未取得显著效果。
近年来研究证实,端粒缩短导致衰老。
本文就端粒、端粒酶与衰老的关系做一综述。
关键词:端粒、端粒酶、衰老最早观察染色体末端的科学家始于19世纪末期,Rabl[1]在1885年注意到染色体上所有的末端都处于细胞核的一侧。
20世纪30年代,两个著名的遗传学家McClintock B [2]和Muller HJ [3]发现了染色体的末端可维持染色体的稳定性和完整性。
Muller将它定义为“telomere”,这是由希腊词根“末端”(telos)及“部分”(meros)组成的。
30多年前,Hayflick[4]首次提出将体外培养的正常人成纤维细胞的“有限复制力”作为细胞衰老的表征。
在此过程中,细胞群中的大部分细胞经历了一定次数的分裂后便停止了,但它们并没有死亡,仍保持着代谢活性,只是在基因表达方式上有一定的改变。
于是Hayflick猜测细胞内有一个限制细胞分裂次数的“钟”,后来通过细胞核移植实验发现,这种“钟”在细胞核的染色体末端——端粒。
但端粒究竟是怎样的复杂结构呢?Blackburn和Gall[5] 于1978年首次阐明了四膜虫rDNA分子的末端结构,他们发现这种rDNA每条链的末端均含有大量的重复片段,并且这些大量重复的片段多是由富含G、C的脱氧核苷酸形成的简单序列串联而成。
在1985年,CW·Greider和EH·Blackburn发现将一段单链的末端寡聚核苷酸加至四膜虫的提取物中后,端粒的长度延长了,这就说明了确实有这样的一种酶存在[6],并将它命名为“端粒酶”(telomerase)。
之后,耶鲁大学Morin于1989年在人宫颈癌细胞中也发现了人端粒酶[7] 。
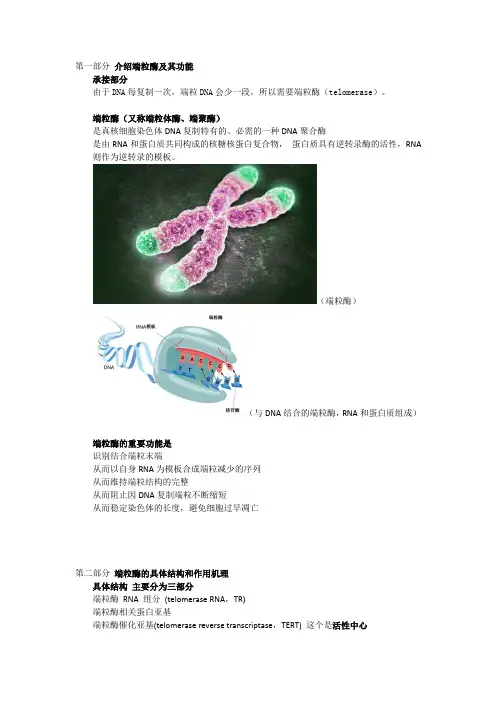
第一部分介绍端粒酶及其功能承接部分由于DNA每复制一次,端粒DNA会少一段,所以需要端粒酶(telomerase)。
端粒酶(又称端粒体酶、端聚酶)是真核细胞染色体DNA复制特有的、必需的一种DNA聚合酶是由RNA和蛋白质共同构成的核糖核蛋白复合物,蛋白质具有逆转录酶的活性,RNA 则作为逆转录的模板。
(端粒酶)(与DNA结合的端粒酶,RNA和蛋白质组成)端粒酶的重要功能是识别结合端粒末端从而以自身RNA为模板合成端粒减少的序列从而维持端粒结构的完整从而阻止因DNA复制端粒不断缩短从而稳定染色体的长度,避免细胞过早凋亡第二部分端粒酶的具体结构和作用机理具体结构主要分为三部分端粒酶RNA 组分(telomerase RNA,TR)端粒酶相关蛋白亚基端粒酶催化亚基(telomerase reverse transcriptase,TERT)这个是活性中心(图中有TERT及许多其他的亚基)RNA部分分为模板区与非模板区模板区决定合成端粒的特异性模板区的一部分序列突出在外,处于单链状态,便于与端粒区的重复序列结合,并有效地充当逆转录的模板。
非模板区具有酶与底物的结合位点,与端粒DNA最后一段重复序列配对蛋白质亚基区原本认为有7个蛋白亚基,其中包括活性中心所在的TERT10月《science》上科学家最新研究表明又发现了2种新Teb蛋白其中蛋白p80 及其同源物,人类中称为TP1,位于氨基末端,与TR特异性结合而其他一些蛋白有的起到折叠作用,有的起到辅助TERT催化的作用活性中心TERT在各种生物中高度保守,起到催化作用,人类的TERT是含有1132个氨基酸的蛋白质所有这些端粒酶催化亚基都具有逆转录酶的共同结构7 个蛋白质域以及端粒酶催化亚基独特的保守区域,T 模体TERT 的三维结构由三部分组成:RNA结合区(TRBD)、逆转录区(the reverse transcriptase domain)和羧基末端延伸区(carboxy-terminal extension,CTE)。

一、端粒和端粒酶二、端粒端粒是真核生物染色体末端由许多简单重复序列和相关蛋白组成的复合结构,具有维持染色体结构完整性和解决其末端复制难题的作用。
端粒酶是一种逆转录酶,由RNA和蛋白质组成,是以自身RNA为模板,合成端粒重复序列,加到新合成DNA链末端。
在人体内端粒酶出现在大多数的胚胎组织、生殖细胞、炎性细胞、更新组织的增生细胞以及肿瘤细胞中。
正因如此,细胞每有丝分裂一次,就有一段端粒序列丢失,当端粒长度缩短到一定程度,会使细胞停止分裂,导致衰老与死亡。
但是许多问题用端粒学说还不能解释。
体细胞端粒长度与有丝分裂能力呈正比,这一点实验已经证实了,而不同的体细胞其有丝分裂能力是不尽相同的,胃肠黏膜细胞的分裂增殖速度就比较快,神经细胞分裂的速度就比较慢。
曾有人就不同年龄供体角膜内皮细胞的端粒长度进行研究发现角膜内皮细胞内端粒长度长期维持在一个较高的水平,而端粒酶却不表达。
另外,Kippling发现,鼠的端粒比人类长近5-10倍,寿命却比人类短的多。
这些都提示体细胞端粒长度与个体的寿命及不同组织器官的预期寿命并非一致。
生殖细胞的端粒酶活性长期维持较高的水平却不会象肿瘤那样无限制分裂繁殖;端粒长度由端粒酶控制,那何种因素控制端粒酶呢?生殖细胞内端粒酶活性较高,为什么体细胞中没有较高的端粒酶活性。
看来端粒的长度缩短是衰老的原因还是结果尚需进一步研究。
2009年,诺贝尔瑞典卡罗林斯卡医学院将诺贝尔奖生理学或医学奖授予美国加利福尼亚旧金山大学的伊丽莎白·布莱克本(ElizabethBlackburn)、美国巴尔的摩约翰·霍普金斯医学院的卡罗尔-格雷德(CarolGreider)、美国哈佛医学院的杰克·绍斯塔克(JackSzostak)以及霍华德休斯医学研究所,以表彰他们发现了端粒和端粒酶保护染色体的机理。
端粒酶英文名称:telomerase一种反转录酶,由蛋白质和RNA两部分组成核糖蛋白复合体,其中RNA是一段模板序列,指导合成端粒DNA的重复序列片段。


端粒酶端粒酶的结构目前存在有众多的衰老学说,其中盛行了一种学说,那就是端粒学说。
①端粒是真核生物染色体线性DNA分子末端的结构。
形态学上,染色体DNA末端膨大成粒状,这是因为DNA和它的结合蛋白紧密结合,像两顶帽子那样盖在染色体两端,因而得名。
研究发现,培养的人成纤维细胞随着培养传代次数增加,端粒长度是逐渐缩短的。
而端粒的长度和端粒酶的活性直接相关。
端粒酶(telomerase)是一种能延长端粒末端的核糖蛋白酶,主要成分是RNA和蛋白质,其中还有特异性引物识别位点,可以以自身RNA为模版,合成端粒重复序列并加到染色体末端,以补偿因“末端复制问题”而导致的端粒片段丢失,从而延长细胞寿命甚至使其永生化。
②由于端粒酶可被热、蛋白酶K和RNA酶破坏,因此认为它是由蛋白质和RNA两部分组成的。
人端粒酶RNA组分基因命名为hTR,定位于3号染色体,约有450个碱基的转录本,其中包括11个碱基的模版互补序列,即5·-CUAACCCUAAC,这个模版互补序列刚好每次与1.5个(TTAGGG)互补而特意的合成人染色体DNA的端粒。
通过电穿孔法将hTR反义核酸表达质粒转染Hela细胞并在Hela细胞中表达,结果发现端粒长度明显缩短,Hela细胞分裂增殖受到抑制。
从23~26代开始死亡,说明hTR对于维持端粒酶结构的完整性十分重要。
人端粒酶蛋白成分包括两者:人端粒重复结合因子(hTRF)和人端粒酶逆转录酶(hTERT)。
hTRF又称端粒酶相关蛋白1(TPI),是端粒酶调节亚单位,相对分子质量为300×103,能够与双链端粒性的肿瘤细胞株HT1080的端粒渐进性缩短;相反,hTRF1功能区诱导突变将会引起端粒加长。
因此,hTRF1是端粒生长抑制因子,起负反馈调节作用。
hTERT又称端粒酶相关蛋白2(TP2),是端粒酶结构蛋白,蛋白序列含有48个氨基酸,分子质量为130kD,其编码基因为单拷贝,定位于5p15.33,长度约为40kb。

端粒酶端粒酶-简介细胞中有种酵素负责端粒的延长,其名为端粒酶。
端粒酶的存在,算是把 DNA 克隆机制的缺陷填补起来,藉由把端粒修复延长,可以让端粒不会因细胞分裂而有所损耗,使得细胞分裂克隆的次数增加。
端粒酶让人类看到长生不老的曙光。
定义端粒酶(Telomerase),在细胞中负责端粒的延长的一种酶,是基本的核蛋白逆转录酶,可将端粒DNA加至真核细胞染色体末端。
端粒在不同物种细胞中对于保持染色体稳定性和细胞活性有重要作用,端粒酶能延长缩短的端粒(缩端粒酶端粒酶短的端粒其细胞复制能力受限),从而增强体外细胞的增殖能力。
端粒酶在正常人体组织中的活性被抑制,在肿瘤中被重新激活,端粒酶可能参与恶性转化。
端粒酶在保持端粒稳定、基因组完整、细胞长期的活性和潜在的继续增殖能力等方面有重要作用。
端粒酶的存在,就是把 DNA 克隆机制的缺陷填补起来,即由把端粒修复延长,可以让端粒不会因细胞分裂而有所损耗,使得细胞分裂克隆的次数增加。
但是,在正常人体细胞中,端粒酶的活性受到相当严密的调控,只有在造血细胞、干细胞和生殖细胞,这些必须不断分裂克隆的细胞之中,才可以侦测到具有活性的端粒酶。
当细胞分化成熟后,必须负责身体中各种不同组织的需求,各司其职,于是,端粒酶的活性就会渐渐的消失。
对细胞来说,本身是否能持续分裂克隆下去并不重要,而是分化成熟的细胞将背负更重大的使命,就是让组织器官运作,使生命延续。
应用端粒酶使细胞“长生不老”美国德克萨斯大学西南医学中心的细胞生物学及神经系统科学教授杰里.谢伊和伍德林.赖特做了这样一项试验:在采集的包皮细胞(包皮环切术的附带产物)端粒酶端粒酶中导入某种基因,该基因可使细胞产生一种酶——端粒酶(telomerase)。
一般来说,包皮细胞在变老之前可分裂60次左右。
但在上述试验中,细胞已分裂了300多次却毫无终止的征兆,也没有显示任何异常的迹象。
“细胞在端粒酶的作用下,就像被注入了兴奋剂的小兔子,”谢伊说,“它们只管没完没了地分裂繁殖。

端粒酶名词解释细胞生物学端粒酶是一种在细胞生物学中起着重要作用的酶。
它主要参与细胞的端粒修复和维护,对于细胞的生命周期和寿命起着关键的调控作用。
在本文中,我们将对端粒酶的定义、结构、功能以及其在细胞老化和癌症等疾病中的作用进行详细解释。
首先,让我们来了解一下什么是端粒。
端粒是染色体末端的一段DNA序列,它们的主要功能是保护染色体免受损伤和降解。
然而,每次细胞分裂时,端粒都会逐渐缩短,导致染色体稳定性下降。
为了防止端粒缩短过度,细胞需要一种特殊的酶来补充和修复端粒,这就是端粒酶。
端粒酶是一种具有逆转录酶活性的酶,它能够在DNA末端合成新的端粒序列。
具体来说,端粒酶通过使用RNA模板将DNA序列添加到染色体末端,从而延长和修复端粒。
这种逆转录过程使得端粒酶能够保护染色体的完整性,并延长细胞的寿命。
端粒酶由两个主要组分组成:一个叫做端粒RNA(TERC)的RNA分子和一个叫做端粒酶蛋白(TERT)的蛋白质。
TERC是一个非编码RNA分子,它提供了RNA模板,用于合成新的端粒序列。
TERT则是一个蛋白质酶,它负责将RNA模板转录成DNA序列,并将其添加到染色体末端。
除了维护染色体稳定性外,端粒酶还对细胞的生命周期和老化起着重要的调控作用。
在正常情况下,细胞分裂一定次数后会进入衰老期,并最终停止分裂。
这是由于每次细胞分裂时,端粒都会缩短一段长度,当端粒缩短到一定程度时,细胞就无法再分裂了。
然而,在一些特殊情况下,如干细胞和癌细胞中,端粒酶能够保持活跃状态,从而延长细胞的寿命和增加其分裂次数。
这种对细胞寿命的调控作用使得端粒酶成为一个重要的研究领域。
科学家们发现,在某些疾病中,如癌症和衰老相关疾病中,端粒酶的功能异常或失活可能会导致细胞功能紊乱和异常增殖。
因此,研究端粒酶的机制和调控方式对于理解这些疾病的发生和发展具有重要意义。
除了在正常细胞中的功能外,端粒酶还被广泛应用于医学领域。
例如,在干细胞治疗中,科学家们利用端粒酶技术来延长干细胞的寿命,并增加其分裂次数,从而提高治疗效果。

端粒学说线性染色体"末端复制问题"早在20世纪三十年代,科学家Barbara McClintock 和Hermann Muller就发现,区别于一般的DNA断裂,染色体末端不会发生相互融合;此外,只有包含有末端的染色体片段才能被完整复制。
因此,科学家们推测,真核生物线性染色体的末端是一种特化的结构,Muller将之命名为端粒(Telomere,在古希腊语中,telos 表示末端,而meros表示片段)。
然而在当时,人们还不知道端粒与随机产生的DNA断裂末端有什么差异。
20世纪五六十年代,当科学家们尝试解析真核生物如何实现染色体DNA的精确复制时,又一个端粒相关的难题产生了。
DNA聚合酶进行每一轮线性DNA的复制都会导致少量末端核苷酸的丢失,其结果是,真核生物线性染色体,作为基因的载体,会在细胞分裂过程中逐渐缩短。
1972年,James Watson提出了"末端复制问题",他同时推测,真核生物需要一种特殊机制来确保线性染色体末端的完整复制。
同时,Alexey Olovnikov也推测,染色体末端的逐渐缩短将导致细胞的衰老。
端粒能够稳定线性染色体七十年代后期,Blackburn在耶鲁大学Joseph Gall实验室进行博士后研究,她希望能确定真核生物染色体末端的DNA序列。
她选择了四膜虫(Tetrahymena thermophila)作为模式动物,因为相较于其他真核生物,它包含有大量的微小染色体(minichromosome),这也就意味着她能够获得大量的染色体的末端片段。
最终,她测定到四膜虫的染色体末端是(CCCCAA)的六核苷酸重复序列。
紧接着,她发现类似的序列在其它线虫中也同样存在。
但当时她们还不知道这种古怪的序列特征在其它真核生物中是否也同样存在。
1980年,Blackburn在加州大学成立了自己的实验室。
在一次研究会议上,她与酵母遗传学家Jack Szostak进行了交流,他们决定在酿酒酵母中检测四膜虫端粒的功能。
2017高中生物端粒学说知识点端颗学说是指在端粒DNA序列被“解”短后,端粒内侧的正常基因的DNA序列受到损伤,这也是高中生物重要的知识点。
下面是店铺为大家整理的高中生物端粒学说知识点,欢迎参考!高中生物端粒学说知识点一、端粒学说概述每条染色体的两端都有一段特殊序列的DNA,称为端粒。
端粒DNA序列在每次细胞分裂后会缩短一解。
随着细胞分裂次数的增加,解短的部分会逐渐向内延伸。
在端粒DNA序列被“解”短后,端粒内侧的正常基因的DNA序列就会受到损伤,结果使细胞活动渐趋异常。
二、学说的由来编辑端粒学说由Olovnikov提出,认为细胞在每次分裂过程中都会由于DNA聚合酶功能障碍而不能完全复制它们的染色体,因此最后复制DNA序列可能会丢失,最终造成细胞衰老死亡。
端粒是真核生物染色体末端由许多简单重复序列和相关蛋白组成的复合结构,具有维持染色体结构完整性和解决其末端复制难题的作用。
端粒酶是一种逆转录酶,由RNA和蛋白质组成,是以自身RNA 为模板,合成端粒重复序列,加到新合成DNA链末端。
在人体内端粒酶出现在大多数的胚胎组织、生殖细胞、炎性细胞、更新组织的增生细胞以及肿瘤细胞中。
正因如此,细胞每有丝分裂一次,就有一段端粒序列丢失,当端粒长度缩短到一定程度,会使细胞停止分裂,导致衰老与死亡。
三、与细胞衰老的联系大量实验说明端粒、端粒酶活性与细胞衰老及永生有着一定的联系。
第一个提供衰老细胞中端粒缩短的直接证据是来自对体外培养成纤维细胞的观察,通过对不同年龄供体成纤维细胞端粒长度与年龄及有丝分裂能力的关系观察到随着增龄,端粒的长度逐渐变短,有丝分裂的能力明显渐渐变弱;Hastie发现结肠端粒限制性片段的长度随供体年龄增加逐渐缩短,平均每年丢失33bp的重复序列;植物中不完整的染色体在受精作用中得以修复,而不能在已经分化的组织中修复,这在较为高等的真核生物中也证实了体细胞中端粒酶的活性受抑制;精子的端粒要比体细胞长,体细胞缺失端粒酶活性就会逐渐衰老,而生殖细胞系的端粒却可以维持其长度;转化细胞能够通过端粒酶的活性完全复制端粒以得永生。
端粒酶端粒酶-简介细胞中有种酵素负责端粒的延长,其名为端粒酶。
端粒酶的存在,算是把 DNA 克隆机制的缺陷填补起来,藉由把端粒修复延长,可以让端粒不会因细胞分裂而有所损耗,使得细胞分裂克隆的次数增加。
端粒酶让人类看到长生不老的曙光。
定义端粒酶(Telomerase),在细胞中负责端粒的延长的一种酶,是基本的核蛋白逆转录酶,可将端粒DNA加至真核细胞染色体末端。
端粒在不同物种细胞中对于保持染色体稳定性和细胞活性有重要作用,端粒酶能延长缩短的端粒(缩端粒酶端粒酶短的端粒其细胞复制能力受限),从而增强体外细胞的增殖能力。
端粒酶在正常人体组织中的活性被抑制,在肿瘤中被重新激活,端粒酶可能参与恶性转化。
端粒酶在保持端粒稳定、基因组完整、细胞长期的活性和潜在的继续增殖能力等方面有重要作用。
端粒酶的存在,就是把 DNA 克隆机制的缺陷填补起来,即由把端粒修复延长,可以让端粒不会因细胞分裂而有所损耗,使得细胞分裂克隆的次数增加。
但是,在正常人体细胞中,端粒酶的活性受到相当严密的调控,只有在造血细胞、干细胞和生殖细胞,这些必须不断分裂克隆的细胞之中,才可以侦测到具有活性的端粒酶。
当细胞分化成熟后,必须负责身体中各种不同组织的需求,各司其职,于是,端粒酶的活性就会渐渐的消失。
对细胞来说,本身是否能持续分裂克隆下去并不重要,而是分化成熟的细胞将背负更重大的使命,就是让组织器官运作,使生命延续。
应用端粒酶使细胞“长生不老”美国德克萨斯大学西南医学中心的细胞生物学及神经系统科学教授杰里.谢伊和伍德林.赖特做了这样一项试验:在采集的包皮细胞(包皮环切术的附带产物)端粒酶端粒酶中导入某种基因,该基因可使细胞产生一种酶——端粒酶(telomerase)。
一般来说,包皮细胞在变老之前可分裂60次左右。
但在上述试验中,细胞已分裂了300多次却毫无终止的征兆,也没有显示任何异常的迹象。
“细胞在端粒酶的作用下,就像被注入了兴奋剂的小兔子,”谢伊说,“它们只管没完没了地分裂繁殖。
”与此同时,谢伊和赖特的合作伙伴——美国杰龙(Geron)公司的研究人员,采用人体视网膜细胞做了相同的试验。
结果,这些细胞似乎也变得长生不老了。
诱人的希望研究人员由此看到了诱人的希望,但他们却不知道,这种控制细胞衰老过程的方法,最终是否能同样有效地延缓人体的衰老。
因此,迄今尚无人提议在大家的日常饮食中添加端粒酶。
实际上,这种酶也有令人忧虑之处:人们发现它也存在于85%的肿瘤之中,可能是造成癌细胞无节制增生的元凶。
尽管如此,只要研究人员充分认识其作用原理,就完全可能开发出既可防止衰老,又能制服癌症的新技术。
21世纪初人类开始的生命方舟计划对于细胞衰老过程的研究取得了突破性的进展,这让人们似乎看到了治愈癌症的曙光。
国内相关研究人类为什么会衰老中国医学专家童坦君、张宗玉两位教授经过10多年的研究,破解了人类衰老之谜,得出了人类衰老细胞基因调控能力减退与特异转录因子相关的结论。
端粒酶测定端粒酶测定童坦君、张宗玉夫妇是北京大学医学部生物化学与分子生物学系教授。
他们对人类衰老的研究始于上世纪80年代,并接受了国家自然科学基金重点项目———衰老分子机理与生物学年龄指征的研究。
今年3月,在全国人大常委会副委员长、北京大学副校长、北大医学部主任韩启德的倡导和支持下,童坦君、张宗玉夫妇成立了国内首家衰老研究中心。
据童坦君介绍,人类衰老的机理极其复杂,其学说不下几十种,如免疫学说、神经内分泌学说、自由基因学说、蛋白质合成差错累积学说等。
近年从分子与基因水平上提出的基因调控学说、DNA 损伤修复学说、线粒体损伤学说以及端区假说已成为国际研究热点,这也是童坦君、张宗玉夫妇在人类衰老机理方面研究的成果。
在衰老中心简陋的办公室内,两位老人接受了记者的专访,他们用通俗的语言解释了人类为什么会衰老?衰老机理如何?童坦君首先介绍了一个专业名词———端粒(又称端区),它是细胞染色体末端的一种用显微镜可以见到的呈条状的物质。
端粒有长短,随年龄增加而越来越短,端粒的消失,会使染色体发生畸变,从而使人类细胞丧失复制能力,最终导致细胞衰老。
专家所言童坦君说,端粒中还存在一种端粒酶,它具有调控端粒长短的能力,其活性也随年龄大小而不同,年轻时,活性大,较容易延长端粒,这是年轻人不易显老的原因。
此外,男性端粒长度缩短略快于女性,这也是男性平均年龄低于女性的原因。
张宗玉说,端粒酶的特性让人们看到了长生不老的曙光。
根据端区学说的原理,可否将人类体细胞引入端粒酶使细胞不断生长,从而达到青春常驻,这是人类未来研究的方向。
端粒DNA功能和端粒酶功能及生物特性功能及生物特性端粒(Telomere)是真核细胞染色体末端的特殊结构。
人端粒是由6个碱基重复序列(TTAGGG)和结合蛋白组成。
端粒有重要的生物学功能,可稳定染色体的功能,防止染色体DNA降解、末端融合,保护染色体结构基因DNA,调节正常细胞生长。
正常细胞由于线性DNA 复制5'末端消失,随体细胞不断增殖,端粒逐渐缩短,当细胞端粒缩至一定程度,细胞停止分裂,处于静止状态。
故有人称端粒为正常细胞的“分裂钟” (Mistosis clock) ,端粒长短和稳定性决定了细胞寿命,并与细胞衰老和癌变密切相关。
浙江大学孔德华博士介绍,端粒酶(Telomerase)是使端粒延伸的反转录DNA合成酶。
是个由RNA和蛋白质组成的核糖核酸-蛋白复合物。
其RNA组分为模板,蛋白组分具有催化活性,以端粒3'末端为引物,合成端粒重复序列。
端粒酶的活性在真核细胞中可检测到,其功能是合成染色体末端的端粒,使因每次细胞分裂而逐渐缩短的端粒长度得以补偿,进而稳定端粒长度。
主要特征是用它自身携带的RNA作模板,以dNTP为原料,通过逆转录催化合成模板链5‘端DNA 片段或外加重复单位。
端粒酶在细胞中的主要生物学功能是通过其逆转录酶活性复制和延长端粒DNA来稳定染色体端粒DNA的长度。
近年有关端粒酶与肿瘤关系的研究进展表明,在肿瘤细胞中端粒酶还参与了对肿瘤细胞的凋亡和基因组稳定的调控过程。
与端粒酶的多重生物学活性相对应,肿瘤细胞中也存在复杂的端粒酶调控网络。
通过蛋白质-蛋白质相互作用在翻译后水平对端粒酶活性及功能进行调控,则是目前研究端粒酶调控机制的热点之一。
功能附加说明以及合成端粒的存在是为了维持染色体的稳定。
没有端粒,则末端暴露,易被外切酶水解。
而报道说端粒与生命长短有关,这只是个说法,还没成定论。
端粒不是用DNA聚合酶来合成的,是用端粒酶来合成的。
端粒酶中含有RNA模板,用来合成端粒。
端粒酶-端粒学假说及研究解决端粒酶问题人就可以长生吗?衰老机制(链接)首先要明确的问题就是人为什么会死亡,只有对这个过程端粒酶端粒酶的机制了解的足够透彻,做到永生并非不可能。
关于人衰老和死亡的机制,比如体内自由基清除与生成机制失衡,导致有害自由基日积月累,并进而破坏细胞器,线粒体已被证实参与了这一过程。
端粒酶也是其中一种解释。
由于正常人细胞没有端粒酶,无法修复DNA复制所造成的DNA缩短的问题,因此随着细胞复制次数的增多,DNA短到一定程度,可能就触发了死亡机制,或者死亡是一个渐近的过程。
关于细胞衰老分子机制的主流假说其中一个就是端粒酶。
但是98年就证明了二倍体叙利亚仓树胚细胞在复制分裂的各阶段始终表达端粒酶,但是仍然衰老。
而剔除端粒酶基因的小鼠尚未观测到相应的表型的变化。
所以端粒钟学说并不完全正确。
1、氧化性损伤。
来自自由基的积累。
2、RDNA。
染色体复制时可能出现错配膨起染色体外RDNA环,叫ERC。
它的积累导致细胞衰老,并伴随核仁的裂解。
3、沉默信息调节蛋白复合物。
它可以阻止它所在位点的DNA转录。
4、SGS1基因和WRN基因。
这是两个同源的基因,对于保证细胞正常生命周期是必须的,但是容易突变导致早老症。
5、发育程序。
6、线粒体DNA。
随着时间的推移,线粒体DNA的突变是相当显著的。
7、生命是最最神奇的魔法。
细胞里的行动是复杂而精确的,往往是外来刺激导致蛋白质磷酸化,一级一级地传递,激活一定基因,开始转录翻译出平时不存在的蛋白质,这蛋白质再引起接下来的一系列级联反应。
要推翻自然的规律,解决一个酶的问题,无异于杯水车薪。
可是即使假设人体具有了端粒酶,长生也是个值得打上问号的问题。
因为端粒酶仅仅解决了复制长度的问题,并不能解决DNA复制时的变异问题,当然这有专门的机构来负责。
可是这也说明,长生并非如想像中那么简单,不单单一个端粒酶就能解决。
开发应用的艰辛历程发现端粒染色体末端的端粒端粒是染色体末端的一段DNA片段。
排在线上的DNA决定人体性状,它们决定人头发的直与曲,眼睛的蓝与黑,人的高与矮等等,甚至性格的暴躁和温和。
其实端粒也是DNA,只不过端粒是染色体头部和尾部重复的DNA。
把端粒当作一件绒线衫,袖口脱落的线段,绒线衫像是结构严密的DNA。
细胞学家从来不对染色体棒尾巴拖出的DNA感兴趣。
他们把注意力聚集在46条染色的基因图上面,而且把绘制的人类基因组草图的事大声喧哗。
端粒与人体衰老1990年起Calvin Harley把端粒与人体衰老挂上了钩。
他讲了三端粒端粒点,将它记录如下:第一、细胞愈老,其端粒长度愈短;细胞愈年轻,端粒愈长,端粒与细胞老化有关系。
衰老细胞中的一些端粒丢失了大部分端粒重复序列。
当细胞端粒的功能受损时,出现衰老而当端粒缩短至关键长度后,衰老加速,临近死亡。
第二、正常细胞端粒较短。
细胞分裂会使端粒变短,分裂一次,缩短一点,就像磨损铁杆一样,如果磨损得只剩下一个残根时,细胞就接近衰老。
细胞分裂一次其端粒的DNA丢失约30-200bp(碱基对),鼠和人的一些细胞一般有大约10000bp。
第三、研究发现,细胞中存在一种酶,它合成端粒。
端粒的长短,是由酶决定的。
细胞内酶多酶少可预测端粒的长短。
正常人体细胞中检测不到端粒酶。
一些良性病变细胞,体外培养的成纤维细胞中也测不到端粒酶活性。
但在生殖细胞睾丸、卵巢、胎盘及胎儿细胞中此酶为阳性。
令人注目的发现是,恶性肿瘤细胞具有高活性的端粒酶,端粒酶阳性的肿瘤有卵巢癌、淋巴瘤、急性白血病、乳腺癌、结肠癌、肺癌等等。
人类肿瘤中广泛地存在着较高的端粒酶活性。
这样一来,我们又发现了一种肿瘤细胞的特异物质。
寻找衰老钟的故事人体是由细胞组成的,人有衰老,细胞是否也有衰老呢?这就像一座大厦,它的寿命很大程度上与组成它的砖块有关。
细胞是有寿命的,这是细胞学家海弗列克(Hayflick)在四十年前发现的,他培养人体的成纤维细胞,一代又一代。
但是在营养充分供给的情况下,细胞分裂到50代左右就停止活动了,真正地进入衰老期,这一发现似乎告诉人们在细胞内有一口衰老钟,这限定了细胞分裂的次数,也就限定了生物的寿命。