课件1-2-4惰性电极电解规律、有关电解的计算
- 格式:ppt
- 大小:562.50 KB
- 文档页数:26









电化学提要1.原电池电极构成:负极: 较活泼金属(电子流出的极);正极: 较不活泼的金属(或能导电的非金属)(电子流入的极)电极反应:负极: 氧化反应, 一般是金属失电子;正极: 还原反应,溶液中的阳离子得电子或者氧气得电子(吸氧腐蚀)溶液中带电粒子移动:阳离子向正极移动;阴离子向负极移动电解池电极构成:阳极:与电源正极相连的极;阴极:与电源负极相连的极电极反应:阳极: 氧化反应, 溶液中的阴离子失电子, 或电极金属失电子;阴极: 还原反应, 溶液中的阳离子得电子溶液中带电粒子移动:阳离子向阴极移动;阴离子向阳极移动电池的两极是正、负极, 电解的两极则是阴、阳极。
实际上,负极和阳极是起氧化反应的电极; 正极和阴极则是起还原反应的电极。
2. 原电池、电解池、电镀池判定规律若无外接电源,可能是原电池,然后依据原电池的形成条件分析判定,主要思路是“三看”。
先看电极:两极为导体且活泼性不同。
再看溶液:两极插入电解质溶液中。
后看回路:形成闭合回路或两极接触。
若有外接电源,两极插入电解质溶液中,则可能是电解池或电镀池。
当阳极金属与电解质溶液中的金属阳离子相同则为电镀池,其余情况为电解池。
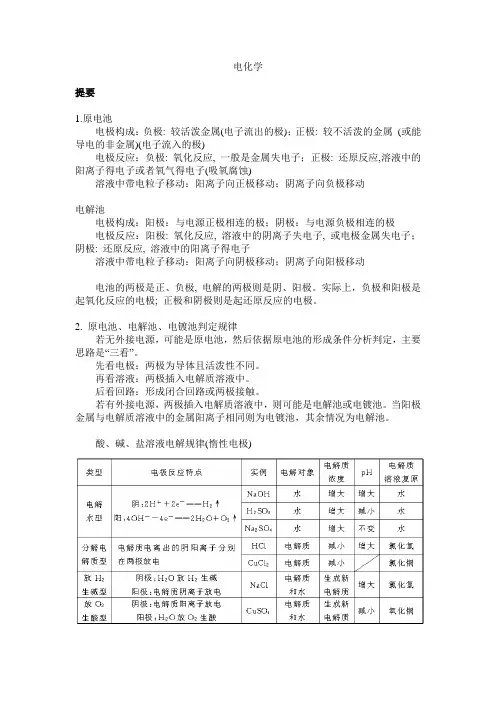
酸、碱、盐溶液电解规律(惰性电极)(1)分解水型:含氧酸、强碱、活泼金属的含氧酸盐(如NaOH、H2SO4、K2SO4等)的电解。
阴极:4H++4e-=2H2↑ 阳极:4OH--4e-=O2↑+2H2O总反应:2H2O2H2↑+O2↑阴极产物:H2;阳极产物:O2。
电解质溶液复原加入物质:H2O。
pH变化情况:原来酸性的溶液pH变小,原来碱性的溶液pH变大,强酸(含氧酸)强碱的正盐溶液pH不变。
(2)分解电解质型:无氧酸(除HF外)、不活泼金属的无氧酸盐(氟化物除外)的电解,如HCl、CuCl2等。
阴极:Cu2++2e-=Cu 阳极:2Cl--2e-=Cl2↑总反应:CuCl2 Cu+Cl2↑阴极产物:酸为H2,盐为金属;阳极产物:卤素等非金属单质。
