中考化学与化学溶解度有关的压轴题含答案解析
- 格式:doc
- 大小:285.00 KB
- 文档页数:19

备战中考化学—化学溶解度的综合压轴题专题复习含答案一、初中化学溶解度1.根据如图的溶解度曲线判断,下列说法正确的是A.50℃时,A 物质的溶解度为 80B.20℃时,B 的溶解度大于 A 的溶解度C.升温可使 C 物质的饱和溶液变成不饱和溶液D.将 50℃三种物质的饱和溶液分别降温到 20℃时,A 析出固体最多【答案】B【解析】【详解】A、50℃时,A物质的溶解度为80g,此选项错误;B、通过分析溶解度曲线可知,20℃时,B的溶解度大于A的溶解度,此选项正确;.C、 C物质的溶解度随温度的降低而增大,所以降温可使C物质的饱和溶液变成不饱和溶液,此选项错误;D、将 50℃三种物质的饱和溶液分别降温到20℃时,饱和溶液的质量不能确定,析出晶体的质量也不能确定,此选项错误。
故选B。
2.KCl和KNO3的溶解度表及溶解度曲线如图所示,下列说法不正确的是()温度/℃20304050KCl34.037.040.042.6溶解度S/gKNO331.645.863.985.5A.甲表示KNO3溶解度曲线B.温度t1℃应在20~30℃之间C.40℃时,10gKC1加入20g水中,可得到33.3%的溶液D.50℃时,30gKNO3加入50g水,充分溶解,再降温到30℃,有晶体析出【答案】C【解析】【分析】【详解】A、通过分析溶解度表中的数据可知,硝酸钾的溶解度受温度变化影响较大,所以甲表示KNO3溶解度曲线,故A正确,不符合题意;B、20~30℃,氯化钾的溶解度从34g增大到37g,硝酸钾的溶解度从31.6g增大到45.8g,所以温度t1℃应在20~30℃之间,故B正确,不符合题意;C、40℃时,氯化钾的溶解度是40.0g,所以10gKCl加入20g水中,有固体剩余,形成的是该温度下的氯化钾饱和溶液,故溶液的质量分数为:40.0g100%28.6% 100g+40.0g⨯≈,故C错误,符合题意。
D、30℃时,硝酸钾的溶解度是45.8g,所以50℃时,30g KNO3加入50g水,充分溶解,再降温到30℃,有晶体析出,故D正确,不符合题意。

2020-2021备战中考化学与化学溶解度有关的压轴题及详细答案一、初中化学溶解度1.甲、乙两种固体物质的溶解度曲线如图所示.下列叙述中正确的是()A.甲物质的溶解度大于乙物质的溶解度B.t1℃时,甲、乙两物质饱和溶液的溶质质量分数一定相等C.t2℃时,将30g甲物质放入70g水中,所得饱和溶液的质量为100gD.t2℃时,甲、乙两物质的饱和溶液降温到t1℃,析出晶体质量甲>乙【答案】B【解析】试题分析:A、比较物质的溶解度大小,须确定温度,不知温度,则无法比较,故错误;B、t1℃时,甲、乙物质的溶解度相等,饱和溶液的溶质质量分数= S/(100+S)×100%.甲、乙物质的饱和溶液的溶质质量分数相等,故正确;C、t2℃时,甲的溶解度是30g,100g水中最多溶解30g,30g甲溶解在70g水中形成溶液的质量=21g+70g=91g,不是100g溶液;故错误;D、甲、乙的饱和溶液的质量不确定,所以从t 2℃降到t1℃,析出晶体的质量也不确定,故错误;考点:溶解度曲线。
2.下图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列有关说法正确的是()A.t2℃时,在两个各盛有100g水的烧杯中,分别加入50g的甲、乙两种固体,充分搅拌,所得甲、乙溶液中溶质的质量不等B.t1℃时,等质量甲、乙溶液中所含溶剂的质量甲等于乙C.乙中含有少量甲,可以用冷却热饱和溶液的方法提纯甲D.t2℃时,将甲、乙的饱和溶液降温至t1℃,甲溶液析出晶体的质量大于乙【答案】A【解析】试题分析:A、从溶解度曲线可看出,t2℃时,甲的溶解度=50g,而乙的溶解度<50g,故在两个各盛有l00g水的烧杯中,分别加入50g的甲、乙两种固体,充分搅拌,甲能全部溶解,而乙有剩余,故所得甲、乙溶液中溶质的质量不等,正确,B、t1℃时,甲、乙物质的溶解度相等,但没有指明是饱和溶液,故等质量甲、乙溶液中所含溶剂的质量甲不一定等于乙,错误, C、从溶解度曲线可看出,甲的溶解度随温度的升高变化较大,而乙的溶解度随温度的升高而变化较小,故乙中含有少量甲,可以用冷却热饱和溶液的方法提纯乙,错误,D、没有指明高温时的溶液是否是等质量,故无法判断析出晶体量的多少,错误,故选A考点:溶解度曲线的意义3.下列有关溶解度的说法错误的是()A.20℃时,甲和乙的溶解度相等B.40℃时,若将40g乙放入160g水中充分溶解,所得溶液的溶质质量分数为20% C.40℃时,将甲、乙两物质的饱和溶液各100g,降温至20℃,析出晶体(均不含结晶水)的质量关系是:m(甲)=m(乙)D.20℃时,将甲物质的饱和溶液升温到40℃,溶液变为不饱和溶液【答案】C【解析】【详解】A、通过分析溶解度曲线可知,20℃时,甲和乙的溶解度相等,故A正确,不符合题意;B、40℃时,乙物质的溶解度是40g,所以若将40g乙放入160g水中充分溶解将完全溶解,故所得溶液的溶质质量分数为40g200g100%=20%,故B正确,不符合题意;C、40℃时,甲物质的溶解度大于乙物质的溶解度,将甲、乙两物质的饱和溶液各100g,降温至20℃,甲、乙物质的溶解度相等,所以析出晶体(均不含结晶水)的质量关系是:m(甲)>m(乙),故C错误,符合题意;D、20℃时,将甲物质的饱和溶液升温到40℃,溶解度增大,所以溶液变为不饱和溶液,故D正确,不符合题意。

九年级中考化学化学溶解度解答题压轴题提高专题练习及答案解析一、初中化学溶解度1.如图是a、b、c三种物质的溶解度曲线。
由此可知下列说法中不正确的是()A.在t1℃时,a的溶解度等于c的溶解度B.c物质的溶解度随温度的升高而变小C.a的饱和溶液从t2℃降温至t1℃时变为不饱和溶液D.当a中含有少量b时,可以用降温结晶的方法提纯a【答案】C【解析】试题分析:由溶解度曲线知A.在t1℃时,a的溶解度等于c的溶解度是准确的叙述;B选项c的溶解度随温度的升高而减少是正确的叙述;C选项a的饱和溶液从t2℃降温至t1℃时变为不饱和溶液是错误的叙述,降温时溶液仍然为饱和溶液;D选项当a中含有少量b时,可以用降温结晶的方法提纯a是正确的叙述,因为a的溶解度受温度的影响比b的大,所以采用降温结晶;故答案选择C考点:溶解度曲线2.如图是A、B、C三种物质的溶解度曲线,下列说法错误的是A.t1℃时,A、B、C的饱和溶液恒温蒸发等质量的水,析出晶体质量: B>A=CB. t1℃时,物质C饱和溶液的溶质质量分数为20%C.A中混有少量C时,应采用降温结晶的方法提纯AD.将t2℃时的物质A、B饱和溶液降温到t1℃时,两溶液的溶质质量分数: A>B【答案】D【解析】【分析】【详解】A、在t1℃时,B的溶解度比A、C的溶解度大,当饱和溶液恒温蒸发等质量的水,析出晶体质量:B>A=C,说法正确;故不符合题意;B、在t1℃时,物质C饱和溶液的溶质质量分数为:25g100%20%10025g g⨯=+,说法正确;故不符合题意;C、由于A的溶解度受温度的升高而升高,且变化较大,C的溶解度随温度的升高溶解度下降,因此当A中混有少量C时,应采用降温结晶的方法提纯A,说法正确;故不符合题意;D、将t2℃时的物质A、B饱和溶液降温到t1℃时,两物质的溶解度均降低,但是A物质降低的更大,析出的晶体更多;因此,此时两溶液的溶质质量分数:B > A,说法错误;故符合题意;故选D3.图是A、B、C三种物质的溶解度曲线,当等质量的A、B、C三种物质的饱和溶液同时从t=2℃降温到t=1℃时,其中溶质质量分数没有发生改变的是A.AB.BC.CD.AB【答案】C【解析】试题分析:由题中所给的坐标曲线可知,A、B两物质的溶解度随温度升高而升高,C物质随温度的升高而降低,所以当等质量的A、B、C三种物质的饱和溶液同时从t=2℃降温到t=1℃时,C物质的溶解度增大,没有物质析出,所以溶质质量分数不变,A、B均有溶质析出,所以溶质质量分数减小。

2020-2021中考化学—化学溶解度的综合压轴题专题复习及答案一、初中化学溶解度1.如图是A,B,C三种物质的溶解度曲线,下列说法正确的是()A.将C的饱和溶液变为不饱和溶液,可采用升温的方法B.等质量的A,B溶液降温后,析出晶体的质量一定是A>BC.t2℃时三种物质的饱和溶液中溶质质量分数的大小关系是A>B>CD.t2℃时,将50gA放入50g水中,得到A的饱和溶液,其中溶质和溶液的质量比为1:2【答案】C【解析】【详解】A、C溶解度随温度升高而减小,将C的饱和溶液变为不饱和溶液,可采用降温的方法,故选项错误;B、等质量的A,B溶液降温后,因没有确定是否为饱和,所以析出晶体的质量不能确定,故选项错误;C、t2℃时,三种物质的溶解度A>B>C,故此温度下三种物质的饱和溶液中溶质质量分数的大小关系是A>B>C ,故选项正确;D、t2℃时,A的溶解度为50克,将50gA放入50g水中,只能溶解25克,得到A的饱和溶液,其中溶质和溶液的质量比为25g:75g=1:3,故选项错误。
故选C。
2.现有30℃时的氯化钾饱和溶液,在下列情况下溶液中溶质的质量分数不变的是()A.温度不变,向溶液中加入氯化钾晶体B.温度不变,向溶液中加入水C.降低温度至10℃D.升高温度蒸发掉一部分水,温度保持在40℃【答案】A【解析】【分析】=100% 溶质质量溶质的质量分数溶液质量【详解】 A 、因温度不变,虽向溶液中加入氯化钾晶体,但溶质及溶液的质量未变,溶质的质量分数也不变,故A 正确;B 、因溶液的质量变了,所以溶质的质量分数也相应发生变化,故B 不正确;C 、降低温度有晶体析出,溶剂质量不变,其溶质的质量分数变小,故C 不正确;D 、因溶液中溶剂质量减小,所以溶质的质量分数将增大,故D 不正确。
故选A 。
3.如图是X 、Y 、Z 三种固体物质的溶解度曲线图,以下说法错误的是A .要配制相同浓度的Y 、Z 饱和溶液,需要把温度控制在t2℃B .t1℃时,将X 、Y 、Z 的饱和溶液都升温到t3℃,仍然是饱和溶液C .t3℃时,将X 、Y 、Z 的饱和溶液都降温到t1℃,溶液中溶质质量分数由大到小的顺序为Y>Z>XD .若0℃时,Y 的溶解度为20g ,此温度下Y 饱和溶液的质量分数是16.7%【答案】B【解析】【分析】【详解】A 、要配制相同浓度的Y 、Z 饱和溶液,需要把温度控制在t 2℃正确,因为此温度下两物质的溶解度相等,正确但不符合题意,故选项错误;B 、t 1℃时,将X 、Y 、Z 的饱和溶液都升温到t 3℃,仍然是饱和溶液错误,X 、Y 的溶解的都随温度升高而增大,属于不饱和溶液,Z 的溶解度随温度升高而减小,是饱和溶液,错误符合题意,故选项正确;C 、根据溶解度曲线可知,t 3℃时,将X 、Y 、Z 的饱和溶液都降温到t 1℃,溶液中溶质质量分数由大到小的顺序为Y >Z >X 正确,正确但不符合题意,故选项错误;D 、若0℃时,Y 的溶解度为20g ,此温度下Y 饱和溶液的质量分数=20g 120g×100%≈16.7%,正确但不符合题意,故选项错误;故选B 。
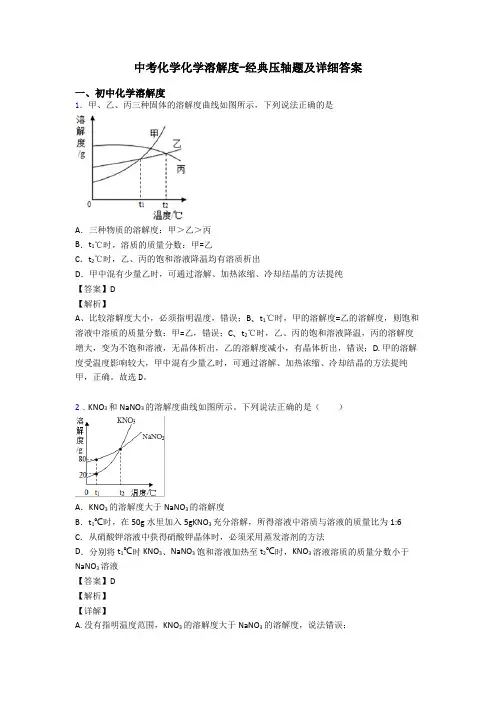
2020 年中考化学压轴题专题复习:溶解度一、选择题1.(2019•安徽)压强为101k P a下,硝酸钾和氨气在不同温度下的溶解度如下表。
下列说法正确的是()A.两种物质的溶解度均随温度升高而增大B.0℃时,K N O3饱和溶液中溶质的质量分数为31.6%C.60℃的KNO3 饱和溶液降温至30℃,有晶体析出D.NH3 的溶解度与压强大小无关【答案】C【解答】解:A、由表中的数据可知,硝酸钾的溶解度均随温度升高而增大,氨气的溶解度均随温度升高而减小,故 A 错误;B、20℃时,K N O3的溶解度是31.6g,饱和溶液中溶质的质量分数为:≈24%,故 B 错误;C、由于硝酸钾的溶解度随温度的升高而增大,所以 60℃的 KNO3 饱和溶液降温至 30℃,有晶体析出,故C 正确;D、NH3 是气体,NH3 的溶解度随压强增大而增大,故 D 错误。
故选:C。
2.(2019•铜仁市)下表为甲、乙、丙三种物质的溶解度,请结合表中信息判断下列说法正确的是()A.三种物质的溶解度大小为:甲>乙>丙B.随着温度变化,甲的溶解度变化最小C.0℃时,100g丙的饱和溶液中,溶质的质量为36.3gD.分别将 50℃时甲、乙的饱和溶液降温至 T℃,两种溶液中溶质的质量分数相等【答案】D【解答】解:A、比较溶解度必须在同一温度下,故 A 错误;B、由表中的数据可知,随着温度变化,丙的溶解度变化最小,故 B 错误;C、在30℃时丙的溶解度是36.3g,由溶解度的含义可知,30℃时,100g丙的饱和溶液中,溶质的质量为26.6g,故C错误;D、由于甲、乙的溶解度都随温度的降低而减小,在 T℃时甲、乙的溶解度相同,分别将 50℃时甲、乙的饱和溶液降温至 T℃,两种溶液中溶质的质量分数相等,故D 正确。
故选:D。
3.(2019•株洲)如图为K N O3和N a C l的溶解度曲线,下列说法不正确的是()A.20℃时,K N O3的溶解度为31.6gB.a点处K N O3和N a C l两种溶液中溶质的质量分数相等C.40℃时,100g水中可溶解K N O3固体63.9gD.0℃时,N a C l饱和溶液中溶质的质量分数为35.7%【答案】D【解答】解:A、通过分析溶解度曲线可知,20℃时,K N O3的溶解度为31.6g,故A 正确;B、a点处K N O3和N a C l两种物质的溶解度相等,所以a点处溶液中溶质的质量分数相等,故B 正确;C、40℃时,硝酸钾的溶解度是63.9g,所以100g水中可溶解K N O3固体63.9g,故C 正确;D、0℃时,氯化钠的溶解度是35.7g,所以N a C l饱和溶液中溶质的质量分数为×100%≠35.7%,故D错误。

备战中考化学压轴题专题化学溶解度的经典综合题含答案解析一、初中化学溶解度1.NaOH、Na2CO3分别在水、酒精中的溶解度如下表所示,结合图表数据下列说法正确的是NaOH Na2CO320℃40℃20℃40℃水109g129g21.8g49g酒精17.3g40g不溶不溶A.图表示Na2CO3在水、酒精中的溶解度曲线B.将CO2通入所得NaOH的酒精溶液中,无明显现象C.40℃时,将50gNaOH投入到100g酒精中,形成饱和溶液D.20℃升到40℃时,NaOH在水中的溶解度变化大于Na2CO3在水中的溶解度变化【答案】C【解析】【详解】A. 根据NaOH、Na2CO3分别在水、酒精中的溶解度数据可知,图表示NaOH在水、酒精中的溶解度曲线,此选项错误;B. 将CO2通入所得NaOH的酒精溶溶液中,2NaOH +CO2=Na2CO3 +H2O,由于碳酸钠在酒精中不能溶解,所以会有白色晶体析出,此选项错误;C. 40℃时,NaOH在酒精中的溶解度是40g,则将50gNaOH投入到100g酒精中,能形成饱和溶液,此选项正确;D. 20℃升到40℃时,NaOH在水中的溶解度变化是129g-109g=20g,20℃升到40℃时,Na2CO3在水中的溶解度变化是49g-21.8g=27.2g,所以Na2CO3的溶解度变化较大,此选项错误。
故选C。
2.下列有关溶液的说法中,错误的是A.外界条件不改变,溶质不会从溶液中分离出来B.餐具上的油污可利用洗涤剂的乳化功能将其洗去C.相同质量的同一溶质的饱和溶液一定比它的不饱和溶液所含的溶质多D.对于同一溶质的溶液,在同一温度时,其饱和溶液一定比其不饱和溶液浓【答案】C【解析】【分析】【详解】A、溶液是均一的,稳定的混合物,只要外界条件不改变,溶质就不会从溶液中分离出来,说法正确;故不符合题意;B、洗涤剂具有乳化作用,因此餐具上的油污可利用洗涤剂的乳化功能将其洗去,说法正确;故不符合题意;C、同种物质在不同温度下溶解度不同,因此相同质量的同一溶质的饱和溶液不一定比它的不饱和溶液所含的溶质多,说法错误,故不符合题意;D、由于温度一定,溶剂一定,根据溶解度可知,饱和溶液一定比不饱和溶液的质量分数更大;因此对于同一溶质的溶液,在同一温度时,其饱和溶液一定比其不饱和溶液浓,说法正确;故不符合题意;故选C【点睛】溶液是均一的、稳定的混合物,物质的溶解度随温度的变化而变化,若温度不变,则溶解度不改变。

2020-2021中考化学压轴题之化学溶解度(中考题型整理,突破提升)附详细答案一、初中化学溶解度1.下图是A、B、C三种物质的溶解度曲线,下列说法错误的是( )A.将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是C>B>AB.当A中含有少量B时,可以通过降温结晶的方法提纯AC.升高温度可使接近饱和的C溶液变为饱和D.t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A【答案】A【解析】A、由溶解度曲线可知,AB两种物质的溶解度随温度的升高而升高,C物质的溶解度随温度的升高和降低,将t2℃时A、B、C的饱和溶液同时降温至t1℃后AB两种物质仍然为饱和溶液,C为不饱和溶液,C溶液中溶质的质量分数不变,t1℃时B的溶解度大于A的溶解度,故B 的质量分数大于A 的质量分数,C 的质量分数小于B的质量分数,故错误;B、A的溶解度随温度的变化较大,B 的溶解度随温度的变化不大,故当A中含有少量B 时,可以通过降温结晶的方法提纯A,正确;C、由图可知,C物质的溶解度随温度的升高而降低,故升高温度可使接近饱和的C溶液变为饱和,正确;D、由图可知,t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A,正确。
故选A。
2.如图为甲、乙两种固体物质(不含结晶水)的溶解度曲线。
下列说法错误的是A.t2℃时,甲的溶解度大于乙B.t1℃时,甲、乙各25g加到50g水中,均得70g溶液C.t1℃时,甲、乙两种物质的溶液中溶质质量分数相等D.t2℃时,将溶剂均为100g的甲、乙的饱和溶液分别降温到t1℃时,析出晶体的质量甲>乙【答案】C【解析】【分析】【详解】A.由图像可知,t2℃时,甲的溶解度大于乙,正确;B、t1℃时,甲、乙两种物质的溶解度是40g,所以各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70g,故B正确;C、t1℃时,溶液的饱和状态不确定,所以甲溶液的溶质质量分数不一定等于乙溶液的溶质质量分数,故C错误;D. t2℃时,甲的溶解度大于乙,将溶剂均为100g的甲、乙的饱和溶液分别降温到t1℃时,析出晶体的质量甲>乙,正确;故选C。

2020-2021中考化学——化学溶解度的综合压轴题专题复习附答案一、初中化学溶解度1.下列有关溶液的说法中,错误的是A.外界条件不改变,溶质不会从溶液中分离出来B.物质的溶解过程通常会伴随着能量的变化C.溶液中的溶质以分子或离子的形式均匀分散在溶剂中保持静止不动,所以溶液具有均一性和稳定性D.改变条件,能够使饱和溶液与不饱和溶液相互转化【答案】C【解析】【分析】【详解】A.溶液是均一稳定的混合物,外界条件不改变,溶质不会从溶液中分离出来,正确;B.微观上看,物质溶解时都有扩散过程(吸热)和水合(放热)两个过程,物质的溶解过程通常会伴随着能量的变化,正确;C.溶液中的溶质以分子或离子的形式均匀分散在溶剂中,相互混合的微粒间以几乎相同的速度远动着,所以溶液具有均一性和稳定性,错误;D.饱和溶液是在一定温度下、一定量的溶剂里不能再溶解某物质的溶液叫该物质的饱和溶液,反之为不饱和溶液。
因此物质的溶解能力受溶质、溶剂、温度的影响,所以改变条件,能够使饱和溶液与不饱和溶液相互转化,正确;选C。
2.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是()A.t1℃时,甲、乙的溶解度相等B.t2℃时,甲的溶解度为50C.甲中混有少量的乙时,可用降温结晶的方法提纯甲D.t1℃时,甲、乙两种饱和溶液恒温蒸发等质量的水,析出晶体的质量相等【答案】B【解析】【详解】A、通过分析溶解度曲线可知,t1℃时,甲、乙的溶解度相等,故A正确,不符合题意;B、t2℃时,甲的溶解度为50g,题中未加单位,故B错误,符合题意;C、甲物质的溶解度受温度变化影响较大,所以甲中混有少量的乙时,可用降温结晶的方法提纯甲,故C正确,不符合题意;D、t1℃时,甲、乙的溶解度相等,所以甲、乙两种饱和溶液恒温蒸发等质量的水,析出晶体的质量相等,故D正确,不符合题意。
故选B。
3.如图是X、Y、Z三种固体的溶解度曲线,下列有关说法中不正确的是()A.Z的溶解度随温度的升高而降低B.t1℃时,Y的溶解度大于Z的溶解度C.t3℃时,X的饱和溶液中溶质的质量分数为40%D.t2℃时,X的溶解度和Y的溶解度相等【答案】C【解析】根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况;还可以判断或比较某一物质在不同温度下的溶解度大小;饱和溶液中溶质的质量分数=×100%。

压轴题02 溶解度及其应用溶解度曲线是中考必考内容,出题概率几乎100%,考查方式有“一线型”、“二线型”、“三线型”、实验与曲线融合型等。
出题方式主要有一下几种:1.溶解度大小的判断及比较2.饱和溶液与不饱和溶液的判断及转化3.改变温度时溶液中各种量的变化情况4.一定温度下配制不同物质的饱和溶液时,溶液质量、溶剂质量、溶质质量的比较5.溶液的稀释6.根据溶解度曲线的升降情况判断提纯方法7.质量分数的计算与比较溶解度曲线的意义:点——曲线上的点表示物质在对应温度时的溶解度,两曲线的交点表示两物质在t℃时的溶解度相等。
线——曲线的走向表示物质的溶解度随温度改变而变化的趋势,曲线的陡缓表示物质溶解度受温度影响的大小。
面——曲线下方的点表示溶液为不饱和溶液,曲线上方的点表示溶液饱和且有未溶解固体 命题角度 1.溶解度大小的判断及比较 溶解度曲线的交点表示两物质在该温度下溶解度相等,同温度下溶解度曲线的交点越高溶解度越大。
2.饱和溶液与不饱和溶液的判断及转化 (1)饱和溶液与不饱和溶液的判断 若g100m m 溶解度溶剂溶质<,为不饱和溶液; 若g100m m 溶解度溶剂溶质=,恰好为饱和溶液; 若g 100m m 溶解度溶剂溶质>,为饱和溶液,且有未溶解的溶质; (2)饱和溶液与不饱和溶液的转化℃温度不变时,改变溶质或溶剂质量不饱和溶液饱和溶液增加溶质或蒸发溶剂增加溶剂℃改变温度时,升温或降温取决于物质的溶解度随温度的变化趋势3.改变温度时溶液中各种量的变化情况改变温度若有溶质析出则溶质质量分数减小,若无溶质析出则溶质质量分数不变4.一定温度下配制不同物质的饱和溶液时,溶液质量、溶剂质量、溶质质量的比较℃溶质的质量与一定时,溶解度越大,配制饱和溶液所需溶剂的质量越小。
℃溶剂的质量一定时,溶解度越大,配制饱和溶液所需溶质的质量越大℃饱和溶液的质量一定时,溶解度越大,所含溶质质量越大,所含溶剂质量越小。

中考化学——化学溶解度的综合压轴题专题复习附详细答案一、初中化学溶解度1.NaOH、Na2CO3分别在水、酒精中的溶解度如下表所示,结合图表数据下列说法正确的是NaOH Na2CO320℃40℃20℃40℃水109g129g21.8g49g酒精17.3g40g不溶不溶A.图表示Na2CO3在水、酒精中的溶解度曲线B.将CO2通入所得NaOH的酒精溶液中,无明显现象C.40℃时,将50gNaOH投入到100g酒精中,形成饱和溶液D.20℃升到40℃时,NaOH在水中的溶解度变化大于Na2CO3在水中的溶解度变化【答案】C【解析】【详解】A. 根据NaOH、Na2CO3分别在水、酒精中的溶解度数据可知,图表示NaOH在水、酒精中的溶解度曲线,此选项错误;B. 将CO2通入所得NaOH的酒精溶溶液中,2NaOH +CO2=Na2CO3 +H2O,由于碳酸钠在酒精中不能溶解,所以会有白色晶体析出,此选项错误;C. 40℃时,NaOH在酒精中的溶解度是40g,则将50gNaOH投入到100g酒精中,能形成饱和溶液,此选项正确;D. 20℃升到40℃时,NaOH在水中的溶解度变化是129g-109g=20g,20℃升到40℃时,Na2CO3在水中的溶解度变化是49g-21.8g=27.2g,所以Na2CO3的溶解度变化较大,此选项错误。
故选C。
2.如图为甲、乙两种固体物质(不含结晶水)的溶解度曲线。
下列说法错误的是A .t 2℃时,甲的溶解度大于乙B .t 1℃时,甲、乙各25g 加到50g 水中,均得70g 溶液C .t 1℃时,甲、乙两种物质的溶液中溶质质量分数相等D .t 2℃时,将溶剂均为100g 的甲、乙的饱和溶液分别降温到t 1℃时, 析出晶体的质量甲>乙【答案】C【解析】【分析】【详解】A.由图像可知,t2℃时,甲的溶解度大于乙,正确;B 、t 1℃时,甲、乙两种物质的溶解度是40g ,所以各25g 分别加入到50g 水中,充分溶解,得到的溶液质量都是70g ,故B 正确;C 、t 1℃时,溶液的饱和状态不确定,所以甲溶液的溶质质量分数不一定等于乙溶液的溶质质量分数,故C 错误;D. t 2℃时,甲的溶解度大于乙,将溶剂均为100g 的甲、乙的饱和溶液分别降温到t 1℃时, 析出晶体的质量甲>乙,正确;故选C 。
2020-2021中考化学压轴题之化学溶解度(中考题型整理,突破提升)含答案解析一、初中化学溶解度1.下图是甲、乙两种固体物质的溶解度曲线。
下列说法中错误的是( )A .20℃时,甲、乙饱和溶液中溶质质量分数相等B .40℃时,甲的溶解度大于乙的溶解度C .40℃时,乙的饱和溶液中溶质的质量分数为40%D .将40℃甲的饱和溶液降温到20℃,会有晶体析出 【答案】C 【解析】A 、由溶解度曲线可知,20 ℃时,甲、乙两种物质的溶解度相等,根据饱和溶液的溶质质量分数=100100g ⨯+溶解度%溶解度,故20 ℃时,甲、乙饱和溶液中溶质质量分数相等,正确;B 、由溶解度曲线可知,40 ℃时,甲的溶解度大于乙的溶解度,正确;C 、由图可知,40 ℃时,乙的溶解度为40 g ,故40 ℃时,乙的饱和溶液中溶质的质量分数为40g100100g 40g⨯+%=28.6%,故错误;D 、甲物质的溶解度随温度的升高而升高,故将40 ℃甲的饱和溶液降温到20 ℃,会有晶体析出,正确。
故选C 。
2.下列排序正确的是 A .利用金属的年代 B .铁元素质量分数C .碳元素的化合价:D .物质在水中的溶解性:【答案】B 【解析】 【详解】A 、金属的活动性越弱,使用的年代越早,人类最早使用的金属是铜、其次是铁和铝,错误;B 、氧化亚铁中铁元素的质量分数是,氧化铁中铁元素的质量分数是,硫化亚铁中铁元素的质量分数是,铁元素的质量分数依次降低,正确;C、甲烷中碳元素的化合价为-4价,一氧化碳中碳元素的化合价为+2价,C60是单质,元素的化合价为0,错误;D、氯化钙易溶于水,碳酸钙难溶于水,氢氧化钙微溶于水,错误。
故选B。
【点睛】本题考查金属的活动性与使用年代的关系,元素质量分数的求算,元素的化合价和物质的溶解性等知识。
3.20℃时,将等质量的a、b两种不含结晶水的固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后,现象如图1;然后升温到50℃时,现象如图2;a、b两种物质的溶解度曲线如图3.由这一过程可知()A.30℃时a、b溶液溶质质量分数不相等B.40℃时a、b溶液溶质质量分数大小无法比较C.从20℃到50℃,b溶液质量分数不变D.图3中表示a的溶解度曲线是N【答案】C【解析】【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.【详解】图1中,溶剂质量相等,甲中物质溶解的质量小于乙中物质,所以M表示的是a物质的溶解度曲线,N表示的是b物质的溶解度曲线;A、30℃时,甲、乙溶液是否达到饱和状态不能确定,所以甲、乙溶液溶质质量分数也不能确定,错误;B、40℃时,a的溶解度大于b,故二者都是全部溶解,a、b溶液溶质质量分数大小相等,错误;C、从20℃到50℃,b溶液质量分数不变,正确;D、M表示的是a物质的溶解度曲线,错误。
备战中考化学—化学溶解度的综合压轴题专题复习附详细答案一、初中化学溶解度1.固体硝酸钾的溶解度曲线如图所示,下列说法正确的是()A.70℃时,硝酸钾的溶解度为114B.70℃时,C点为硝酸钾的不饱和溶液C.70℃时,B点为硝酸钾的饱和溶液D.A、C两点对应溶液的溶质质量分数相同【答案】D【解析】A、由溶解度曲线可知,70℃时,硝酸钾的溶解度为144g,故A错误;B、由溶解度曲线可知,70℃时,C点在溶解度曲线的上面,应为硝酸钾的饱和溶液,故B 错误;C、由溶解度曲线可知,70℃时,B点在溶解度曲线的下面,应为硝酸钾的不饱和溶液,故C错误;D、由溶解度曲线可知,A、C两点对应溶液的都是同一温度下同一种溶质的饱和溶液,溶液中溶质的质量分数是一定值,所以,A、C两点对应溶液的溶质质量分数相同.故D正确.故选D.2.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是()A.t1℃时,甲、乙的溶解度相等B.t2℃时,甲的溶解度为50C.甲中混有少量的乙时,可用降温结晶的方法提纯甲D.t1℃时,甲、乙两种饱和溶液恒温蒸发等质量的水,析出晶体的质量相等【答案】B【解析】【详解】A、通过分析溶解度曲线可知,t1℃时,甲、乙的溶解度相等,故A正确,不符合题意;B、t2℃时,甲的溶解度为50g,题中未加单位,故B错误,符合题意;C、甲物质的溶解度受温度变化影响较大,所以甲中混有少量的乙时,可用降温结晶的方法提纯甲,故C正确,不符合题意;D、t1℃时,甲、乙的溶解度相等,所以甲、乙两种饱和溶液恒温蒸发等质量的水,析出晶体的质量相等,故D正确,不符合题意。
故选B。
3.下图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列有关说法正确的是()A.t2℃时,在两个各盛有100g水的烧杯中,分别加入50g的甲、乙两种固体,充分搅拌,所得甲、乙溶液中溶质的质量不等B.t1℃时,等质量甲、乙溶液中所含溶剂的质量甲等于乙C.乙中含有少量甲,可以用冷却热饱和溶液的方法提纯甲D.t2℃时,将甲、乙的饱和溶液降温至t1℃,甲溶液析出晶体的质量大于乙【答案】A【解析】试题分析:A、从溶解度曲线可看出,t2℃时,甲的溶解度=50g,而乙的溶解度<50g,故在两个各盛有l00g水的烧杯中,分别加入50g的甲、乙两种固体,充分搅拌,甲能全部溶解,而乙有剩余,故所得甲、乙溶液中溶质的质量不等,正确,B、t1℃时,甲、乙物质的溶解度相等,但没有指明是饱和溶液,故等质量甲、乙溶液中所含溶剂的质量甲不一定等于乙,错误, C、从溶解度曲线可看出,甲的溶解度随温度的升高变化较大,而乙的溶解度随温度的升高而变化较小,故乙中含有少量甲,可以用冷却热饱和溶液的方法提纯乙,错误,D、没有指明高温时的溶液是否是等质量,故无法判断析出晶体量的多少,错误,故选A考点:溶解度曲线的意义4.下列有关溶解度的说法错误的是()A.20℃时,甲和乙的溶解度相等B.40℃时,若将40g乙放入160g水中充分溶解,所得溶液的溶质质量分数为20% C.40℃时,将甲、乙两物质的饱和溶液各100g,降温至20℃,析出晶体(均不含结晶水)的质量关系是:m(甲)=m(乙)D.20℃时,将甲物质的饱和溶液升温到40℃,溶液变为不饱和溶液【答案】C【解析】【详解】A、通过分析溶解度曲线可知,20℃时,甲和乙的溶解度相等,故A正确,不符合题意;B、40℃时,乙物质的溶解度是40g,所以若将40g乙放入160g水中充分溶解将完全溶解,故所得溶液的溶质质量分数为40g200g100%=20%,故B正确,不符合题意;C、40℃时,甲物质的溶解度大于乙物质的溶解度,将甲、乙两物质的饱和溶液各100g,降温至20℃,甲、乙物质的溶解度相等,所以析出晶体(均不含结晶水)的质量关系是:m(甲)>m(乙),故C错误,符合题意;D、20℃时,将甲物质的饱和溶液升温到40℃,溶解度增大,所以溶液变为不饱和溶液,故D正确,不符合题意。
2020-2021中考化学与化学溶解度有关的压轴题含答案一、初中化学溶解度1.甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是()A.t1℃时,甲乙的溶解度相等,它们饱和溶液的溶质质量分数也相等,都为20%B.t1℃时,30g甲加入到50g水中最多可得80g溶液C.t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲>乙D.t2℃,等质量的甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液质量的大小关系为:甲>乙【答案】C【解析】【详解】A、t1℃时,甲乙的溶解度相等,它们饱和溶液的溶质质量分数也相等,都为:20g×100%≈16.7%,20%错误,故选项错误;120gB、t1℃时,50g水中最多溶解10g甲,30g甲加入到50g水中最多可得溶液的质量=10g+50g=60g,80g溶液错误,故选项错误;C、t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲>乙正确,因为降温后甲的质量分数变小,乙的不变,但还是甲的质量分数大于乙的质量分数,故选项正确;D、t2℃,等质量的甲、乙两物质的饱和溶液分别降温到t1℃时,甲有晶体析出,质量减少,乙的质量不变,所得溶液质量的大小关系为:乙>甲,甲>乙错误,故选项错误。
故选C。
2.如图是X、Y、Z三种固体的溶解度曲线,下列有关说法中不正确的是()A.Z的溶解度随温度的升高而降低B.t1℃时,Y的溶解度大于Z的溶解度C.t3℃时,X的饱和溶液中溶质的质量分数为40%D.t2℃时,X的溶解度和Y的溶解度相等【答案】C【解析】根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况;还可以判断或比较某一物质在不同温度下的溶解度大小;饱和溶液中溶质的质量分数=×100%。
观察溶解度曲线,可以看出Z的溶解度随温度的升高而降低,A正确;观察溶解度曲线,可以看出t1℃时,Y的溶解度大于Z的溶解度,B正确;观察溶解度曲线,可以看出t3℃时,X的溶解度是100g,所以其饱和溶液溶质的质量分数是:×100%=50%,故C错误;观察溶解度曲线,可以看出t2℃时,X的溶解度和Y的溶解度相交于一点,说明二者的溶解度在此温度下相等, D正确。
备战中考化学压轴题专题复习—化学溶解度的综合附答案解析一、初中化学溶解度1.NaOH、Na2CO3分别在水、酒精中的溶解度如下表所示,结合图表数据下列说法正确的是NaOH Na2CO320℃40℃20℃40℃水109g129g21.8g49g酒精17.3g40g不溶不溶A.图表示Na2CO3在水、酒精中的溶解度曲线B.将CO2通入所得NaOH的酒精溶液中,无明显现象C.40℃时,将50gNaOH投入到100g酒精中,形成饱和溶液D.20℃升到40℃时,NaOH在水中的溶解度变化大于Na2CO3在水中的溶解度变化【答案】C【解析】【详解】A. 根据NaOH、Na2CO3分别在水、酒精中的溶解度数据可知,图表示NaOH在水、酒精中的溶解度曲线,此选项错误;B. 将CO2通入所得NaOH的酒精溶溶液中,2NaOH +CO2=Na2CO3 +H2O,由于碳酸钠在酒精中不能溶解,所以会有白色晶体析出,此选项错误;C. 40℃时,NaOH在酒精中的溶解度是40g,则将50gNaOH投入到100g酒精中,能形成饱和溶液,此选项正确;D. 20℃升到40℃时,NaOH在水中的溶解度变化是129g-109g=20g,20℃升到40℃时,Na2CO3在水中的溶解度变化是49g-21.8g=27.2g,所以Na2CO3的溶解度变化较大,此选项错误。
故选C。
2.图是A、B、C三种物质的溶解度曲线,当等质量的A、B、C三种物质的饱和溶液同时从t=2℃降温到t=1℃时,其中溶质质量分数没有发生改变的是A.AB.BC.CD.AB【答案】C【解析】试题分析:由题中所给的坐标曲线可知,A、B两物质的溶解度随温度升高而升高,C物质随温度的升高而降低,所以当等质量的A、B、C三种物质的饱和溶液同时从t=2℃降温到t=1℃时,C物质的溶解度增大,没有物质析出,所以溶质质量分数不变,A、B均有溶质析出,所以溶质质量分数减小。
考点:溶解度曲线的意义点评:关于溶解度曲线的题目属于中考必考的题型,通常在选择题较为靠后的位置出现,有一定的难度,考生应熟知基础知识点,仔细审题,理解其曲线的含义。
中考化学与化学溶解度有关的压轴题附详细答案一、初中化学溶解度1.甲、乙两种固体物质的溶解度曲线如图所示.下列叙述中正确的是()A.甲物质的溶解度大于乙物质的溶解度B.t1℃时,甲、乙两物质饱和溶液的溶质质量分数一定相等C.t2℃时,将30g甲物质放入70g水中,所得饱和溶液的质量为100gD.t2℃时,甲、乙两物质的饱和溶液降温到t1℃,析出晶体质量甲>乙【答案】B【解析】试题分析:A、比较物质的溶解度大小,须确定温度,不知温度,则无法比较,故错误;B、t1℃时,甲、乙物质的溶解度相等,饱和溶液的溶质质量分数= S/(100+S)×100%.甲、乙物质的饱和溶液的溶质质量分数相等,故正确;C、t2℃时,甲的溶解度是30g,100g水中最多溶解30g,30g甲溶解在70g水中形成溶液的质量=21g+70g=91g,不是100g溶液;故错误;D、甲、乙的饱和溶液的质量不确定,所以从t 2℃降到t1℃,析出晶体的质量也不确定,故错误;考点:溶解度曲线。
2.如图是A、B、C三种固体物质的溶解度曲线。
下列分析正确的是()A.t1℃时,A、C两种物质的饱和溶液中溶质的质量相等B.t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:3 C.将t2℃时A、B、C三种物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数的大小关系是B=C>AD.将t1℃时C的饱和溶液变为不饱和溶液,可采用的方法是升高温度【答案】B【解析】【详解】A 、t 1℃时,A 、C 两种物质的溶解度相等,但是饱和溶液的质量不能确定,所以饱和溶液中溶质的质量也不能确定,选项错误;B 、t 2℃时,A 物质的溶解度是50g ,所以把50gA 放入50g 水中能得到A 的饱和溶液,其中溶质和溶液的质量比为25g :75g =1:3,选项正确;C 、t 1℃时,B 物质的溶解度最大,A 、C 物质的溶解度相等,降低温度,A 、B 物质的溶解度减小,C 物质的溶解度增大,应该按照t 2℃时的溶解度计算,所以将t 2℃时A 、B 、C 三种物质的饱和溶液降温到t 1℃,所得溶液的溶质质量分数的大小关系是B >A >C ,选项错误;D 、C 物质的溶解度随温度的升高而减小,所以将t 1℃时C 的饱和溶液变为不饱和溶液,可采用的方法是降低温度,选项错误,故选B 。
中考化学与化学溶解度有关的压轴题及详细答案一、初中化学溶解度1.向t℃时饱和的Na2CO3溶液中加入ng无水Na2CO3,会析出mgNa2CO3·10H2O,则(m-n)的值为()A.饱和溶液失去水的质量B.饱和溶液失去溶质的质量C.饱和溶液失去水和溶质的质量之和D.其数值为0,即溶液质量不变【答案】C【解析】【详解】解:设原溶液共为xg,析出mg Na2CO3·10H2O后溶液为yg。
则x+n-m=y,解得,x-y=m-n,即饱和溶液失去水和溶质的质量之和=m-n;故选C。
2.下列有关溶液的说法中,错误的是A.外界条件不改变,溶质不会从溶液中分离出来B.餐具上的油污可利用洗涤剂的乳化功能将其洗去C.相同质量的同一溶质的饱和溶液一定比它的不饱和溶液所含的溶质多D.对于同一溶质的溶液,在同一温度时,其饱和溶液一定比其不饱和溶液浓【答案】C【解析】【分析】【详解】A、溶液是均一的,稳定的混合物,只要外界条件不改变,溶质就不会从溶液中分离出来,说法正确;故不符合题意;B、洗涤剂具有乳化作用,因此餐具上的油污可利用洗涤剂的乳化功能将其洗去,说法正确;故不符合题意;C、同种物质在不同温度下溶解度不同,因此相同质量的同一溶质的饱和溶液不一定比它的不饱和溶液所含的溶质多,说法错误,故不符合题意;D、由于温度一定,溶剂一定,根据溶解度可知,饱和溶液一定比不饱和溶液的质量分数更大;因此对于同一溶质的溶液,在同一温度时,其饱和溶液一定比其不饱和溶液浓,说法正确;故不符合题意;故选C【点睛】溶液是均一的、稳定的混合物,物质的溶解度随温度的变化而变化,若温度不变,则溶解3.几种固体物质在水中的溶解度如下表所示:温度/℃2030405060溶解度/gNaCl36.036.336.637.037.3KNO331.645.863.985.5110Ca(OH)20.170.150.130.120.11分析上表中的数据不能得出的结论是()A.KNO3在水中的溶解度随温度的升高而增大B.NaCl在水中的溶解度受温度变化影响不大C.固体物质在水中溶解度的大小与溶质的种类有关D.固体物质在水中溶解度的大小与溶剂的种类有关【答案】D【解析】【详解】A、由表中的数据可知,KNO3在水中的溶解度随温度的升高而增大,选项正确;B、由表中的数据可知,NaCl在水中的溶解度受温度变化影响不大,选项正确;C、由表中的数据可知,不同溶质的溶解度在同一温度的溶解度不同,可以得出固体物质在水中溶解度的大小与溶质的种类有关,选项正确;D、由题意可知,表中的数据是不同物质在水中的不同温度时的溶解度,溶剂相同,得不出固体物质在水中溶解度的大小与溶剂的关系,选项错误,故选D。