常见的酸和碱常见的酸第2课时上课用
- 格式:ppt
- 大小:2.37 MB
- 文档页数:15
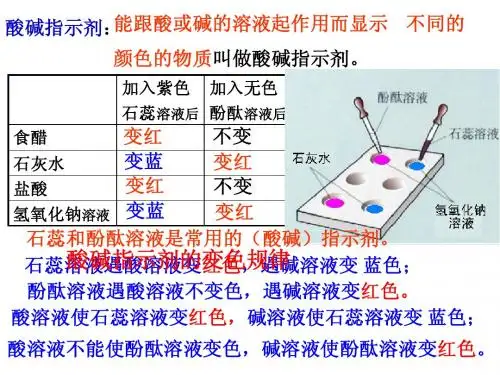



第二节常见的酸和碱(2)一、常见的酸一、教学设计说明本节课是常见酸和碱的第2课时,在第1节课中我们已初步了解了两种重要的酸盐酸和硫酸,本节课的目的是在复习原有与酸有关的知识,在此基础上归纳总结盐酸和硫酸的化学性质,并最后引导出酸具有通性的原因。
本节课的重点是酸的化学性质和金属活动性顺序。
通过对酸的学习,可以为碱和盐的学习打下基础,完善有机物之间的关系网络,同时探究酸的学习方法,可以为第3课时碱的学习提供知识基础和学习帮助。
二、教学目标(一)知识与技能:1.掌握酸的化学性质。
2.认识常见的酸在生产生活中的应用。
3.掌握常见金属的活动性顺序的意义及其应用;(二)过程与方法1.培养学生的观察和动手能力;2.培养学生学以致用,理论联系实际的能力;3.实验探究酸的化学性质,归纳酸具有共同性质的微观原因;4.实验探究金属活动性顺序的科学方法。
(三)情感态度与价值观培养学生热爱生活、热爱自然的情怀。
三、重点及难点重点:酸的化学性质;金属的活动性顺序;难点:对酸的相关性质化学方程戒指书写;金属的活动性顺序的应用。
实验探究一【实验1】将用砂纸打磨过的镁条和锌粒、铜片,分别放入到相同质量相同溶质质量分数的盐酸中。
【实验目的】是不是所有的金属都能和酸反应生成氢气;不同的金属与相同的酸反应的速度是否相同。
教师巡视,指导学生进行实验【实验结论】1.并不是所有的金属都能与酸反应生成氢气。
2.不同的金属与酸反应的速率不同。
【过渡】金属单质与酸溶液能否发生反应,发生反应的剧烈程度,可以说明金属的活动性强弱,人们通过反复的实验和研究,总结出了常见金属的活动性顺序。
【课件展示】课件第4页,金属活动性顺序表及其应用。
注意:A .在金属活动性顺序表中,排在氢前面的金属能置换出酸中的氢,排在氢后面的金属则不能;B.排在金属活动性顺序表越前面的金属,反应现象越剧烈,速度越快,如Mg反应有明显放热现象;【过渡】镁、锌、铁的活动性都在氢的前面,所以都能和稀硫酸或盐酸反应生成氢气,请同学们写出三种金属与盐酸反应的化学方程式。


课题1 常见的酸和碱(第二课时) 教学目标1.知识与技能(1)知道几种常见酸和碱的主要性质和用途。
(2)会用酸碱指示剂检验溶液的酸碱性。
(3)认识酸和碱的腐蚀性及使用时的安全注意事项。
(4)能完成简单的探究实验。
2.过程与方法(1)进一步认识和体验科学探究的过程。
(2)运用实验的方法获取信息,运用比较概括等方法对获取的信息进行加工。
(3)增强对化学现象的探究欲,发展善于合作、勤于思考的科学精神。
3.情感态度与价值观进一步增强探究物质的好奇心和求知欲。
教学重点1.运用酸碱指示剂检验溶液的酸碱性。
2.酸碱各自相似的化学性质。
教学难点酸和碱各自具有相似化学性质的原因。
教学方法复习、总结、联系实际、实验探究、巩固练习。
教具准备教师用具:仪器:烧杯、玻璃棒、锥形瓶、双孔塞、分液漏斗、短玻璃导管、镊子、投影仪;药品:浓硫酸、鸡爪、NaOH溶液(20%)。
学生用具:仪器:滴管、研钵、烧杯、纱布、纸、小木棍、布、玻璃片、玻璃棒、点滴板、镊子、表面皿、蒸发皿、溶液导电性实验仪器;药品:食醋、稀盐酸、稀硝酸、稀硫酸、食盐水、石灰水、氢氧化钠溶液、紫色石蕊试液、无色酚酞试液、酒精、花(果实)、浓盐酸、浓硫酸、生锈的铁钉、NaOH固体、生石灰、蒸馏水。
课时安排3课时第一课时:酸和碱溶液与酸碱指示剂的反应。
第二课时:几种常见酸和碱的主要性质和用途。
第三课时:酸和碱各自具有相似化学性质的原因。
教学过程[引入]上节课我们学习了酸碱指示剂,并熟悉了几种酸和碱,这节课我们重点探讨几种酸和碱的性质和用途。
[板书]二、几种常见的酸[活动与探究](投影展示)(1)观察盐酸、硫酸的状态。
(2)分别打开盛有浓盐酸、硫酸的试剂瓶的瓶盖,观察现象并闻气味。
盐酸硫酸颜色、状态打开瓶盖后的现象气味[教师]强调闻气味的方法。
[学生活动][讨论交流][总结]无色液体无色液体瓶口出现白雾无明显现象刺激性气味无味[引导]探究了盐酸、硫酸的一些简单性质,你是否想了解它们的用途呢?[投影]用途盐酸(HCl)重要化工产品。
第八章常见的酸、碱、盐8.2常见的酸和碱第2课时常见的碱碱溶液的化学性质教材解读本节课通过熟石灰的制取引导学生区分“石灰石”“生石灰”“熟石灰”,并解释生活中的一些现象。
通过对碱的化学性质的学习,鼓励学生大胆细心地独立完成实验,引导学生在实验过程中发现问题、提出假设、设计实验方案,让学生从实验中不仅获取有关知识并学习探究的方法,而且体验探究的乐趣。
通过分析、讨论,从碱的化学组成中找碱的共同点,认识碱具有共同性质的原因,学会通过表象挖掘事物所具有的共性和本质。
教学目标知识与技能1.认识氢氧化钠的吸水性和腐蚀性,了解其用途。
2.认识氢氧化钠和氢氧化钙的化学性质。
3.探究CO2和NaOH的反应。
过程与方法通过一些探究活动,进一步认识并体验科学探究的过程;学会用碱的有关性质解释生活中的一些现象。
情感、态度与价值观1.通过实验设计及实验分析,培养学生的创新能力。
2.通过学生亲身参与科学探究活动,激发学习化学的兴趣,培养学生尊重事实的科学态度,发展善于合作,勤于思考的科学精神。
教学重点教学难点,重点:认识碱的化学性质和用途。
难点:理解NaOH与CO2反应实验的设计。
教学环节教师活动学生活动设计意图活动探究二活动二:探究Ca(OH)2的性质及用途[材料引入]1.冬天园林工人用石灰浆将认真阅读材料,并进行思考、分析,回答问题。
联系生活实际,引出所讲化学物质,又从实验的角度感知若树干底部刷白。
2.用石灰砂浆砌砖抹墙很牢固。
3.装石灰水的试剂瓶用久后瓶壁上有一层白色的薄膜。
[问题] 上述材料中涉及的物质和化学性质是什么?[演示实验] 取生石灰加水观察现象。
[问题] 1.该实验的现象及反应的化学方程式是什么?2.Ca(OH)2的用途是什么?3.使用Ca(OH)2有哪些注意事项?认真观察实验现象,针对提出的问题进行思考,带着问题阅读教材,对Ca(OH)2的性质及用途进行归纳。
干关于氢氧化钙的知识。
学生在轻松的氛围中快乐学习的同时,真正体会到生活中处处有化学,并学以致用。



