脂肪酶测定试剂盒(甲基试卤灵底物法)产品技术要求baiding
- 格式:docx
- 大小:13.89 KB
- 文档页数:3

脂肪酶测定试剂盒(甲基试卤灵底物法) 适用范围:用于体外定量测定人血清中脂肪酶的活性。
1.1规格试剂1:2×60mL,试剂2:1×60mL;试剂1:2×60mL,试剂2:2×15mL;试剂1:3×40mL,试剂2:1×30mL;试剂1:2×60mL,试剂2:2×12mL;试剂1:2×60mL,试剂2:2×20mL;试剂1:1×45mL,试剂2:1×15mL;试剂1:1×4L,试剂2:1×1L;试剂1:2×4L,试剂2:1×2L。
1.2主要组成成分试剂1主要组分:试剂2主要组分:2.1 净含量应不低于试剂瓶标示装量。
2.2 外观试剂1:无色或淡黄色透明溶液;试剂2:无色或淡黄色透明溶液。
外包装完好、无破损,标签完好、字迹清晰。
2.3 试剂空白2.3.1 试剂空白吸光度在570nm处测定试剂空白吸光度,应≤0.9;2.3.2 试剂空白吸光度变化率试剂空白吸光度变化率△A/min≤0.5。
2.4 分析灵敏度测试50U/L的被测物时,吸光度变化率(ΔA/min)应不低于0.0025 。
2.5 准确度在样品中加入一定体积的纯品,计算回收率,应介于90%-110%之间。
2.6 重复性批内变异系数(CV)应不超过10%。
2.7 线性2.7.1在[5,500]U/L区间内,线性相关系数r应不低于0.990;2.7.2[5,60)U/L区间内绝对偏差不超过±7.2U/L;[60,500]U/L区间内相对偏差不超过±12%。
2.8 批间差对同一份样品进行重复测定,相对极差不大于12%。
2.9 稳定性取在2℃~8℃条件下贮存达到12个月后的试剂进行检测,应符合本标准2.2、2.3、2.4、2.5、2.6、2.7之规定。
脂肪酶测定试剂盒(甲基试卤灵底物法)适用范围:用于体外定量测定人血清或血浆中脂肪酶的含量。
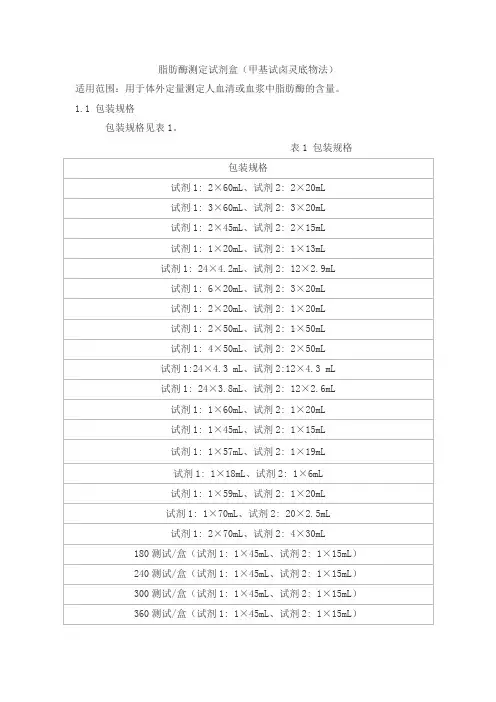
1.1 包装规格包装规格见表1。
表1 包装规格1.2 试剂成分试剂成分见表2。
表2 试剂成分注:不同批号的校准品、质控品赋值有差异。
2.1 外观试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂2为橘黄色到橘红色液体,目测不得有任何沉淀及絮状悬浮物;校准品为黄色粉末状物质,复溶后为淡黄色或黄色液体,目测不得有任何沉淀及絮状悬浮物;质控品微黄色粉末状物质,复溶后为淡黄色或黄色液体,目测不得有任何沉淀及絮状悬浮物。
试剂盒标签标识清晰,外包装完整无损。
2.2 净含量试剂的净含量应不少于标称量。
2.3 试剂空白吸光度A570nm下测定空白吸光度应≤ 0.8000。
2.4 准确度与已上市产品进行比对试验:在[5,300]U/L区间内,线性相关系数r≥0.975,在[5,50]U/L区间内测定的绝对偏差应不超过±7.5U/L,在(50,300]U/L 区间内测定的相对偏差应不超过±15%。
2.5 分析灵敏度样本浓度为100 U/L时,其吸光度变化率在0.0150~0.0450之间。
2.6 线性区间在[5,300]U/L区间内,线性相关系数r≥0.990,在[5,50]U/L区间内测定的绝对偏差应不超过±7.5U/L,在(50,300]U/L区间内测定的相对偏差应不超过±15%。
2.7 测量精密度2.7.1重复性对高、低浓度的血清样本或质控品重复测定10次,其测定值的变异系数(CV%)应不大于5%。
2.7.2批间差随机抽取三批试剂盒的批间相对极差(R)应不大于10%。
2.8 瓶间差校准品、质控品的瓶间差应≤10%。
2.9 稳定性2.9.1 效期稳定性试剂在2℃~25℃密封避光保存,校准品、质控品在2℃~8℃密封避光保存,有效期为12个月。
在试剂盒有效期满后一个月以内,分别检测2.1、2.3、2.4、2.5、2.6、2.7.1项,结果应符合各项目的要求。

脂肪酶测定试剂盒(甲基试卤灵底物法)适用范围:用于体外定量测定人血清中脂肪酶的活性。
1. 产品型号/规格及其划分说明1.1规格规格1(试剂1:15ml×1;试剂2:5ml×1);规格2(试剂1:30ml×1;试剂2:10ml×1);规格3(试剂1:60ml×1;试剂2:20ml×1);规格4(试剂1:60ml×2;试剂2:20ml×2);规格5(试剂1:60ml×3;试剂2:20ml×3);校准品(选配):规格1(0.3ml×1;1水平);规格2(0.5ml×1;1水平);规格3(1.0ml×1;1水平);质控品(选配):规格1(0.3ml×2;2水平);规格2(0.5ml×2;2水平);规格3(1.0ml×2;2水平);1.2组成试剂盒组成见表1表1 脂肪酶测定试剂盒组成2.1外观试剂盒外观应整洁,液体无渗漏,文字符号标识清晰;试剂1为无色透明液体,试剂2为无色至橙黄色透明液体,不得有沉淀和絮状物。
校准品和质控品为无色至淡黄色液体。
2.2 装量每瓶不少于标示值。
2.3试剂空白吸光度用指定的空白样品测试试剂(盒),在光径1cm下,在波长570nm处测定试剂空白吸光度A≤0.50;试剂空白吸光度变化率△A/min≤0.010A。
2.4分析灵敏度试剂测定50U/L被测物,吸光度变化率△A/min≥ 0.005。
2.5线性范围2.5.1在[4,300]U/L内,相关系数R≥0.990。
2.5.2[4,100] U/L内,线性绝对偏差不超过±10U/L;在(100, 300)U/L内,线性相对偏差不超过±10%。
2.6精密度2.6.1重复性重复测试(50±10) U/L 和(150±30)U/L的样本,所得结果的变异系数(CV%)应不大于5%。

脂肪酶测定试剂盒(甲基试卤灵底物法)适用范围:本试剂用于体外定量测定人血清或血浆中脂肪酶的活性。
1.1规格液体双剂型试剂1(R1):40mL×1,试剂2(R2):10mL×1;试剂1(R1):60mL×1,试剂2(R2):15mL×1。
1.2规格划分说明根据净含量划分规格。
1.3主要组成成分试剂盒由试剂1(R1)液体和试剂2(R2)液体组成。
1.3.1 试剂1(R1)液体:甘氨酸 450mmol/L 氢氧化钠 3.6mmol/L 共脂肪酶 1mg/L脱氧胆酸钠 1.6mmol/L 1.3.2 试剂2(R2)液体:酒石酸缓冲液 19mmol/L脂肪酶生色底物 3.4mmol/L2.1 外观试剂盒中各组件的外观应满足:a) 试剂1 (R1)应为无色透明溶液,无杂质、无絮状物,外包装完整无破损;b) 试剂2 (R2)应为橙色至红色微浊液体,外包装完整无破损。
2.2 试剂空白2.2.1 试剂空白吸光度在波长570nm(550nm~600nm)(光径1cm)处,试剂空白吸光度(A)应≤0.7000。
2.2.2试剂空白吸光度变化率在波长570nm(550nm~600nm)(光径1cm)处,试剂空白吸光度变化率(△A/min)≤ 0.200。
2.3.准确度测定BCR693,相对偏差应不超过±15%。
2.4分析灵敏度对应于浓度为100U/L的脂肪酶所引起的吸光度变化率(△A/min)的绝对值应在0.020 ~0.200的范围内。
2.5重复性重复测定高、中、低浓度样本,变异系数(CV)应≤15%。
2.6批间差测定同一样本,批间差(R)应≤15%。
2.7线性范围在[3,300]U/L范围内,线性相关系数(r)应≥0.990;在(50,300]U/L范围内,线性相对偏差应不超过±10%;在[3,50]U/L范围内,线性绝对偏差应不超过±5U/L。
2.8稳定性原包装的试剂盒在2℃~8℃避光贮存,有效期为12月。

脂肪酶测定试剂盒(甲基试卤灵底物法)适用范围:本试剂适用于体外定量测定人血清或血浆中脂肪酶活性。
1.1规格试剂1(R1):4×70ml 试剂2(R2):1×70ml试剂1(R1):4×50ml 试剂2(R2):2×25ml试剂1(R1):2×64ml 试剂2(R2):2×16ml试剂1(R1):2×80ml 试剂2(R2):1×40ml试剂1(R1):4×45ml 试剂2(R2):1×45ml试剂1(R1):1×64ml 试剂2(R2):1×16ml2.1外观2.1.1包装完整,标签清晰;2.1.2试剂1为无色透明溶液、无悬浮物、无沉淀物;试剂2为橘红色微乳液。
2.2净含量试剂盒内液体的装量应不低于标示值。
2.3试剂空白2.3.1 试剂空白吸光度用试剂盒测定空白样本,记录试剂盒在570nm波长条件下,试剂空白吸光度A应不大于0.50。
2.3.2 试剂空白吸光度变化率试剂吸光度变化率(△A/min)应不超过0.035。
2.4分析灵敏度测定50U/L样本时,吸光度变化率(△A/min)应符合:0.010~0.150。
2.5线性范围试剂盒线性范围在[3.0,300.0]U/L:线性相关系数r≥0.990;在[3.0,30]U/L线性范围内,绝对偏差不超过±3 U/L;在(30,300]U/L线性范围内,相对偏差不超过±10%。
2.6测量精密度2.6.1重复性用高、低2个水平的血清样品或质控品测试同一批号试剂盒,测试结果应符合CV≤10%。
2.6.2 批间差用3个不同批号的试剂盒测定同一份样本,测得结果极差R≤10%。
2.7准确度以选定的上市分析系统对照试剂作为比对方法进行方法学比对测试,比对结果应满足:a)在[3.0,300]U/L 范围内,线性相关系数r≥0.975;b)在[3.0,30]U/L 范围内,绝对偏差不超过±3 U/L;在(30,300]U/L范围内,相对偏差不超过±10%。

脂肪酶测定试剂盒(甲基试卤灵底物法)适用范围:本试剂盒用于体外定量测定人血清中的脂肪酶的活性浓度。
1.1产品规格1.2产品组成试剂1:BICN缓冲液(pH8.0)50mmol/L,脱氧胆酸钠1.6mmol/L,氯化钙10mmol/L,共脂肪酶≥1mg/L。
试剂2:酒石酸缓冲液(pH4.0)10mmol/L,牛黄脱氧胆酸盐8.8mmol/L,1,2-邻-二月桂基-消旋-甘油-3-戊二酸-(6-甲基试卤灵)酯0.27mmol/L。
2.1 外观试剂1为无色透明溶液,试剂2为黄色透明溶液;试剂盒各组分齐全、完整,液体无渗漏,包装标签文字符号清晰牢固不易脱落,外包装完整无破损。
2.2 装量液体试剂的净含量应不少于标示量。
2.3 试剂空白吸光度在37℃、570nm波长、1cm光径条件下,试剂空白吸光度应不大于0.80。
2.4分析灵敏度测定80U/L脂肪酶时,吸光度变化率在(0.04±0.02)/min范围内。
2.5 准确度采用比对试验,相关系数r≥0.98;[3,30]U/L区间内,线性绝对偏差不超过±3U/L;(30,300]U/L区间内,线性相对偏差不超过±10% 。
2.6 精密度2.6.1 重复性用血清样品或质控样品重复测试所得的变异系数(CV)应不大于10.0%。
2.6.2 批间差试剂(盒)批间相对极差应不大于10.0%。
2.7 线性区间试剂线性在[3,300]U/L(37℃)区间内:a) 线性相关系数|r|应不小于0.990;b) [3,30]U/L区间内,线性绝对偏差应不超过±3U/L;(30,300]U/L区间内,线性相对偏差应不超过±10%。
2.8稳定性原包装试剂2~8℃避光保存有效期12个月,到效期后的样品检测试剂空白、分析灵敏度、准确度、重复性、线性区间应符合2.3、2.4、2.5、2.6.1、2.7的要求。

脂肪酶(LPS)测定试剂盒(甲基试卤灵底物法)适用范围:本产品用于体外定量测定人血清或血浆中脂肪酶的含量。
1.1 包装规格试剂1(R1):2×40mL;试剂2(R2):2×20mL;校准品(选配):1×5mL。
1.2 主要组成成分试剂盒由试剂和校准品(选配)组成。
试剂1(R1):PB缓冲液:100mmol/L pH=7.2;牛磺脱氧胆酸:34mmol/L;NaCl:40mmol/L。
试剂2(R2)(启动液):酒石酸缓冲液:9.5mmol/L,pH=4.0;共脂肪酶:500KU/L;1,2邻-二月桂宗甘油-3-戊二酸-(6’-甲基试卤灵)-酯:0.20mmol/L。
校准品:单水平冻干品,在牛血清基质中添加脂肪酶,定值范围:(80~200)U/L。
稳定剂<0.1%。
注:校准品浓度具有批特异性,具体浓度见标签。
2.1 外观液体双试剂:试剂1(R1)(缓冲液):无色透明液体,试剂2(R2)(启动液):桔红色液体。
校准品:冻干品,溶解后无色至浅黄色液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 溯源性根据GB/T 21415及有关规定提供校准品的来源、赋值过程及测量不确定度等内容,该校准品溯源至利德曼企业标准品,且与已上市产品比对赋值。
2.4 试剂空白2.4.1空白吸光度在37℃、(570nm±10%范围内的)波长、1cm光径条件下,用去离子水或(生理盐水)作为样品加入试剂测试时,试剂空白吸光度应<0.5 ABS。
2.4.2空白吸光度变化率在37℃、(570nm±10%范围内的)波长、1cm光径条件下,用去离子水或(生理盐水)作为样品加入试剂测试时,试剂空白吸光度变化率(ΔA/min)应≤0.015 ABS/min。
2.5 分析灵敏度浓度为50U/L时,吸光度变化范围在(0.01~0.15)之间。
2.6 线性在[4,700]U/L线性范围内,线性相关系数r2≥0.996。

血清脂肪酶测定标准操作规程1 检验申请单独检验项目申请:血清脂肪酶(缩写LPS)测定;组合项目申请:胰腺炎检测。
临床医生根据需要提出检验申请。
2 标本采集与处理2.1标本采集2.1.1常规静脉采血约2 ml,不抗凝,置普通试管中。
或采用含分离胶的真空采血管。
2.1.2检验申请单和血标本试管标上统一且唯一的标识符。
2.1.3急诊标本采集后,在检验申请单上填写标本采集时间。
2.1.4标本采集后与检验申请单一起及时运送至检验科。
专人负责标本的接收并记录标本的状态,对不合格标本予以拒收。
2.1.5下列标本为不合格标本2.1.5.1标本量不足:少于0.3ml的全血标本,或少于0.1ml的血清或血浆。
2.1.5.2对反应吸光度有干扰的标本,包括严重溶血标本。
2.1.5.3无法确认标本与申请单对应关系的。
2.1.5.4其他如标识涂改、标本试管破裂等。
2.2标本保存2.2.1接收标本后在30min内将标本离心分离出血清。
2.2.2标本保存时间:室温(15~25℃)下可稳定1天,普通冰箱中(2~8℃)稳定7天。
-20℃可保存数月;-70℃至少可保存半年;应避免标本反复冻溶。
为避免标本中水分挥发使血清浓缩,对保存时间超过1天的标本均加塞密闭或覆盖湿巾。
2.2.3已完成测试的标本保持完整的识别号,置4~8℃冰箱内保存7天。
2.3标本采集的注意事项2.3.1采血前使受检者保持平静、松弛和空腹状态。
抽血前3天内避免高脂饮食,24小时内不饮酒。
2.3.2如果使用血浆,推荐的抗凝剂是肝素。
EDTA、草酸盐、氟化钠、枸橼酸对酶有抑制作用。
2.1.5 抽血前最好停用影响血脂的药物(如调脂药、避孕药、某些降压药、激素等)数天或数周,否则应记录用药情况。
3 方法原理采用1,2-邻-二月桂宗甘油-3-戌二酸-(6'-甲基试卤灵)-酯作为底物,OH-脂肪酶1,2-邻-二月桂宗甘油-3-戌二酸-(6'-甲基试卤灵)-酯 ----------1,2-邻-二月桂宗甘油 + 戌二酸 + 甲基试卤灵在570nm波长下,根据产物红色的甲基试卤灵生成速率测定脂肪酶的活性。

脂肪酶测定试剂盒(甲基试卤灵底物法)适用范围:本产品用于体外定量测定人血清中脂肪酶的活性。
1.1 规格具体产品规格见下表:1.2 组成成分1.2.1 试剂的组成试剂1:BICINE 缓冲液≥50mmol/L牛磺脱氧胆酸≥3.4mmol/L去氧胆酸≥1.6mmol/L 氯化钙≥10mmol/L共脂肪酶≥1mg/L试剂2:1,2-邻-二月桂基甘油-3-戌二酸-(6'-甲基试卤灵)-酯≥0.20mmol/L酒石酸缓冲液≥9.5mmol/L牛磺脱氧胆酸≥8.8mmol/L稳定剂适量1.2.2 校准品的组成(选配)水平1:脂肪酶(20.0~60.0)U/L该校准品为血清基质冻干校准品水平2:脂肪酶(55.0~200.0)U/L该校准品为血清基质冻干校准品1.2.3 质控品的组成(选配)水平1:脂肪酶(20.0~60.0)U/L该质控品为血清基质冻干质控品水平2:脂肪酶(60.1~200.0)U/L该质控品为血清基质冻干质控品校准品、质控品有批特异性,具体靶值见靶值表。
2.1 外观2.1.1 外包装完整无破损;2.1.2 试剂1:无色澄清透明无杂质的液体;2.1.3 试剂2:黄色或橙色澄清无杂质的液体;2.1.4 校准品:白色或浅黄色冻干粉,复溶后为浅黄色溶液,无不溶物;2.1.5 质控品:白色或浅黄色冻干粉,复溶后为浅黄色溶液,无不溶物。
2.2 净含量净含量不低于标示值。
2.3 试剂空白2.3.1 试剂空白吸光度在主波长570nm、副波长700nm、37℃条件下,试剂空白吸光度不大于0.5;2.3.2 试剂空白吸光度变化率在主波长570nm、副波长700nm、37℃条件下,试剂空白吸光度变化率不大于0.01。
2.4 线性2.4.1 线性范围[20.0,200.0]U/L,相关系数r不小于0.990。
2.4.2 线性偏差(60.0,200.0]U/L线性范围内,相对偏差不超过±10%;[20.0,60.0]U/L线性范围内,绝对偏差不超过±6.0U/L。
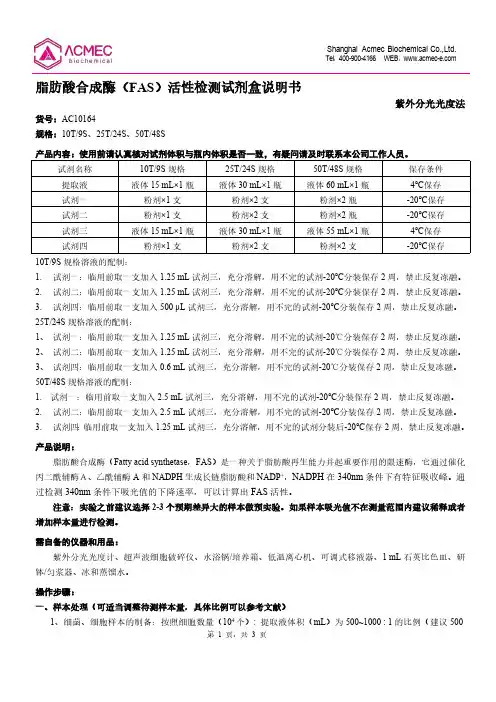
第 1 页,共 3 页脂肪酸合成酶(FAS )活性检测试剂盒说明书紫外分光光度法货号:AC10164规格:10T/9S 、25T/24S 、50T/48S产品内容:使用前请认真核对试剂体积与瓶内体积是否一致,有疑问请及时联系本公司工作人员。
试剂名称10T/9S 规格25T/24S 规格50T/48S 规格保存条件提取液液体15 mL×1瓶液体30 mL×1瓶液体60 mL×1瓶4℃保存试剂一粉剂×1支粉剂×2支粉剂×2瓶-20℃保存试剂二粉剂×1支粉剂×2支粉剂×2瓶-20℃保存试剂三液体15 mL×1瓶液体30 mL×1瓶液体55 mL×1瓶4℃保存试剂四粉剂×1支粉剂×2支粉剂×2支-20℃保存10T/9S 规格溶液的配制:1.试剂一:临用前取一支加入1.25 mL 试剂三,充分溶解,用不完的试剂-20℃分装保存2周,禁止反复冻融。
2.试剂二:临用前取一支加入1.25 mL 试剂三,充分溶解,用不完的试剂-20℃分装保存2周,禁止反复冻融。
3.试剂四:临用前取一支加入500 μL 试剂三,充分溶解,用不完的试剂-20℃分装保存2周,禁止反复冻融。
25T/24S 规格溶液的配制:1、试剂一:临用前取一支加入1.25 mL 试剂三,充分溶解,用不完的试剂-20℃分装保存2周,禁止反复冻融。
2、试剂二:临用前取一支加入1.25 mL 试剂三,充分溶解,用不完的试剂-20℃分装保存2周,禁止反复冻融。
3、试剂四:临用前取一支加入0.6 mL 试剂三,充分溶解,用不完的试剂-20℃分装保存2周,禁止反复冻融。
50T/48S 规格溶液的配制:1.试剂一:临用前取一支加入2.5 mL 试剂三,充分溶解,用不完的试剂-20℃分装保存2周,禁止反复冻融。
2.试剂二:临用前取一支加入2.5 mL 试剂三,充分溶解,用不完的试剂-20℃分装保存2周,禁止反复冻融。

脂肪酶测定试剂盒(甲基试卤灵底物法)适用范围:用于体外定量检测人血清脂肪酶(LPS)活性。
1.1包装规格a) 试剂1:2×40ml,试剂2: 2×20ml;b) 试剂1:2×200ml,试剂2: 2×100ml;c) 试剂1:12×16ml,试剂2: 12×8ml;d) 试剂1:1×20ml,试剂2: 1×10ml。
1.2试剂主要组成成分试剂1主要组成成分BICIN缓冲液100mmol/l牛磺脱氧胆酸 34mmol/L氯化钠 40mmol/L试剂2主要成成分酒石酸缓冲液 9.5mmol/L共脂肪酶 500 U/L1,2-邻-二月桂宗甘油-3-戊二酸-(6-甲基试卤灵)-酯0.2mmol/L 2.1 外观和性状2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;外包装完好、无破损,标签完好、字迹清晰。
2.1.2 试剂1应为无色或淡粉色液体,无沉淀、无悬浮物、无絮状物。
2.1.3 试剂2应为橙黄色液体,无沉淀、无悬浮物、无絮状物。
2.2 净含量液体试剂的净含量应不少于标示值。
2.3 试剂空白2.3.1 试剂空白吸光度在570nm处测定试剂空白吸光度,应<0.5。
2.3.2 试剂空白吸光度变化率试剂空白吸光度变化率△A/min≤0.01。
2.4 分析灵敏度测试500U/L的被测物时,吸光度变化率(ΔA/min)应不低于0.05。
2.5 准确性与比对试剂盒同时测试40例线性范围内的不同浓度的血清样本,样本浓度在(4,700)U/L范围内,其相关系数(r)≥0.975;测定浓度点在(4,100]U/L范围内绝对偏差不超过±15U/L;测定浓度在(100,700)U/L范围内相对偏差不超过±15%。
2.6 重复性批内变异系数(CV)应不超过5%。
2.7 线性2.7.1在(4,700)U/L区间内,线性相关系数r应不低于0.990;2.7.2 在(100,700)U/L区间内,相对偏差不超过±10%;在(4,100]U/L区间内,绝对偏差不超过±10U/L。
脂肪酶测定试剂盒(甲基试卤灵底物法)
适用范围:适用于体外定量测定人血清中脂肪酶的含量。
1.1 产品规格
1.2主要组成成分
2.1外观
2.1.1试剂盒标签标识清晰,外包装完整无破损;
2.1.2试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;
2.1.3试剂2为黄色澄清液体,目测不得有任何沉淀及絮状悬浮物。
2.2净含量
净含量不低于标示值。
2.3试剂空白
2.3.1 空白吸光度
测定待检试剂在主波长570nm、副波长700nm、37℃条件下:A≤1.0;
2.3.2 空白吸光度变化率
空白吸光度变化率△A/min≤0.01。
2.4 线性范围
(10,260)U/L范围内,相关系数r≥0.990;
(10,50]U/L范围内,绝对偏差不超过±5U/L;
(50,260)U/L范围内,相对偏差不超过±10.0%。
2.5分析灵敏度
在产品说明书规定参数设定条件下,测定浓度为78U/L的样本,△A/min ≥0.02。
2.6 精密度
2.6.1批内重复性
CV≤10.0%。
2.6.2 批间差
相对极差R≤10.0%。
2.7 准确度
与已上市产品比对:(10,260)U/L范围内,相关系数r≥0.990;(10,50]U/L范围内,绝对偏差不超过±5U/L;(50,260)U/L范围内,相对偏差不超过±10.0%。
2.8 稳定性
未开封试剂2℃~8℃储存,可稳定12个月。
取到效期后2个月内产品进行检测, 检测结果应满足2.3、2.4和2.7的规定。
脂肪酶测定试剂盒技术审评要点概述杨笑鹤;寇艳芹;董沁芳;叶朝付;甄辉【摘要】脂肪酶是急性胰腺炎诊断的重要参考指标,目前脂肪酶测定试剂盒尚无国家标准及行业标准发布.文章从产品说明书、产品技术要求、临床评价等方面对该试剂盒在技术审评中的要点进行简要概述,旨在帮助注册申报人更好地把握产品的技术要点,有效指导注册申报工作.【期刊名称】《中国医疗器械信息》【年(卷),期】2017(023)015【总页数】3页(P33-35)【关键词】体外诊断试剂;脂肪酶;技术审评要点【作者】杨笑鹤;寇艳芹;董沁芳;叶朝付;甄辉【作者单位】浙江省医疗器械审评中心浙江杭州 310012;浙江省医疗器械审评中心浙江杭州 310012;浙江省医疗器械审评中心浙江杭州 310012;浙江省医疗器械审评中心浙江杭州 310012;浙江省医疗器械审评中心浙江杭州 310012【正文语种】中文【中图分类】R197.39Abstract: Lipase is an important reference indicatiors of risk stratifying acute pancreatitis. Currently there is no national standard existed, no industry standard is published. A research is carried out focused on in the product technical requirements, the brochures, the clinical evaluationl andother aspects in this paper. We hope it will help the manufacturer grasp of the key points of the product and help the registration application effectively.Key words: in vitro diagnostic reagents, lipase, evaluation guidance急性胰腺炎具有起病迅急、病情凶险,病死率高的特点,所以早期及时而正确的诊断显得尤为重要。
脂肪酶(LPS)活性检测试剂盒说明书可见分光光度法货号:UPLC-MS-4404规格:50T/48S产品组成:使用前请认真核对试剂体积与瓶内体积是否一致,有疑问请及时联系工作人员。
试剂名称规格保存条件试剂一液体80mL×1瓶4℃保存试剂二液体10mL×1瓶常温保存试剂三液体20mL×1瓶4℃保存标准品液体59.3μL×1支4℃保存溶液的配制:标准品:临用前加入 1.435mL无水乙醇配成125µmol/mL的油酸标准溶液,充分溶解。
用前注意解冻溶解。
产品说明:LPS又称甘油酯水解酶,催化甘油三酯水解生成脂肪酸和甘油(或者甘油二酯和单酯)。
LPS广泛的存在于各种生物中。
血清中LPS的异常增高常见于胰腺炎和胰腺癌。
LPS催化油酯水解成脂肪酸,利用铜皂法测定脂肪酸生成速率,即可计算LPS活性。
注意:实验之前建议选择2-3个预期差异大的样本做预实验。
如果样本吸光值不在测量范围内建议稀释或者增加样本量进行检测。
需自备的仪器和用品:研钵/匀浆器、台式离心机、震荡混匀器、可见分光光度计、1mL玻璃比色皿、可调式移液枪、甲苯、无水乙醇、冰和蒸馏水。
操作步骤:一、样本处理(可适当调整待测样本量,具体比例可以参考文献)组织样本:称取约0.1g样本,加试剂一1.0mL充分研磨,于4℃,15000rpm离心30min,取上清液待测。
血清样本:直接检测。
二、测定步骤1、分光光度计预热30min以上,调节波长至710nm,甲苯调零。
2、试剂一和试剂二置于37℃水浴预热30min以上。
3、标准溶液的稀释:将125µmol/mL的油酸标准溶液用无水乙醇稀释为125、62.5、31.25、15.625、7.8125、3.9µmol/mL的标准溶液待测。
4、操作表:加入试剂(mL)空白管测定管标准管试剂一0.3750.3750.375试剂二0.1250.1250.125反复震荡混匀蒸馏水0.2上清液/血清0.2标准溶液0.2迅速震荡混匀后置于37℃水浴准确反应10min甲苯111反复震荡混匀后,室温4000rpm离心10min取出离心管,小心吸取上层溶液0.9mL,加入另一2mL塑料离心管中,按下表操作:试剂三0.2250.2250.225反复震荡混匀;室温4000rpm离心10min,小心吸取上层溶液800μL,加入1mL玻璃比色皿,于710nm处测定吸光值。
脂肪酶测定试剂盒(甲基试卤灵底物法)适用范围:用于体外定量测定人血清中脂肪酶的活性。
1.1规格
1.2组成
2.1 外观
2.1.1试剂1:无色液体,无浑浊,无不溶物。
2.1.2试剂2:黄色液体,无浑浊,无不溶物。
2.1.3包装外观应整洁,标签字迹清晰,不易脱落。
2.2 净含量
液体试剂的净含量不低于标示体积。
2.3 试剂空白
2.3.1试剂空白吸光度
试剂空白吸光度≤0.5。
2.3.2试剂空白吸光度变化率
试剂空白吸光度变化率(ΔA/分)≤0.05。
2.4 分析灵敏度
样本浓度为50 U/L时,ΔA/分≥0.01。
2.5 线性区间
在[5,300] U/L范围内,线性相关系数r≥0.990;测试浓度在[5,50] U/L时,绝对偏差不超过±5 U/L,测试浓度在(50,300] U/L时,相对偏差不超过±10%。
2.6 精密度
2.6.1 批內精密度
用高、中、低3个浓度的样本测试试剂盒,各重复测试10次,其变异系数(CV)
应不大于10%。
2.6.2批间差
用样本分别测试3个不同批次的试剂盒,每个批次测试3次,其相对极差(R)应不大于10%。
2.7 准确度
回收率在85%-115%范围内。
2.8稳定性
原包装试剂盒在2℃~8℃避光保存条件下有效期为12个月。
有效期满后3个月内测试,应满足2.3、2.4、2.5、2.6.1和2.7的要求。