第四章 立体化学 习 题
- 格式:doc
- 大小:70.50 KB
- 文档页数:2

上海交通大学网络教育学院医学院分院有机化学课程练习册第一章绪论一、是非题1.有机化合物是含碳的化合物。
〔〕2.有机化合物只含碳氢两种元素。
〔〕3.有机化合物的官能团也称为功能团。
〔〕4.sp3杂化轨道的形状是四面体形。
〔〕5.sp杂化轨道的形状是直线形。
〔〕6.sp2杂化轨道的形状是平面三角形。
〔〕7.化合物CH3-CH=CH2中双键的稳定性大于单键。
〔〕二、选择题1. 有机化合物的共价键发生均裂时产生〔〕A. 自由基B. 正离子C. 负离子D. 产生自由基和正碳离子2. 有机化合物的共价键发生异裂时产生〔〕A. 自由基B. 产生自由基和负碳离子C. 正碳离子或负碳离子D. 产生自由基和正碳离子三、填空题1. 以下化合物中的主要官能团2. 按共价键断裂方法不同,有机反响分为和两种类型。
3. 游离基反响中,反响物的共价键发生裂;离子型反响中,反响物的共价键发生裂。
第二章链烃一、是非题2. 甲烷与氯气光照下的反响属于游离基取代反响。
〔〕3. 乙烷只有交叉式和重叠式两种构象异构体。
〔〕4. 碳碳双键中的两条共价键都是 键。
〔〕CH 3CHCH 2CHCH 3CH 3CH 3 CH 3C CH 3CH CH 2C CH 5. 烯烃加溴的反响属于亲电加成反响。
〔 〕 6. 共轭体系就是 π-π 共轭体系。
〔 〕 二、选择题的一氯代产物有 〔 〕1. A. 1种 B.2种 C.3种 D.4种2. 含有伯、仲、叔、季碳原子的化合物 〔 〕3. 既有sp 3杂化碳原子,又有sp 2杂化碳原子的化合物是 〔 〕A. CH 3CH 2CH 3B. CH 3C ≡CHC. CH 2=CH 2D. CH 3CH=CH 24. 室温下能与硝酸银的氨溶液作用生成白色沉淀的是 〔 〕A. CH 3CH 2CH 3B. CH 3C ≡CHC. CH 3CH=CH 2D. CH 3CH=CHCH 35. 烯烃与溴水加成反响可产生的现象是 〔 〕A. 沉淀B. 气泡C. 褪色D. 无变化6. 在2-甲基戊烷分子中,叔碳原子的编号为 〔 〕A. 1B. 2C. 3D. 4三、填空题1. 烯烃的官能团为 ,炔烃的官能团为 。

第四章立体化学习题
4-1 命名或写出结构式。
(ⅰ)
(ⅱ)
(ⅲ)
(ⅳ)(Z)-2-氯-3-溴-2-丁烯
(ⅴ)(2Z,4Z)-2-溴-2,4-辛二烯
(ⅵ)顺-3,顺-5-二甲基环己-r-1-醇
4-2 将下列化合物改写成费歇尔投影式,并用R、S标记法标记其构型。
(ⅰ)(ⅱ)(ⅲ)(ⅳ)4-3 写出下列化合物的费歇尔投影式,并命名。
(ⅰ)(ⅱ)
(ⅲ)
4-4将下列构象按稳定性大小排列成序。
(ⅰ)(ⅱ)(ⅲ)(ⅳ)
4-5化合物1,3-二甲基环己烷(ⅰ)有几个构型异构体?用平面式表示其构型,并指出各异构体之间的关系。
(ⅱ)画出每个异构体的优势构象。
4-6 写出下列反应的主要产物。
(ⅰ)
(ⅱ)
(ⅲ)
(ⅳ)
4-7由(R)-2-丁醇〔α〕20D= -15O(10%甲醇溶液)制成对甲苯磺酸二级丁酯,然后用碱水解,得(S)-(+)--2-丁醇,〔α〕20D=+15O(10%甲醇溶液)。
用反应式表示改反应的立体化学过程,并加以解释。

第一章习题1.何为共价键的饱和性和方向性?2.下列分子中哪些具有极性键?哪些是极性分子?(1)CH4 (2) CH2C12 (3) CH3Br (4) CH3OH (5) CH30CH3 (6) HC=CH3.按碳架形状分类,下列化合物各属哪一类化合物?第二章习题1.用系统命名法命名下列化合物:(1) (CH3CH2)2CHCH3C2H5 (2) CH3CCH2CH3CH2CH2CH3CH3CH2 CH2CH3(3)\ c // \(CH3)3C CH(CH3)2(4) (C2H5)2CHCH(C2H5)CH2CH(CH3)2CH(CH3)2(5)CH3—CH—CH2—CH—CH—CH3CH2CH3 CH3CH2CH34.指出下列每个分子中存在的官能团类型:⑺ H3C ----- < C(CH3)3 (8)2. 写出下列化合物的构造式:(1) 由一个叔丁基和异丙基组成的烷炷; (2) 含一侧链甲基,分子量为98的环烷炫(3) 分子量为114,同时含有1°、2°、3。
、4。
碳的烷炷。
3.写出下列化合物的结构式,如其名称与系统命名原则不符,请予以改正。
(1)3, 3-二甲基丁烷 (2)2, 3-二甲基-2-乙基丁烷 (3) 4 -异丙基庚烷(4) 3> 4-二甲基-3 -乙基戊烷(5)3, 4, 5-三甲基-4-正丙基庚烷 ⑹2 -叔丁基-4, 5 -二甲基己烷4. 相对分子质量为72的烷任进行高温氯化反应,根据氯化产物的不同,推测各种烷炷的结构式。
(1)只生成一种一氯代产物(2)可生成三种不同的一氯代产物(3) 生成四种不同的一氯代产物 (4)只生成二种二氯代产物 5.不查表将下列烷炷的沸点由高至低排列成序: (1)2, 3-二甲基戊烷 (2) 2-甲基己烷 (3)正庚烷 (4) 正戊烷(5)环戊烷6. 写出下列化合物的优势构象—( 「CH2CH3 (1) BrCH 2CH 2Cl (2) CH 3CH 2CH 2CH 2CH 3 (3) '、'、—/(4)反-1-甲基-4-叔丁基环己烷7. 写出1, 3-二甲基环已烷和1-甲基-4-异丙基环已烷的顺、反异构体优势构象,并比较每组中哪个稳定。

立体化学(一) 在氯丁烷和氯戊烷的所有异构体中,哪些有手性碳原子?解:氯丁烷有四种构造异构体,其中2-氯丁烷中有手性碳:氯戊烷有八种构造异构体,其中2-氯戊烷(C 2*),2-甲基-1-氯丁烷(C 2*),2-甲基-3-氯丁烷(C 3*)有手性碳原子:(二) 各写出一个能满足下列条件的开链化合物:(1) 具有手性碳原子的炔烃C 6H 10;(2) 具有手性碳原子的羧酸C 5H 10O 2 (羧酸的通式是C n H 2n+1COOH)。
解: (1)(2)(三) 相对分子质量最低而有旋光性的烷烃是哪些?用Fischer 投影式表明它们的构型。
解: 和 和 (四) 是一个具有旋光性的不饱和烃,加氢后生成相应的饱和烃。
不饱和烃是什么?生成的饱和烃有无旋光性? 解:不饱和烃是或,生成的饱和烃无旋光性。
CH 3C CH 3CH 3ClCH 3CH 2CH 3ClCH 3CH 2CH 2CH 2Cl*3ClCH 3CH 2CH 3C CH 3CH 32ClCH 3(CH 2)4ClCH 3CH 2CH 2CHCH 3Cl CH 3CH 22CH 3ClCH 3CHCHCH 3CH 3CH 3CHCH 2CH 3CH 2ClCH 3CCH 2CH 3CH 3CH 3CHCH 2CH 2ClCH 3***CH 3CH 2CHC CH 3*CH 3CH 2CHCOOHCH 3*CH 2CH 32CH 2CH 3H CH 3CH 2CH 32CH 2CH 3H CH 3CH 2CH 3CH(CH 3)2H CH 3CH 2CH 3CH(CH 3)2HCH 3C 6H 12C 6H 12C 6H 12CH 2CH 3CH=CH 2H CH 3CH 2CH 3CH=CH 2H CH 3(五) 比较左旋仲丁醇和右旋仲丁醇的下列各项:(1) 沸点 (2) 熔点 (3) 相对密度 (4) 比旋光度 (5) 折射率 (6) 溶解度 (7) 构型 解: (1)、(2)、(3)、(5)、(6)相同;(4)大小相同,方向相反; (7)构型互为对映异构体。

第四章 脂环烃(习题和答案)一、命名下列化合物:1.2.1-甲基-2-异丙基环戊烷 1,6-二甲基螺[4.5]癸烷3. CH 3C 2H 54.1-甲基-2-乙基环戊烷 螺[3.4]辛烷5. 6. CH 3CH 3二环[2.2.1]庚烷 反-1,2-二甲基环丙烷7. CH(CH 3)28.Br异丙基环丙烷 5-溴螺[3.4]辛烷9.3)2310.顺-1-甲基-2-异丙基环己烷 2,7,7-三甲基二环[2.2.1]庚烷11.CH 312.Cl Cl6-甲基螺[2.5]辛烷 7,7-二氯二环[4.1.0]庚烷二、写出下列化合物的结构式:1、环戊基甲酸2、4-甲基环己烯COOHCH 33、二环[4.1.0]庚烷4、反-1-甲基-4-叔丁基环己烷 (CH 3)3CH 35、3-甲基环戊烯6、5,6-二甲基二环[2.2.1]庚-2-烯CH 3 CH 3CH 37、7-溴双环[2.2.1]庚-2-烯 8、2,3-二甲基-8-溴螺[4.5]癸烷HBrCH 3CH 3Br9、4-氯螺[2.4]庚烷 10、反-3-甲基环己醇ClCH11、8-氯二环[3.2.1]辛烷 12、1,2-二甲基-7-溴双环[2.2.1]庚烷ClCH 3H CH 3Br二、完成下列反应式:1.+CH 3O 2.+ CH 2CHClC OCH 33.CH 3CHCH 2CH 2+ HBr4.+COOEtCOOEtCH CH 2CH 3CH 3BrCOOEtCOOEt5.CH 3CH CH 2CH 2+ HCl6.CH 3+COOCH 3COOCH 3Cl CH CH 2CH 3CH 3COOCH 3CH 3COOCH 37.CH 3+CH 3COOCH 3COOCH 38. H 3CH 3CCH 2CH 3Cl 2+COOCH 3CH 3CH 3COOCH 3C 2H 5Cl C CH 2CH CH 3ClCH 39.+OCH 310. HBrH 3CH 3CCH 2CH 3+C OCH 3CH 3CH 3CH C CH CH 3Br11.CH OHCH CH 3KMnO 412.CH C +CH 3CH3KMnO 4CH 3CH OH OHCH H 3CC CH 3OCH 3+COOH13.H 2SO 4H 2O+CH 314.+COOCH 3CH 3OOCOH CH CH 2CH 3CH 33315.+CO 2CH 316. CHO+COOCH 3CHO17.+18. C O C O+OC O C OO19. +CH 3320.+COOCH 3COOCH 333COOCH 3COOCH321. NO 2CH 2+22. hvNO 2CH 2三、回答下列问题:1.请写出顺-1-甲基-4-叔丁基环己烷的稳定构象。
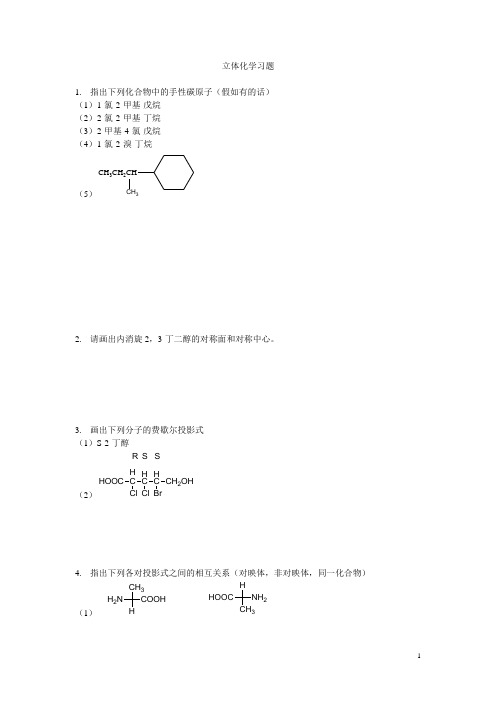
立体化学习题1.指出下列化合物中的手性碳原子(假如有的话)(1)1-氯-2-甲基-戊烷(2)2-氯-2-甲基-丁烷(3)2-甲基-4-氯-戊烷(4)1-氯-2-溴-丁烷(5)CH3CH2CHCH32.请画出内消旋2,3-丁二醇的对称面和对称中心。
3.画出下列分子的费歇尔投影式(1)S-2-丁醇(2)HCHOOCHCHC CH2OHR SS4.指出下列各对投影式之间的相互关系(对映体,非对映体,同一化合物)(1)H2NCH3COOH HOOCHNH23(2)HOHCH3OHCH3HHOCH3HOHHCH3(3)HOOCOHCH3H3C COOHOHHOCH3COOHHOOC OH35.下列化合物有几个手性碳?应有几个构型异构体?(1)CHOOHHOHHOHHCH2OH(2)CH2OHOHHOHHOHHCH2OH6.给出以下化合物中每个手性碳的构型。
(1)(2)HCH3OCH3OHCH3H(3)HCH2CH3CH3CH3CH2CH3 H7.你认为下列阐述那些是正确的?那些是错误的?(1)一对对映体总有实物和镜象的关系。
(2)所有手性分子都有非对映异构体。
(3)所有具有手性碳的化合物都是手性分子。
(4)有手性的化合物一定能被测出旋光度。
(5)具有R-构型的手性化合物必定有右旋的旋光方向。
(6)如果一个化合物没有对称平面,它必然是手性的。
(7)内消旋体和外消旋体都是非手性分子,因为它们都是无旋光性。
(8)构象异构都没有光学活性。
(9)对映异构体可通过单键旋转相互重合。
(10)某光学异构体经化学反应后得到构型符号相同的产物,因此反应过程中没有改变愿结构。
(11)每个对映异构体的构象只有一种,它们也呈对映关系。
(12)由一种异构体转变成其对映体时,必须断裂与手性碳相连的键。
8.某纯液体试样在1分米长的盛液管中测得的旋光度为+40度,怎样用实验手段证明它的旋光度确是+40度,而不是-320度或+400度?9.判断下列化合物是否为手性分子?10.(R)-3,4-二甲基-1-戊烯: CH2=CH(CH3)CH(CH3)2用Pt催化加氢还原时,写出反应式,并标明反应物、产物立体构型和命名。
⾼等有机化学习题⾼等有机化学习题第⼀章化学键⼀、⽤共振轮说明下列问题1)联本中的C 1-C 2键长为什么⽐⼄烷中的键长短?联苯的硝化反应为什么主要发⽣在2-位和4-位?联苯的共振结构式可表是如下:(1)由共振结构式可以看出C 1-C 2键有双键结构的贡献,故⽐⼄烷的C 1-C 2键短。
(2)由共振结构式可以看出邻对位负电荷相对集中,故有利于发⽣硝化反应。
2)⽅酸为什么是强酸?(强于硫酸)⽅酸的共振结构式可表是如下:对吗?由⽅酸的共振结构式可以看出⽅酸的电⼦离域效果更好。
⼆、试推测6,6-⼆苯基富烯的亲电取代发⽣于哪个环,哪个位置?亲核取代发⽣于哪个环,哪个位置?6,6-⼆苯基富烯的共振式如下:由6,6-⼆苯基富烯的共振式可以看出,亲电取代发⽣在五元环的2位上,⽽亲核取代发⽣在苯环的2位上。
三、计算烯丙基正离⼦和环丙烯正离⼦π分⼦轨道的总能量,并⽐较两者的稳定性。
烯丙基正离⼦有两个电⼦在成键轨道上其总能量为 E 烯丙基正离⼦=2E 1=2(α+1.414β)=2α+2.828β11'OH OOO OO HOOOO HO OOH OOO O S O OH OOS OO O H O S O O O HOS O O OH环丙烯正离⼦有两个电⼦在成键轨道上其总能量为E 环丙烯正离⼦=2E 1=2(α+2β)=2α+2β能量差值为E 烯丙基正离⼦- E 环丙烯正离⼦=(2α+2.828β)- (2α+2β)=0.828β因此,环丙烯正离⼦⽐烯丙基正离⼦稳定。
四、⽤HMO 法分别说明烯丙基负离⼦和环丙烯负离⼦的电⼦排布和成键情况,并⽐较两者稳定性。
五、简要说明1)吡咯和吡啶分⼦的极性⽅向相反,为什么?吡咯分⼦中氮原⼦给出⼀对为共⽤电⼦参与了共轭分⼦的⼤π键,也就是电⼦从氮原⼦流向五员环,⽽吡啶分⼦中氮原⼦只拿出⼀个电⼦参与共轭,并且氮原⼦的电负性⼤于碳原⼦使电⼦流向氮原⼦的⽅向。
因此,两个分⼦的极性正好相反。
配合物的立体化学习题答案配合物的立体化学习题答案配合物的立体化学是无机化学中的重要分支,它研究的是配合物分子中金属离子与配体之间的空间排布关系。
通过学习配合物的立体化学,我们能够更好地理解配合物的性质和反应机制。
下面是一些配合物的立体化学习题及其答案,希望能够对大家的学习有所帮助。
题目一:对于以下配合物,判断其是否具有光学活性。
1. [Co(en)3]3+2. [PtCl4]2-3. [Ni(CN)4]2-答案一:光学活性是指分子或离子具有旋光性质,即能够使偏振光产生旋光现象。
在配合物中,只有具有手性中心的配合物才会具有光学活性。
手性中心是指一个原子或一个原子团的排列方式,其镜像不能通过旋转或翻转重合的点。
根据这个定义,我们可以判断以下配合物的光学活性:1. [Co(en)3]3+:该配合物中的Co离子与三个en配体形成八面体结构,没有手性中心,因此不具有光学活性。
2. [PtCl4]2-:该配合物中的Pt离子与四个Cl配体形成四面体结构,没有手性中心,因此不具有光学活性。
3. [Ni(CN)4]2-:该配合物中的Ni离子与四个CN配体形成四面体结构,没有手性中心,因此不具有光学活性。
综上所述,以上三个配合物均不具有光学活性。
题目二:对于以下配合物,判断其是否具有光学异构体。
1. [Co(en)3]2+2. [Pt(NH3)2Cl2]3. [Cr(en)2Cl2]+答案二:光学异构体是指具有相同化学式但空间结构不同的化合物。
在配合物中,光学异构体的存在是由于配体的排列方式不同所导致的。
根据这个定义,我们可以判断以下配合物是否具有光学异构体:1. [Co(en)3]2+:该配合物中的Co离子与三个en配体形成八面体结构,en配体是双齿配体,可以形成两种不同的排列方式,因此具有光学异构体。
2. [Pt(NH3)2Cl2]:该配合物中的Pt离子与两个NH3配体和两个Cl配体形成四面体结构,NH3配体和Cl配体可以分别在Pt离子的两个顶点上排列,因此具有光学异构体。
第四章立体化学习题
4-1 命名或写出结构式。
(ⅰ)
(ⅱ)
(ⅲ)
(ⅳ)(Z)-2-氯-3-溴-2-丁烯
(ⅴ)(2Z,4Z)-2-溴-2,4-辛二烯
(ⅵ)顺-3,顺-5-二甲基环己-r-1-醇
4-2 将下列化合物改写成费歇尔投影式,并用R、S标记法标记其构型。
(ⅰ)(ⅱ)(ⅲ)(ⅳ)4-3 写出下列化合物的费歇尔投影式,并命名。
(ⅰ)(ⅱ)
(ⅲ)
4-4将下列构象按稳定性大小排列成序。
(ⅰ)(ⅱ)(ⅲ)(ⅳ)
4-5化合物1,3-二甲基环己烷(ⅰ)有几个构型异构体?用平面式表示其构型,并指出各异构体之间的关系。
(ⅱ)画出每个异构体的优势构象。
4-6 写出下列反应的主要产物。
(ⅰ)
(ⅱ)
(ⅲ)
(ⅳ)
4-7由(R)-2-丁醇〔α〕20D= -15O(10%甲醇溶液)制成对甲苯磺酸二级丁酯,然后用碱水解,得(S)-(+)--2-丁醇,〔α〕20D=+15O(10%甲醇溶液)。
用反应式表示改反应的立体化学过程,并加以解释。