有机物C5-C1沸点
- 格式:xlsx
- 大小:27.79 KB
- 文档页数:4

有机化合物沸点高低的判断有机化合物的沸点高低,这可真是个有趣的话题啊!你知道吗,就好像人有高矮胖瘦之分,有机化合物的沸点也各不相同呢!这其中的奥秘可不少。
先来说说碳原子数吧。
一般情况下,碳原子数越多,沸点往往就越高。
这就好比是一支队伍,人越多,那场面就越大,越不容易散掉。
那些碳原子多的有机化合物,就像是一支庞大的队伍,需要更高的能量才能让它们“解散”,也就是达到沸点。
再看看分子间的作用力。
这就如同人与人之间的关系一样,如果关系紧密,那可就不容易分开啦!有机化合物分子间的作用力越大,沸点也就越高。
比如醇类,它们之间可以形成氢键,就像好朋友紧紧拉着手,所以沸点就相对较高。
还有啊,支链的多少也会影响沸点呢!支链多了,就好像一个人身上挂满了各种零碎,行动起来就没那么顺畅了。
有机化合物也是如此,支链多会让分子变得不那么规整,分子间的接触就没那么紧密了,沸点也就相应降低了。
想想看,烷烃不就是个很好的例子吗?直链烷烃的沸点随着碳原子数增加而升高,但是相同碳原子数的烷烃,支链越多沸点越低。
这不就像是在比较谁更“厉害”一样吗?再比如说芳香烃,苯的沸点就比甲苯低一些,这又是为什么呢?不就是因为甲苯多了个甲基嘛!这小小的一个甲基,却能让沸点发生变化,是不是很神奇呢?有机化合物的世界就是这么奇妙,这么丰富多彩!每一种有机化合物都有它独特的性质和沸点。
我们通过研究它们,可以更好地了解这个世界,更好地利用它们。
所以啊,不要小看这些小小的有机化合物,它们蕴含的奥秘可多着呢!有机化合物沸点高低的判断真的很重要,它能让我们更深入地理解化学反应、物质的性质等等。
我们应该认真去探索,去发现其中的乐趣和价值!。

五氯乙烷沸点概述说明以及解释1. 引言1.1 概述本篇文章旨在探讨五氯乙烷的沸点特性,并对其进行深入的分析和解释。
五氯乙烷是一种常见的有机化合物,其性质和应用领域备受关注。
了解其沸点的测定方法、范围以及影响因素,对于加深我们对五氯乙烷的认识具有重要意义。
1.2 文章结构本文共分为四个部分进行论述,即引言、正文、结果与讨论以及结论。
其中,正文部分介绍了五氯乙烷的性质并阐述了液体沸点与气体沸点的概念;随后详细解析了测定五氯乙烷沸点的方法。
在结果与讨论部分,我们将对五氯乙烷的沸点范围及其影响因素进行解析,并说明不同环境条件下其沸点变化情况。
最后,我们将比较五氯乙烷与其他物质的沸点,并展望它在应用领域中可能发挥的作用。
1.3 目的本文主要目的有三个方面:首先,通过介绍五氯乙烷的性质,使读者对该化合物有一个全面的了解;其次,阐述液体沸点与气体沸点的概念,帮助读者理解五氯乙烷在不同状态下发生相变的原理;最后,探究测定五氯乙烷沸点的方法,并分析其沸点范围及受影响因素,以期为相关实际应用提供指导和有价值的评价。
2. 正文:2.1 五氯乙烷的性质介绍五氯乙烷是一种有机化合物,分子式为C2Cl5H和分子量为201.3 g/mol。
它是无色液体,在常温下具有刺激性气味。
五氯乙烷主要用作工业溶剂和农药成分,具有较高的挥发性和不容易挥发的特点。
2.2 液体沸点与气体沸点的概念液体沸点是指在给定压力下,液体开始转变为气体状态(也称为饱和蒸汽)的温度。
而气体沸点则是指在标准大气压下,液体开始转变为气体状态的温度。
2.3 五氯乙烷的沸点测定方法五氯乙烷的沸点可以通过实验测定来确定。
一个常用的方法是采用常压蒸馏法。
该方法中,将样品加入装有热源的容器中,在恒定压力下进行加热。
当样品温度上升时,在某一温度达到液体与饱和蒸汽平衡时,开始观察到液体汽化,此时该温度即为五氯乙烷的沸点。
此外,还可以使用气相色谱法进行沸点测定。
该方法利用了不同物质在不同温度下的沸点差异,在分析仪器中通过气相色谱柱将五氯乙烷样品加热至其开始挥发的温度,记录并分析挥发物质的特征峰,从而确定沸点。

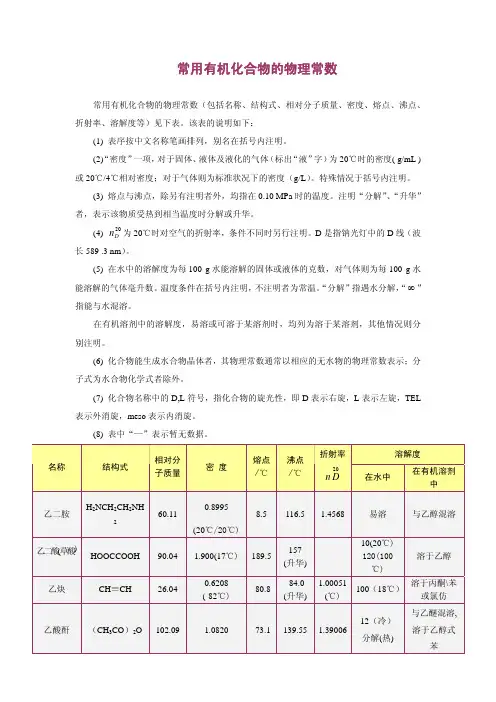

有机化和物的沸点高低有一定的规律,现总结如下:一、同系物沸点大小判断,一般随着碳原子数增多,沸点增大。
如甲烷<乙烷<丙烷<丁烷<戊烷<.....二、链烃同分异构体沸点大小判断,一般支链越多,沸点越小。
如:正戊烷>异戊烷>新戊烷三、芳香烃的沸点大小判断,侧链相同时,临位>间位>对位。
如:临二甲苯》间二甲苯》对二甲苯四、对于碳原子数相等的烃沸点大小判断,烯烃<烷烃<炔烃五、同碳原子的脂肪烃的衍生物沸点大小判断,烯烃的衍生物沸点低于烷烃的同类衍生物。
如:油酸的沸点<硬脂酸。
六、不同类型的烃的含氧衍生物的沸点比较,相对分子质量相近的脂肪羧酸>脂肪醇>脂肪醛,七、酚和羧酸与它们对应的盐沸点比较,酚和羧酸<对应盐的沸点。
如乙酸<乙酸钠八、分子量相近的烃的沸点一般低于烃的衍生物。
例1、下列沸点大小,前者低,后者高的是().A、苯酚和苯酚钠B、软脂酸和油酸C、丁烯和乙烯D、丁烷和2-甲基丙烷解析:A对,苯酚盐的熔沸点大于苯酚;B错,软脂酸常温固态,油酸常温液态,碳原子相近的高级一元脂肪酸,烃基中C=C越多,沸点越低;C错,同系物中C数越多,沸点越高;D错,同类同分异构体,支链多,沸点低。
答案是A。
点评:本题考查不同情况不同物质之间沸点的大小,考查的范围大,知识跨度大,知识零散,决定沸点高低的因素不同,从理论的角度、平时积累和生活的实践多角度理解,总结规律。
例2、(08年宁夏)下列说法错误的是().A.乙醇和乙酸都是常用调味品的主要成分B.乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高C.乙醇和乙酸都能发生氧化反应D.乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应解析:A对,乙醇和乙酸分别是日常生活中料酒和食醋的主要成分;B对,乙醇和乙酸分子极性强,分子之间可以形成氢键,而C2H6、C2H4非极性分子,所以前者熔沸点远远高于后者;C对,氧化反应种类繁多,乙醇和乙酸都能燃烧;D错,皂化反应仅指高级脂肪酸甘油酯在碱性条件下的水解反应,乙酸乙酯在碱性条件下的水解不叫皂化反应。

常用溶剂的沸点、溶解性和毒性溶剂名称沸点(101.3kPa溶解性毒性液氨-33.35℃特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性液态二氧化硫-10.08溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒甲胺-6.3是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃二甲胺7.4是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性石油醚不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似乙醚34.6微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶麻醉性戊烷36.1与乙醇、乙醚等多数有机溶剂混溶低毒性二氯甲烷39.75与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,麻醉性强二硫化碳46.23微溶与水,与多种有机溶剂混溶麻醉性,强刺激性溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大丙酮56.12与水、醇、醚、烃混溶低毒,类乙醇,但较大1,1-二氯乙烷57.28与醇、醚等大多数有机溶剂混溶低毒、局部刺激性氯仿61.15与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强麻醉性甲醇64.5与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性,四氢呋喃 THF66优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒1,4-二氧六环101.32能与水及多数有机溶剂混溶,仍溶解能力很强微毒,强于乙醚2~3倍己烷68.7甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。
麻醉性,刺激性三氟代乙酸71.78与水,乙醇,乙醚,丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物1,1,1-三氯乙烷74与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶低毒类溶剂四氯化碳76.75与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强乙酸乙酯77.112与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,麻醉性乙醇78.3与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,麻醉性丁酮79.64与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性强于丙酮苯80.1难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶强烈毒性环己烷80.72与乙醇、高级醇、醚、丙酮、烃、氯代烃、高级脂肪酸、胺类混溶低毒,中枢抑制作用乙睛81.6与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃混溶,但是不与饱和烃混溶中等毒性,大量吸入蒸气,引起急性中毒异丙醇82.4与乙醇、乙醚、氯仿、水混溶微毒,类似乙醇1,2-二氯乙烷83.48与乙醇、乙醚、氯仿、四氯化碳等多种有机溶剂混溶高毒性、致癌乙二醇二甲醚85.2溶于水,与醇、醚、酮、酯、烃、氯代烃等多种有机溶剂混溶。

化合物的物理性质《烷烃的物理性质》一. 物质的状态室温下,C1-C4为气体,C5-C16为液体,C17以上是固体。
二.熔点和沸点烷烃的熔点和沸点都很低,并且熔点和沸点随分子量的增加而升高。
但值得注意的是:(1)对同数碳原子的烷烃来说,结构对称的分子熔点高。
因为结构对称的分子在固体晶格中可紧密排列,分子间的色散力作用较大,因而使之熔融就必须提供较多的能量。
(2)含偶数碳原子的正烷烃比奇数碳原子的熔点高。
这主要取决于晶体中碳链的空间排布情况。
X光证明,固体正烷烃的碳链在晶体中伸长为锯齿形,奇数碳原子的链中两端的甲基处在同一边,而偶数碳原子的链中,两端的甲基处在相反的位置,从而使这种碳链比奇数碳链的烷烃可以彼此更为靠近,于是它们之间的色散力就大些。
烷烃的沸点上升比较有规则,每增加一个CH2基,上升20-30℃,越到高级系列上升越慢。
在相同碳原子数的烷烃中,直链的沸点比带支链的高,这是由于在液态下,直链的烃分子易于相互接近,而有侧链的烃分子空间阻碍较大,不易靠近。
三. 比重、溶解度、折光率(略)环烷烃的物理性质在常温常压下环丙烷及环丁烷为气体,环戊烷为液体,高级环烷烃为固体。
环烷烃的熔点较同数碳原子的直链烷烃高,因为环烷烃比直链烷烃在晶格中排列更紧密。
环烷烃的密度为0.688~0.853g•c m-3 。
环烷烃不溶于水。
一些环烷烃的熔点和沸点见表3-2。
表3.2 环烷烃的熔点、沸点、张力能(kJ·mol-1)和每一个-CH2-单元的燃烧热(kJ·mol-1 )《芳烃的物理性质》苯及其同系物大多为液体,故有特殊的香气,但它们的蒸气有毒。
高浓度的苯蒸气作用于中枢神经,引起急性中毒。
长期接触低浓度的苯蒸气能损害造血器官。
因此,应尽量注意少接触苯。
有时可以用甲苯代替苯作溶剂,因少量甲苯在人体中可以与甘氨酸作用被人体中酶催化形成马尿酸(C6H5CONHCH2CO2H)而排出体外,故甲苯毒性相对较小。

C5特性C5主要指石油产品中含有五个碳原子的烃类混合物,因其密度小,辛烷值高,在汽油调合原料中性比价较高C5又名碳五即戊烷,化学式C5H12,烷烃中的第五个成员。
碳五有3种同分异构体:正戊烷(沸点36°C)、异戊烷(系统命名法为“2-甲基丁烷”,沸点28°C)和新戊烷(系统命名法为“2,2-二甲基丙烷”,沸点10°C),“C5”通常指正戊烷,即其直链异构体。
C5又名碳五即戊烷,化学式C5H12,烷烃中的第五个成员。
碳五有3种同分异构体:正戊烷(沸点36°C)、异戊烷(系统命名法为“2-甲基丁烷”,沸点28°C)和新戊烷(系统命名法为“2,2-二甲基丙烷”,沸点10°C),“C5”通常指正戊烷,即其直链异构体。
正戊烷分子结构:C原子以sp3杂化轨道成键、分子为非极性分子。
主要成分:纯品外观与性状:无色液体,有微弱的薄荷香味。
溶解性:微溶于水,溶于乙醇、乙醚、丙酮、苯、氯仿等多数有机溶剂。
主要用途:用作溶剂,制造人造冰、麻醉剂,合成戊醇、异戊烷等。
健康危害:高浓度可引起眼与呼吸道粘膜轻度刺激症状和麻醉状态,甚至意识丧失。
慢性作用为眼和呼吸道的轻度刺激。
可引起轻度皮炎。
燃爆危险:本品极度易燃。
溶解性:不溶于水,可混溶于乙醇、乙醚等多数有机溶剂。
主要用途:用于有机合成,也作溶剂。
健康危害:主要有麻醉及轻度刺激作用。
可引起眼和呼吸道的刺激症状,重者有麻醉症状,甚至意识丧失。
慢性影响:眼和呼吸道的轻度刺激。
皮肤长期接触可发生轻度皮炎。
燃爆危险:本品极度易燃。
危险特性:极易燃,其蒸气与空气可形成爆炸性混合物,遇明火、高热极易燃烧爆炸。
与氧化剂接触发生强烈反应, 甚至引起燃烧。
其蒸气比空气重,能在较低处扩散到相当远的地方,遇火源会着火回燃。
若遇高热,容器内压增大,有开裂和爆炸的危险。
新戊烷无色气体或极易挥发的液体;蒸汽压146.63kPa;闪点<-7℃;熔点-19.5℃;沸点9.5℃;溶解性:不溶于水,溶于乙醇等;密度:相对密度(水=1)0.59;相对密度(空气=1)2.48;稳定性:稳定;危险标记4(易燃液体);主要用途:是汽油的主要成分对环境的影响编辑一、健康危害侵入途径:吸入、食入、经皮吸收。

有机实验室常用溶剂的沸点、溶解性和毒性常用溶剂的沸点、溶解性和毒性溶剂名称沸点(101.3kPa)溶解性毒性液氨-33.35℃特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性液态二氧化硫-10.08 溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒甲胺-6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃二甲胺7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性石油醚不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似乙醚34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶麻醉性戊烷36.1 与乙醇、乙醚等多数有机溶剂混溶低毒性二氯甲烷39.75 与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,麻醉性强二硫化碳46.23 微溶与水,与多种有机溶剂混溶麻醉性,强刺激性溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大丙酮56.12 与水、醇、醚、烃混溶低毒,类乙醇,但较大1,1-二氯乙烷57.28 与醇、醚等大多数有机溶剂混溶低毒、局部刺激性氯仿61.15 与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强麻醉性甲醇64.5 与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性,四氢呋喃66 优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒己烷68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。
麻醉性,刺激性三氟代乙酸71.78 与水,乙醇,乙醚,丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物1,1,1-三氯乙烷74.0 与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶低毒类溶剂四氯化碳76.75 与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强乙酸乙酯77.112 与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,麻醉性乙醇78.3 与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,麻醉性丁酮79.64 与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性强于丙酮苯80.10 难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶强烈毒性环己烷80.72 与乙醇、高级醇、醚、丙酮、烃、氯代烃、高级脂肪酸、胺类混溶低毒,中枢抑制作用乙睛81.60 与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃混溶,但是不与饱和烃混溶中等毒性,大量吸入蒸气,引起急性中毒异丙醇82.40 与乙醇、乙醚、氯仿、水混溶微毒,类似乙醇1,2-二氯乙烷83.48 与乙醇、乙醚、氯仿、四氯化碳等多种有机溶剂混溶高毒性、致癌乙二醇二甲醚85.2 溶于水,与醇、醚、酮、酯、烃、氯代烃等多种有机溶剂混溶。

碳五烯烃沸点-概述说明以及解释1.引言1.1 概述概述碳五烯烃是一种由五个碳原子组成的烃类化合物,具有独特的分子结构和性质。
它们是由五个碳原子形成一个环状结构,并且每个碳原子上都有一个氢原子。
碳五烯烃在化学研究和工业应用中都具有重要的地位,引起了广泛的关注。
本文将对碳五烯烃的沸点进行研究和探讨。
沸点是指在特定压力下,物质从液相转变为气相所需的温度。
了解碳五烯烃的沸点有助于我们对其性质和应用进行更深入的了解。
本文将首先介绍碳五烯烃的定义,包括其组成和分子结构。
接着,我们将探讨碳五烯烃的性质,如化学稳定性、溶解性、电导性等。
在了解了碳五烯烃的基本性质后,我们将进一步研究其在各个领域的应用,如材料科学、生物医学、能源等。
本文还将总结碳五烯烃的沸点研究成果,并讨论其对其应用的影响。
沸点的高低可以反映出物质在不同温度下的稳定性和可操作性,因此对于碳五烯烃的应用来说具有重要意义。
最后,本文将展望碳五烯烃沸点研究的未来发展方向,希望能够为相关领域的研究者提供参考和启示。
通过对碳五烯烃沸点的深入研究和分析,我们可以更好地理解碳五烯烃的性质和应用,为其在材料科学、生物医学和能源等领域的开发和应用提供有力的支持。
随着研究的不断深入,相信碳五烯烃的应用前景将会更加广阔。
1.2 文章结构本文将分为三个主要部分进行论述:引言部分、正文部分和结论部分。
在引言部分,将会对文章的主题进行概述,介绍碳五烯烃的基本定义、性质和应用,并明确文章的目的。
通过引言部分,读者可以快速了解本文的主题和内容。
正文部分将涵盖三个主要方面。
首先,会对碳五烯烃的定义进行详细介绍,包括其结构和化学成分等方面的内容。
其次,我们将探讨碳五烯烃的性质,包括物理性质和化学性质,并对其特殊性质进行深入分析。
最后,我们将介绍碳五烯烃的应用领域,包括实际应用和未来潜在的应用领域。
在结论部分,我们将总结碳五烯烃沸点的相关研究成果,并分析碳五烯烃沸点对其应用的影响。
在此基础上,我们还将对碳五烯烃沸点研究的展望进行探讨,提出未来可能的研究方向和发展趋势。
C5特性C5主要指石油产品中含有五个碳原子的烃类混合物,因其密度小,辛烷值高,在汽油调合原料中性比价较高C5又名碳五即戊烷,化学式C5H12,烷烃中的第五个成员。
碳五有3种同分异构体:正戊烷(沸点36°C)、异戊烷(系统命名法为“2-甲基丁烷”,沸点28°C)和新戊烷(系统命名法为“2,2-二甲基丙烷”,沸点10°C),“C5”通常指正戊烷,即其直链异构体。
C5又名碳五即戊烷,化学式C5H12,烷烃中的第五个成员。
碳五有3种同分异构体:正戊烷(沸点36°C)、异戊烷(系统命名法为“2-甲基丁烷”,沸点28°C)和新戊烷(系统命名法为“2,2-二甲基丙烷”,沸点10°C),“C5”通常指正戊烷,即其直链异构体。
正戊烷分子结构:C原子以sp3杂化轨道成键、分子为非极性分子。
主要成分:纯品外观与性状:无色液体,有微弱的薄荷香味。
溶解性:微溶于水,溶于乙醇、乙醚、丙酮、苯、氯仿等多数有机溶剂。
主要用途:用作溶剂,制造人造冰、麻醉剂,合成戊醇、异戊烷等。
健康危害:高浓度可引起眼与呼吸道粘膜轻度刺激症状和麻醉状态,甚至意识丧失。
慢性作用为眼和呼吸道的轻度刺激。
可引起轻度皮炎。
燃爆危险:本品极度易燃。
溶解性:不溶于水,可混溶于乙醇、乙醚等多数有机溶剂。
主要用途:用于有机合成,也作溶剂。
健康危害:主要有麻醉及轻度刺激作用。
可引起眼和呼吸道的刺激症状,重者有麻醉症状,甚至意识丧失。
慢性影响:眼和呼吸道的轻度刺激。
皮肤长期接触可发生轻度皮炎。
燃爆危险:本品极度易燃。
危险特性:极易燃,其蒸气与空气可形成爆炸性混合物,遇明火、高热极易燃烧爆炸。
与氧化剂接触发生强烈反应, 甚至引起燃烧。
其蒸气比空气重,能在较低处扩散到相当远的地方,遇火源会着火回燃。
若遇高热,容器内压增大,有开裂和爆炸的危险。
新戊烷无色气体或极易挥发的液体;蒸汽压146.63kPa;闪点<-7℃;熔点-19.5℃;沸点9.5℃;溶解性:不溶于水,溶于乙醇等;密度:相对密度(水=1)0.59;相对密度(空气=1)2.48;稳定性:稳定;危险标记4(易燃液体);主要用途:是汽油的主要成分对环境的影响编辑一、健康危害侵入途径:吸入、食入、经皮吸收。
有机化合物沸点排序有机化合物的沸点是衡量其挥发性和热稳定性的重要指标。
沸点的高低取决于分子间的相互作用力以及分子的结构和分子量。
下面将根据有机化合物的沸点进行分类和排序,以便更好地了解有机化合物的性质。
一、低沸点有机化合物:低沸点有机化合物通常指沸点低于100℃的化合物。
这类化合物一般分子量较小,分子间作用力较弱。
常见的低沸点化合物有甲醇、乙醇、丙酮等。
这些化合物常用作溶剂和反应的中间体,在实验室中常用于提取和纯化有机化合物。
二、中沸点有机化合物:中沸点有机化合物通常指沸点在100℃到200℃之间的化合物。
这类化合物分子量较大,分子间作用力较强。
常见的中沸点化合物有醋酸、苯、乙酸乙酯等。
这些化合物在实验室中常用作溶剂、反应的原料和中间体,并且广泛应用于工业生产中。
三、高沸点有机化合物:高沸点有机化合物通常指沸点高于200℃的化合物。
这类化合物分子量较大,分子间作用力非常强。
常见的高沸点化合物有蓖麻油、硫酸二甲酯、甘油等。
这些化合物在实验室和工业上一般用作润滑剂、增塑剂、溶剂等。
四、升华性有机化合物:升华性有机化合物通常指在常温下直接从固态升华为气态,无液态存在的化合物。
这类化合物的分子间作用力非常强,常见的有机升华物有碘、萘、苯胺等。
这些化合物在实验室中常用于制备纯净试剂和标准品。
五、变性沸点有机化合物:变性沸点有机化合物指的是在特定条件下,沸点发生变化的化合物。
这类化合物在特定条件下可能发生分解、聚合、异构化等反应,导致沸点发生变化。
常见的变性沸点化合物有酚类、醛类、羧酸等。
这些化合物在实验室和工业上常用于合成、催化和反应控制。
有机化合物的沸点是其挥发性和热稳定性的重要指标。
根据沸点的高低可以对有机化合物进行分类和排序,从而更好地了解其性质和应用。
通过对低沸点、中沸点、高沸点、升华性和变性沸点有机化合物的介绍,我们可以更全面地认识有机化合物的特性和用途。
在实验和应用中,合理选择具有适当沸点的有机化合物,能够提高实验效果和产品质量。
烷烃、环烷烃烷烃烷烃即饱和烃(saturated group),是只有碳碳单键的链烃,是最简单的⼀类有机化合物。
烷烃分⼦⾥的碳原⼦之间以单键结合成链状(直链或含⽀链)外,其余化合价全部为氢原⼦所饱和。
烷烃分⼦中,氢原⼦的数⽬达到最⼤值,它的通式为CnH2n+2。
分⼦中每个碳原⼦都是sp3杂化。
最简单的烷烃是甲烷。
烷烃中,每个碳原⼦都是四价的,采⽤sp3杂化轨道,与周围的4个碳或氢原⼦形成牢固的σ键。
连接了1、2、3、4个碳的碳原⼦分别叫做伯、仲、叔、季碳;伯、仲、叔碳上的氢原⼦分别叫做伯、仲、叔氢。
为了使键的排斥⼒最⼩,连接在同⼀个碳上的四个原⼦形成四⾯体(tetrahedro n)。
甲烷是标准的正四⾯体形态,其键⾓为109°28′(准确值:arccos(-1/3))。
理论上说,由于烷烃的稳定结构,所有的烷烃都能稳定存在。
但⾃然界中存在的烷烃最多不超过50个碳,最丰富的烷烃还是甲烷。
由于烷烃中的碳原⼦可以按规律随意排列,所以烷烃的结构可以写出⽆数种。
直链烷烃是最基本的结构,理论上这个链可以⽆限延长。
在直链上有可能⽣出⽀链,这⽆疑增加了烷烃的种类。
所以,从4个碳的烷烃开始,同⼀种烷烃的分⼦式能代表多种结构,这种现象叫同分异构现象。
随着碳数的增多,异构体的数⽬会迅速增长烷烃还可能发⽣光学异构现象。
当⼀个碳原⼦连接的四个原⼦团各不相同时,这个碳就叫做⼿性碳,这种物质就具有光学活性。
烷烃失去⼀个氢原⼦剩下的部分叫烷基[1],⼀般⽤R-表⽰。
因此烷烃也可以⽤通式RH来表⽰。
烷烃最早是使⽤习惯命名法来命名的。
但是这种命名法对于碳数多,异构体多的烷烃很难使⽤。
于是有⼈提出衍⽣命名法,将所有的烷烃看作是甲烷的衍⽣物,例如异丁烷叫做2-⼀甲基丙烷。
现在的命名法使⽤IUPAC命名法,烷烃的系统命名规则如下:找出最长的碳链当主链,依碳数命名主链,前⼗个以天⼲(甲、⼄、丙、丁、戊、⼰、庚、⾟、壬、癸)代表碳数,碳数多于⼗个时,以中⽂数字命名,如:⼗⼀烷。
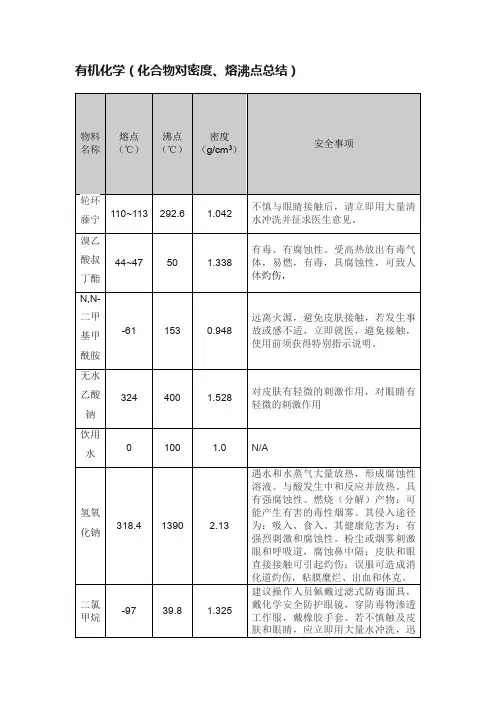
有机化合物熔点
有机化合物的熔点受到多种因素的影响,包括分子结构、分子间相互作用力、分子量等。
因此,不同有机化合物的熔点范围和数值会有很大的差异。
以下是几种有机化合物的熔点范围示例:
1. 甲烷(CH₄): -18
2.5°C
2. 乙醇(C₂H₅OH): -114.1°C
3. 苯(C₆H₆): 5.5°C
4. 油酸(C₁₈H₃₆O₂): 13.4°C
5. 苯甲酸(C₆H₅COOH): 42.0°C
6. 蜡烛石蜡(C₂₅H₅₂): 62-66°C
7. 棕榈酸(C₁₆H₃₂O₂): 63.3°C
8. 辛酸(C₈H₁₆O₂): 16.7°C
需要注意的是,这些数值只是一些常见有机化合物的熔点范围,具体数值可能会受到实验条件的影响。
对于具体的有机化合物,可以通过文献、化学数据库或实验数据来获得其准确的熔点数值。
此外,有机化合物的熔点也可以受到杂质的影响,纯度较高的化合物通常具有更准确的熔点。