电解池中阴阳离子放电顺序
- 格式:docx
- 大小:11.46 KB
- 文档页数:1


1.电解池的反应①阳离子的放电顺序的影响因素A.离子本性:氧化性越强的阳离子越易得电子。
如Fe3+>Cu2+>Fe2+>Zn2+。
B.离子浓度:离子浓度越大,离子还原倾向越大。
在中性溶液里[H+]=10-7mol/L,此时还原倾向显著减弱。
所以在中性或酸性溶液里Fe2+、Sn2+离子比H+易还原。
C.超电压的影响:在中性溶液中H+比Zn2+还原倾向大,但实际上Zn先析出,而不是H2.因为有些物质,特别是气体在电极上析出,需要比理论电压更高的电压(即超电压)。
因此氢气在金属电极上析出,需要更高的超电压,所以它们在中性溶液中比锌更难析出。
②阴离子的放电顺序:惰性电极做阳极时(离子浓度相同),它们的放电顺序为:S2->I->Fe2+>Br->Cl->OH->含氧酸根离子。
含氧酸根离子在水溶液中一般比OH-难放电,所以电解含氧酸及其盐溶液时,阳极都是OH-放电。
2.浓度、温度对氧化性、还原性的影响温度高会增强氧化剂的氧化性和还原剂的还原性。
如许多金属跟酸要加热:如MnO2和盐酸反应制Cl2要加热,C、CO与金属的反应要加热等。
浓度大会增强氧化剂的氧化性和还原剂的还原性。
3.不同介质对氧化还原反应的影响1.在酸性溶液中若氧化剂中含有氧元素,,生成物中一般含有水。
2.酸性溶液中有多少种金属,生成物中就有多少种盐。
3.酸性溶液中,若还原剂中含有非金属元素离子,它一般被氧化成非金属单质。
4.酸性介质可增强氧化剂的氧化性。
综上所述,氧化剂和还原剂发生反应的一般模式我:强氧化剂+强还原剂→弱氧化剂+弱还原剂氧化剂和还原剂二者都强则反应容易,二者都弱则反应难,甚至不反应。
其实,原电池和电解池都可以看作是氧化还原反应的具体应用。

电解时离子放电顺序一、放电的概念放电:阴离子失去电子而阳离子得到电子的过程叫放电。
二、离子放电顺序1、决定离子放电顺序的因素:①离子得失电子的能力②离子的浓度③电极材料多种阴阳离子分别移向阴极阳极时,优先放电的是:氧化性、还原性强的离子2、电极反应(1)阴极:(阳离子得电子)Ag+>Hg2+>Fe3+>Cu2+>H+(酸)>Pb2+>Sn2+>Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>Ca2+>K+(2)阳极:(阴离子失电子)若阳极是活泼金属(金属活动顺序表Ag以前),溶液中的阴离子一律不放电,而是电极材料失电子。
注:电解题优先看阳极材料若阳极是惰性(Pt、Au、石墨),则放电顺序如下:S2->I->Br->Cl->OH->含氧酸根离子3、电解规律(用惰性电极电解时)⑴、电解含氧酸、强碱溶液、活泼金属的含氧酸盐溶液时,实质上是电解水。
如电解H2SO4、HNO3、NaOH、Na2SO4等溶液时其电极反应式为:阳极:4OH--4e-=2H2O +O2↑阴极:4H+ +4e-=2H2 ↑总反应:2H2O =O2↑ +2H2↑电解后溶液中溶质的质量分数增大,若要恢复原来的浓度,只需加入一定量的水即可。
⑵、电解无氧酸溶液(氢氟酸除外)、不活泼金属的无氧酸盐溶液时,实质上是电解质本身被电解。
如电解盐酸、CuCl2溶液等时。
电解盐酸阳极:2Cl --2e-=Cl2↑阴极:2H+ +2e-=H2 ↑总反应:2HCl =Cl2↑ + H2↑电解后溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需加入一定量的溶质(通入一定量的HCl气体)。
⑶、电解不活泼金属的含氧酸盐时,电解质和水都有一部分被电解,如电解CuSO4溶液、AgNO3溶液等。
电解CuSO4溶液阳极:4OH--4e-=2H2O +O2↑阴极:2Cu2+ +4e-=2Cu总反应:2CuSO4 +2H2O =2Cu+O2↑ +2H2SO4电解后原溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需加入一定量金属氧化物。

电解池原理(1)电解液离子放电顺序:1、阳离子的放电顺序:2、阴离子的放电顺序:(2)采用惰性电极(Pt\石墨)电解电解质溶液:1、用Pt电极电解 CuCl2溶液:阳极:阴极:电解反应方程式:电子数2、用Pt电极电解 HCl溶液:阳极:阴极:电解反应方程式:电子数3、用Pt电极电解 H2SO4溶液:阳极:阴极:电解反应方程式:电子数4、用Pt电极电解 NaOH溶液:阳极:阴极:电解反应方程式:电子数5、用Pt电极电解 K2SO4溶液:阳极:阴极:电解反应方程式:电子数6、用Pt电极电解 KCl溶液:阳极:阴极:电解反应方程式:电子数7、用Pt电极电解 AgNO3溶液:阳极:阴极:电解反应方程式:电子数8、用Pt电极电解 CuSO4溶液:阳极:阴极:电解反应方程式:电子数(3)采用惰性电极(Pt\石墨)电解熔融电解质:9、用Pt电极电解熔融的Al2O3:阳极:阴极:电解反应方程式:电子数(4)活性阳极电解电解质溶液:10、铁作阳极、石墨作阴极,电解NaCl溶液:阳极:阴极:电解反应方程式:电子数11、铜作阳极、石墨作阴极,电解Na2SO4溶液:阳极:阴极:电解反应方程式:电子数12、铜作阳极、石墨作阴极,电解H2SO4溶液:阳极:阴极:电解反应方程式:电子数13、铜作阳极、铁作阴极,电解CuSO4溶液:阳极:阴极:电解反应方程式:电子数14、锌作阳极、铜作阴极,电解ZnSO4溶液:阳极:阴极:电解反应方程式:电子数15、铜作阳极,铜作阴极,电解CuSO4溶液:阳极:阴极:电解反应方程式:电子数16、粗铜(含锌、铁、银)作阳极,纯铜作阴极,电解CuSO4溶液:阳极:阴极:电解反应方程式:电子数。
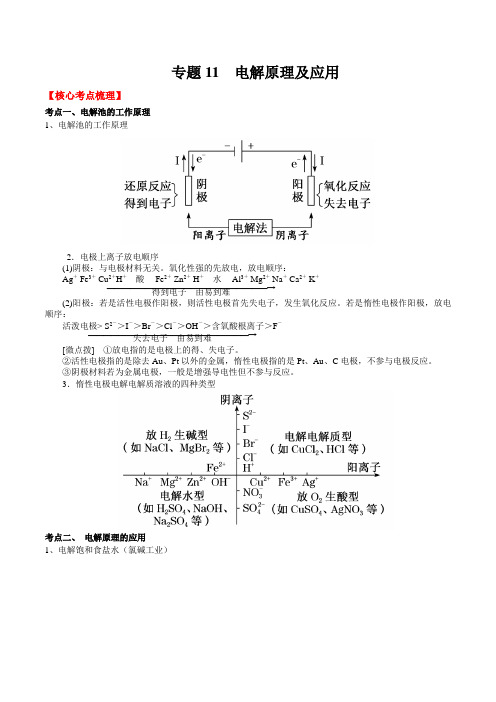
专题11 电解原理及应用【核心考点梳理】考点一、电解池的工作原理 1、电解池的工作原理2.电极上离子放电顺序(1)阴极:与电极材料无关。
氧化性强的先放电,放电顺序: ―――――――――――――――――――――→Ag + Fe 3+ Cu 2+H +酸 Fe 2+ Zn 2+ H +水 Al 3+ Mg 2+ Na + Ca 2+ K+得到电子 由易到难(2)阳极:若是活性电极作阳极,则活性电极首先失电子,发生氧化反应。
若是惰性电极作阳极,放电顺序:―――――――――――――――――――――→活泼电极> S 2->I ->Br ->Cl ->OH ->含氧酸根离子>F-失去电子 由易到难[微点拨] ①放电指的是电极上的得、失电子。
②活性电极指的是除去Au 、Pt 以外的金属,惰性电极指的是Pt 、Au 、C 电极,不参与电极反应。
③阴极材料若为金属电极,一般是增强导电性但不参与反应。
3.惰性电极电解电解质溶液的四种类型考点二、 电解原理的应用 1、电解饱和食盐水(氯碱工业)阳极反应式:2Cl --2e -===Cl 2↑(氧化反应)阴极反应式:2H ++2e -===H 2↑(还原反应)总反应方程式:2NaCl +2H 2O =====电解2NaOH +H 2↑+Cl 2↑ 2、电解精炼铜(1)电极材料:阳极为粗铜;阴极为纯铜。
(2)电解质溶液:含Cu 2+的盐溶液。
(3)电极反应:阳极:Zn -2e -==Zn 2+、Fe -2e -==Fe 2+、Ni -2e -==Ni 2+、Cu -2e -==Cu 2+; 阴极:Cu 2++2e -==Cu 。
(4)阳极泥的形成:在电解过程中,活动性位于铜之后的银、金等杂质,难以在阳极失去电子变成阳离子而溶解,它们以金属单质的形式沉积在电解槽底部,形成阳极泥。
3、电镀图为金属表面镀银的工作示意图,据此回答下列问题:(1)镀件作阴极,镀层金属银作阳极。

化学“电解池”基础知识详解一、电解池的基本概念:1、电解池的主要应用用于工业制纯度高的金属,是将电能转化为化学能的一个装置(构成:外加电源,电解质溶液,阴阳电极)。
使电流通过电解质溶液或熔融电解质而在阴,阳两极引起还原氧化反应的过程。
2、通过电流使电解质溶液发生电解反应的装置。
电解池的主要部件:电源(直流电)、电解质溶液(含有可以导电的离子)、电极(插入电解质溶液中,导电并发生氧化还原反应)。
3、电解池的反应原理:在电解池中,电流通过电解质溶液时,正离子向阴极移动,负离子向阳极移动,从而形成电流。
在电极上,发生氧化还原反应,电子通过导线从电源流向电解池。
二、电解定义:1、电解是使电流通过电解质溶液(或者是熔融的电解质)而在阴、阳两极引起还原氧化反应的过程。
2、电解过程中的能量转化(装置特点)阴极一定不参与反应不一定是惰性电极;阳极不一定参与反应也不一定是惰性电极。
三、反应条件:1、连接直流电源2、阴阳电极:与电源负极相连为阴极;与电源正极相连为阳极。
3、两极处于电解质溶液或熔融电解质中。
4、两电极形成闭合回路。
四、电极反应:1、电极反应与电源的正极相连的电极称为阳极。
2、物质在阳极上失去电子,发生氧化反应。
3、阳极反应式:简记为阳氧;与电源的负极相连的电极成为阴极。
物质在阴极上得到电子,发生还原反应。
4、阴极反应式:简记为阴还(阴还)。
五、分析电解过程的思维程序:1、⾸先判断阴、阳极,分析阳极材料是惰性电极还是活泼电极。
2、再分析电解质⾸溶液的组成,找全离⾸并分阴、阳两组(不要忘记⾸溶液中的H+和OH-)。
3、然后排出阴、阳两极的放电顺序:①、阴极:阳离⾸放电顺序Ag+→Fe3+→Cu2+→H+(酸)→Fe2+→Zn2+→H+(⾸)→Al3+→Mg2+→Na+→Ca2+→K+。
②、阳极:活泼电极>S2->I->Br->Cl->OH->含氧酸根离⾸。
4、分析电极反应,判断电极产物,写出电极反应式,要注意遵循原⾸守恒和电荷守恒。
化学中原电池分正负两极,负极一般为金属失去电子,正极一般本身不参与反应,会有物质在正极得到负极转移过来的电子,可能是离子也可能是分子,所以原电池没有离子的放点顺序。
化学中与原电池相对应的有电解池,电解池的阴阳极分别有自己的离子放点顺序。
阴极放电顺序:Ag+>Hg2+>Fe3+>Cu2+>H+
阳极放点顺序:活泼电极:Mg~Ag的金属做电极,金属失去电子。
石墨或Pt做电极:S2->I->Br->Cl->OH-
在化学反应中,金属元素原子失去最外层电子,非金属原子得到电子,从而使参加反应的原子或原子团带上电荷。
带电荷的原子叫做离子,带正电荷的原子叫做阳离子,带负电荷的原子叫做阴离子。
阴、阳离子由于静电作用而形成不带电性的化合物。
与分子、原子一样,离子也是构成物质的基本粒子。
如氯化钠就是由氯离子和钠离子构成的。
电解池知识点总结同学们,今天咱们来一起总结一下电解池的知识点,这可是化学里很重要的一部分哦!咱们得明白啥是电解池。
简单来说,电解池就是通过直流电让电解质溶液或者熔融的电解质发生氧化还原反应的装置。
那电解池的构成要素有哪些呢?它要有两个电极,一个叫阳极,一个叫阴极。
阳极和电源的正极相连,在电解过程中会发生氧化反应;阴极和电源的负极相连,会发生还原反应。
还有电解质溶液或者熔融的电解质,这是反应发生的“舞台”。
再来说说电解池的工作原理。
直流电通过电极进入电解池,让溶液中的离子发生定向移动。
阳离子向阴极移动,阴离子向阳极移动。
在电极表面,离子得失电子,发生氧化还原反应。
比如说,电解氯化铜溶液的时候,铜离子会在阴极得到电子变成铜单质析出,氯离子在阳极失去电子生成氯气。
电解池的电极反应式也很重要哦!写电极反应式的时候,要先判断电极是惰性电极还是活性电极。
惰性电极像铂、金,它们本身不参与反应;活性电极像铁、铜,它们会参与反应。
然后根据离子的放电顺序来写。
在阴极,常见阳离子的放电顺序是:银离子>汞离子>三价铁离子>铜离子>氢离子>……;在阳极,常见阴离子的放电顺序是:活泼金属电极>硫离子>碘离子>溴离子>氯离子>氢氧根离子>含氧酸根离子。
比如说,电解氯化钠溶液,阴极是氢离子放电生成氢气,阳极是氯离子放电生成氯气。
电解池还有很多应用呢!比如说电解精炼铜,粗铜放在阳极,纯铜放在阴极,通过电解可以把粗铜中的杂质去掉,得到纯度更高的铜。
还有电镀,在金属表面镀上一层其他金属,增强金属的抗腐蚀性或者美观度。
给大家举个例子,在电镀的时候,如果想要在铁制品上镀铜,那就把铁制品放在阴极,铜放在阳极,电镀液用含铜离子的溶液。
咱们说说电解池和原电池的区别。
原电池是把化学能转化为电能,而电解池是把电能转化为化学能。
原电池的电极反应是自发进行的,电解池的电极反应是在外加电源的作用下进行的。
电解池的知识点虽然有点多,但只要咱们认真理解、多做练习,就一定能掌握好!同学们,加油哦!现在大家对电解池的知识点是不是更清楚啦?。
电解规律【学习目标】1、通过电解装置中离子或者电极的放电顺序,能正确地判断阴极和阳极,分析电解产物;2、进行有关电化学的简单计算。
【要点梳理】要点一、电解时电极产物的判断1.阳极产物的判断。
首先看电极,如果是活性电极(除Au、Pt、石墨以外的材料作电极),则电极材料失电子,电极被溶解,溶液中的阴离子不能失电子。
如果是惰性电极(Pt、Au、石墨),则要再看溶液中阴离子的失电子能力,此时根据阴离子放电顺序加以判断。
阴离子放电顺序:S2->I->Br->Cl->OH->含氧酸根(SO42-、NO3-等)。
2.阴极产物的判断。
直接根据阳离子放电顺序进行判断,阳离子放电顺序:Ag+>Hg2+>Fe3+>Cu2+>H+(H+浓度较大时)>Pb2+>Sn2+>Fe2+>Zn2+>H+(H+浓度较小时)>Al3+>Mg2+。
要点诠释:(1)离子的放电顺序主要取决于离子的本性,但还与其他的因素有关(如离子的浓度、溶液的酸碱性等),如在电镀条件下Fe2+、Zn2+的放电顺序在H+之前。
(2)阳离子的放电顺序基本上与金属活动性顺序相反,即越活泼的金属,其阳离子越难结合电子,但需注意:Fe3+氧化性较强,排在Cu2+之前。
要点二、酸、碱、盐溶液电解规律类型电极反应特点实例电解对象电解质浓度pH 电解质溶液复原电解水型阴:2H++2e-=H2↑阳:4OH--4e-=2H2O+O2↑NaOH 水增大增大水H2SO4水增大减小水Na2SO4水增大不变水电解电解质型电解质电离出的阴、阳离子分别在两极放电HCl 电解质减小增大氯化氢CuCl2电解质减小——氯化铜放H2生碱型阴极:H2O放H2生碱阳极:电解质阴离子放电NaCl 电解质和水生成新电解质增大氯化氢放O2生酸型阴极:电解质阳离子放电阳极:H2O放O2生酸CuSO4电解质和水生成新电解质增大氧化铜并分为阴、阳离子两组,然后排出阴、阳离子的放电顺序,写出两极上的电极反应式,根据两极的电极反应式写出反应的总方程式。