化学工程基础第4章传质分离基础分析
- 格式:ppt
- 大小:1.33 MB
- 文档页数:13



《化学工程基础》复习资料化学与化工学院应用化学专业彭梦杰0815020219 第二章、流体流动与输送1、连续性假定:化学工程中所研究的液体流动规律,不论是液体分子的微观运动,还是流涕在生产装置内的整体机械运动,它都是由无数流体质点所组成的连续介质,因此可以取大量流体分子组成的微团为流体运动质点,并以这样的质点为研究对象。
2、理想流体:无黏性、在流动中不产生摩擦阻力的流体。
3、相对密度:物质密度与4℃纯水密度之比,用符号d表示,量纲为一。
4、平均密度:各组分密度与其相对体积分数乘积之和。
5、流体静力学方程应用:U行管压差计、微差压差计、液位计、液封。
6、流量:单位时间内通过导管任意横截面积的流体量为流量。
7、流速:单位时间内流体在导管内流过的距离称为流速。
8、流速的选择:建设投资费用和运行操作费用综合考虑经济流速。
9、稳态流动:在流体流动系统内,任一空间位置上的流量、流速、压力和密度等物理参数,只随空间位置的改变而改变,而不随时间变化的流动。
10、层流:管中流动流体的质点只沿管轴方向平行流动,而不作垂直于管轴的径向扰动。
(或称滞留)11、湍流:管中流动流体的质点相互扰混,使六题质点的流动速率和方向呈现不规则变化,甚至形成涡流。
(或称紊流)12、黏性:流体流动时,往往产生阻碍流体流动的内摩擦力的流动特性。
13、黏度:一般由实验测定,与压强关系不大,但受温度影响。
液体的黏度随温度的升高而减小,气体的黏度随温度的升高而增大。
单位1P=100cP=0.1Pa·s=0.1N·s·m-214、运动黏度:流体黏度μ与密度ρ之比,符号用ν表示,单位m2·s-115、边界层:壁面附近流速变化较大的区域,u=0~99%u,流动阻力主要集中在此区域。
16、主流区:流苏基本不变化,u≥98%u,流动阻力可忽略。
17、稳定段长度L:流体流动从管道入口开始形成边界层起直到发展到边界层在管道中心汇合为止的长度。



传质分离过程教学设计一、背景简介传质分离是化工工程中常见的一种分离工艺,其原理是利用不同物质在不同介质中扩散或渗透速率不同的差异,实现物质分离。
本教学设计旨在通过理论基础讲解、计算实例演练和实验操作等方式,提高学生对传质分离过程的理解和掌握能力。
二、教学目标1.了解传质分离的基本概念和基本原理。
2.学习传质分离的计算公式及其应用。
3.掌握传质分离实验中的相关操作方法和注意事项。
4.提高学生的实验操作能力和数据处理能力。
三、教学内容1. 传质分离的基本概念和基本原理讲解内容包括:1.传质分离的定义和分类。
2.传质分离的基本原理和影响因素。
3.传质分离的术语及其含义。
4.传质分离在工业生产中的应用。
2. 传质分离的计算公式及其应用讲解内容包括:1.基于质量守恒和物质平衡的传质方程。
2.浓度梯度与传质速度的关系。
3.不同传质形式的计算公式及应用。
4.传质分离过程的计算实例讲解。
3. 传质分离实验的相关操作方法和注意事项讲解内容包括:1.实验室安全和操作规范。
2.实验中使用的设备和试剂。
3.实验中涉及到的数据采集和处理方法。
4.实验结果的分析和讨论。
4. 实践环节在教学过程中,安排学生参与传质分离实验操作,并让学生使用已学知识对实验数据进行分析和处理。
通过实践环节,让学生加深对传质分离原理的理解和实验技能的掌握。
四、教学方法采用多种教学方法,包括:1.讲授法:通过PPT讲解、实例演示等方式传达知识点。
2.互动讨论:鼓励学生在教学过程中参与课堂讨论,提高学生的思辨和创新能力。
3.实验操作:安排学生参与传质分离实验操作,提高学生的实验操作技能和数据处理能力。
4.评估反馈:通过考试、实验报告等方式对学生进行评估,及时调整教学进度和方式。
五、教学评估1.考试:考查学生对传质分离原理和应用方面的掌握能力。
2.实验报告:对学生实验数据处理和结果分析能力进行评估。
3.课堂表现:包括学生参与度、提问能力和思考能力等方面的评估。

化学工程中的传质过程分析与计算方法传质过程是化学工程中至关重要的一部分,涉及物质从一个相态传递到另一个相态的过程。
在化学工程的设计和优化中,准确地分析和计算传质过程的速率和效率至关重要。
本文将介绍化学工程中传质过程的基本原理和常用的分析与计算方法。
一、传质过程的基本原理传质过程主要涉及物质的扩散、对流和反应等现象。
扩散是指物质分子在浓度梯度驱动下由高浓度区向低浓度区传递的过程。
对流是指由于流体的运动而导致物质传递的现象,可以进一步分为属于流体本身的动量传递和物质传递。
反应是指物质在传递过程中发生化学反应,形成新的物质。
二、传质过程的计算方法1. 扩散通量计算方法在扩散过程中,物质的传递速率可以通过计算扩散通量来确定。
扩散通量是指通过单位截面积在单位时间内传递过的物质的量。
根据菲克定律,扩散通量可以通过以下公式计算:J = -D∙∇C其中,J为扩散通量,D为扩散系数,∇C为浓度梯度。
2. 对流传质计算方法对流传质过程中,物质的传递速率与流体速度和浓度梯度有关。
常用的计算方法包括阻力和质量传递的计算,以及对流传质的计算模型(如Sherwood数、雷诺数等)。
3. 反应速率计算方法在传质过程中,物质的转化速率与化学反应有关。
根据反应动力学理论,可以利用反应速率方程来计算反应速率。
根据不同的反应类型和反应机理,反应速率方程可以采用不同的形式,如一级反应、二级反应等。
4. 多组分传质计算方法在实际应用中,传质过程往往涉及多个组分的传递。
此时,需要考虑组分之间的相互作用和竞争。
常用的计算方法包括质量守恒方程和组分平衡方程的联立求解,以及利用吉布斯自由能和互相作用系数等的方法。
三、传质过程分析与优化传质过程分析和优化是化学工程的核心任务之一。
通过合理的传质过程分析,可以确定传质速率和效率的影响因素,为优化设计提供依据。
常用的分析方法包括流体力学模拟、传质速率计算、实验测量和模型拟合等。
通过这些方法,可以准确地分析传质过程中的瓶颈和优化空间,提高工艺的效率和经济性。

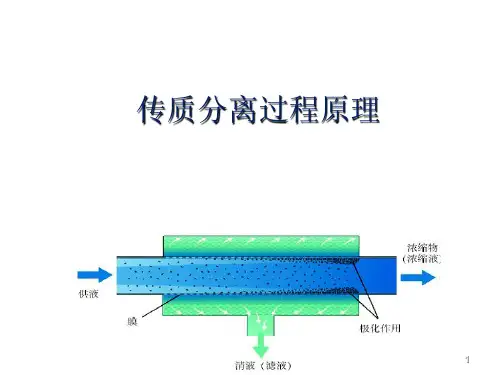

化学工程中的传质过程分析与计算在化学工程中,传质过程是一个关键的环节。
它涉及到物质从一个相的传输到另一个相的过程,如气相到液相、液相到固相等。
理解传质过程对于设计和优化化学工程过程具有重要意义。
本文将从传质的基本概念、传质的机制、传质过程的数学建模以及传质计算方法等方面进行分析与探讨。
一、传质的基本概念在化学工程过程中,物质传质是指通过物质的扩散、对流和反应等方式,使两相之间的组分发生变化的过程。
传质过程最常见的几种方式包括:气体和气体之间的扩散传质、气体和液体之间的气液传质、液体和液体之间的液液传质以及固体和液体之间的固液传质等。
不同的传质方式对应着不同的传质机制和计算方法。
二、传质机制1. 扩散传质:扩散传质是指物质在浓度梯度的作用下,由高浓度区向低浓度区自发性地传输的过程。
在扩散传质中,物质的传质速率与浓度梯度、物质的扩散系数以及系统的温度等因素有关。
2. 对流传质:对流传质是指通过流体的运动将物质从一个地方转移到另一个地方的过程。
对流传质的速率与流体的速度、物质的浓度以及系统的流动特性等因素有关。
3. 反应传质:反应传质是指在化学反应中,物质的传质与反应同时进行的过程。
反应传质的速率不仅受到物质的传质速率的限制,还受到反应速率的限制。
三、传质过程的数学建模为了描述传质过程中物质的传递规律,化学工程中常使用质量守恒和动量守恒以及物质传递过程的理论,建立数学模型。
传质过程的数学建模一般包括质量守恒方程、动量守恒方程和质量传递方程等。
1. 质量守恒方程:质量守恒方程描述了传质过程中物质浓度随时间和空间的变化规律。
通常表示为:∂C/∂t = -∇·(J)+R其中,C表示物质的浓度,J表示物质的传递通量,R表示源项或汇项。
2. 动量守恒方程:动量守恒方程描述了传质过程中流体速度随时间和空间的变化规律。
通常表示为:ρ(∂u/∂t+u·∇u) = -∇P+μ∇^2u+F其中,ρ表示流体的密度,u表示流体的速度,P表示压力,μ表示流体的动力粘度,F表示体积力。
化工基础传质总结汇报材料化工基础传质是研究物质在流动状态下的扩散、对流与质量传递的过程。
本次报告主要从传质的基本概念、传质的机理、传质过程的描述和传质的应用方面进行总结。
一、传质的基本概念传质是指物质从高浓度区域到低浓度区域的移动过程,有助于在不同相界面上的短距离传递物质。
传质过程可以通过扩散和对流两种方式实现。
扩散传质是指离子、分子或颗粒在浓度梯度的驱动下从高浓度区域到低浓度区域的移动。
而对流传质是指物质通过流体的流动而在不同位置间传递。
二、传质的机理1. 扩散传质机理:扩散是基于分子间相互作用力的结果,其中包括浓度、温度、粒径等因素。
分子扩散的速率与浓度梯度成正比,与温度和粒径成反比。
扩散的速度可以通过弗立策定律进行计算。
2. 对流传质机理:对流传质与扩散传质相比,对流传质在流体中较快。
对流传质通常包括液相传质和气相传质两种方式。
液相传质是指在液体中溶质的移动,流体的速度较慢,传质主要靠扩散。
气相传质是指气体中溶质的扩散,此时溶质分子与气流相比速度较快。
三、传质过程的描述传质过程的描述可以采用Fick定律进行模拟。
Fick第一定律描述了扩散传质的速率与浓度梯度的关系,表达式为J = -D(dC/dx),其中J是扩散通量,D是扩散系数,dC/dx是浓度梯度。
Fick第二定律描述了扩散速率与时间和距离的关系,表达式为∂C/∂t = D(∂²C/∂x²),其中∂C/∂t是时间变化率,∂²C/∂x²是浓度梯度。
四、传质的应用1. 化学反应:在化学反应中,传质可以使反应物质更快地达到反应场所,加快反应速率。
2. 分离过程:传质在分离过程中扮演重要角色,包括萃取、吸附、蒸馏等。
这些过程依赖于物质的传质过程来实现分离纯化的目的。
3. 制药工业:在药物的制造过程中,传质可以控制药物的扩散速度,确保最终药物的质量和稳定性。
4. 环境保护:传质在空气和水等介质中的传递可以帮助我们理解污染物的扩散和防治措施,如大气和水体污染的控制和修复。
化工传质与分离过程范文模板及概述1. 引言1.1 概述化工传质与分离过程是化学工程领域一个重要的研究方向。
传质作为化工过程中物质转移的基本现象,对于提高反应效率,优化分离过程以及实现工业生产具有至关重要的作用。
分离过程则是指将混合物中的不同组分分离出来的一系列工艺和技术手段。
本文将结合传质基础知识,探讨传质在分离过程中的作用以及分离过程对传质性能的影响,并进一步探讨如何优化实际分离过程以提高效率。
1.2 文章结构本文总共包括五个主要部分:引言、传质基础、分离过程概述、传质与分离过程的关系和结论。
在引言部分,我们首先概述了化工传质与分离过程的研究背景和意义,并介绍了本文所涵盖的内容。
之后,文章将详细阐述传质基础知识,包括传质定义、传质机制和传质模型。
接着,在第三部分中,我们会对各种常见的分离过程进行概述,包括定义、分类和应用领域。
第四部分将重点讨论传质在分离过程中的作用以及分离过程对传质性能的影响,并探讨如何通过优化过程来提高效率。
最后,在结论部分,我们将总结文章的主要观点和要点,并展望未来发展方向。
1.3 目的本文的目的是介绍化工传质与分离过程的基础知识和关系,并探讨如何通过优化分离过程来提高传质性能。
通过深入了解传质基础知识和各种常见的分离过程,读者可以更好地理解传质在实际工程中的应用。
此外,本文还旨在为相关领域研究者提供一个全面而清晰的概述,帮助他们在自己的研究项目中更好地设计和优化分离过程。
2. 传质基础2.1 传质定义传质是指在不同相的两个物质之间发生物质或能量交换的过程。
在化工领域中,传质通常涉及物质的扩散、溶解和析出等过程。
2.2 传质机制传质机制是指描述物质在不同相之间传递的方式和规律。
主要有以下几种传质机制:2.2.1 扩散扩散是指物质由浓度高的区域向浓度低的区域自发移动的过程。
根据扩散介质的性质,可以分为气体扩散、液体扩散和固体扩散三种形式。
2.2.2 对流对流是指由于流体的运动而导致物质传递的过程。
化工分离工程第一章 化工分离工程概述分离过程的分类:机械分离、传质分离传质分离过程用于各种均相混合物的分离,其特点是有质量传递现象发生,按所依据的物理化学原理不同,工业上常用的传质分离过程又可分为两大类,即平衡分离过程和速率分离过程。
平衡分离过程是借助分离媒介(如热量、溶剂或吸附剂)使均相混合物系统变成两相系统,再以混合物中各组分在处于相平衡的两相中不等同的分配为依据而实现分离。
分离媒介可以是能量媒介(ESA )或物质媒介(MSA ),有时也可两种同时应用。
蒸发、蒸馏、吸收、萃取、结晶、离子交换、吸附、干燥、浸取、泡沫吸附速率分离过程是在某种推动力(浓度差、压力差、温度差、电位差等)的作用下,有时在选择性透过膜的配合下,利用各组分扩散速率的差异实现组分的分离。
气体扩散、热扩散、电渗析、电泳、反渗透、超过滤 分离因子表示任一分离过程所达到的分离程度,其定义为2211//j i j i s ijx x x x =α分离方法的选择可行性、分离过程类别的选择、产品的价格、产品的热敏性、物质与分子的性质、经济性、安全与环保、经验分离过程类别的选择▪ 分子特性:分子重量、V an der Waals 体积、Van der Waals 面积、 偶极矩、极化度、双电常数、电荷、旋转半径▪ 热力学与传递性质:蒸气压、溶解度、吸附活性、扩散特性第二章 精馏蒸馏(Distillation ):借助液体混合物中各组分挥发性的差异而进行分离的一种操作方法。
简单蒸馏(simple distillation):混合液受热部分汽化,产生的蒸汽进入冷凝器种冷凝,分批收集不同组成的馏出液产品。
平衡蒸馏(equilibrium distillation):釜内液体混合物被部分汽化,使气相与液相处于平衡状态,然后将气相与液相分开,是一种单级蒸馏操作。
精馏 (rectification):液体混合物多次进行部分冷凝或部分汽化后,最终可以在气相中得到较纯的易挥发组分,而在液相中得到较纯的难挥发组分。