上海大学 材料 文档
- 格式:doc
- 大小:52.00 KB
- 文档页数:5

没有目标的人很容易中途放弃,一定坚持自己的目标!①如果你现在有目标院校,那最好不过了,去查找或者咨询历年的分数线,包括单科线、初试线、复试线。
去了解录取比例和每年报考人数,寻找理想院校的学长学姐进行基本的了解,了解她们是怎样复习的,包括专业课的用书。
要对你所报考的院校专业信息了如指掌,比如说近年是否连续扩招等等。
②如果你现在还没有想好要报考的学校,我只给你一个建议,择你所爱。
选择你特别喜欢的城市,或者特别喜欢向往的高校。
先不要考虑我选择的这个学校好不好考,竞争激烈不激烈,因为到最后无论你考的是什么学校你都一样是要付出全部的精力去认真对待的。
这个过程很辛苦,所以心里要有热爱要有梦想才能坚持下去,并且甘之如饴。
第一章要求掌握的内容第一节晶体与非晶体,晶体结构与空间点阵,晶胞与原胞,晶系,布拉菲点阵,点阵常数。
第二节晶面指数、晶向指数的确定,晶面族,晶向族,晶带轴,晶面与晶向平行或垂直。
第三节面心立方、体心立方、密排六方晶胞结构,原子数,配位数,紧密系数,间隙种类,间隙大小(定性),间隙位置,第四节面心立方和密排六方的堆垛方式,堆垛层错第一章(一)内容及习题引言金属由于其性能的多样性,而被人们广泛的应用。
金属的性能由其成分、结构所决定。
成分、结构、性能之间的关系,以及它们的变化规律,构成了本课程的基础。
金属(或非金属)在固态通常是晶体,故金属的结构通常被称为金属的晶体结构。
第一章介绍的是学习和研究晶体结构所需要掌握的一些基本知识――晶体学基础。
本节课要求1 要求掌握“晶体与非晶体、晶体结构与空间点阵、晶胞与原胞、晶系、布拉菲点阵、点阵常数”概念,理解布拉菲点阵的唯一性。
2 看完第一节,并完成习题1~3。
习题1描述晶体与非晶体的区别,从结构、性能等方面。
2何谓空间点阵,简述晶体结构与空间点阵的区别。
3 对于图1-4(n)的面心立方点阵,如果在该点阵的上下两个底面的面中心各添加一个阵点,请问,新的结构是属于14种空间点阵的哪一种。

上海大学854材料科学基础考研大纲2012考研政治新大纲总体稳定,变化有限,虚实结合,以虚为主变化:一.文字表述的调整二.考点的分合三.位置的移动注意:其中多处假变化实体变化①增加五个考点(有效考点一个,无效增加四个)②减少15个考点(马原减少一个)③调整时政范围(考2011全年)有效变化删除的十五个考点:马原1 第二章第二节:联系与发展2 第二节:唯物辩证法是认识世界和改造世界的根本方法毛中特3 第三章:新民主主义革命理论,革命统一战线的建立及其主义经验.4 武装斗争是中国革命的主要斗争形式.5 党的建设和主要内容和基本经验.6 十四章第二节:中国特色军事变革近代史7 第八章第三节:社会主义改造基本完成8 第九章第一节:整风运动,反右派斗争9 第九章第二节:庐山会议与纠左进程的中断10 第十章第一节:工作重心转移到经济建设上来11 第十章第三节:三个代表重要思想的提出思修12 第一章:学习和践行社会主义核心价值体系的重大意义13 当代大学生的历史使命14 第四章第二节:继承和弘扬中华民族优良道德传统的重大意义.15 第七章第三节:确定新德国家安全管理新增了四个考点马原16 第七章:社会主义在改革中的自我发展和自我完善社会主义改革应当追寻的原则有:①.坚持正确的理论指导.②坚持改革的正确方向③选择正确的改革方式和步骤.④妥善处理改革,发展,稳定的关系毛中特17 第六章:十二五规划关于发展战略的主要内容.①. 主题:科学发展,为了实现科学发展要做到四个更加注重②. 主线:加快转变经济发展方式,其基础要求是五个坚持③. 实现十二五规划的重大措施:五点2. 2011胡锦涛七一讲话①.建党九十年来,中共完成的三件大事.A,实现了民族独立,人民解放,开启新的历史纪元.B确定了社会的基本制度,实现了中国历史上最广泛最深刻的社会变革.C开创,坚持,发展了中国特色社会主义,推动社会主义现代化建设取得了举世瞩目的伟大成就.以上三件大事中得出的结论:A在近代以来中共社会发展,社会的进程中,历史和人民选择了中国共产党.B中国共产党不愧为领导人民不断开创事业发展的核心力量3.在推进改革开放中走好中国道路需做到五个坚定不移.4.第十二章:武力解决台湾的方针.特别需要关注的是:两个考点1.历史近现代史第八章第二节:选择社会主义道路改为--社会主义道路:历史和人民的选择。
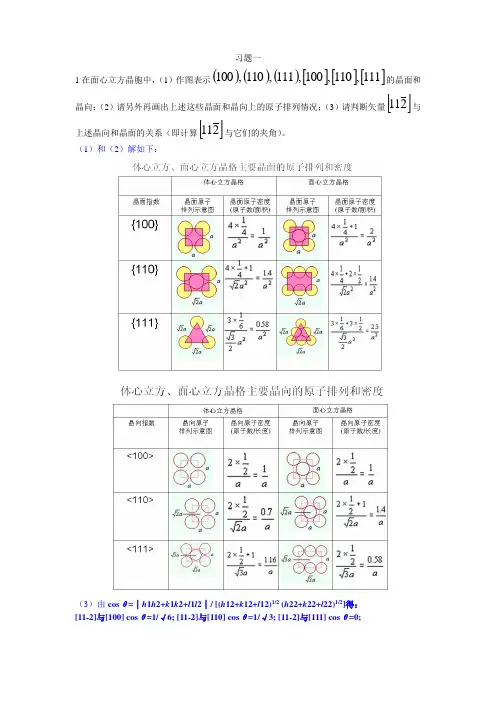
习题一1在面心立方晶胞中,(1)作图表示()()()[][][]111,110,100,111,110,100的晶面和晶向;(2)请另外再画出上述这些晶面和晶向上的原子排列情况;(3)请判断矢量[]211与上述晶向和晶面的关系(即计算[]211与它们的夹角)。
(1)和(2)解如下:(3)由cos θ=│h 1h 2+k 1k 2+l 1l 2│/ [(h 12+k 12+l 12)1/2 (h 22+k 22+l 22)1/2]得: [11-2]与[100] cos θ=1/√6; [11-2]与[110] cos θ=1/√3; [11-2]与[111] cos θ=0;2 请在六方晶系的晶胞上画出)(2110晶面、[]0211和[]1011晶向。
先把四指数换算成三指数:(10-12) = (102), [11-20] = [330] = [110], [-1101] = [-111],再作图3 碳具有哪些晶体结构?分别具有怎样的性能?(上网查)石墨、金刚石、碳60、碳纳米管等都是碳元素的单质,它们互为同素异形体。
石墨是元素碳的一种同素异形体,石墨为层状结构,一层中每个碳原子的周边连结着另外三个碳原子(排列方式呈蜂巢式的多个六边形)以共价键结合,层之间以范德华力结合,构成分子晶体。
由于每个碳原子均会放出一个电子,那些电子能够自由移动,因此石墨属于导电体。
石墨是其中一种最软的矿物。
它的用途包括制造铅笔芯和润滑剂等。
金刚石是自然界中最坚硬的物质。
金刚石的用途非常广泛,例如:工艺品、工业中的切割工具。
碳可以在高温、高压下形成金刚石。
碳原子按四面体成键方式互相连接,组成无限的三维骨架,是典型的原子晶体。
每个碳原子都以SP3杂化轨道与另外4个碳原子形成共价键,构成正四面体。
由于钻石中的C-C键很强,所以所有的价电子都参与了共价键的形成,没有自由电子,所以钻石不仅硬度大,熔点极高,而且不导电。
在工业上,钻石主要用于制造钻探用的探头和磨削工具,形状完整的还用于制造手饰等高档装饰品,其价格十分昂贵。

2.给出物相定性分析与定量分析的原理及一般步骤。
物相分析,定性分析,定量分析答:定性分析:原理:目前所知结晶物质,之所以表现出种类的差别,是由于不同的物质个具有自己特定的原子种原子排列方式和点阵常数,进而呈现出特定的衍射花样;多相物质的衍射花样互不干扰、相互独立,只是机械的叠加;衍射花样可以表明物相中元素的化学结合态。
这样只要把晶体全部进行衍射或照相再将衍射花样存档,试验时,只要把试样的衍射花样和标准衍射花样相对比,从中选出相同者就可以确定了。
步骤:先求出晶面间距d和相对强度I/I1后有以下三个程序:(1)根据待测相得衍射数据,得出三强面的晶面间距值d1、d2、d3.(2)根据d1值,在数值索引中检索适当d组,找出与d1、d2、d3值复合较好的一些卡片。
(3)把待测相的三强线的d值和I/I1值与这些卡片上各物质的三强线d值和I//I1值相比较,淘汰不相符的卡片,最后获得与试验数据一一吻合的卡片,卡片上所示物质即为待测相。
(4)若待测试样为复相混合物时,需反复测试定量分析:原理87页X射线物相分析法原理根据晶体对X射线的衍射特征-衍射线的位置、强度及数量来鉴定结晶物质之物相的方法,就是X射线物相分析法。
每一种结晶物质都有各自独特的化学组成和晶体结构。
没有任何两种物质,它们的晶胞大小、质点种类及其在晶胞中的排列方式是完全一致的。
因此,当X射线被晶体衍射时,每一种结晶物质都有自己独特的衍射花样,它们的特征可以用各个衍射晶面间距d和衍射线的相对强度I/I1来表征。
其中晶面间距d与晶胞的形状和大小有关,相对强度则与质点的种类及其在晶胞中的位置有关。
所以任何一种结晶物质的衍射数据d和I/I1是其晶体结构的必然反映,因而可以根据它们来鉴别结晶物质的物相。
3、说明影响光学显微镜和电磁透镜分辨率的关键因素是什么?如何提高电磁透镜的分辨率?解:光学显微镜的分辨本领取决于照明光源的波长。
电磁透镜的分辨率由衍射效应和球面像差来决定,球差是限制电磁透镜分辨本领的主要因素。

上海大学材料成型技术第一篇:上海大学材料成型技术绪论“材料成形技术基础”是机械工程专业和相关工程专业学生的一门重要的技术基础课程,主要研究机器零件的常用材料和材料成形方法,即从选择材料到毛坯或零件成形的综合性课程。
通过本课程的学习,可获得常用工程材料及材料成形工艺的知识,培养学生工艺分析的能力,了解现代材料成形的先进工艺、技术和发展趋势,为后续课程学习和工作实践奠定必要的基础。
材料是科学与工业技术发展的基础。
先进的材料已成为当代文明的主要支柱之一。
人类文明的发展史,是一部学习利用材料、制造材料、创新材料的历史。
如果查看一下诺贝尔物理、化学奖的获得者,不难发现20世纪的物理学家和化学家们曾对材料科学做过一系列的贡献。
Laue(1914)发现X光晶体衍射,Guillaume(1920)发现合金中的反常性质,Bridgeman(1946)发现高压对材料的作用,Schockley、Bardeen、Brattain(1956)三人发现了半导体晶体管,Landau(1962)的物质凝聚态理论,T ownes(1964)发现导致固体激光的出现,Neel(1970)发现材料的反铁磁现象,Anderson、Mott、van Vleck(1977)研究了非晶态中的电子性状,Wilson (1982)对相变的研究成功,Bednorz、Müller(1987)发现了30°K的超导氧化物,Smaller、Kroto(1996)发现C-60,Kilby (2000)发明第一块芯片,上述物理领域的诺贝尔获奖者的不少工作是直接针对材料的。
至于化学家们,可以举出Giauque(1949)研究低温下的物性,Staudinger(1953)研究高分子聚合物,Pauling (1954)研究化学键,Natta、Ziegler(1963)合成高分子塑料,Barton、Hassel(1969)研究有机化合物的三维构象,Heegler、Mcdermild、白川英树(2000)三人发现导电高分子。

上海大学材料科学基础知识点第一章材料中的原子排列第一节原子的结合方式1原子结构2原子结合键(1)离子键与离子晶体原子结合:电子转移,结合力大,无方向性和饱和性;离子晶体;硬度高,脆性大,熔点高、导电性差。
如氧化物陶瓷。
(2)共价键与原子晶体原子结合:电子共用,结合力大,有方向性和饱和性;原子晶体:强度高、硬度高(金刚石)、熔点高、脆性大、导电性差。
如高分子材料。
(3)金属键与金属晶体原子结合:电子逸出共有,结合力较大,无方向性和饱和性;金属晶体:导电性、导热性、延展性好,熔点较高。
如金属。
金属键:依靠正离子与构成电子气的自由电子之间的静电引力而使诸原子结合到一起的方式。
(3)分子键与分子晶体原子结合:电子云偏移,结合力很小,无方向性和饱和性。
分子晶体:熔点低,硬度低。
如高分子材料。
氢键:(离子结合)X-H---Y(氢键结合),有方向性,如O- H—O(4)混合键。
如复合材料。
3结合键分类(1)一次键(化学键):金属键、共价键、离子键。
(2)二次键(物理键):分子键和氢键。
4原子的排列方式(1)晶体:原子在三维空间内的周期性规则排列。
长程有序,各向异性。
(2)非晶体:――――――――――不规则排列。
长程无序,各向同性。
第二节原子的规则排列一晶体学基础1 空间点阵与晶体结构(1)空间点阵:由几何点做周期性的规则排列所形成的三维阵列。
特征:a 原子的理想排列;b 有14种。
其中:空间点阵中的点-阵点。
它是纯粹的几何点,各点周围环境相同。
描述晶体中原子排列规律的空间格架称之为晶格。
空间点阵中最小的几何单元称之为晶胞。
(2)晶体结构:原子、离子或原子团按照空间点阵的实际排列。
特征:a 可能存在局部缺陷; b 可有无限多种。
2晶胞(1)――-:构成空间点阵的最基本单元。
(2)选取原则:a 能够充分反映空间点阵的对称性;b 相等的棱和角的数目最多;c 具有尽可能多的直角;d 体积最小。
(3)形状和大小有三个棱边的长度a,b,c及其夹角α,β,γ表示。

《材料科学基础》学习要求一考试题型及分数分布:选择题(20%)、判断题(10%)、名词解释(20%)、简答题或论述题(30%)和计算题(20%)二考试内容及要求:第一章绪论1 知道材料化学领域重要的中外文期刊各3种(填空题)中文:??外文:??2 掌握材料科学与工程的四个基本要素,并理解他们之间的相互关系(论述题)答:使用效能、性能、合成与制备、组成与结构。
材料的组成与结构决定材料的性质,而组成与结构又是合成与制备的产物,材料作为产品必须具有一定的效能以满足使用条件和环境要求,从而取得应有的经济和社会效应。
因此,上述四个组元之间存在者相互依赖的关系。
无机材料科学与工程就是一门研究无机材料的合成与制备、组成与结构、性能与使用效能四者之间相互关系与制约规律的科学。
3 了解几种材料的分类方法(填空题)答:??4 论述材料的重要性(是非判断题)(1)促进科学技术发展(2)推动工业及社会进步(3)巩固国防和发展军用技术(4)推动生物医学的发展5 了解材料研究的前沿与热点(填空题)功能陶瓷、结构陶瓷、半导体材料、特种玻璃、人工晶体、耐火材料、水泥。
第二章晶体结构1 掌握晶体与非晶体的概念、区别及联系。
(填空题或论述题)晶体:构晶离子在三维空间有规则的周期性重复排列包含:单晶、多晶举例:天然金刚石、水晶、方解石、结晶盐非晶体:一种过冷状态的液体特点是近程有序、远程无序举例:玻璃、塑料、树脂等晶体和非晶体之间可以相互转化:非晶体经过热处理,可以转化为晶体,晶体经快速冷却或特殊制备方法可获得非晶体晶体Vs非晶体结构差异导致性质不同1.晶体:最小内能、热力学稳定2.晶体:固定熔点3.晶体:各向异性4.晶体:均匀性5.晶体:自范性-自发形成规则几何多面体外形6晶体:对称性77.晶体:衍射效应。
2 掌握空间点阵(名词解释)、晶胞(名词解释)的概念与抽取原则;熟悉七种晶系、十四种布拉菲点阵的结构关系。
(简答题)3 掌握立方晶系晶向、晶面、晶向指数、晶面指数的概念及确定。

铝率(IM):表示熟料中Al2O3与Fe2O3含量之比,反映熟料中C3A和C4AF的相对含量,也反映煅烧过程中液相的性质。
IM大,C3A大、C4AF小,液相的n大,物料难烧结;反之,烧结范围小。
硅率(SM):表示熟料中SiO2与Al2O3、Fe2O3之和的比例,反映熟料硅酸盐矿物与溶剂矿物的相对含量。
SM大,硅矿多、溶剂矿物少,液相少,C3S形成难;反之,水泥强度低。
石灰饱和系数:全部SiO2被CaO所饱和形成C3S的程度。
石灰最大含量:水泥熟料中主要酸性氧化物理论生成熟料矿物所需的石灰最高含量。
校正原料:石灰质原料和粘土质原料配合所得生料的成分不满足配料的要求,需根据缺少的成分添加的原料。
铁质校正原料:含铁(Fe2O3)量大于40%的原料;硅质校正原料:含硅量在70%-80%的原料。
石灰岩:由CaCO3组成的化学及生物化学沉积岩;泥灰岩:由CaCO3与粘土物质共同沉积而成的均匀混合物沉积岩。
化学缩减:在水泥的水化过程中,无水的熟料矿物转变为水化物,固相体积逐渐增加,但水泥-水的体积总和不断减小,由于这种体积缩减是化学反应所致,故称化学缩减。
混凝土:以凝胶材料、水、粗集料、细集料按适当比例拌合均匀,经浇捣成型后硬化而成的一种材料。
防辐射水泥:具有防辐射性能的水泥,包括钡锶水泥、镁质水泥、重混凝土。
熔块:以无机玻璃的原料,融化成熔融或半熔,然后淬冷而处于破碎状态的玻璃态物质。
瓷釉:熔块或者熔块与磨加物一起粉碎,然后涂烧在金属表面上的物质。
道路水泥:混凝土路面所用水泥,不易损坏使用年限长路面阻力小抗油类侵蚀性强雨天不打滑保点养简单等优点。
提高性能:a.改变熟料矿物组成(C3S,C4AF升);b.改变石膏的添加量;c.控制粉磨细度(5%-10%);d.加入外加剂(<5%的石英砂)。
砌筑水泥:凡由活性混合材料加入适量硅酸盐水泥熟料或石膏经磨细制成的水硬性胶凝材料。
要求:a.SO3<4%;b.细度<10%;c.初凝>45min,终凝<12h;d.安全性良好。
1. 描述晶体与非晶体的区别,从结构、性能等方面。
2. 描述晶体结构与空间点阵的区别。
3. 在简单立方晶系中,作图表示下述的晶面和晶向,并指出其中哪些晶面与
晶向是垂直的,哪些是平行的。
()()()[][][]211,110,111,201,011,111
4. 试在六方晶系的晶胞上画出)(2110晶面、[]0211和[]1011晶向。
5. 铜为面心立方结构,X 射线衍射测定a=0.3615nm ,(1)按刚球密堆模型
计算最近邻原子中心距离是多少?以任一原子为中心,这样距离的原子数目是多少?(2)原子密排面和密排方向是什么?堆垛顺序如何?(3)原子密排面{hkl}和密排方向<uvw>组成的{hkl}<uvw>(注意:[uvw]须位于(hkl)面上)共有多少组?
6. 铁有两种结构,分别为体心立方A2(α-Fe )和面心立方A1(γ-Fe ),
铁和碳的原子半径分别为0.127nm 和0.077nm ,问:碳更易进入两种铁的四面体间隙还是八面体间隙?为什么?当碳进入铁的间隙后,铁的结构会发生怎样的变化?
7. 分别对面心立方A1和体心立方A2的(100)、(110)、(111)面,请问:
(1)计算上述晶面的紧密系数,指出最紧密排列的晶面。
(2)画出上述晶面的原子排列方式。
(3)计算上述晶面的晶面间距。
8. 请计算密排六方A3的(0001)、(1-100)、(-12-10)晶面的紧密系数,指出
最紧密排列的晶面。
请画出这些晶面的原子排列方式。
9. 请指出面心立方A1和密排六方A3的原子堆垛顺序,同时指出是以哪个晶
面进行堆垛的。
第二章 内容及习题
第二节 波尔理论和波动力学理论对原子核外电子的运动轨道的描
述。
波粒两相性的基本方程。
第三节 五种结合键的特点
第四节 结合键与晶体结构
第五节 合金,合金系,合金相结构分类
第六节影响相结构因素
第七节固溶体,置换固溶体,间隙固溶体,有限固溶体,无限固溶
体,有序固溶体,无序固溶体,端部固溶体,中间固溶体
第八节离子化合物的结构类型和特点
第九节硅酸盐结构的一般特点
习题
1.波尔理论和波动力学理论在对原子核外电子的运动轨道的描述上有何差
异。
2.粒子具有波粒二象性,请计算下列粒子的波长:
A质量为20g,速度为1000m/s的子弹;
B质量为10-15kg,速度为0.01m/s的尘埃;
C质量为9.1×10-31kg,速度为106m/s的电子。
3.指出形成离子键、共价键、金属键、分子键和氢键时键合作用力的来源。
4.从结合键的角度简述元素晶体结构特点和周期性,并指出下述元素的结合键类型和
结构类型:铝、硅、砷、碘、α-Fe、镁。
5.简述下列概念:纯金属、合金、相、固溶体、化合物、固溶度、原子半径、负电性、
价电子浓度。
6.简述影响固溶度的影响。
7.简述固溶体的分类。
8.简述NaCl型、CsCl型、立方ZnS型、六方ZnS型、CaF2型、金红石型结构特点。
9.简述硅酸盐结构的基本特点。
第三章内容及习题
第一节理想晶体与晶体缺陷,缺陷种类
第二节点缺陷种类,空位形成本质,点缺陷平衡浓度,空位种类,点缺陷对性能的影响
第三节位错与滑移,螺位错,刃位错,混合位错,柏矢量
第四节螺位错和刃位错的特征,应变能,线张力,位错线受力
第五节滑移,攀移,割界,应力集中
第六节 位错反应,全位错,不全位错,扩展位错
第七节 晶界,亚晶界,相界,共格界,孪晶界
习 题
1. 何谓理想晶体,何谓晶体缺陷
2. 缺陷可以分为几类?对每一类缺陷说出一种具体的缺陷名称。
3. 点缺陷的存在,对晶体结构将造成怎样的影响?对晶体的性能将造成怎样
的影响?形成点缺陷的驱动力是什么?
4. 何谓肖脱基空位、弗仑克尔空位、点缺陷的平衡浓度
5. 简述刃型位错和螺型位错的特点。
6. (1)请说明柏氏矢量的物理意义。
(2)在一个简单立方的二维晶体中画出一
个正刃型位错和一个负刃型位错,用柏氏回路分别求出正、负刃型位错的柏氏矢量,并具体写出柏氏矢量的方向和大小。
(3)求出上述两个位错的柏氏矢量和。
7. 从热力学上说,空位是稳定缺陷,位错是不稳定缺陷,这句话对吗?为什
么。
8. 已知铁的空位形成能为104.6kJ/mol 。
试求,从20℃加热到850℃,空位
的数目将增加多少倍?简要解释快速淬冷到室温后,这些“额外”的空位会出现什么情况?
9. 在简单立方晶体中,假定有一个柏氏矢量在[0-10]晶向的刃型位错沿着
(100)晶面滑移。
(a )如果有另一个柏氏矢量在[010]方向,沿着(001)晶面上运动的刃型位错,通过上述位错时该位错将发生什么情况?请作图表示。
(b )如果有一个柏氏矢量方向为[100],并在(001)晶面上滑动的螺型位错通过上述位错,试问它将发生什么情况?请作图表示。
并指出与(a )相比有何差异?,
10.位错反应的基本条件是什么?判断下列位错反应是否能进行,为什么?
[][][]111321161102a a a
=+
11.何谓全位错、不全位错?说明弗兰克不全位错和肖克莱不全位错分别是如
何形成的。
指出形成弗兰克不全位错和肖克莱不全位错时的堆垛方式。
12.指出界面的种类。
指出小角度晶界和大角度晶界的区别。
第四章内容及习题
第一节扩散条件
第二节扩散定律的描述,第二定律在渗碳中的应用
第三节换位机制,空位机制,间隙机制,D = D0exp(-Q /RT)中参数的物理意义第四节柯肯达尔效应描述及其意义
第五节针对D = D0exp(-Q /RT)说明影响扩散的因素
习题
1.描述在金属固体中发生扩散时,原子是如何运动的。
指出扩散的条件。
2.有一球壳,内半径为r1,外半径为r2。
在T温度保温,有物质从球壳内
向球壳外扩散,当扩散达到平衡后,球壳内表面扩散物质的浓度为C1,外表面的浓度为C2,并测得在单位时间内从球壳内向球壳外扩散的物质总量为Q。
设扩散系数为常数。
求:
A,扩散系数。
B,r=(r1+r2)/2处的浓度。
3.指出第一定律、第二定律中的不同解分别适用的场合。
4.对于第二节第15页上的例子,问:扩散7×107s后,表面、距表面4和8
μm处的硼浓度分别是多少?(1100℃时硼在硅中的扩散系数D为
4×10-17m2/s,硼膜质量为M=9.43×1019原子/m2)
5.钢可以在870℃渗碳也可以在930℃渗碳,问:A)计算钢在870℃和930℃
渗碳时,碳在钢(奥氏体)中的扩散系数。
已知D0=2.0×10-5m2s-1,Q=144×103J/mol。
B)在870℃渗碳要用多长时间才能获得930℃渗碳10小时的渗层深度?(渗层深度:在浓度-距离曲线中,某一浓度所对应的离表面的距离。
)
6.简述置换原子和间隙原子的扩散机制。
7.何谓柯肯达尔效应,简述柯肯达尔效应的意义。
8.简述晶体结构对扩散的影响。