2.3 晶体结构
- 格式:ppt
- 大小:3.87 MB
- 文档页数:62


三种晶体结构的最密排晶面和最密排晶向1.引言1.1 概述晶体是具有长程有序排列的原子、离子或分子的固体物质。
晶体的结构是由最密排列的晶面和晶向构成的。
最密排晶面是指在晶体结构中,原子、离子或分子最紧密地靠近的面,而最密排晶向则指的是在晶体中最紧密地排列的方向。
本文将分析三种不同的晶体结构,探讨它们各自的最密排晶面和最密排晶向。
通过深入研究这些结构的排列方式,可以更好地理解晶体的性质和行为。
第一种晶体结构是立方晶系,也是最简单的晶体结构之一。
它的最密排晶面是(111)晶面,最密排晶向则是[110]晶向。
这些晶面和晶向在晶体中具有紧密的排列,使晶体的结构呈现出高度的对称性。
第二种晶体结构是六方晶系,它相对于立方晶系而言稍复杂一些。
在六方晶系中,最密排晶面是(0001)晶面,最密排晶向是[10-10]晶向。
与立方晶系不同,六方晶系具有六方对称性,呈现出更复杂的晶体结构。
第三种晶体结构是四方晶系,它也是一种常见的晶体结构。
在四方晶系中,最密排晶面是(100)晶面,最密排晶向是[110]晶向。
四方晶系的晶体结构与立方晶系相似,但具有更多的对称性和排列方式。
通过对这三种晶体结构的最密排晶面和最密排晶向进行研究,我们可以更好地理解晶体的基本结构和性质。
这对于材料科学、凝聚态物理和相关领域的研究具有重要意义,同时也有助于开发新材料和改进现有材料的性能。
1.2文章结构文章结构部分的内容可以包括以下几个方面的介绍:1.2 文章结构本文主要分为引言、正文和结论三个部分。
引言部分概述了晶体结构和最密排晶面、最密排晶向的研究背景和重要性,并提出了本文研究的目的和意义。
正文部分分为三个小节,分别介绍了三种晶体结构的最密排晶面和最密排晶向。
每个小节将首先介绍该种晶体结构的一般特点和常见应用,然后详细讨论最密排晶面和最密排晶向的确定方法和规律,并给出具体的实例和数据进行说明。
结论部分对于每种晶体结构的最密排晶面和最密排晶向进行总结和回顾,并指出各种晶体结构最密排晶面和最密排晶向的综合特点和应用前景。

高中化学必修二课本目录第一部分:物质结构与性质第一章原子结构与元素性质1.1 原子结构1.2 元素周期表与元素周期律1.3 元素性质与原子结构的关系第二章化学键与分子结构2.1 化学键的形成与类型2.2 分子结构与性质2.3 晶体结构第三章氧化还原反应3.1 氧化还原反应的概念3.2 氧化还原反应的规律3.3 氧化还原反应的平衡第四章溶液与电解质4.1 溶液的形成与性质4.2 电解质与非电解质4.3 电解质溶液中的离子平衡第五章有机化合物5.1 有机化合物的结构与性质5.2 有机化合物的分类与命名5.3 有机化合物的反应类型第二部分:化学反应原理第六章化学反应速率与化学平衡6.1 化学反应速率的概念与测定6.2 化学平衡的概念与影响因素6.3 化学平衡的计算与应用第七章电化学7.1 原电池与电解池7.2 电极电位与电动势7.3 电解质溶液中的电化学过程第八章化学反应的热力学8.1 化学反应热力学的基本概念8.2 化学反应热力学第一定律8.3 化学反应热力学第二定律第三部分:实验化学第九章实验化学基础9.1 实验室安全与环境保护9.2 实验室常用仪器与试剂9.3 实验操作的基本技能第十章化学实验设计与实践10.1 化学实验设计的原则与方法10.2 化学实验实践与数据处理高中化学必修二课本目录第一部分:物质结构与性质第一章原子结构与元素性质1.1 原子结构1.2 元素周期表与元素周期律1.3 元素性质与原子结构的关系第二章化学键与分子结构2.1 化学键的形成与类型2.2 分子结构与性质2.3 晶体结构第三章氧化还原反应3.1 氧化还原反应的概念3.2 氧化还原反应的规律3.3 氧化还原反应的平衡第四章溶液与电解质4.1 溶液的形成与性质4.2 电解质与非电解质4.3 电解质溶液中的离子平衡第五章有机化合物5.1 有机化合物的结构与性质5.2 有机化合物的分类与命名5.3 有机化合物的反应类型第二部分:化学反应原理第六章化学反应速率与化学平衡6.1 化学反应速率的概念与测定6.2 化学平衡的概念与影响因素6.3 化学平衡的计算与应用第七章电化学7.1 原电池与电解池7.2 电极电位与电动势7.3 电解质溶液中的电化学过程第八章化学反应的热力学8.1 化学反应热力学的基本概念8.2 化学反应热力学第一定律8.3 化学反应热力学第二定律第三部分:实验化学第九章实验化学基础9.1 实验室安全与环境保护9.2 实验室常用仪器与试剂9.3 实验操作的基本技能第十章化学实验设计与实践10.1 化学实验设计的原则与方法10.2 化学实验实践与数据处理第四部分:化学与社会生活第十一章化学与能源11.1 化石燃料与新能源11.2 化学在能源转换中的应用11.3 能源与环境问题第十二章化学与环境保护12.1 环境污染与化学治理12.2 化学在环境保护中的应用12.3 绿色化学与可持续发展第十三章化学与医药13.1 化学与药物研发13.2 化学在疾病诊断与治疗中的应用13.3 化学与人类健康第五部分:化学前沿与探索第十四章现代化学研究方法14.1 量子化学与分子模拟14.2 化学信息学与数据挖掘14.3 化学纳米技术与材料科学第十五章化学前沿领域的探索15.1 纳米化学与纳米材料15.2 界面化学与表面活性剂15.3 生物化学与生物技术16.1 化学与人类文明的进步16.2 化学在解决全球性问题中的作用16.3 化学教育的未来与发展。



药物分析中的药物结晶研究药物结晶是药物分析中的重要研究方向之一,它通过探究药物的晶体结构和性质,为药品的研发和生产提供了重要的理论基础和技术支持。
本文将从药物结晶的基本原理、研究方法和应用角度进行论述。
1. 药物结晶的基本原理药物结晶是在适当的溶剂中,由于药物分子之间的相互作用力而形成具有一定有序性的晶体。
药物结晶的基本原理可归纳为溶剂选择、溶剂温度、溶剂浓度和溶剂pH值等因素的影响。
1.1 溶剂选择溶剂选择是影响药物结晶的重要因素。
药物溶解度与溶剂的极性、键能、饱和度和存在形式等有密切关系。
在选择溶剂时,需要考虑溶剂的亲疏水性和溶剂的溶解能力,以及药物的特点和研究目的。
1.2 溶剂温度溶剂温度对药物结晶过程中的晶体形态和结晶速率有重要影响。
一般来说,温度升高会促进溶液中药物分子的运动,有利于形成较大晶体颗粒。
但是温度过高又会导致晶体粗大、结晶度低、晶型转变等问题。
因此,在药物结晶研究中需要根据具体药物的特性选择合适的结晶温度。
1.3 溶剂浓度溶剂浓度是影响药物结晶的重要因素之一。
过高或过低的溶剂浓度都会对药物的结晶产率和纯度造成影响。
通常来说,合适的溶剂浓度能够提供较好的晶体形态和结晶度。
1.4 溶剂pH值溶剂的pH值对药物结晶也有一定的影响。
药物分子在不同pH值的溶液中,其离子态和非离子态的比例不同,从而影响了溶剂的溶解性和药物分子的相互作用力。
因此,在药物结晶研究中,合适的溶剂pH值也是需要考虑的因素。
2. 药物结晶的研究方法药物结晶研究涉及许多实验技术和分析方法,包括晶体生长动力学研究、晶体形态表征、晶体结构分析等。
2.1 晶体生长动力学研究晶体生长动力学研究是药物结晶研究中的重要方向之一。
通过实验室制备不同条件下的药物晶体,观察晶体的生长形态和速率,分析晶体生长的动力学过程,推测药物结晶的机制和影响因素。
2.2 晶体形态表征晶体形态表征是药物结晶研究中必不可少的内容。
通过显微镜观察药物晶体的外形、尺寸和形态,利用非接触式测量方法如显微照相、光学显微镜、电子显微镜等,对药物晶体形态进行表征和测量。

材料科学基础第2 章2.3.9尖晶石型晶体结构分析AB 2O 4的单位晶胞24化学式AB 2O 4A: 2价阳离子B: 3价阳离子晶体结构立方晶系Z=8离子堆积情况O 2-按立方紧密堆积排列,A 2+填充八分之一四面体空隙,B 3+填充二分之一八面体空隙24尖晶石晶体结构[AlO6]八面体[MgO4]四面体代表性物质镁铝尖晶石MgAl2O4a0=0.808nm,Z=8有缘学习更多驾卫星ygd3076或关注桃报:奉献教育(店铺)[AlO 6]八面体[MgO 4]四面体24[AlO 6]八面体[MgO 4]四面体[AlO 6]八面体[MgO 4]四面体共顶连接共棱连接彼此孤立通过八面体共顶连接共顶连接尖晶石晶体结构(a)(b)M 区(c) N 区Mg 2+O 2-Mg 2+O 2-At 3+24反尖晶石24 如果二价阳离子分布在八面体空隙中,而三价阳离子一半在四面体空隙中,另一半在八面体空隙中的尖晶石,称为反尖晶石。
性能与用途①性能②用途典型的磁性非金属材料,性能比磁性金属材料更优越。
具有强磁性,高电阻,低松弛损耗等特点可做无线电、电视、电子装置的元件,计算机中做记忆元件,微波器中做永久磁石24尖晶石型结构晶体氟、氰化物氧化物硫化物BeLi 2F 4TiMg 2O 4ZnCr 2O 4ZnFe 2O 4MgAl 2O 4MnCr 2S 4MoNa 2F 4VMg 2O 4CdCr 2O 4CoCo 2O 4MnAl 2O 4CoCr 2S 4ZnK 2(CN)4MgV 2O 4ZnMn 2O 4CuCo 2O 4FeAl 2O 4FeCr 2S 4CdK 2(CN)4ZnV 2O 4MnMn 2O 4FeNi 2O 4MgGa 2O 4CoCr 2S 4MgK 2(CN)4MgCr 2O 4MgFe 2O 4GeNi 2O 4CaGa 2O 4FeNi 2S 4FeCr 2O 4FeFe 2O 4TiZn 2O 4MgIn 2O 4AB 2O 4型无机化合物(尖晶石)的晶体结构MgAl2O4性能与用途①性能②用途硬度较大,莫氏硬度为8级,熔点为2105℃,ρ=3.55g/cm3,化学性质较稳定,热稳定性好(热膨胀系数小,为7.6×10-6)镁铝尖晶石是用途很广泛的优良耐高温材料24Al-O键与Mg-O离子结合键强24在镁铝尖晶石结构中,在一个氧离子周围,有一个镁离子和三个铝离子,由静电价规则:由此可见,氧离子的电价是饱和的。

第2章晶体结构提纲:2.1 晶体学基础2.2 金属的晶体结构2.3 合金相结构2.4 离子晶体结构2.5 共价晶体结构2.6 聚合物的晶态结构2.7 非晶态结构学习要求:掌握晶体学基础及典型晶体的晶体结构,了解复杂晶体(包括合金相结构、离子晶体结构,共价晶体的结构,聚合物的晶态结构特点)、准晶态结构、液晶结构和非晶态结构。
1.晶体学基础(包括空间点阵概念、分类以及它与晶体结构的关系;晶胞的划分,晶向指数、晶面指数、六方晶系指数、晶带和晶带定律、晶面间距的确定、极射投影);2.三种典型金属晶体结构(晶胞中的原子数、点阵常数与原子半径、配位数与致密度、堆垛方式、间隙类型与大小);3.合金相结构(固溶体、中间相的概念、分类与特征);4.离子晶体的结构规则及典型晶体结构(AB、AB2、硅酸盐);5、共价晶的结构规则及典型晶体结构体(金刚石)6、聚合物的晶态结构、准晶态结构、液晶结构和非晶态结构。
重点内容1.选取晶胞的原则;Ⅰ) 选取的平行六面体应与宏观晶体具有同样的对称性;Ⅱ)平行六面体内的棱和角相等的数目应最多;Ⅲ)当平行六面体的棱角存在直角时,直角的数目应最多;Ⅳ)在满足上条件,晶胞应具有最小的体积。
2.7个晶系,14种布拉菲空间点阵的特征;(1)简单三斜(2)简单单斜底心单斜(3)简单正交底心正交体心正交面心正交(4)简单六方(5)简单四方体心四方(6)简单菱方(7)简单立方体心立方面心立方3.晶向指数与晶面指数的标注,包括六方体系,重要晶向和晶面需要记忆。
4.晶向指数,晶面指数,晶向族,晶面族,晶带轴,共带面,晶面间距5.8种,即1,2,3,4,6,i,m,。
或C1,C2,C3,C4,C6 ,C i,C s,S4。
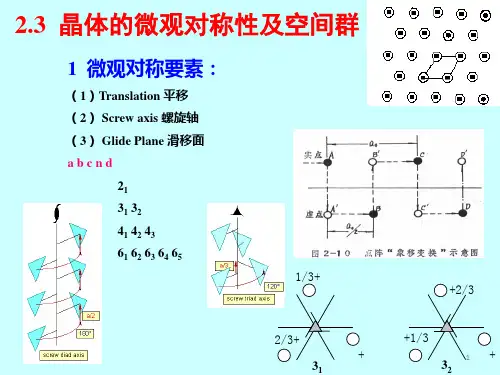
微观对称元素6.极射投影与Wulff网;标hkl直角坐系d4⎧⎨⎩微观11213215243滑动面 a,b,c,n,d螺旋轴 2;3,3;4,4,4;6,6,6,6,67.三种典型金属晶体结构的晶体学特点;在金属晶体结构中,最常见的是面心立方(fcc)、体心立方(bcc)和密排六方(hcp)三种典型结构,其中fcc和hcp系密排结构,具有最高的致密度和配位数。


材料科学基础第 2 章2.3.8钙钛矿的晶体结构分析钙钛矿型晶体结构属于复合氧化物钙钛矿属立方晶系,面心立方格子B离子占据立方体体心位置A 离子占据立方体角顶位置O 离子占据立方体面心位置3有缘学习更多驾卫星ygd3076或关注桃报:奉献教育(店铺)结构通式ABO3,其中A代表二价金属离子,B代表四价金属离子。
它是一种复合氧化物结构,该结构也可以是A为一价金属离子,B为五价金属离子。
3CaTiO3(钙钛矿型)晶体结构化学式CaTiO3晶体结构立方晶系,a0=0.385nm立方面心格子Ca2+ O2- Ti4+Z=4CaTiO3(钙钛矿型)晶体结构Ti4+配位CN=6与6个氧离子配位,构成[TiO6]八面体配位,共顶连接O2-配位CN=6与4个钙离子和2个钛离子配位,构成[OCa4TiO6] 配位Ca2+配位CN=12与12个氧离子配位,构成[CaO12] 配位为什么与O离子配位的分别是4个Ca2+,2个Ti4+?箭头所指的氧离子与立方体(010)面上的4个Ca2+配位,2个立方体体心位置的Ti4+配位。
Ca2+ O2- Ti4+为什么Ca离子的配位数为12?箭头所指钙离子与每个立方体3个面心位置的氧离子配位角顶上钙离子被周围8个立方体公用周围共有3 ×8=24个氧离子氧离子在面心位置,为相邻两个立方体公用,故CN=24 ÷2=12个Ca2+ O2- Ti4+Ca2+ O2- Ti4+钙钛矿结构中氧离子电价是否平衡?如何验证?箭头所指氧离子与立方体(010)面上的4个Ca2+配位,2个立方体体心位置的Ti4+配位。
根据静电价规则电价平衡钙钛矿中半径关系r O ——O 离子半径r A ——A离子半径r B ——B 离子半径半径有容差因子t=0.77-1.10CaTiO 3(钙钛矿型)晶体结构钙钛矿晶体结构中离子半径关系钙钛矿型结构晶体举例氧化物(1+5)氧化物(2+4)氧化物(3+3)氟化物(1+2)NaNbO3CaTiO3SrZrO3CaCeO3YAlO3KMgF3KNbO3SrTiO3BaZrO3BaCeO3LaAlO3KNiF3NaWO3BaTiO3PbZrO3PbCeO3LaCrO3KZnF3PbTiO3CaSnO3BaPrO3LaFeO3CaZrO3BaSnO3BaHfO3LaMnO3在不同温度时存在晶型转变结构特点结构畸变结构畸变立方晶系(高温)四方晶系正交晶系CaTiO 3(钙钛矿型)晶体结构性能与用途①性能②用途重要的功能材料,可通过掺杂改善其性能钙钛矿型BaTiO3,是典型的铁电材料,在居里温度以下有良好的铁电性能,是一种很好的光折变材料,可用于光储存。
《固体物理教案》PPT课件第一章:引言1.1 固体物理的重要性介绍固体物理在科学技术领域中的应用,如半导体器件、磁性材料等。
强调固体物理对于现代科技发展的关键性作用。
1.2 固体物理的基本概念定义固体物理的研究对象和方法。
介绍晶体的基本特征和分类。
1.3 教案安排简介本教案的整体结构和内容安排。
第二章:晶体结构2.1 晶体的基本概念解释晶体的定义和特点。
强调晶体结构在固体物理中的核心地位。
2.2 晶体的点阵结构介绍点阵的基本概念和分类。
讲解点阵的周期性和空间群的概念。
2.3 晶体的空间结构介绍晶体的空间结构描述方法。
讲解晶体中原子的排列方式和空间群的对称性。
第三章:晶体物理性质3.1 晶体物理性质的基本概念介绍晶体物理性质的分类和特点。
强调晶体物理性质与晶体结构的关系。
3.2 晶体介电性质讲解晶体的介电性质及其与晶体结构的关系。
介绍介电材料的制备和应用。
3.3 晶体磁性质讲解晶体的磁性质及其与晶体结构的关系。
介绍磁材料的制备和应用。
第四章:固体能带理论4.1 能带理论的基本概念介绍能带理论的起源和发展。
强调能带理论在固体物理中的重要性。
4.2 紧束缚模型讲解紧束缚模型的基本原理和应用。
介绍紧束缚模型的数学表达式和计算方法。
4.3 平面紧束缚模型讲解平面紧束缚模型的基本原理和应用。
介绍平面紧束缚模型的数学表达式和计算方法。
第五章:半导体器件5.1 半导体器件的基本概念介绍半导体器件的定义和特点。
强调半导体器件在现代电子技术中的重要性。
5.2 半导体二极管讲解半导体二极管的工作原理和特性。
介绍半导体二极管的制备和应用。
5.3 半导体晶体管讲解半导体晶体管的工作原理和特性。
介绍半导体晶体管的制备和应用。
第六章:超导物理6.1 超导现象的基本概念介绍超导现象的发现和超导材料的特点。
强调超导物理在凝聚态物理中的重要性。
6.2 超导微观理论讲解超导微观理论的基本原理,如BCS理论。
介绍超导材料的制备和应用。