热平衡计算
- 格式:pdf
- 大小:165.30 KB
- 文档页数:6

热平衡方程
热平衡方程计算公式:QρCa(tg1-ta)T=GCg(tg1-tg2)GCg(tg1-tg2)T=QρCa(tg1-ta)。
热平衡指同外界接触的物体,其内部温度各处均匀且等于外界温度的状况。
在热平衡时,物体各部分以及物体同外界之间都没有热量交换。
在热工和化学中,如物体在同一时间内吸收和放出的热量恰好相抵消,也称该物体处于热平衡。
倘若组成单个系统的各部分之间没有热量的传递,且与外界也没有热量的传递,则系统处于热平衡。
这时系统内各部分温度相等且等于外界温度。
在热平衡时,物体各部分以及物体同外界之间都没有热量交换。
在热工和化学中,如物体在同一时间内吸收和放出的热量恰好相抵消,也称该物体处于热平衡。
指温度不同的两个或几个系统之间发生热量的传递,直到系统的温度相等。
在热量交换过程中,遵从能量的转化和守恒定律。
从高温物体向低温物体传递的热量,实际上就是内能的转移,高温物体内能的减少量就等于低温物体内能的增加量。
热平衡定律:
若有A、B、C三个处于任意确定的平衡态的系统,而系统A和系统B是互相绝热的。
令A和B同时与系统C相互热接触,经过足够长的时间后,A和B都将与C达到热平衡。
这时使A和B不再绝热而相互热接触,实验证明,A和B的状态都不发生变化,即A
和B也是处于热平衡的。
此实验事实说明,如果两个热力学系统各自与第三个热力学系统处于热平衡,则它们彼此也必处于热平衡。


沸石转轮+co热平衡计算
沸石转轮和CO的热平衡计算可能涉及一定的化学工程和热力学知识。
以下是一般情况下的步骤,但具体的计算会取决于系统的具体参数和条件:
系统描述:
* 定义沸石转轮和CO系统的初始状态,包括温度、压力、流量等参数。
化学反应:
* 确定涉及的化学反应,例如沸石吸附CO的反应。
这可能涉及到反应的平衡常数等信息。
热平衡计算:
* 使用热平衡计算方法,考虑系统中的能量转移。
这可能包括传热、吸放热等。
物质平衡计算:
* 考虑系统中CO的流动和吸附等物质平衡。
温度和压力变化:
* 在各个阶段考虑系统中温度和压力的变化,特别是在吸附和解吸附过程中。
热力学性质:
* 使用适当的热力学性质和方程,例如热力学图表或计算工具,来确定系统在不同条件下的热平衡状态。
系统优化:
* 如果需要,可以对系统进行优化,以满足特定的热平衡要求或效率要求。
实验数据验证:
* 将计算结果与实验数据进行比较,以验证模型的准确性。
这只是一个一般的框架,具体的计算方法可能需要深入了解系统的详细特性和要求。
在进行这样的热平衡计算时,确保使用准确的热力学数据和适当的计算工具是非常重要的。
可能需要使用专业的化学工程软件或模拟工具,具体选择取决于系统的复杂性和你的需求。
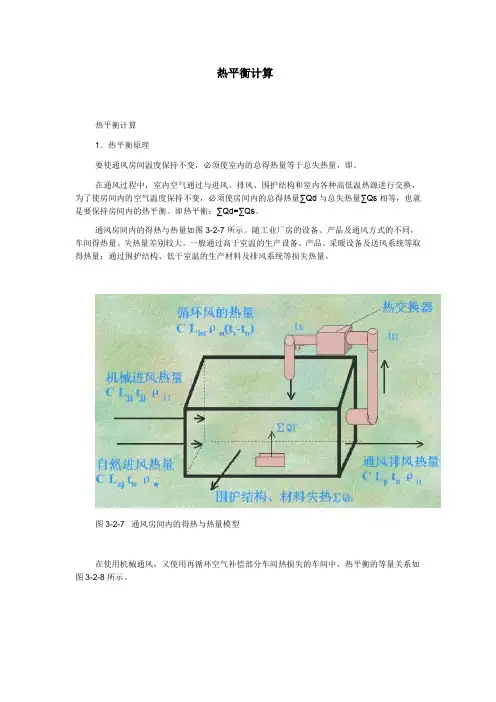
热平衡计算热平衡计算1.热平衡原理要使通风房间温度保持不变,必须使室内的总得热量等于总失热量,即。
在通风过程中,室内空气通过与进风、排风、围护结构和室内各种高低温热源进行交换,为了使房间内的空气温度保持不变,必须使房间内的总得热量∑Qd与总失热量∑Qs相等,也就是要保持房间内的热平衡。
即热平衡:∑Qd=∑Qs。
通风房间内的得热与热量如图3-2-7所示。
随工业厂房的设备、产品及通风方式的不同,车间得热量、失热量差别较大。
一般通过高于室温的生产设备、产品、采暖设备及送风系统等取得热量;通过围护结构、低于室温的生产材料及排风系统等损失热量。
图3-2-7 通风房间内的得热与热量模型在使用机械通风,又使用再循环空气补偿部分车间热损失的车间中,热平衡的等量关系如图3-2-8所示。
图3-2-8 热平衡的等量关系由图3-2-8的热平衡等量关系,即的通风房间热平衡方程式为:(3-2-16)式中——围护结构、材料吸热的总失热量,kW;——生产设备、产品及采暖散热设备的总放热量,kW;Lp——局部和全面排风风量,m3/s;Ljj——机械进风量,m3/s;Lzj——自然进风量,m3/s;Lhx——再循环空气量,m3/s;pu ——室内空气密度,kg/ m3;Pw——室外空气密度,kg/ m3;tu——室内排出空气湿度,℃;tjj——机械进风湿度,℃;to——再循环送风温度,℃;c——空气的质量比热,其值为1.01kj/kg·℃;tw——室外空气计算湿度,℃,tw的确定:在冬季,对于局部排风及稀释有害气体的全面通风,采用冬季采暖室外计算湿度。
对于消除余热、余湿及稀释低毒性有害物质的全面通风,采用冬季通风室外计算温度是指历年最冷月平均温度的平均值。
通风房间的风量平衡、热平衡是风流运动与热交换的客观规律要求,设计时应根据通风要求保证满足设计要求的风量平衡与热平衡。
如果实际运行时所达到的新平衡状态与设计要求的平衡状态差别较大,室内通风参数就达不到设计预期的要求。

专题16 热平衡方程一、热平衡方程1.对于一个与外界没有热交换的系统,一个物体放热,另一个物体吸热,且Q吸= Q放当物体温度相同时,热交换停止。
据此我们可以列出热平衡方程。
(1)高温物体放热公式:Q放=c1m1(t01-t)(2)低温物体吸热公式:Q吸=c2m2(t-t02)2.热平衡方程思想拓展高温物体和低温物体混合达到热平衡时,高温物体温度降低放出的热量等于低温物体温度升高吸收的热量。
这时Q放=c1m1(t01-t),Q吸=c2m2(t-t02)。
燃料完全燃烧放出的热量等于另外物体吸收的热量。
这时Q放=qm1,或者Q放=qV,Q吸=cm2(t-t0)。
电热器通电流放出的热量等于另外物体吸收的热量,这时Q放=I2Rt(焦耳定律公式),Q吸=cm(t-t0)。
利用热平衡方程可以求解很多问题,有时结合比例式,解题更简单。
3.比热容(1)定义:我们把单位质量的某种物质温度升高(或者降低)1℃所吸收(或者放出)的热量叫做这种物质的比热容,简称比热。
符号:c。
(2)公式:Q cm t =⋅∆(3)常用单位:焦耳/(千克·℃)(4)符号:J/(kg ·℃)(5)读作焦耳每千克摄氏度(6)同种物质来讲,比热容是一个确定的数值(相等的),跟物体质量的大小,温度改变的多少,物体的形状、体积、位置等无关,它仅与物质的种类和状态有关。
对不同物质来讲,比热容一般是不相同的。
(7)记住水的比热容:c水=4.2×103J/(kg·℃),物理意义为:1kg的水温度升高(或降低)1℃,吸收(或放出)的热量为4.2×103J。
因为水的比热容较大,所以水常用来调节气温、取暖、作冷却剂、散热等。
4.燃料完全燃烧放出热量(1)燃料完全燃烧释放出的热量公式为:Q放=mq。
(2)气体燃料完全燃烧释放出的热量公式也可为:Q放=qV。
推导过程如下:说明:①中的公式对固体、液体、气体、均适用。

热平衡计算
压降计算和相平衡计算中均需已知管段人口处的温度,:,而t:必须经过管段的热平衡
计算才能求得。
这里所说的热平衡即能量平衡。
其根据是管段的柏努利方程。
由于管段内的作功为零,忽略位能变化,可得
水蒸气注人炉管前后的焙差△Is有两种处理办法;一种是考虑水蒸气注人炉管后立即吸收油料热量,迅速达到与油料相同的温度。
这样考虑比较符合实际。
但计算时比较麻烦,因为难以确定注汽后经过多长的管段两者温度才达到相等。
另一种办法是将△Is平均分推在整个汽化段炉管上,这样处
理计算起来比较方便。
由于△1s值较小,对整个热平衡计算影响也不大,因此一般采用后一种办法,即。

高炉热平衡计算4.1热平衡计算的目的热平衡计算的目的,是为了了解高炉热量供应和消耗的状况,掌握高炉内热能的利用情况,研究改善高炉热能利用和降低消耗的途径。
通过计算调查高炉冶炼过程中单位生铁的热量收入与热量支出,说明热量收支各项对高炉冶炼的影响,从而寻找降低热消耗与提高能量利用的途径,达到使高炉冶炼过程处于能耗最低和效率最高的最佳运行状态。
同时还可以绘制热平计算表研究高炉冶炼过程的基本方法[2]。
4.2热平衡计算方法热平衡计算的量论依据是能量守恒定律,即单位生铁投入的能量总和应等于中位个铁各项热消耗总和。
热平衡计算采用差值法,即热损失是以总的热量收入减去各项热量的消耗而得到的,即把热量损失作为平衡项,所以热平衡表面上没有误差,因为一切误差都集中掩盖在所有热损失之中。
根据计算的目的和分析的需要,热平衡可分为全炉热平衡与区域热平衡。
全炉热平衡是把整个高炉作为研究对象、计算它的各项热收入与支出,用来分析高炉冶炼过程令的能量利用情况。
而区域热平衡是把高炉的某一个区域作为研究对象,计算和分析这个区域内的能量利用情况。
虽然计算热平衡的部位与方法不向,但计算的目的都是为寻找降低能耗的途径和确定一定冶炼条件下的能耗指标。
理论上可以以把高炉内的任何一个部位当作区域热平衡的计算对象,但由于决定向炉冶炼能耗指标的主要因素存在于高炉下部的高温区。
因此,常用高炉下部属温区热平衡进行计算。
本例采用第一热平衡法计算进行热平衡计算。
第一种热平衡法,亦称热工法热平衡。
它是根据羔斯定则,不考虑炉内的实际反应过程.耍以物料最初与最终状态所具有的热力学参数为依据,确定高炉内的过程中所提供和消耗的热量。
它的热收入规定为焦炭和喷吹物的热值(即全部C完全燃烧成CO2和H2全部燃烧成H2O时放出的热量)、热风与炉料带入的物理热及少量成渣热。
而热支出为氧化物、硫化物和碳酸盐的分解热,喷吹燃料的分解热,水分分解热。
脱S反应耗热,渣铁和炉顶煤气热焓与热值,冷却水代走的热量和炉体散热损失等项。


二、高温区域热平衡计算高温区热平衡与全炉热平衡计算的原则是相同的,而不同点是进入1000℃以上区域的物料要按l00℃左右温度差区别考虑,即煤气温度按1000℃、而物料按900℃计算。
【7】1 热量收入高温区热量收入主要是风口前焦炭、煤粉、重油的燃烧及热风带入的热量,与全炉热平衡计算方法相同。
(1) 风口前碳的燃烧放热(QC)首先计算总碳量:1)焦炭带入的碳量=455.6×0.8567=390.31kg2)煤粉带入的碳量=120×0.778=93.36 kg其次计算风口前燃烧碳量:1)每1kg燃烧时需氧根据 2C+O2=2COm3/kg C2)已知风量为1262m3;3)风口前燃烧的总碳量(C风口总):4)风口前燃烧的焦炭中的碳量( C风口,焦炭)所以它们的发热量为:QC=q焦炭+q煤=2173640 + 975985.44 =3149625.44 kJ(2)热风带入的热量式中,V风、C风、t风分别为风量、风的比热容与风温,查热力学数据表,1000℃时的比热容1.185kJ/(kg·℃)【15】2 热量支出计算铁等元素的还原、脱硫、石灰石分解、水分分解等均与全炉热平衡相同,(1)还原耗热(Q还原) 【8】1) Fe的直接还原耗热:(2890 kJ/kgFe)2) Si的还原耗热:3) Mn的还原耗热qMn=1.64×4877=7998.28 kJ4) P的还原耗热qP=2.65×26520=70278 kJQ还原=qFe+qSi+qMn+qP=1701633.775kJ (2) 脱硫耗热(QS)取qS 4600 kJ/kg 【8】QS=渣量×(S)× qS=439.69 ×0.0078× 4600= 15776kJ(3 )石灰石分解与反应热(Q石灰石)CaCO3=CaO十CO2 (3182 kJ/kg CaO)CO2十 C=2CO (3768.3 kJ/kg CO2)Q石灰石分解=58.2×0.496×3182 = 91855.43 kJQ石灰石反=58.2×0.496×0.4×3768.3 = 43512.11 kJ(4 )水分分解耗热(Q水分)H2O十C=H2十CO (13440 kJ/kg H2)Q水分=17.75×13440 = 238560kJ(5) 炉渣带走热量(Q渣)前述计算中取每lkg炉渣离开高炉时的焓为1780kJ/kg渣。

HRM2800原料立磨热平衡计算一、计算原始数据1、原料立磨设计产量G:120t/h2、原料立磨主电机功率P:1250 KW3、原料立磨主电机效率Y1:0.924、原料立磨传动效率Y2:0.85、原料立磨粉磨效率Y3:0.56、原料综合水分W1 %:8 %7、入磨热风温度T1:220℃8、入磨物料平均温度T s 1:25℃9、出磨热风温度T 2:90℃10、出磨物料温度T s 2:80℃11、出磨物料水分W2 %:0.5%12、磨机漏风率K1(占入磨热风量):10%13、入磨热风平均比热C1:0.347kcal/Nm3·℃14、磨机漏风平均比热C2:0.3 kcal /Nm3·℃15、磨机漏风平均温度T 3:25℃16、原料平均比热C C:0.223 kcal /㎏·℃17、水蒸气由0℃至90℃平均比热C S:0.45 kcal /㎏·℃18、出磨热风平均比热C3:0.34 kcal /Nm3·℃19、磨机散热系数α:16.3kcal/m2·℃20、磨机表面积F:150 m2二、热平衡计算热平衡计算以0℃、1小时为基准,磨机进出口截面为计算界限。
1、热收入A、入磨热风带入的热量:Q1=L· C1·T1=L×0.347×220=76.34L(kcal/h)设入磨热风量为L,Nm3/h。
B、粉磨产生的热量:Q2=860·P·Y1·Y2·(1-Y3)=860×1250×0.92×0.8×(1-0.5)=395600(kcal/h)C、磨机漏风带入的热量:Q3= K1·L· C2·T3=10%×L×0.3×25=0.75L(kcal/h)D、原料带入的热量:Q4= G·T S1·[C C+(W1-W2)/(100-W1)]=120000×25×[0.223+(8-0.5)/(100-8)]=913565.22(kcal/h)2、热支出A、水分蒸发消耗热量:Q5= G·(W1-W2)/(100-W1)·[595+C S T2-T S1] =120000×(8-0.5)÷(100-8)×[595+0.45×90-25]=5972282.61(kcal/h)蒸发水份体积:120000×[(8-0.5)/(100-8)] ÷0.805=12152.31Nm3/hB、出磨热风带走热量:(不包括水蒸气)Q6= L·(1+K1)·C3·T2=L×(1+10%)×0.34×90=33.66L(kcal /h)C、生料带走热量:Q7= G·(100-W2)/100·[C C+W2/(100- W2)]×(T S2- T S1)=120000×(100-0.5)/100·[0.223+0.5/(100- 0.5)]×(80- 25)=1497441(kcal/h)D、磨机散热损失:Q8=α·F·T2=16.3×150×90=220050(kcal/h)3、热平衡:热收入=热支出Q1+Q2+Q3+Q4 =Q5+Q6+Q7+Q876.34L+395600+0.75L+913565.22=5972282.61+33.66L+1497441+220050入磨热风量L=146917.07(Nm3/h)出磨风量L’=(1+10%)×146917.07+12152.31=173761.09(Nm3/h) L’-----仅为烘干物料时的出磨风量故,此时出磨的工况风量为:90℃;231044.96(m3/h)三、风量平衡决定风机风量应考虑以下几点:1、为带走磨机生产的生料所需要的最小风量(本台设备出磨最小风量120000000g/h÷800g/N m3≈150000(Nm3/h)。

二、 高温区域热平衡计算高温区热平衡与全炉热平衡计算的原则是相同的,而不同点是进入1000℃以上区域的物料要按l00℃左右温度差区别考虑,即煤气温度按1000℃、而物料按900℃计算。
【7】 1 热量收入高温区热量收入主要是风口前焦炭、煤粉、重油的燃烧及热风带入的热量,与全炉热平衡计算方法相同。
(1) 风口前碳的燃烧放热(Q C) 首先计算总碳量:1)焦炭带入的碳量=455.6×0.8567=390.31kg 2)煤粉带入的碳量=120×0.778=93.36 kg 其次计算风口前燃烧碳量: 1)每1kg 燃烧时需氧 根据 2C+O2=2CO933.02124.22=⨯m3/kg C2)已知风量为1262m3;3)风口前燃烧的总碳量(C 风口总):kgC 05.284933.0121.01262933.01=⨯⨯=⨯⨯=风中氧量风量风口总4)风口前燃烧的焦炭中的碳量( C 风口,焦炭)kg C 81.22124.6205.284,=-=焦炭风口所以它们的发热量为:Q C =q焦炭+q煤=2173640 + 975985.44 =3149625.44 kJ(2) 热风带入的热量风风风风t C V Q =式中,V 风、C 风、t 风分别为风量、风的比热容与风温,查热力学数据表,1000℃时的比热容1.185kJ /(kg·℃)【15】KJt C V Q 625.19254171000185.1825.1624=⨯⨯==风风风风kJq 217364098008.221=⨯=焦炭KJq 44.9759851045436.93=⨯=煤kJ Q Q Q C 065.5075043=+=风收入2 热量支出计算铁等元素的还原、脱硫、石灰石分解、水分分解等均与全炉热平衡相同, (1)还原耗热(Q 还原) 【8】1) Fe 的直接还原耗热:(2890 kJ /kgFe)kJqq Fe 095.1503047289055.061.945r 945.61d =⨯⨯=⨯⨯=2) Si 的还原耗热:3) Mn 的还原耗热q Mn =1.64×4877=7998.28 kJ4) P 的还原耗热q P =2.65×26520=70278 kJQ 还原=q Fe +q Si +q Mn +q P =1701633.775kJ (2) 脱硫耗热(Q S)取q S 4600 kJ/kg 【8】 Q S =渣量×(S )× q S=439.69 ×0.0078× 4600 = 15776kJ(3 )石灰石分解与反应热(Q 石灰石)CaCO3=CaO 十CO2 (3182 kJ /kg CaO)CO2十 C=2CO (3768.3 kJ /kg CO2) Q 石灰石分解=58.2×0.496×3182 = 91855.43 kJQ 石灰石反=58.2×0.496×0.4×3768.3 = 43512.11 kJ(4 )水分分解耗热(Q 水分)H2O 十C =H2十CO (13440 kJ /kg H2) Q 水分=17.75×13440 = 238560kJ(5) 炉渣带走热量(Q 渣)前述计算中取每lkg 炉渣离开高炉时的焓为1780kJ /kg 渣。
回转窑系统热平衡计算回转窑是一种重要的热工设备,广泛应用于水泥生产中。
对于回转窑系统的热平衡计算是评估系统运行状态和发现问题的重要工作。
本文将介绍回转窑系统热平衡计算的基本原理和方法。
物料热量输入是指物料在回转窑中的煅烧过程中释放的热量。
物料热量输入可以通过测量物料的热容量和温度差来计算,即Q=mcΔT,其中Q为热量,m为物料质量,c为物料比热容,ΔT为温度差。
燃料热量是指在回转窑系统中燃烧燃料产生的热量。
燃料热量计算需要考虑燃料的组成、燃烧产生的反应热和燃料的热值等因素。
常用的燃料有煤、天然气和重油等。
计算燃料热量时需要知道燃料的热值和燃烧效率,燃烧效率可以通过燃烧后排放物的含碳量和燃料的理论热值来计算。
烟气热量是指燃料燃烧后剩余的烟气中的热量。
烟气热量计算需要考虑燃料的完全燃烧和燃烧产生的烟气成分等因素。
烟气热量可以通过烟气的排放量、温度和烟气的比热容来计算,即Q=mcΔT。
在回转窑系统的热平衡计算中,还要考虑到热量的传递和损失。
热量的传递主要通过辐射、对流和传导等方式进行,但同时也会有一定的传热损失。
传热损失主要包括窑体表面的散热、未被物料吸收的辐射热量和烟气中的热量损失等。
为了准确计算回转窑系统的热平衡,需要获取系统各个部件的热参数和系统运行数据。
热参数可以通过实验和测试获得,如物料的比热容、燃料的热值和烟气的排放量等。
而系统运行数据则需要通过检测和监控来获取,如物料流量、燃料消耗量和烟气温度等。
在热平衡计算中,还需要考虑到系统的能量守恒原理。
即系统的输入热量等于输出热量,即Qin=Qout。
如果系统的输入热量大于输出热量,则系统处于热超负荷状态;如果系统的输入热量小于输出热量,则系统处于热负荷不足状态。
回转窑系统的热平衡计算是通过上述原理和方法进行的。
通过对系统的热量输入和输出进行计算和分析,可以评估系统的热平衡状态、检测问题和优化系统运行等。
同时,对于不同类型的回转窑系统,还可以通过比较和分析来确定最佳燃料和操作参数等。
天然气锅炉热平衡计算【原创实用版】目录1.天然气锅炉热平衡计算的背景和意义2.天然气锅炉的工作原理3.热平衡计算的基本原理和方法4.天然气锅炉热平衡计算的具体步骤5.天然气锅炉热平衡计算的应用实例6.天然气锅炉热平衡计算的发展趋势和展望正文天然气锅炉热平衡计算是研究天然气锅炉工作过程中热量平衡状态的一种科学方法。
天然气锅炉作为一种常见的热能转换设备,广泛应用于工业生产和居民生活中的供暖、热水供应等领域。
天然气锅炉的热平衡计算对于提高锅炉的热效率、降低能源消耗、减少环境污染具有重要意义。
天然气锅炉的工作原理是利用天然气作为燃料,通过燃烧产生高温烟气,将热量传递给锅炉中的水,使水升温变成蒸汽或热水。
在这个过程中,天然气锅炉需要维持一个良好的热平衡状态,以保证热量的充分吸收和有效利用。
热平衡计算的基本原理是能量守恒定律,即系统中的热量收入等于热量支出。
在天然气锅炉热平衡计算中,需要考虑以下几个方面的热量:燃料的热量、烟气的热量、水的热量、散热的热量等。
通过计算这些热量的平衡关系,可以得到天然气锅炉的热平衡状态。
天然气锅炉热平衡计算的具体步骤如下:1.确定计算模型:根据锅炉的具体结构和工作条件,选择合适的计算模型,如简化模型、半简化模型或详细模型等。
2.确定热平衡方程:根据能量守恒定律,列出系统中的热量平衡方程。
3.确定各部分的热负荷:通过测量或计算,确定燃料的热量、烟气的热量、水的热量、散热的热量等。
4.求解热平衡方程:通过数值计算方法,如迭代法、直接法等,求解热平衡方程,得到天然气锅炉的热平衡状态。
天然气锅炉热平衡计算的应用实例包括优化锅炉结构、提高热效率、降低能耗等方面。
通过热平衡计算,可以找出锅炉工作中存在的问题,为锅炉的改进提供理论依据。
随着科技的发展,天然气锅炉热平衡计算将更加精确和便捷。
未来的发展趋势包括:计算模型的完善、计算方法的优化、计算机技术的应用等。
炼钢过程物料平衡和热平衡计算炼钢过程是将生铁或者其他铁合金通过熔炼等一系列工艺操作得到所需成分和性能的钢的过程。
在炼钢过程中,物料平衡和热平衡计算是非常重要的。
物料平衡计算是炼钢过程中的一项重要工作,其目的是通过计算物料的进出量,确定每个工序中原料和产物的平衡情况,以便控制和优化炼钢过程。
炼钢过程中常用的物料平衡计算方法有材料平衡和元素平衡两种。
材料平衡计算主要是根据原料的进出量和成分,以及每个工序中材料的变化情况,来计算各种物料的平衡情况。
以炼钢高炉为例,其主要原料是铁矿石、焦炭和空气,通过冶金反应得到生铁和炉渣。
在材料平衡计算中,需要考虑到进料的质量和数量,以及冶金反应中矿石的还原程度、焦炭的燃烧程度等因素。
通过对每个工序中原料和产物的物料平衡计算,可以确定炉内各种物料的流动情况和变化规律,以便优化炼钢过程,提高钢的质量和产量。
元素平衡计算是针对炼钢过程中的元素进行的平衡计算。
炼钢过程中,除了铁、碳、硅、锰等主要元素外,还有许多杂质元素,如磷、硫、氧等。
元素平衡计算需要考虑每个工序中元素的进出量,以及元素在冶金反应中的分配情况。
通过元素平衡计算,可以确定炼钢过程中每个工序的杂质元素的分布情况,以便进行相应的处理和控制,保证钢的质量符合要求。
热平衡计算是炼钢过程中的另一个重要工作,其目的是通过计算炼钢过程中的热量进出量,了解各个工序的热平衡情况,以便合理利用热能,优化炼钢过程。
炼钢过程中产生的热量主要有焦炭燃烧产生的热量、冶金反应放热产生的热量、热风和燃料的预热热量等。
热平衡计算中需要考虑的因素有炉内热量的进出量、热量的耗散和损失等。
通过热平衡计算,可以确定每个工序中热量的平衡情况,以便根据热量的分布和变化,进行相应的热能利用优化。
在炼钢过程中进行物料平衡和热平衡计算,可以帮助把握炼钢过程中材料和热量的变化规律,从而更好地控制和优化整个过程。
这对于提高炼钢质量、降低成本具有重要意义。
同时,物料平衡和热平衡计算也为炼钢过程的模拟和仿真提供了基础数据,为炼钢工艺的改进和创新提供了理论依据。
回转窑系统热平衡计算1 热平衡计算基准、范围及原始数据1.1 热平衡计算基准物料基准:一般以1kg熟料为基准;温度基准:一般以0℃为基准;1.2 热平衡范围热平衡范围必须根据回转窑系统的设计或热工测定的目的、要求来确定。
在回转窑系统设计时,其平衡范围,可以回转窑、回转窑加窑尾预热分解系统、或再加冷却机和煤磨作平衡范围。
范围选得大,则进出口物料、气体温度较低,数据易测定或取得,但往往需要的数据较多,计算也烦琐。
因此一般选回转窑加窑尾预热分解系统作为平衡范围。
1.3 原始数据根据确定的计算基准和平衡范围,取得必要的原始数据,这是一项非常重要的工作。
计算结果是否符合实际情况,主要取决于所选用的数据是否合理。
对新设计窑或改造窑来说,主要是根据同类型窑的生产资料,结合工厂具体条件和我国实际情况、合理地确定各种参数;对于生产窑来说,主要通过热工测定取得实际生产中各种参数。
若以窑加窑尾预热系统为平衡范围,一般要取得如下原始数据:生料用量、化学组成、水分、入窑温度;燃料成分、工业分析和入窑温度;一、二次空气的比例和温度;空气过剩系数、漏风系数;废气温度;飞灰量、灰温度及烧失量;收尘器收尘效率;窑体散热损失;熟料形成热等等。
熟料形成热可根据熟料形成过程中的各项物理化学热效应求得,也可用经验公式计算或直接选定。
2 物料平衡与热量平衡计算方法与步骤说明于下:窑型:悬浮预热器窑基准:1kg熟料;0℃平衡范围:窑+预热器系统根据确定的平衡范围,绘制物料平衡图和热量平衡图,如图1和图2所示。
图1 物料平衡图图2 热量平衡图2.1 物料平衡计算 2.1.1 收入项目(1)燃料消耗量 m r (kg/kg 熟料)设计新窑或技术改造时,m r 是未知量,通过热平衡方程求得,已生产的窑,通过热工测定得到。
(2)入预热器物料量 ① 干生料理论消耗量sar r gsL 100100L aA m m --=式中,m gsL —干生料理论消耗量,kg/kg 熟料;A ar —燃料收到基灰分含量,%;a —燃料灰分掺入熟料中的量,%;L s —生料的烧失量,%。
化学能与热平衡的计算方法化学反应中的能量转化是研究化学反应热平衡的重要方面。
热平衡是指化学反应在一定条件下达到能量守恒的状态,即反应体系中的各反应物和产物的热力学能量之和保持不变。
为了计算化学能与热平衡,我们需要了解热力学基本概念,以及相关的计算方法。
热力学第一定律表明了能量守恒的原理,即能量可以转化形式但总量保持不变。
化学反应中,反应物和产物之间的能量转化可以通过计算焓变来描述。
焓变(ΔH)定义为反应物和产物之间的能量差,可以正负相反,取决于反应方向。
根据热力学第一定律,焓变等于反应物的热能减去产物的热能。
反应过程中,吸热反应(放热物质呈吸热反应)需要外界给予能量,其焓变为正值;放热反应(产物放热)则由反应系统向外界释放热量,其焓变为负值。
计算焓变的常用方法之一是利用反应的热容量(Cp)和温度变化(ΔT)。
热容量是物质在单位温度变化下吸收或放出的热量。
对于理想气体,其热容量与温度无关,可以用摩尔热容量(Cp,m)表示。
根据热力学方程,焓变可以表示为:ΔH = Cp,m × n × ΔT,其中n为反应物的摩尔数,ΔT为温度变化。
通过实验测定反应物和产物的热容量,并测定反应前后的温度变化,我们可以计算出焓变。
实验中,常用的例如流动式量热计和反应热计,可以得到较为准确的焓变值。
通过测定焓变的符号和数值,我们可以判断反应是吸热还是放热,并进一步分析反应的热平衡情况。
除了焓变,熵变(ΔS)也是计算热平衡的重要参数。
熵变是描述反应过程中体系无序度变化的物理量,与状态函数有关。
根据热力学第二定律,对于可逆反应,熵的增加(ΔS>0)使反应趋向于正向方向进行,而熵的减少(ΔS<0)使反应趋向于逆向方向进行。
通过比较反应物和产物的熵变,我们可以预测反应的方向性和可能性。
在热平衡计算中,根据吉布斯自由能(G)的变化可以进一步判断反应的方向性。
吉布斯自由能是一个能量函数,可以表示为G = H - TS,其中H为焓变,T为温度,S为熵变。