(完整word版)高中化学必修一知识网络结构图.doc
- 格式:doc
- 大小:1.00 MB
- 文档页数:8
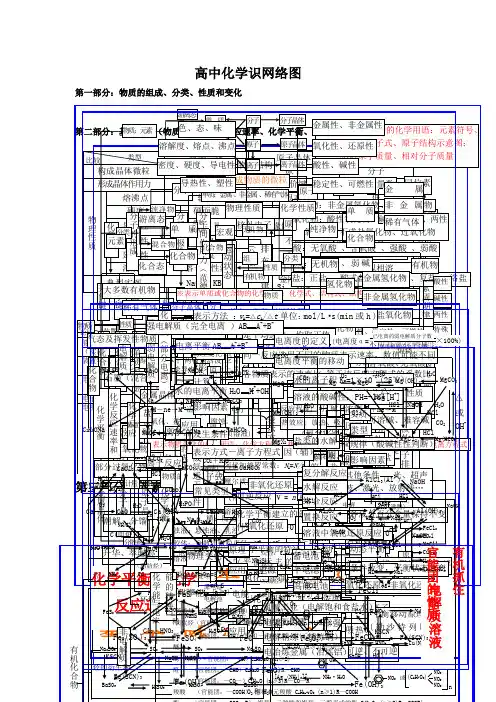
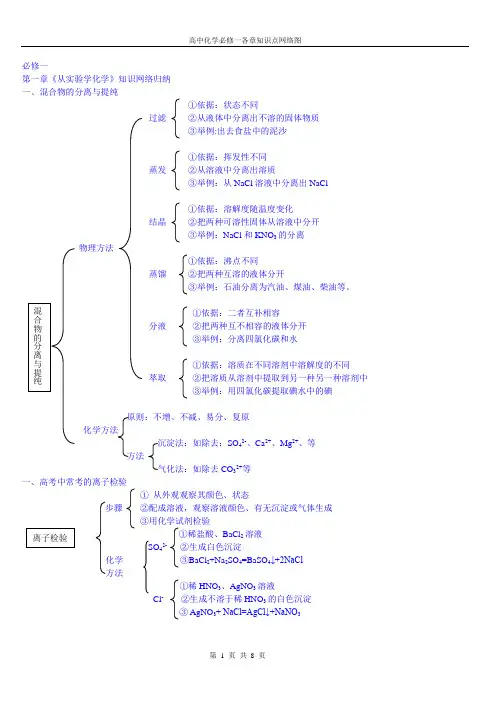
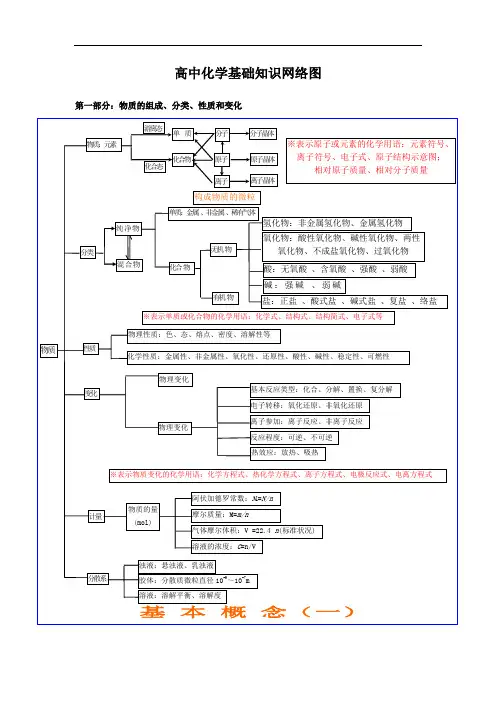
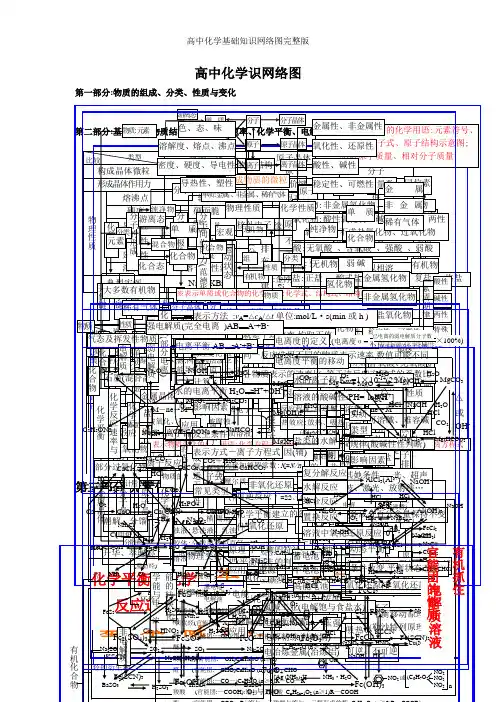

高中化学基础知识网络图第一部分:物质的组成、分类、性质和变化大纲要求(1)了解分子、原子、离子等概念的含义。
了解原子团的定义。
(2)理解物理变化与化学变化的区别与联系。
(3)理解混合物和纯净物、单质和化合物、金属和非金属的概念。
(4)理解酸、碱、盐、氧化物的概念及其相互联系。
第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)大纲要求物质结构和元素周期律(1)了解元素、核素和同位素的含义。
(2)了解原子构成。
了解原子序数、核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系。
(3)了解原子核外电子排布。
(4)掌握元素周期律的实质。
了解元素周期表(长式)的结构(周期、族)及其应用。
(5)以第3周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系。
(6)以IA和VIIA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
(7)了解金属、非金属在元素周期表中的位置及其性质递变的规律。
(8)了解化学键的定义。
了解离子键、共价键的形成。
化学反应与能量(1)了解氧化还原反应的本质是电子的转移。
了解常见的氧化还原反应。
掌握常见氧化还原反应的配平和相关计算。
(2)了解化学反应中能量转化的原因,能说出常见的能量转化形式。
(3)了解化学能与热能的相互转化。
了解吸热反应、放热反应、反应热等概念。
(4)了解热化学方程式的含义。
(5)了解能源是人类生存和社会发展的重要基础。
了解化学在解决能源危机中的重要作用。
(6)了解焓变与反应热的含义。
了解△H=H(反应产物)—H(反应物)表达式的含义。
(7)理解盖斯定律,并能运用盖斯定律进行有关反应焓变的简单计算。
(8)了解原电池和电解池的工作原理,能写出电极反应和电池反应方程式。
了解常见化学电源的种类及其工作原理。
(9)理解金属发生电化学腐蚀的原因,金属腐蚀的危害,防止金属腐蚀的措施。
化学反应速率和化学平衡(1)了解化学反应速率的概念、反应速率的定量表示方法。

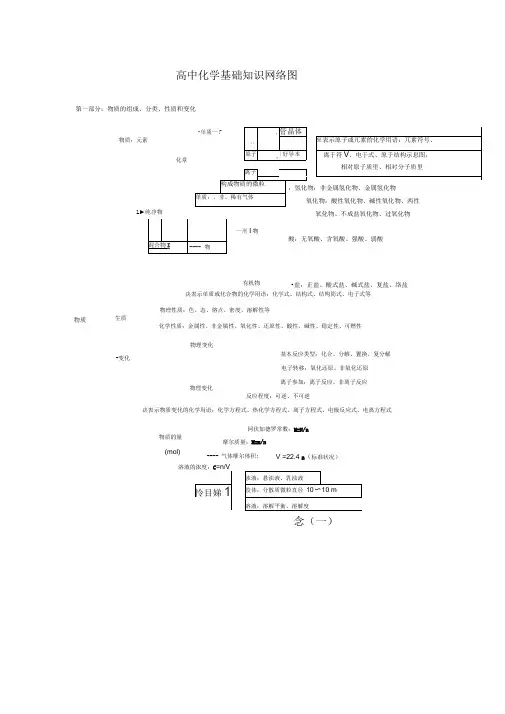
高中化学基础知识网络图第一部分:物质的组成、分类、性质和变化氧化物、不成盐氧化物、过氧化物酸:无氧酸、含氧酸、强酸、弱酸决表示单质或化合物的化学用语:化学式、结构式、结构简式、电子式等物理性质:色、态、熔点、密度、溶解性等反应程度:可逆、不可逆决表示物质变化的化学用语:化学方程式、热化学方程式、离子方程式、电极反应式、电离方程式阿伏加德罗常数:M=N/n念(一)物质:元素化章L ►纯净物|—刑I 物有机物•盐:正盐、酸式盐、碱式盐、复盐、络盐物质 生质化学性质:金属性、非金属性、氧化性、还原性、酸性、碱性、稳定性、可燃性物理变化-变化基本反应类型:化合、分解、置换、复分解 电子转移:氧化还原、非氧化还原物理变化离子参加:离子反应、非离子反应物质的量摩尔质量:M=m/n (mol)---- 气体摩尔体积:V =22.4 n (标准状况)色、态、味溶解度、熔点、沸点 密度、硬度、导电性导热性、塑性「单质兀素游离态宏观化合态原子晶体物质变化分类石墨(混合晶体)金属晶体微观大多数盐离子晶体pl 纯净物-无机物碱性氧化物*6分过氧化新潮解、分储升华、萃取溶解、盐析裂化、裂解念(二)第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)金属 稀有气体-氢化物--氧化物一不成盐氧化物含氧酸、无氧酸 强酸、弱酸,可溶碱、难容碱 正盐 酸式盐 碱式盐 复盐;络盐物质结构荷电 一实质.Si排布规律、分层1能 量最低原理层最多容纳29个次外层不超过18个最外层不超过8个一运动状态——特殊性•,电子云分子间作用力{范德华力•分子的极性L分子的形成属键一L葛子健 化学键I n ———共价键核外电子排布周期性元素性质的周期性元素周期律编制一 元素周期表表的结构示方法,影响物理性质2812---8188213Bn ABw WA BI m••族族族族 、王副o族 56 7 一一 一一 一L化学反应速率和化学平衡表示方法 :V A = △ C A /△ t 单位:mol/L - s(min 或 h是平均速率,均取正值同一反应选用不同的物质表示速率,数值可能不同 各物质表示的速率比等于该反应方程式的系数比化学平衡件学平衡、化学 反应速率反应物的结构、性质 浓度温度]催化剂 ___________________ 其他条件—光、超声 波、激光、放射线…影响化学平衡因素压强 温度平衡移动原理强电解质(完全电离)AB -^A '+B化合物电解质弱电解质装:能的转换:化学能与电化学能非电解质电冶炼金属(冶炼铝)电解质溶液第三部分:元素化合物转化关系H2O H2OMg(OH) ------ MgCO3NaOH /H2O/HCI/ CO:/ HCl .. /OHCaCl2 ・JHClCl2 为/ HCl Na2CO3HClCl* CaCO3飞CO2+ H2OAlCl 3(AI 3+)[、NaOHHClHCW " Ji/电解1Al 2O3.、O2NaOHCl HCl *Fl H2°(沸腾).»OH)3NaOH 或H C z^C02ZT S^u NaOHNaAl O 2NaOHKSCNFe(ScN)3FeSNa2SH2SO4FeONaOH H2SO4Fe3O4Fe(OH) 2O2 和H2O・ FeCl2Cl FeKSCNFeCl3 :Fe(SCN)3NaOH HCl♦ Fe(OH)3SCU2S 一HNO3 或H2SO4(浓NH3H2O 2+• Cu(OH) 2 ■ [Cu(NH 3)4]CuS ♦Na2S Cu2+(NO3、S°42)金属部分:按照单质-氧化物一氢氧化物一►盐为线索进行搜罗寻找关系非金属:按照化合价寻找各类物质,主要有氢化物、单质、氧化物、含氧酸、及其盐第四部分:有机化学—醇 (官能团:一OH ):饱和一元醇C n H 2n+1OH (n 法1)R — OH 酬 C n H 2n+2O (n A2)R O R _____ 酚(苯酚)(官能团:OH ) C n H 2n-6。

高中化学知识结构网络图化学基本概念和基本理论元素与化合物有机化学基础化学计算化学实验化学工业知识化学基本概念和基本理论物质的分类组成原子的粒子间的关系核电荷数( Z) =核内质子数 =核外电子数质量数( A) =质子数( Z)+中子数( N)元素周期律与周期表化学键与分子结构晶体类型与性质晶体类型离子晶体分子晶体原子晶体金属晶体性质比较组成粒子阴、阳离子分子原子金属阳离子和自由电子结构粒子间作用离子键范德华力共价键金属键熔沸点较高低很高有高有低硬度硬而脆小大有大有小、有延展性易溶于极性溶剂,极性分子不溶于任何溶难溶(钠等溶解性难溶于非极性溶易溶于极性溶剂与水反应)物理剂剂性质晶体不导电,溶晶体不导电;于水后能电离能溶于水的其水不良(半导体良导体(导导电性的,其水溶液可溶液导电;熔化导Si)电传热)导电;熔化不导电电NaCl 、NaOH 干冰、白磷金刚石、 SiO2 Na 、 Mg 、典型实例AlNa2O、 CaCO3 冰、硫磺晶体硅、 SiCFe、Cu 、Zn 化学反应类型离子反应氧化还原反应的有关概念的相互关系化学反应中的能量变化化学平衡弱电解质的电离平衡溶液的酸碱性盐类的水解酸碱中和滴定电化学返回页顶元素与化合物钠及其化合物碱金属氯及其化合物卤素氧族元素硫的重要化合物碳及其化合物硅及其化合物材料氮族元素氮和磷氨硝酸镁和铝铁及其化合物铜及其化合物返回页顶有机化学基础烃不饱和链烃芳香烃分通式类结构特点化学性质物理性质同分异构①与卤素取代反应烷C n H 2n+2 烃(n≥ 1)烯C n H2n 烃(n≥ 2)炔C n H 2n-2 烃(n≥ 2)苯及其C n H 2n-6 同(n≥ 6) 系物①C-C 单键②链烃①含一个 C C键②链烃①含一个 C C键②链烃①含一个苯环②侧链为烷烃基(光照 )②燃烧③裂化反应①与卤素、 H :、 H2O等发生加成反应②加聚反应③氧化反应:燃烧,被 KMnO 4酸性溶液氧化①加成反应②氧化反应:燃烧,被 KMnO4 酸性溶液氧化①取代反应:卤代、硝化、磺化②加成反应③氧化反应:燃烧,苯的同系物能被KMnO 4酸性溶液氧化一般随分子碳链异构中碳原子数的增多,沸点升高,液态时密度增大。
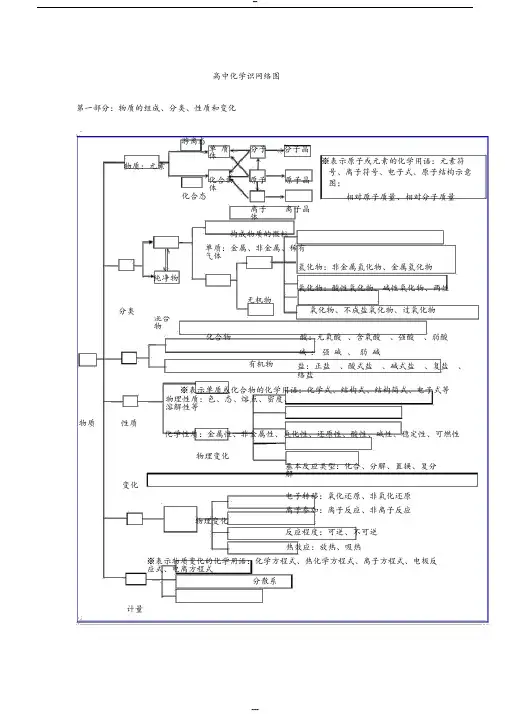
高中化学识网络图第一部分:物质的组成、分类、性质和变化游离态单质分子分子晶体物质:元素化合物原子原子晶体化合态离子离子晶体构成物质的微粒单质:金属、非金属、稀有气体※表示原子或元素的化学用语:元素符号、离子符号、电子式、原子结构示意图;相对原子质量、相对分子质量纯净物氢化物:非金属氢化物、金属氢化物氧化物:酸性氧化物、碱性氧化物、两性分类无机物氧化物、不成盐氧化物、过氧化物混合物化合物酸:无氧酸、含氧酸、强酸、弱酸碱:强碱、弱碱有机物盐:正盐、酸式盐、碱式盐、复盐、络盐※表示单质或化合物的化学用语:化学式、结构式、结构简式、电子式等物理性质:色、态、熔点、密度、溶解性等物质性质化学性质:金属性、非金属性、氧化性、还原性、酸性、碱性、稳定性、可燃性物理变化变化基本反应类型:化合、分解、置换、复分解电子转移:氧化还原、非氧化还原离子参加:离子反应、非离子反应物理变化反应程度:可逆、不可逆热效应:放热、吸热※表示物质变化的化学用语:化学方程式、热化学方程式、离子方程式、电极反应式、电离方程式计量分散系阿伏加德罗常数:NA=N/n 物质的量摩尔质量:M=m/n(mol) 气体摩尔体积:V =22.4 n ( 标准状况 ) 溶液的浓度: C=n/V浊液:悬浊液、乳浊液-9-7胶体:分散质微粒直径10 ~10 m 基本概念(一)色、态、味溶解度、熔点、沸点密度、硬度、导电性导热性、塑性物理性质游离态单质宏观元素化合物组金属性、非金属性氧化性、还原性酸性、碱性稳定性、可燃性金属化学性质单质非金属纯净物稀有气体化合物分类化合态大多数有机物稀有气体分子晶体分子酸气态及挥发性物质原子晶体原石墨(混合晶体)子金属晶体大多数盐离强碱离子晶体子碱性氧化物部分过氧化物微观性质无机物有机物金属氢化物酸性氢化物物质非金属氢化物碱性成盐氧化物两性氧化物特殊变化不成盐氧化物含氧酸、无氧酸酸强酸、弱酸强碱、弱碱碱可溶碱、难容碱正盐酸式盐盐碱式盐复盐;络盐潮解、分馏混合物有机、无机升华、萃取物理变化化学变化化合、分解、置换、复分解风化、干馏氧化还原;非氧化还原溶解、盐析裂化、裂解分子、离子基本概念(二)吸热、放热可逆、不可逆第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)物质结构分子原子分分分核外电子原子核化子子子学的的间(键形极作运排成性用分动力层布状()规范态律共离金德价子属极非华键键键力特性极最次各能)殊分性外外层量性子分共离金层层最最子不不多低价子属超超容原化化单电过过纳理合合质子影818 2n物物及云响个2 合个个金物理性质中子质子质量数同位素核电荷数元素性质规律原子序数变化元素周期律表现形式元素周实期质律表元元元核晶示方素编素归素外体决制类结构简图法周周纳性定电型表期期质子表律 的 排的 电子式结周布 构 期 周金 分 原 离 性 期性 属 子 子 子晶晶晶晶横:周期 元素种类体 体 体 体 起止序号n=1 21~ 2n=2 8短周期3~10元素性质 n=3 8 11~18周 原 n=4 18 19~36 期 子表 n=5 18 长周期37~54 结位 构 n=6 32 55~86 置n=721 不完全周期 87~111纵:族 主族:ⅠA ~Ⅶ A副族 :ⅢB ~Ⅶ B 、Ⅰ B Ⅱ B Ⅷ族0 族比较类型构成晶体微粒形成晶体作用力熔沸点硬度物理导电性性传热性质延展性溶解性典型实例离子晶体原子晶体分子晶体阴、阳离子原子分子离子键共价键范德华力较高很高低硬而脆大小熔融 .导电绝缘体 (半导体 ) 不良不良水溶液不良不良不良不良不良不良易溶于极性溶剂不溶于任何溶剂相似相溶NaCl , KBr单质:金刚石、 SiC、单质:H2、O2Si、 SiO2 化合物:冰、干冰化化学化学反学应反平速应衡化表示方法学反应速特点率计算影响因素应用:vA =△cA /△t 单位: mol/L ·s(min 或 h )是平均速率,均取正值同一反应选用不同的物质表示速率,数值可能不同各物质表示的速率比等于该反应方程式的系数比内因 (主 ) 反应物的结构、性质浓度压强率和的合选成择氨适于化条学件平衡外因(辅)可逆反应化学平衡建立的条件: v 正=v逆≠ 0化学平衡的特征(平衡标志的判断)温度催化剂其他条件光、超声波、激光、放射线⋯定各成分百分含量保持不变等v 正 =v 逆≠ 0动动态平衡变条件改变,平衡状态改变化学平衡、化学反应速率浓度平衡移动原理影响化学平衡因素压强(勒沙特列原理)温度强电解质(完全电离 ) AB A -+B -已电离的弱电解质分子数(电电离平衡 AB - +B- 电离度的定义 (电离度 α= 弱电解质的分子总数×100%)弱 部 A 解 电 分 电离度平衡的移动质解 电化质 离 -14合水的离子积 ℃ ))K W =1×10 (25物 水的电离平衡 H 2O + +OH - +H 溶液的酸碱性: PH=-log[H]实质装置发生条件表示方式-离子方程式离子反应非氧化还原 常见类型氧化还原类型盐类的水解规律(酸碱性性判断) 影响因素复分解反应水解反应络合反应置换反应溶液中氧化还原反应原理 蓄电池 化 能 应用 电源 干电池 高能电池 学 的原电池能 转 化学能电解池 电能与换 原理 氯碱工业(电解饱和食盐水)电:电镀应用非电解精练(精练铜) 电解 电冶炼金属(冶炼铝)质电 解 质 溶 液比较 装置能量转换 (实质) 装置特点电极名称电子流向电极反应--原电池 电解池化学能→电能 电能→化学能(两极分别发生氧化还原反应产生电流) (在电流作用下两极分别发生氧化还原反应)外电路无电源;两极为活泼性不同外电路必须有直流电源;两极材料均(或其中之一为能导电的非金属)的金属 能导电即可负极(-)——较活泼 阴极——连接电源负极正极(+)较不活泼 阳极——连接电源正极 e e e负极(-)→正极(+) 电源负极→阴极 电源正极→阳极氧化 n + + 还原 n + 还原活泼金属失去电子 + ne →M负极: M -ne → M 阴极: 2H +2e →H 2 ↑或 M被氧化、被溶解、被腐蚀。
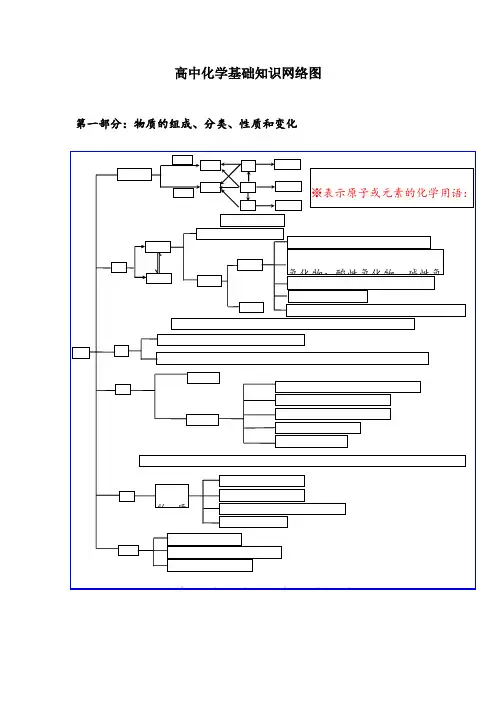
高中化学识网络图
第一部分:物质的组成、分类、性质和变化
第二部分:基本理论(物质结构、化学反应速率、化学平衡、电
解质溶液)
率和化学平
第三部分:元素化合物转化关系
第四部分:有机化学
有机抓住
官能团的性质
烃
烃的衍生物
糖
蛋白质:多肽、氨基酸(官能团:—2和—)
高分子化合物
链烃
(脂肪烃)
环烃
饱和链烃 烷烃:22(n ≥1)R —3 不饱和链烃 烯烃:2n (n ≥2) R —2
二烯烃:22(n ≥4)R ——2 炔烃:22(n ≥2) R —C ≡
环烷烃2n (n ≥3)
芳香烃(苯和苯的同系物)26(n ≥6)
天然高分子:橡胶(聚异戊二烯)、多糖、蛋白质
R
卤代烃(官能团:—X ):饱和一卤代烃21X(n ≥1)R —X 醇 (官能团:—):饱和一元醇21(n ≥1)R —
醚 22O (n ≥2)R —O —R 酚(苯酚)(官能团:—)26O (n ≥2)
羧酸 (官能团:—):饱和一元羧酸 21O 2 (n ≥1)R —
醛 (官能团:—)2 (n ≥1)R — 酮 (官能团:——)2 (n ≥3)R ——R ’
酯 (官能团:——R ):饱和一元羧酸和饱和一元醇形成的酯 22 (n ≥2)R —’ 硝基化合物(官能团—2)R —2 胺(官能团—2)R —2
单糖:葡萄糖、果糖C 6H 12O 6(互为同分异构)
二糖:蔗糖、麦芽糖C 12H 22O 11(互为同分异构) 多糖:淀粉、纤维素(C 6H 12O 6)n (n 值不同)
合成高分子
合成塑料
合成橡胶 合成纤维
有机化合物。
高中化学基础知识网络图第一部分:物质的组成、分类、性质和变化第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)第三部分:元素化合物转化关系第四部分:有机化学有机抓住官能团的性质烃 烃的衍生物糖 蛋白质:多肽、氨基酸(官能团:—NH 2和—COOH ) 高分子化合物链烃(脂肪烃) 环烃 饱和链烃烷烃:C n H 2n+2(n ≥1)R —CH 3 不饱和链烃 烯烃:C n H 2n (n ≥2) R —CH=CH 2二烯烃:C n H 2n-2(n ≥4)R —CH=CH —CH=CH 2 炔烃:C n H 2n-2(n ≥2) R —C ≡CH环烷烃C n H 2n (n ≥3)芳香烃(苯和苯的同系物)C n H 2n-6(n ≥6)天然高分子:橡胶(聚异戊二烯)、多糖、蛋白质R卤代烃(官能团:—X ):饱和一卤代烃C n H 2n+1X(n ≥1)R —X 醇 (官能团:—OH ):饱和一元醇C n H 2n+1OH(n ≥1)R —OH 醚 C n H 2n+2O (n ≥2)R —O —R 酚(苯酚)(官能团:—OH )C n H 2n-6O (n ≥2) OH羧酸 (官能团:—COOH ):饱和一元羧酸 C n H 2n+1O 2 (n ≥1)R —COOH醛 (官能团:—CHO )C n H 2n O (n ≥1)R —CHO 酮 (官能团:—CO —)C n H 2n O (n ≥3)R —CO —R ’酯 (官能团:—COO —R ):饱和一元羧酸和饱和一元醇形成的酯 C n H2n O 2(n ≥2)R —COOR ’硝基化合物(官能团—NO 2)R —NO 2胺(官能团—NH 2)R —NH 2单糖:葡萄糖、果糖C 6H 12O 6(互为同分异构)二糖:蔗糖、麦芽糖C 12H 22O 11(互为同分异构) 多糖:淀粉、纤维素(C 6H 12O 6)n(n 值不同)合成高分子合成塑料 合成橡胶 合成纤维有机化合物。
高中化学基础知识网络图第一部分:物质的组成、分类、性质和变化第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)第三部分:元素化合物转化关系有机抓住官能团的性质烃烃的衍生物糖蛋白质:多肽、氨基酸(官能团:—NH 2和—COOH )高分子化合物链烃(脂肪烃)环烃饱和链烃 烷烃:C n H 2n+2(n ≥1)R —CH 3 不饱和链烃 烯烃:C n H 2n (n ≥2) R —CH=CH 2二烯烃:C n H 2n-2(n ≥4)R —CH=CH —CH=CH 2 炔烃:C n H 2n-2(n ≥2) R —C ≡CH环烷烃C n H 2n (n ≥3)芳香烃(苯和苯的同系物)C n H 2n-6(n ≥6)天然高分子:橡胶(聚异戊二烯)、多糖、蛋白质R卤代烃(官能团:—X ):饱和一卤代烃C n H 2n+1X(n ≥1)R —X 醇 (官能团:—OH ):饱和一元醇C n H 2n+1OH(n ≥1)R —OH醚 C n H 2n+2O (n ≥2)R —O —R 酚(苯酚)(官能团:—OH )C n H 2n-6O (n ≥2)OH羧酸 (官能团:—COOH ):饱和一元羧酸 C n H 2n+1O 2 (n ≥1)R —COOH醛 (官能团:—CHO )C n H 2n O (n ≥1)R —CHO 酮 (官能团:—CO —)C n H 2n O (n ≥3)R —CO —R ’酯 (官能团:—COO —R ):饱和一元羧酸和饱和一元醇形成的酯 C n H 2n O 2 (n ≥2)R —COOR ’ 硝基化合物(官能团—NO 2)R —NO 2 胺(官能团—NH 2)R —NH 2单糖:葡萄糖、果糖C 6H 12O 6(互为同分异构)二糖:蔗糖、麦芽糖C 12H 22O 11(互为同分异构) 多糖:淀粉、纤维素(C 6H 12O 6)n (n 值不同)合成高分子合成塑料 合成橡胶 合成纤维有机化合物。
高中化学基础知识网络图第一部分:物质的组成、分类、性质和变化游离态分子分子晶体单质物质:元素化合物原子原子晶体化合态离子离子晶体构成物质的微粒单质:金属、非金属、稀有气体※表示原子或元素的化学用语:元素符号、离子符号、电子式、原子结构示意图;相对原子质量、相对分子质量纯净物氢化物:非金属氢化物、金属氢化物氧化物:酸性氧化物、碱性氧化物、两性分类无机物氧化物、不成盐氧化物、过氧化物混合物化合物酸:无氧酸、含氧酸、强酸、弱酸碱:强碱、弱碱有机物盐:正盐、酸式盐、碱式盐、复盐、络盐※表示单质或化合物的化学用语:化学式、结构式、结构简式、电子式等物理性质:色、态、熔点、密度、溶解性等物质性质化学性质:金属性、非金属性、氧化性、还原性、酸性、碱性、稳定性、可燃性物理变化变化基本反应类型:化合、分解、置换、复分解电子转移:氧化还原、非氧化还原离子参加:离子反应、非离子反应物理变化反应程度:可逆、不可逆热效应:放热、吸热※表示物质变化的化学用语:化学方程式、热化学方程式、离子方程式、电极反应式、电离方程式计量分散系阿伏加德罗常数:N A=N/n物质的量摩尔质量: M=m/n(mol)气体摩尔体积:V =22.4 n ( 标准状况 )溶液的浓度: C=n/V浊液:悬浊液、乳浊液-9-7胶体:分散质微粒直径10 ~10 m基本概念(一)色、态、味溶解度、熔点、沸点密度、硬度、导电性导热性、塑性游离态物理性质单质宏观元素金属性、非金属性氧化性、还原性酸性、碱性稳定性、可燃性金属化学性质单质非金属纯净物稀有气体化合物化合态化合物组大多数有机物稀有气体分子晶体分酸子气态及挥发性物质原子晶体原石墨(混合晶体)子微观金属晶体大多数盐强碱离子晶体离碱性氧化物子部分过氧化物性质分类无机物物质氢化物氧化物变化酸碱盐有机物金属氢化物酸性非金属氢化物碱性成盐氧化物两性特殊不成盐氧化物含氧酸、无氧酸强酸、弱酸强碱、弱碱可溶碱、难容碱正盐酸式盐碱式盐复盐;络盐潮解、分馏混合物升华、萃取有机、无机物理变化化学变化化合、分解、置换、复分解风化、干馏氧化还原;非氧化还原溶解、盐析裂化、裂解分子、离子基本概念(二)吸热、放热可逆、不可逆第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)物质结构分子化分分分子子子学的的间运键形极作成性用动力状共离金(态范价子属极非德特键键键性极华殊分性共离金力性子分)价子属子电化化单影子合合质物物及响云合物金理性晶质体结构简图类型电子式金分原离属子子子晶晶晶晶横:周期体体体体原子核外电子原子核(分排层布)规律最次各能外外层量层层最最不不多低超超容原过过纳理8 18 2n个个 2个表示方法表的结构元素种类起止序号中子质量数同位素核电荷数元素质子性规质原子序数变律化元素周期律表现形式元素实周质期律元编元元核素素归素决外周制周纳性定电期期质子表律的排周布期周性期性n=1 n=2 n=3 n=4 n=5 n=6 n=7 纵:族2短周期1~ 28 3~10周元素性质8 11~ 18 原18长周期19~36 期子18 37~54 表结位32 55~86 构置21 不完全周期87~111主族:ⅠA ~Ⅶ A副族:ⅢB ~Ⅶ B 、Ⅰ B Ⅱ BⅧ族0族比较类型离子晶体原子晶体分子晶体构成晶体微粒阴、阳离子原子分子形成晶体作用力离子键共价键范德华力熔沸点较高很高低硬度硬而脆大小物导电性不良熔融.导电绝缘体 ( 半导体 ) 不良理水溶液性传热性不良不良不良质延展性不良不良不良溶解性易溶于极性溶剂不溶于任何溶剂相似相溶典型实例NaCl ,KBr 单质:金刚石、 SiC 、单质:H2、O2 Si 、SiO2 化合物:冰、干冰化表示方法学反特点速率算:v A =△c A /△t 位: mol/L ·s(min 或 h )是平均速率,均取正同一反用不同的物表示速率,数可能不同各物表示的速率比等于反方程式的系数比化和化学化反学学反平衡速率影响因素用条合件成的氨化适于学平衡内因 (主 )外因()可逆反化学平衡建立的条件: v 正=v 逆≠ 0化学平衡的特征(平衡志的判断)反物的构、性度温度催化其他条件光、超声波、激光、放射⋯定各成分百分含量保持不等v 正 =v 逆≠ 0平衡条件改,平衡状改化学平衡、化学反应速率度影响化学平衡因素平衡移原理(勒沙特列原理 )温度强电解质(完全电离 ) AB A -+B -已电离的弱电解质分子数(电离度的定义 (电离度α = ×100%)电离平衡 AB A -+B - 弱电解质的分子总数电 弱 部解 电 分电离度平衡的移动化 质解 电质 离水的离子积 K W =1× 10-14(25℃ )合物) 水的电离平衡 H 2OH ++OH-溶液的酸碱性: PH=-log[H + ]实质装置发生条件表示方式-离子方程式离子反应非氧化还原常见类型氧化还原类型盐类的水解规律(酸碱性性判断)影响因素复分解反应水解反应络合反应置换反应溶液中氧化还原反应原理蓄电池化 能应用电源干电池高能电池学 的 原电池能 转化学能电解池电能与 换原理氯碱工业(电解饱和食盐水)电 :电镀应用非电解精练(精练铜)电解 电冶炼金属(冶炼铝)质电解 质 溶 液比较装置能量转换 (实质) 装置特点电极名称电子流向电极反应原电池 电解池化学能→电能电能→化学能(两极分别发生氧化还原反应产生电流) (在电流作用下两极分别发生氧化还原反应)外电路无电源;两极为活泼性不同 外电路必须有直流电源;两极材料均(或其中之一为能导电的非金属)的金属 能导电即可负极(-)——较活泼 阴极——连接电源负极正极(+)较不活泼 阳极——连接电源正极e ee负极(-)→正极(+)电源负极→阴极电源正极→阳极氧化n+活泼金属失去电子+还原n+还原负极: M -ne → M 阴极: 2H +2e →H 2 ↑或 M + ne → M被氧化、被溶解、被腐蚀。
惰性电极(石墨或铂)氧化R n--ne → R还原(例 2Cl - —2e Cl2↑)正极: 2H ++2e →H 2 ↑ ( 酸性电解质溶液 )或 M n+还原-H 2 O +O 2↑ + ne →M (不活泼金属的盐溶液)或 4OH — 4e-金属电极做阳极,电极本身被氧化H 2 O + O 2+ 4e → 4OH (中性、弱酸性条件下的吸氧腐蚀 )氧化n+M - ne →M第三部分:元素化合物转化关系Mg 3N 2 N 2煅烧Na 2SNa 2ONaOHNaClCO 2O 2 H 2O H 2OMgOMgMgO△ Mg(OH) 2MgCO 3NaNa 2O 2Na 2CO 3H 2OHClNaOH H 2O △Cl 2HCl 或Mg(OH) 2HCl C 2H 5ONaNaClCH 3 COONaNaHCO 3HClCO 2 OH -X 2电解MgX 2MgCl 2 Mg(HCO 3)2CaCl 2 Na 2CO 3CO 2+ H 2OHCl CaCO 3△ CaHCO 3AlCl 3(Al 3+)HClNaOHHCl HClCO 2Cl 2 或HClHClHClO 2 H 3PO 4 HCl2电解Al H 2O(沸腾 )NaOHCaHPO 4Al 2O 3Ca CaO H OCa(OH) 2O 2Al(OH) 3CO 2NaOH 或 HClC(电炉 )H 2 ONaOHCO 2 NaOHH 2ONaAl O 2CaC 2Ca(ClO) 2Na 2SHClFeSSFeHCl FeCl 2H 2SO 4COO 2Cl 2 FeCO浓 2H 2 SO 4O 2稀 Na S等Cl 2 、HNO 3H 2SO 4O 2HClKSCN2FeCl3Fe(SCN)3FeOFe OKSCNNaOH H 2 SO 4Fe ONaOHHCl4Fe(SCN)33Fe(OH) 2Fe(OH) 3O 2 和 H 2OCu O2SO 2NH 3H 2O[Cu(NH 3 4 2+Cu 2SCuCO 、Al 、H 2CuOCu(OH) 2) ]HNO3 或 H 2SO 4(浓)H +△H +NaOHCuS Na 2SCu 2+(NO 3 -、 SO42-)金属部分:按照单质 氧化物 氢氧化物 盐为线索进行搜罗寻找关系AgBrH2SO4KClO 3 HgO CH3ClZnHBr NaBrCH4 Na2O2 ClNH 4Cl KMnO 4FeCl2FeCl3 Br2 2CuCl2 CO l CH3CH 2OH H2 H2O O2 CH3COOH PCl3、 PCl5 Cl2 HCl NaCllNaClO I2CuCl2H2O2 HClOCa(ClO)2HI NaI CH 2=CHClNH 3 Cu Ca(OH) 2 Fe3O4 SO2 CO2+H2 OCH 2ClCH 2ClAgIFeSPbSFeS2 S H2S Na2S Mg 3N2 N2 NO NO2 N2 O4CuSNa2 SO3BaSO3PCl 3P PCl 5Na3PO4CaHPO4NH 4Cl NH 3NaNO 3HNO 3Cu(NO3 )2 SO2SO3Na2SO4NO23 2]+NH3·H 2 6 7 2[Ag (NH ) O NO2或(C H O ) NO2 H2SO3 H2SO4 BaSO4 NO2 nP2O5HPO 3CaSiO3 SiH 4 SiF4 CO H2CO3 Ca(HCO3 ) 2Ca3(PO4 )2H3PO4H2SiO 3SiO 2Si C CO2CaCO3Ca (H 2PO4)2H4SiO 4Na 2SiO3SiCl 4CaC2Ca(OH) 2CaO非金属:按照化合价寻找各类物质,主要有氢化物、单质、氧化物、含氧酸、及其盐第四部分:有机化学烃有机化烃的衍生物合物糖链烃饱和链烃烷烃: C n H2n+2 (n≥1)R—CH 3官有(脂肪烃)烯烃: C n H2n (n≥2) R—CH=CH 2能机不饱和链烃二烯烃: C n H2n-2(n ≥4)R—CH=CH — CH=CH2团抓环烷烃 C n H2n (n≥ 3)炔烃: C n H2n-2 (n≥2) R— C≡CH的住环烃性芳香烃(苯和苯的同系物) C n H 2n-6(n≥ 6) R 质卤代烃(官能团:— X):饱和一卤代烃 C n H2n+1 X(n ≥1)R—X醇(官能团:— OH):饱和一元醇 C n H2n+1OH(n ≥1)R —OH醚C n H2n+2O (n ≥2)R —O—R酚(苯酚)(官能团:— OH)C H O (n ≥2)OHn 2n-6醛(官能团:— CHO)C n H2n O (n≥1)R —CHO酮(官能团:— CO—) C n H2n O (n≥3)R— CO—R’羧酸(官能团:— COOH):饱和一元羧酸C n H2n+1O2 (n≥1)R— COOH酯(官能团:— COO—R):饱和一元羧酸和饱和一元醇形成的酯C n H2n O2 (n≥2)R—COOR’硝基化合物(官能团—NO2)R—NO 2胺(官能团— NH 2)R—NH 2单糖:葡萄糖、果糖C6 H12 O6(互为同分异构 )二糖:蔗糖、麦芽糖C12 H22O11(互为同分异构 )多糖:淀粉、纤维素(C6 H12 O6)n (n 值不同 )蛋白质:多肽、氨基酸(官能团:—NH 2和— COOH )天然高分子:橡胶(聚异戊二烯)、多糖、蛋白质高分子化合物合成塑料合成高分子合成橡胶合成纤维。