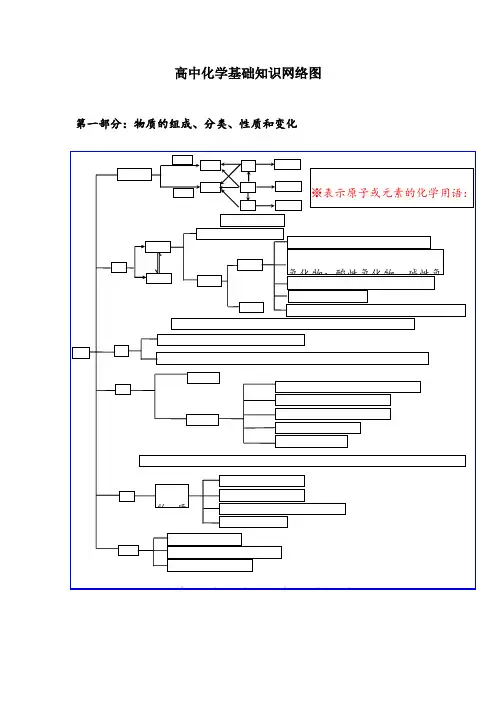
高中化学必修一各章知识点网络图
- 格式:doc
- 大小:161.59 KB
- 文档页数:8
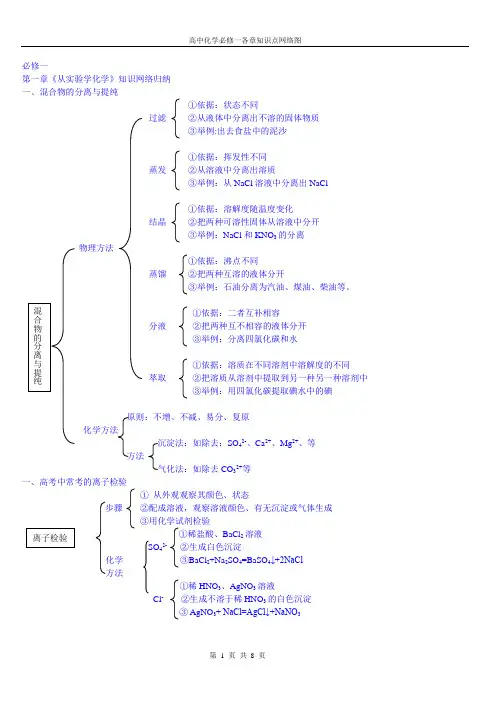

高一化学必修一知识导图导图是一种非常有效的学习工具,可以帮助我们整理和梳理知识,使之更加系统和清晰。
在高一的化学学习中,必修一是基础知识的起点,掌握好这些基础知识对于后续的学习非常重要。
下面是关于高一化学必修一知识的导图,帮助我们更好地理解和记忆这些知识点。
一、物质的组成与性质A. 物质的分类1. 纯净物和混合物的区别2. 纯净物的分类及特点3. 混合物的分类及特点B. 物质的性质1. 物理性质a. 颜色、密度、硬度等b. 熔点、沸点、溶解度等2. 化学性质a. 冷热现象、燃烧现象等b. 酸碱性、氧化性等C. 物质的变化1. 物理变化a. 相变b. 溶解2. 化学变化a. 燃烧b. 酸碱反应二、原子和原子结构A. 原子的概念1. 原子的基本概念2. 元素的概念B. 原子质量与相对原子质量1. 原子质量的定义和计算方法2. 相对原子质量的定义和计算方法C. 原子结构1. 原子核2. 原子的电子层次模型3. 原子序数和核电荷数的联系4. 同位素的概念和应用三、元素周期表与元素A. 元素周期表的发展与分类1. 门捷列夫周期表的特点2. 长表与短表的区别3. 元素周期表的分类B. 元素周期表的组成与规律1. 元素周期表的构造2. 周期表中的主族元素和过渡元素3. 电子结构与元素周期性的关系C. 元素的命名与符号1. 元素命名规则2. 元素符号的含义和规则3. 周期表中元素符号的学习方法四、化学键A. 化学键的概念1. 化学键的基本概念2. 化学键的作用和分类B. 阴离子与阳离子的化学键1. 阴离子的形成和性质2. 阳离子的形成和性质3. 金属与非金属离子的相互作用C. 共价键的形成和特点1. 共价键的形成和特征2. 原子间相互作用和共享电子3. 共价键的类型和特征D. 价键理论和分子结构1. 价键理论的概念和发展2. VB理论和MO理论的比较3. 分子结构的认识和描述方法五、化学方程式与化学计量A. 化学方程式的基本写法1. 反应物与生成物的表示方法2. 反应物与生成物的系数3. 化学方程式的平衡和不平衡B. 化学方程式的平衡1. 平衡状态的描述2. 平衡常数和平衡常量表达式C. 化学计量1. 摩尔概念和摩尔质量2. 化学计量中的物质和物质量3. 用化学方程式计算物质的质量总结:高一化学必修一是化学学习的基础,通过这份知识导图,我们可以更加系统和清晰地了解和记忆这些知识点。

高一化学必修一思维导图,全册知识点分享发布时间: 2022-9-20 | 标签:化学必修一思维导图高一化学必修一思维导图高中化学必修一应该如何画好高一化学必修一思维导图呢?刚刚进入高一的同学们,面对难度倍增的化学知识可真是头大。
高中化学确实不简单,因此知犀为大家整理了一份高一化学必修一思维导图,同学们可以借助导图,从宏观上理清必修一整本书的脉络结构以及一些重难点知识。
知识点再多再杂,也能完全理顺!现在就一起来看一下高一化学必修一思维导图吧~高一化学必修一思维导图(1)大纲高一化学必修书共分六章。
分别是:第一章关于实验化学,第二章关于化学物质及其变化,第三章关于金属及其化合物,第四章关于非金属及其化合物。
高一化学必修一思维导图(2)第一章:从实验学化学第一章是化学实验的入门知识。
学生应了解常用仪器的识别和使用,掌握基本的实验操作,防止实验事故的发生。
高一化学必修一思维导图(3)第二章:物质的分类本节要求学生简单地根据物质的成分进行分类,并掌握常用的分类方法。
高一化学必修一思维导图(4)第二章:离子反应本节内容主要是掌握离子方程式的书写。
高一化学必修一思维导图(5)第二章:氧化还原反应本节要求掌握氧化还原反应的概念,从化学价态变化的分类标准理解氧化还原反应的特点。
高一化学必修一思维导图(6)第三章:金属的化学性质在这一节中,首先给出金属的简要概述,其次已知钠和铝与氧的反应,最后了解金属与酸和水的反应。
高一化学必修一思维导图(7)第三章:钠及其化合物这部分的内容是重点内容。
学生需要认识到钠是一种典型的活性金属元素,从钠的物理性质、化学性质、化合物及相关计算等方面综合控制钠。
高一化学必修一思维导图(8)第三章:铝及其化合物学习铝也是从它的物理性质,化学性质,化合物以及相关的计算。
高一化学必修一思维导图(9)第三章:铁及其化合物学习铁,首先需要对铁的物理化学性质有一个初步的了解,其次是了解铁的氧化物和氢氧化物,最后通过实验学会区分铁盐和盐铁盐。

化学必修一思维导图一、物质及其变化1. 物质的结构原子结构:由原子核和核外电子组成,原子核由质子和中子组成。
分子结构:由原子通过化学键连接而成。
晶体结构:由原子、分子或离子按照一定的规律排列而成。
2. 物质的分类纯净物:由同种元素或化合物组成,具有固定的组成和性质。
3. 物质的性质物理性质:不涉及物质组成和结构变化的性质,如颜色、状态、密度等。
化学性质:涉及物质组成和结构变化的性质,如可燃性、氧化性等。
二、化学键与化学反应1. 化学键离子键:由正负离子之间的静电作用力形成。
共价键:由原子间共享电子对形成。
金属键:由金属原子间的自由电子云形成。
2. 化学反应化学反应类型:合成反应、分解反应、置换反应、复分解反应等。
化学反应条件:温度、压力、催化剂等。
化学反应速率:反应物浓度、温度、催化剂等。
三、元素周期表1. 元素周期律元素周期表按照原子序数排列,具有周期性变化的规律。
元素周期表中,同一周期的元素具有相似的化学性质,同一族的元素具有相似的物理性质。
2. 元素周期表的应用元素周期表可以用于预测元素的化学性质和物理性质。
元素周期表可以用于解释元素的电子结构和化学键的形成。
四、化学计量学1. 物质的量物质的量:表示物质中含有的基本粒子数,单位为摩尔。
摩尔质量:表示1摩尔物质的质量,单位为克/摩尔。
2. 化学反应的计量关系化学方程式:表示化学反应的物质及其量的关系。
化学方程式的平衡:反应物和物的物质的量保持一定的比例。
3. 化学反应的热力学焓变:表示化学反应中能量的变化,单位为焦耳。
反应热:表示化学反应中吸收或释放的热量,单位为焦耳。
五、溶液与胶体1. 溶液溶液的定义:由溶质和溶剂组成的均匀混合物。
溶液的浓度:表示溶液中溶质的含量,单位为摩尔/升。
2. 胶体胶体的定义:由分散相和分散介质组成的混合物,分散相粒子的大小介于分子和宏观粒子之间。
胶体的性质:具有丁达尔效应、布朗运动等特性。
六、酸碱反应1. 酸碱理论酸碱质子理论:酸是质子(H+)的供体,碱是质子的受体。
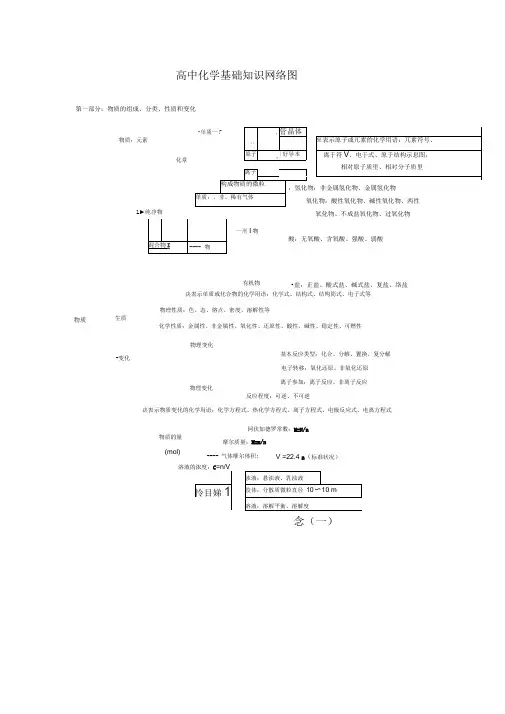
高中化学基础知识网络图第一部分:物质的组成、分类、性质和变化氧化物、不成盐氧化物、过氧化物酸:无氧酸、含氧酸、强酸、弱酸决表示单质或化合物的化学用语:化学式、结构式、结构简式、电子式等物理性质:色、态、熔点、密度、溶解性等反应程度:可逆、不可逆决表示物质变化的化学用语:化学方程式、热化学方程式、离子方程式、电极反应式、电离方程式阿伏加德罗常数:M=N/n念(一)物质:元素化章L ►纯净物|—刑I 物有机物•盐:正盐、酸式盐、碱式盐、复盐、络盐物质 生质化学性质:金属性、非金属性、氧化性、还原性、酸性、碱性、稳定性、可燃性物理变化-变化基本反应类型:化合、分解、置换、复分解 电子转移:氧化还原、非氧化还原物理变化离子参加:离子反应、非离子反应物质的量摩尔质量:M=m/n (mol)---- 气体摩尔体积:V =22.4 n (标准状况)色、态、味溶解度、熔点、沸点 密度、硬度、导电性导热性、塑性「单质兀素游离态宏观化合态原子晶体物质变化分类石墨(混合晶体)金属晶体微观大多数盐离子晶体pl 纯净物-无机物碱性氧化物*6分过氧化新潮解、分储升华、萃取溶解、盐析裂化、裂解念(二)第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)金属 稀有气体-氢化物--氧化物一不成盐氧化物含氧酸、无氧酸 强酸、弱酸,可溶碱、难容碱 正盐 酸式盐 碱式盐 复盐;络盐物质结构荷电 一实质.Si排布规律、分层1能 量最低原理层最多容纳29个次外层不超过18个最外层不超过8个一运动状态——特殊性•,电子云分子间作用力{范德华力•分子的极性L分子的形成属键一L葛子健 化学键I n ———共价键核外电子排布周期性元素性质的周期性元素周期律编制一 元素周期表表的结构示方法,影响物理性质2812---8188213Bn ABw WA BI m••族族族族 、王副o族 56 7 一一 一一 一L化学反应速率和化学平衡表示方法 :V A = △ C A /△ t 单位:mol/L - s(min 或 h是平均速率,均取正值同一反应选用不同的物质表示速率,数值可能不同 各物质表示的速率比等于该反应方程式的系数比化学平衡件学平衡、化学 反应速率反应物的结构、性质 浓度温度]催化剂 ___________________ 其他条件—光、超声 波、激光、放射线…影响化学平衡因素压强 温度平衡移动原理强电解质(完全电离)AB -^A '+B化合物电解质弱电解质装:能的转换:化学能与电化学能非电解质电冶炼金属(冶炼铝)电解质溶液第三部分:元素化合物转化关系H2O H2OMg(OH) ------ MgCO3NaOH /H2O/HCI/ CO:/ HCl .. /OHCaCl2 ・JHClCl2 为/ HCl Na2CO3HClCl* CaCO3飞CO2+ H2OAlCl 3(AI 3+)[、NaOHHClHCW " Ji/电解1Al 2O3.、O2NaOHCl HCl *Fl H2°(沸腾).»OH)3NaOH 或H C z^C02ZT S^u NaOHNaAl O 2NaOHKSCNFe(ScN)3FeSNa2SH2SO4FeONaOH H2SO4Fe3O4Fe(OH) 2O2 和H2O・ FeCl2Cl FeKSCNFeCl3 :Fe(SCN)3NaOH HCl♦ Fe(OH)3SCU2S 一HNO3 或H2SO4(浓NH3H2O 2+• Cu(OH) 2 ■ [Cu(NH 3)4]CuS ♦Na2S Cu2+(NO3、S°42)金属部分:按照单质-氧化物一氢氧化物一►盐为线索进行搜罗寻找关系非金属:按照化合价寻找各类物质,主要有氢化物、单质、氧化物、含氧酸、及其盐第四部分:有机化学—醇 (官能团:一OH ):饱和一元醇C n H 2n+1OH (n 法1)R — OH 酬 C n H 2n+2O (n A2)R O R _____ 酚(苯酚)(官能团:OH ) C n H 2n-6。

化学必修一思维导图一、物质及其变化1. 物质物质是构成宇宙的基本实体,具有质量和体积。
物质由分子、原子和离子等基本粒子组成。
物质可以分为纯净物和混合物。
2. 变化变化是指物质在时间和空间上的状态改变。
变化可以分为物理变化和化学变化。
物理变化是指物质的形态、状态或性质发生改变,但化学组成不变。
化学变化是指物质的化学组成发生改变,新的物质。
二、物质的分类与性质1. 纯净物纯净物是指由一种物质组成的物质。
纯净物可以分为元素和化合物。
2. 混合物混合物可以分为均匀混合物和非均匀混合物。
3. 物质的性质物质的性质是指物质所具有的特定属性。
物质的性质可以分为物理性质和化学性质。
物理性质是指物质在不发生化学变化的情况下所表现出来的性质,如颜色、气味、密度等。
化学性质是指物质在发生化学变化时所表现出来的性质,如可燃性、氧化性等。
三、物质的量与计量1. 物质的量物质的量是指物质所含有的粒子数目的多少。
物质的量可以用摩尔(mol)来表示。
2. 计量计量是指对物质的量进行测量的过程。
计量可以采用天平、量筒等工具进行。
四、化学反应与能量1. 化学反应化学反应是指物质在化学变化过程中发生的原子、离子或分子之间的相互作用。
化学反应可以分为合成反应、分解反应、置换反应和复分解反应。
2. 能量能量是物质所具有的做功的能力。
能量可以分为内能、热能、电能等。
五、溶液与溶解度1. 溶液溶液是指一种或多种物质分散在另一种物质中形成的均匀混合物。
溶液可以分为饱和溶液和不饱和溶液。
2. 溶解度溶解度是指在一定条件下,溶质在溶剂中达到饱和时所能溶解的最大量。
溶解度受到温度、压力等因素的影响。
六、酸碱反应与中和1. 酸碱反应酸碱反应是指酸和碱在溶液中发生的化学反应。
酸碱反应可以分为酸碱中和反应、酸碱盐反应等。
2. 中和中和是指酸和碱在反应中相互抵消,水和盐的过程。
中和反应是酸碱反应的一种特殊情况,是酸碱反应的典型代表。
七、氧化还原反应与电子转移1. 氧化还原反应氧化还原反应是指物质在化学反应中发生电子转移的过程。