吸附作用与多相催化
- 格式:ppt
- 大小:1.02 MB
- 文档页数:78


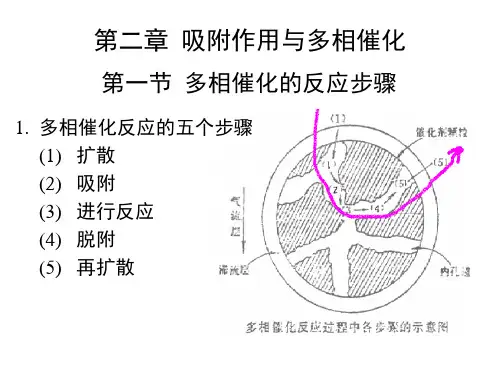
多相催化反应机理
多相催化反应是指在反应中存在两个或更多的相,如气体与固体的催化反应、液体与固体的催化反应等。
其机理可以分为以下几个步骤:
1. 吸附:反应物进入固体催化剂表面,通过吸附与催化剂发生物理或化学吸附作用。
这一步通常是决定整个反应速率的关键步骤,在反应过程中会产生吸附物。
2. 表面反应:吸附物上的反应物与其他吸附物相互作用,发生化学反应。
这一步骤通常是反应物转化为产物的关键步骤,其速率取决于吸附物的浓度和反应物之间的相互作用强度。
3. 解吸:反应物与产物从催化剂表面解吸,离开催化剂,进入反应体系中。
解吸过程可能是可逆的,有时会回到吸附阶段。
以上是一个基本的多相催化反应机理,在实际的多相催化反应中,还可能存在其他的步骤或中间体。
催化剂的种类和特性以及反应条件(如温度、压力、溶剂等)也会对反应机理产生影响。





多相催化的langmuir-hinshelwood机理Langmuir-Hinshelwood 机理是一种用于描述多相催化反应的模型,通常用于气体与固体表面之间的反应。
该模型以Irving Langmuir和Edwin Hinshelwood的名字命名,它基于表面上的活性位点吸附反应物,形成中间体,然后通过反应形成最终产物。
以下是多相催化的Langmuir-Hinshelwood 机理的基本思想:1.吸附:活性位点(通常是固体表面上的催化剂)吸附反应物分子。
这可以是物理吸附或化学吸附,具体取决于反应的性质和条件。
2.中间体形成:吸附的反应物分子在活性位点上发生反应,形成一个中间体。
这个中间体是反应的关键步骤,它是吸附在表面上的反应物分子之间的反应产物。
3.反应:中间体通过反应形成最终产物。
这可以是通过多个步骤完成的,每一步都涉及中间体的转化。
4.解吸附:产物离开催化剂表面,使活性位点重新变得可用。
Langmuir-Hinshelwood 机理可以用数学模型来描述。
对于简单的表面反应,其速率方程可以表示为:r =k⋅PA⋅PB其中:•r是反应速率;•k是速率常数;•P_A和P_B分别是两个反应物的压力。
对于复杂的多相催化反应,可以引入更多的中间体和反应步骤来建立更为详细的模型。
这有助于更准确地描述实际催化反应中的复杂过程。
需要注意的是,虽然Langmuir-Hinshelwood 机理提供了对多相催化反应的基本理解,但在实际应用中,催化反应通常涉及复杂的表面化学和动力学过程,因此更为复杂的模型可能需要考虑更多的因素。

物理吸附与化学吸附在催化中的应用摘要:吸附过程与催化作用在国民经济和环境保护方面具有重要意义。
他们是化学工业,石油炼制以及国民经济其他领域最活跃的研究课题之一。
这两个领域涉及到的都是表面现象,使用的都是多孔固体。
吸附是催化反应得以发展的最关键步骤之一,通过它揭示催化本质和研究催化性质越来越受到人们的重视,因此许多在线原位动态测量技术得以快速发展。
关键词:物理化学吸附表征测定孔结构气体探针1. 吸附现象吸附:当流体与多孔固体接触时, 流体中某一组分或多个组分在固体表面处产生积蓄, 此现象称为吸附。
吸附也指物质(主要是固体物质)表面吸住周围介质(液体或气体)中的分子或离子现象[1,2]。
实际上,人们很早就发现并利用了吸附现象,如生活中用木炭脱湿和除臭等。
随着新型吸附剂的开发及吸附分离工艺条件等方面的研究,吸附分离过程显示出节能、产品纯度高、可除去痕量物质、操作温度低等突出特点,使这一过程在化工、医药、食品、轻工、环保等行业得到了广泛的应用,例如:(1)气体或液体的脱水及深度干燥,如将乙烯气体中的水分脱到痕量,再聚合。
(2)气体或溶液的脱臭、脱色及溶剂蒸气的回收,如在喷漆工业中,常有大量的有机溶剂逸出,采用活性炭处理排放的气体,既减少环境的污染,又可回收有价值的溶剂。
(3)气体中痕量物质的吸附分离,如纯氮、纯氧的制取。
(4)分离某些精馏难以分离的物系,如烷烃、烯烃、芳香烃馏分的分离。
(5)废气和废水的处理,如从高炉废气中回收一氧化碳和二氧化碳,从炼厂废水中脱除酚等有害物质。
1.1吸附吸附属于一种传质过程,物质内部的分子和周围分子有互相吸引的引力,但物质表面的分子,其中相对物质外部的作用力没有充分发挥,所以液体或固体物质的表面可以吸附其他的液体或气体,尤其是表面面积很大的情况下,这种吸附力能产生很大的作用,所以工业上经常利用大面积的物质进行吸附,如活性炭、水膜等。
当液体或气体混合物与吸附剂长时间充分接触后,系统达到平衡,吸附质的平衡吸附量(单位质量吸附剂在达到吸附平衡时所吸附的吸附质量),首先取决于吸附剂的化学组成和物理结构,同时与系统的温度和压力以及该组分和其他组分的浓度或分压有关。