大学有机化学名词解释
- 格式:docx
- 大小:121.83 KB
- 文档页数:7

大学有机化学名词解释大全
1,同分异构体:有相同分子式而结构不同的化合物。
构造异构:指分子式相同而分子中的原子或原子团相互连接的次序不同引起的异构。
顺反异构:由于双键不能自由旋转引起的一种立体异构。
2,构象:分子中由于共价单键的旋转所表现出的原子或基团的不同空间排列。
3,芳香性:化学性质稳定,不易加成,不易氧化,容易取代,而且苯环异常稳定,这些异于一般不饱和化合物的性质总称为芳香性。
4,马氏规则:当不对称烯烃和卤化氢加成时,氢原子主要加到含氢加多的碳原子上。
5,手性分子:化学分子的实物与其镜像不能重叠的现象。
手性碳原子:连有四个不同的原子或原子团的碳原子称为手性碳原子
6,对映异构体:两个互为镜像又不同重叠的异构体称为对映异构体。
7,旋光度:当平面偏振光通过含有某些光学活性物质时,能引起旋光现象,它使偏振光的平面旋转的角度称为旋光度。
8,亲电反应:由亲电试剂的作用引起的加成反应。
9,共轭效应:是指由于共轭π键的形成而使分子性质变得更稳定、内能减小和键长趋于平均化等的效应。
,
10,傅克反应:芳烃在催化剂作用下,与卤代烃等作用,苯环上的氢原子被烷基取代的反应,也称为芳烃的烷基化反应。
11,诱导效应:由于电负性不同的取代基的影响,整个分子中的成键电子云密度向某一方向偏移,使分子发生极化的效应,叫诱导效应。
12,外消旋体:由等量的对映体相混合而形成的混合物叫做外消旋体。
13,氢键:氢原子与一个原子半径较小,而电负性又很强并带有未共用电子对的原子结合时产生的键。

大学有机化学知识点总结一、有机化合物的命名命名是学习有机化学的“语言”,因此,要求学习者必须掌握。
有机合物的命名包括俗名、习惯命名、系统命名等方法,要求能对常见有机化合物写出正确的名称或根据名称写出结构式或构型式。
1、俗名及缩写:要求掌握一些常用俗名所代表的化合物的结构式,如:木醇、甘醇、甘油、石炭酸、蚁酸、水杨醛、水杨酸、氯仿、草酸、苦味酸、肉桂酸、苯酐、甘氨酸、丙氨酸、谷氨酸、巴豆醛、葡萄糖、果糖等。
还应熟悉一些常见的缩写及商品名称所代表的化合物,如:RNA、DNA、阿司匹林、福尔马林、尼古丁等。
2、习惯命名法:要求掌握“正、异、新”、“伯、仲、叔、季”等字头的含义及用法,掌握常见烃基的结构,如:烯丙基、丙烯基、正丙基、异丙基、异丁基、叔丁基、苄基等。
3、系统命名法:系统命名法是有机化合物命名的重点,必须熟练掌握各类化合物的命名原则。
其中烃类的命名是基础,几何异构体、光学异构体和多官能团化合物的命名是难点,应引起重视。
要牢记命名中所遵循的“次序规则”。
4、次序规则:次序规则是各种取代基按照优先顺序排列的规则(1)原子:原子序数大的排在前面,同位素质量数大的优先。
几种常见原子的优先次序为:I>Br>Cl>S>P>O>N>C>H(2)饱和基团:如果第一个原子序数相同,则比较第二个原子的原子序数,依次类推。
常见的烃基优先次序为:(CH3)3C->(CH3)2CH->CH3CH2->CH3- (3)不饱和基团:可看作是与两个或三个相同的原子相连。
不饱和烃基的优先次序为: -C≡CH>-CH=CH2>(CH3)2CH-次序规则主要应用于烷烃的系统命名和烯烃中几何异构体的命名烷烃的系统命名:如果在主链上连有几个不同的取代基,则取代基按照“次序规则”一次列出,优先基团后列出。
按照次序规则,烷基的优先次序为:叔丁基>异丁基>异丙基 >丁基>丙基>乙基>甲基。
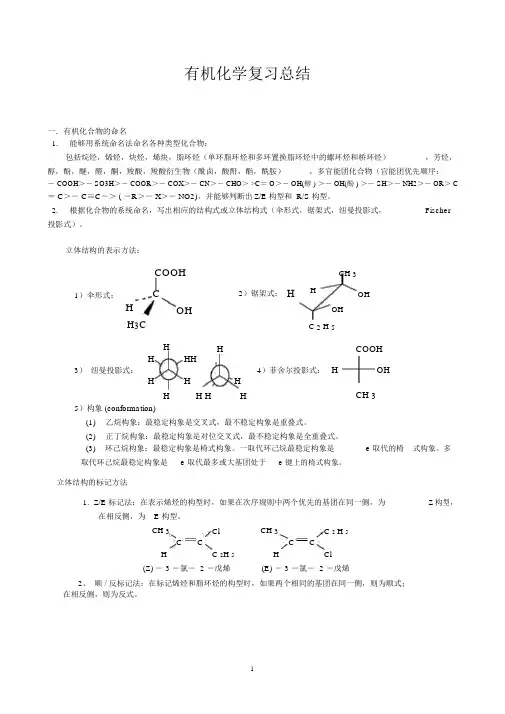
有机化学复习总结一.有机化合物的命名1.能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH>- SO3H>- COOR>- COX>- CN>- CHO> >C= O>- OH(醇 ) >- OH(酚 ) >- SH>- NH2>- OR> C = C>- C≡C-> ( -R>- X>- NO2),并能够判断出Z/E 构型和 R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:COOH CH 31)伞形式: C 2)锯架式:H H OHH OHOHH3C C 2 H 5H H COOHH HH4)菲舍尔投影式:H OH 3)纽曼投影式:H H HCH 3H H H H5)构象 (conformation)(1)乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2)正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是 e 取代的椅式构象。
多取代环己烷最稳定构象是 e 取代最多或大基团处于 e 键上的椅式构象。
立体结构的标记方法1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为 E 构型。
CH 3 Cl CH 3 C 2 H 5C C C CH C 2H 5 H Cl(Z) - 3 -氯- 2 -戊烯(E) - 3 -氯- 2 -戊烯2、顺 / 反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH3 CH3 CH3 H CH3 CH3 H CH3C C C CH H H CH3 H H CH3 H顺- 2-丁烯反- 2-丁烯顺- 1,4-二甲基环己烷反- 1,4-二甲基环己烷3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。

各章练习题1.名词解释:(1)有机化学:研究有机化合物的结构、性能和合成方法的一门科学。
(2)有机化合物:碳的化合物。
(3)官能团:在有机化合物分子中能体现一类化合物性质的原子或基团。
(4)共价键的键长、键角、键能: 键长:成键两原子核间距离。
键角:两个共价键在空间的夹角。
键能:以共价键结合的双原子分子裂解成原子时所吸收的能量。
2.写出氯甲烷分子中碳氯键的异裂和均裂的化学反应式。
H 3CCH 3 + Cl CH 3 + ClClH 3CCl1.解释名词:(1)同系列:具有相同分子通式和结构特征的一系列化合物。
(2)构造异构:分子式相同,分子中原子间相互连接顺序和方式不同而产生的不同化合物。
(3)构象异构:由单键的旋转而产生的异构体。
2.写出含有7个碳烷烃的同分异构体的结构并用系统命名法命名。
CH 3CH 2CH 2CH 2CH 2CH 2CH 3CH 3CH 2CH 2CH 2CHCH 3CH 3CH 3CH 2CH 2CHCH 2CH 3CH 3庚烷 2-甲基己烷 3-甲基己烷CH 3CHCH 2CHCH 3CH 3CH 3CH 3CHCHCH 2CH 3CH 3CH 3CH 3CCH 2CH 2CH 3CH 3CH 32,4-二甲基戊烷 2,3-二甲基戊烷 2,2-二甲基戊烷CH 3CH 2CHCH 2CH 3CH 2CH 3CH 3CH 2CCH 2CH 3CH 3CH 3CH 3CHCCH 3CH 3CH 3CH 33,3-二甲基戊烷 2,2,3-三甲基丁烷 3-乙基戊烷第三章 烯烃和炔烃1.写出单烯烃C 5H 8的所有同分异构体,并用系统命名法命名。
CH 2=CHCH 2CH 2CH 3CH 3CH=CHCH 2CH 31-戊烯 2-戊烯CH 2=CCH 2CH 3CH 3CH 2=CHCHCH 3CH 3CH 3CH=CCH 3CH 32-甲基-1-丁烯 3-甲基-1-丁烯 2-甲基-2-丁烯2.完成下列反应(1)CH 3CH 2C=CH 2 + HBrCH 3CH 3CH 2CCH 3BrCH 3(2)CH 3CH=CCH 2CH 334,HCH 3COOH + O=CCH 2CH 33(3)CH 3CH=CHCH 3 + H 2PtCH 3CH 2CH 2CH 3(4)CH 3CH 2C CH + AgNO 3(NH 3)CH 3CH 2C CAg + NH 4NO 3 + NH 3(5)CH 3C CH + HCl CH 3C=CH 2ClClCH 3CCH 33、用简单的化学方法鉴别戊烷、1-戊烯、1-戊炔。

化学基础有机一、有机化学简介有机化学,又称为碳化合物化学,是化学科学的一个重要分支。
它主要研究含碳元素的化合物的合成、结构、性质、反应机理以及相互转化的规律。
有机化学不仅是合成具有重要实用价值的有机化合物的基础学科,同时也是化学工业的重要组成部分。
二、有机化学发展历程有机化学的发展可以追溯到古代,人类在生产和生活实践中就已经开始接触和利用有机化合物。
然而,真正意义上的有机化学的研究是从18世纪后半叶开始的。
这一时期的化学家们开始对有机化合物的结构、性质和反应机理进行系统的研究。
进入20世纪后,随着科技的不断进步,有机化学的发展取得了巨大的突破。
特别是在20世纪70年代以后,随着计算机技术和谱学分析方法的快速发展,有机化学的研究进入了分子设计和功能化的新阶段。
三、有机化学基本概念1.有机化合物:通常是指含有碳元素的化合物,但不包括碳的氧化物、碳酸盐、碳酸等无机化合物。
2.有机化学反应:是指碳与碳原子之间进行的各种化学反应,主要包括取代反应、加成反应、消除反应、重排反应等。
3.共价键:原子之间通过共享电子而形成的化学键,是有机化合物结构的基础。
4.官能团:是指一种或多种活性原子的组合,可以决定有机化合物的性质。
5.手性:是指一个物体不能与其镜像相重合的性质。
在有机化合物中,手性通常是指分子中存在手性碳原子。
四、有机化学反应类型1.取代反应:有机化合物分子中的某一原子或基团被其他原子或基团取代的反应。
2.加成反应:有机化合物分子中碳碳双键或三键发生断裂,与其它原子或基团结合生成新的化合物的反应。
3.消除反应:在一定的条件下,一分子有机物脱去一分子水或卤化氢等小分子的反应。
4.重排反应:由于基团之间的迁移或交换,使得分子的原有结构发生改变的反应。
5.聚合反应:由小分子重复生成高分子化合物的反应。
6.水解反应:水分子与有机化合物反应,使其分解成两部分或更多部分的反应。
7.氧化还原反应:涉及电子传递的氧化和还原的有机反应。

大学有机化学知识点总结与归纳大学有机化学知识点总结与归纳1.酸性比较α-H存在于羰基的α-C上(这是句废话)它的酸性由旁边的吸电子基团的强弱决定一般的,相邻基团的吸电子效果越强其酸性越强相反则越弱如果连接了硝基之类的效果就相当不错了。
在强碱性环境的条件下可以类似于酸的电离一样从分子上解离被强碱捕获其母体分子形成了碳负离子碳负离子作为富电子基团作为亲核试剂具有很强的亲核活性对高度极化的基团的正电中心进行进攻常见的是羰基碳溶剂的碱性强可以促进这类反应的正反应方向进行可以促进脱质子嘛!比较弱的可以用氢氧化钾(这个太弱了很少用)也可以用乙醇钠LDA之类的强碱。
2.反应活性有很多有机化学反应,反应时对于不同的烷基或者比如卤代反应对于不同的卤代烃有不同的活性,那么活性的不同是由于什么引起的呢?其实化学反应就是电性相反的原子或者基团重新组合,因此,表面上看不同的,烃基或者卤素原子活性不同,其实就是电子云的疏密不一样,电负性也是这个原因。
比如卤代烃的反应活性R3H-x>R2CH-X>R-CH2-X而醚的碳氧键断裂(就是酸和醚反应先形成佯盐然后发生亲电取代反应)醚键断裂顺序刚好相反,因为有些是亲电的反应,要求电子云密度大的,活性高。
有些是亲核的,要求电子云密度小。
是由烷基或卤代基的给电子或吸电子能力不同引起的。
不同的机理,活性刚好是相反的因为烷基给电子而卤代基吸电子。
3.碳正离子碳正离子,也称作碳阳离子,是含有正电碳的活性中间体,通常碳为sp2杂化,与三个基团结合,留下一对垂直于平面的p轨道。
碳正离子在有机化学中具有很重要的地位,如SN1反应即经由碳正离子中间体。
一般具有能稳定正电荷的基团的碳正离子具有较高的稳定性。
一般而言,三级碳正离子的稳定性大于二级碳正离子;二级碳正离子大于一级碳正离子。
反应中间体涉及碳正离子者通常会发生重排,例如SN1反应及E1反应等。
重排的种类则有氢阴离子迁移(Hydrideshift)与甲基迁移(Methylshift)两种。

一、化合物类名无机酸酯:醇与含氧无机酸反应失去一分子水后的生成物称为无机酸酯。
双烯烃:碳碳双键数目最少的多烯烃是二烯烃或称双烯烃。
可分为三类:两个双键连在同一个碳原子上的二烯烃称为累积二烯烃,两个双键被两个或两个以上单键隔开的二烯烃称为孤立二烯烃,两个双键被一个单键隔开的二烯烃称为共轭二烯烃。
内酯:分子内的羧基和羟基失水形成的产物称为内酯。
内酰胺:分子内的羧基和胺(氨)基失水的产物称为内酰胺。
四级铵碱:四级铵盐在强碱(KOH,NaOH)作用下生成的产物称为四级铵碱。
生物碱:从动植物体内得到的一类有强烈生理效能的含氮有机化合物。
游离生物碱绝大多数是固体,难溶于水,易溶于乙醇等有机溶剂。
天然的生物碱多半是有左旋光的手性化合物。
半缩醛或半缩酮:醇具有亲核性,在酸性催化剂如对甲苯磺酸、氯化氢的作用下,很容易和醛酮发生亲核加成,一分子醛或酮和一分子醇加成的生成物称为半缩醛或半缩酮。
有机化合物:除一氧化碳、二氧化碳、碳酸盐等少数简单含碳化合物以外的含碳化合物。
多肽:一个氨基酸的羧基与另一分子氨基酸的氨基通过失水反应,形成一个酰氨键,新生成的化合物称为肽,肽分子中的酰氨键叫做肽键。
二分子氨基酸失水形成的肽叫二肽,多个氨基酸失水形成的肽叫多肽。
杂环化合物:在有机化学中,将非碳原子统称为杂原子,最常见的杂原子是氮原子、硫原子和氧原子。
环上含有杂原子的有机物称为杂环化合物。
分为两类,具有脂肪族性质特征的称为脂杂环化合物,具有芳香特性的称为芳杂环化合物。
因为前者常常与脂肪族化合物合在一起学习,所以平时说的杂环化合物实际指的是芳杂环化合物。
杂环化合物是数目最庞大的一类有机物。
多环烷烃:含有两个或多个环的环烷烃称为多环烷烃。

一、化合物类名无机酸酯:醇与含氧无机酸反应失去一分子水后的生成物称为无机酸酯。
双烯烃:碳碳双键数目最少的多烯烃是二烯烃或称双烯烃。
可分为三类:两个双键连在同一个碳原子上的二烯烃称为累积二烯烃,两个双键被两个或两个以上单键隔开的二烯烃称为孤立二烯烃,两个双键被一个单键隔开的二烯烃称为共轭二烯烃。
内酯:分子内的羧基和羟基失水形成的产物称为内酯。
内酰胺:分子内的羧基和胺(氨)基失水的产物称为内酰胺。
四级铵碱:四级铵盐在强碱(KOH,NaOH)作用下生成的产物称为四级铵碱。
生物碱:从动植物体内得到的一类有强烈生理效能的含氮有机化合物。
游离生物碱绝大多数是固体,难溶于水,易溶于乙醇等有机溶剂。
天然的生物碱多半是有左旋光的手性化合物。
半缩醛或半缩酮:醇具有亲核性,在酸性催化剂如对甲苯磺酸、氯化氢的作用下,很容易和醛酮发生亲核加成,一分子醛或酮和一分子醇加成的生成物称为半缩醛或半缩酮。
有机化合物:除一氧化碳、二氧化碳、碳酸盐等少数简单含碳化合物以外的含碳化合物。
多肽:一个氨基酸的羧基与另一分子氨基酸的氨基通过失水反应,形成一个酰氨键,新生成的化合物称为肽,肽分子中的酰氨键叫做肽键。
二分子氨基酸失水形成的肽叫二肽,多个氨基酸失水形成的肽叫多肽。
杂环化合物:在有机化学中,将非碳原子统称为杂原子,最常见的杂原子是氮原子、硫原子和氧原子。
环上含有杂原子的有机物称为杂环化合物。
分为两类,具有脂肪族性质特征的称为脂杂环化合物,具有芳香特性的称为芳杂环化合物。
因为前者常常与脂肪族化合物合在一起学习,所以平时说的杂环化合物实际指的是芳杂环化合物。
杂环化合物是数目最庞大的一类有机物。
多环烷烃:含有两个或多个环的环烷烃称为多环烷烃。
共轭烯烃:单双键交替出现的体系称为共轭体系,含共轭体系的多烯烃称为共轭烯烃。
纤维二糖:是由两分子葡萄糖通过1,4 两位上的羟基失水而来的,纤维二糖是B-糖苷。
纤维素:由多个纤维二糖聚合而成的大分子。
多稀烃:含有多于一个碳碳双键的烯烃称为多稀烃。

大学有机化学知识点总结有机化学复总结一.有机化合物的命名1.能够用系统命名法命名各种类型化合物,包括烷烃、烯烃、炔烃、烯炔、脂环烃、芳烃、醇、酚、醚、醛、酮、羧酸、羧酸衍生物、多官能团化合物,并能够判断Z/E构型和R/S构型。
2.根据化合物的系统命名,写出相应的结构式或立体结构式,包括伞形式、锯架式、菲舍尔投影式、纽曼投影式。
立体结构的表示方法包括Z/E标记法、顺/反标记法和R/S标记法。
立体结构的标记方法1.Z/E标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z构型,在相反侧,为E构型。
2.顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
3.R/S标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
然后将最不优先的基团放在远离观察者,再以次观察其它三个基团,如果优先顺序是顺时针,则为R构型,如果是逆时针,则为S构型。
有机化学反应及其特点有机化学反应可以分为不同的类型,包括自由基取代、自由基加成、亲电加成、亲电取代、亲核取代、离子型反应、亲核加成、消除反应、协同反应、还原反应和氧化反应。
每种类型的反应都有其特点和规律。
马氏规律是亲电加成反应的规律,即亲电试剂总是加到连氢较多的双键碳上。
过氧化效应是自由基加成反应的规律,即卤素加到连氢较多的双键碳上。
空间效应是体积较大的基团总是取代到空间位阻较小的位置。
定位规律是芳烃亲电取代反应的规律,包括邻、对位定位基和间位定位基。
查依切夫规律是卤代烃和醇消除反应的规律,主要产物是双键碳上取代基较多的烯烃。
休克尔规则是判断芳香性的规则,存在一个环状的大π键,成环原子必须共平面或接近共平面,π电子数符合4n+2规则。
霍夫曼规则是季铵盐消除反应的规律,只有烃基时,主要产物是双键碳上取代基较少的烯烃(动力学控制产物)。
当β-碳上连有吸电子基或不饱和键时,则消除的是酸性较强的氢,生成较稳定的产物(热力学控制产物)。

亲核反应有机反应的一类,电负性高的亲核基团向反应底物中的带正电的部分进攻而芳环上亲核取代反应历程使反应发生,这种反应为亲核反应。
与之相对的为亲电反应。
即在相互作用的两个体系之间,由于一个体系对另一个体系的原子核的吸引所引起的化学反应。
这些反应属于离子反应。
反应试剂在反应过程中,对与之相互作用的原子或体系给予或共享其电子对者,称为亲核试剂。
由亲核试剂如HO、:NR3、CN、H2N、…等与有机分子相互作用而发生的取代反应,称为亲核取代反应(SN)。
在亲核取代反应中,亲核试剂Nu进攻被作用物中的饱和碳原子,取代此饱和碳原子上的一个原子团L芳环上亲核取代反应历程能量变化。
Nu供给碳原子一对电子,生成新的共价键,碳原子与L之间的共价键破裂,L带着一对电子离去:Nu:+RL─→NuR+:L式中R为烷基。
Nu:和L:都带有孤电子对,它们可以是负离子或中性分子。
由亲核试剂HCN、H2O、丙二酸二乙酯等与世轭不饱和醛或酮进行的加成反应称亲核加成反应。
例如共轭不饱和酮与HCN加成,形成氰酮:亲电反应electrophilic reaction亲电反应指缺电子(对电子有亲和力)的试剂进攻另一化合物电子云密度较高(富电子)区域引起的反应。
亲电反应属于离子型反应(ionic reaction)的一种,是有机化学的基本反应之一。
[1]在相互作用的两个体系之间,由于一个体系对另一个体系的电子的吸引所引起的化学反应。
这些反应属于离子反应。
反应试剂在反应过程中,从与之相互作用的原子或体系得到或共享电子对者,称为亲电试剂(E+)。
凡由亲电试剂如HNO3、H2SO4、Cl2、Br2等与有机分子相互作用而发生的取代反应,称为亲电取代反应(SE):E++RX─→RE+X+式中R为烷基。
上述类型的正离子取代反应属于SE类型反应。
例如,CH3:MgBr与溴反应时,溴分子的正电荷部分(相当于上式中的E+)与带着一对电子的甲基反应:CH3:|MgBr+Br+|:Br-─→CH3Br+MgBr2亲电反应在芳香族化合物亲电取代反应中,亲电试剂进攻芳香环,生成σ络合物,然后离去基团变成正离子离开,离去基团在多数情况下为质子:一般,第二步的速率比第一步高(k2》k1,k)。

亲核反应有机反应的一类,电负性高的亲核基团向反应底物中的带正电的部分进攻而芳环上亲核取代反应历程使反应发生,这种反应为亲核反应。
与之相对的为亲电反应。
即在相互作用的两个体系之间,由于一个体系对另一个体系的原子核的吸引所引起的化学反应。
这些反应属于离子反应。
反应试剂在反应过程中,对与之相互作用的原子或体系给予或共享其电子对者,称为亲核试剂。
由亲核试剂如HO、:NR3、CN、H2N、…等与有机分子相互作用而发生的取代反应,称为亲核取代反应(SN)。
在亲核取代反应中,亲核试剂Nu 进攻被作用物中的饱和碳原子,取代此饱和碳原子上的一个原子团L芳环上亲核取代反应历程能量变化。
Nu供给碳原子一对电子,生成新的共价键,碳原子与L之间的共价键破裂,L带着一对电子离去:Nu:+RL─→NuR+:L式中R为烷基。
Nu:和L:都带有孤电子对,它们可以是负离子或中性分子。
由亲核试剂HCN、H2O、丙二酸二乙酯等与世轭不饱和醛或酮进行的加成反应称亲核加成反应。
例如共轭不饱和酮与HCN加成,形成氰酮:亲电反应electrophilic reaction亲电反应指缺电子(对电子有亲和力)的试剂进攻另一化合物电子云密度较高(富电子)区域引起的反应。
亲电反应属于离子型反应(ionic reaction)的一种,是有机化学的基本反应之一。
[1]在相互作用的两个体系之间,由于一个体系对另一个体系的电子的吸引所引起的化学反应。
这些反应属于离子反应。
反应试剂在反应过程中,从与之相互作用的原子或体系得到或共享电子对者,称为亲电试剂(E+)。
凡由亲电试剂如HNO3、H2SO4、Cl2、Br2等与有机分子相互作用而发生的取代反应,称为亲电取代反应(SE):E++RX─→RE+X+式中R为烷基。
上述类型的正离子取代反应属于SE类型反应。
例如,CH3:MgBr与溴反应时,溴分子的正电荷部分(相当于上式中的E+)与带着一对电子的甲基反应:CH3:|MgBr+Br+|:Br-─→CH3Br+MgBr2亲电反应在芳香族化合物亲电取代反应中,亲电试剂进攻芳香环,生成σ络合物,然后离去基团变成正离子离开,离去基团在多数情况下为质子:一般,第二步的速率比第一步高(k2》k1,k)。
延安大学继续教育学院商洛函授站第二学期课程作业课程名称有机化学授课年级2014专业临床班级专升本姓名李金锋《有机化学》课程作业一、名词解释1、对映异构体:互为物体与镜像关系的立体异构体,称为对映异构体(简称为对映体). 对映异构体都有旋光性,其中一个是左旋的,一个是右旋的. 所以对映异构体又称为旋光异构体。
2、碘值:表示有机化合物中不饱和程度的一种指标。
指100g物质中所能吸收(加成)碘的克数。
主要用于油脂、脂肪酸、蜡及聚酯类等物质的测定。
3、酯化反应:酯化反应通常指醇或酚与含氧的酸类(包括有机酸和无机酸)作用生成酯和水的过程,也就是在醇或酚羟基的氧原子上引入酰基的过程, 也称为O-酰化反应.4、波谱分析:《波谱分析》由多位作者根据中国科学院长春应用化学研究所的讲义编写而成,系统地介绍了红外、拉曼、紫外、质谱和核磁共振方面的基础知识。
5、红外光谱:以波长或波数为横坐标以强度或其他随波长变化的性质为纵坐标所得到的反映红外射线与物质相互作用的谱图。
6、重氮化反应:首先由一级胺与重氮化试剂结合,然后通过一系列质子转移,最后生成重氮盐。
7、共振跃迁:“共振跃迁”是天文学专有名词。
来自中国天文学名词审定委员会审定发布的天文学专有名词中文译名,词条译名和中英文解释数据版权由天文学名词委所有。
8、伽特曼反应:以德国化学家路德维希·加特曼(Ludwig Gattermann)命名,可以指:芳香重氮盐中的重氮基,在新制铜粉和盐酸或氢溴酸作用下,被其他基团置换的反应9、中性氨基酸:所谓中性氨基酸是指分子中氨基和羧基的数目相等的一类氨基酸。
因其分子中碱性的“-NH2”与酸性的“-COOH”数目相等,故名。
包括甘氨酸、丙氨酸、亮氨酸、异亮氨酸、半胱氨酸、色氨酸、苏氨酸、丝氨酸、苯丙氨酸、甲硫氨酸、酪氨酸、缬氨酸。
其中,缬氨酸、甲硫氨酸、苯丙氨酸、色氨酸为必需氨基酸。
10、蛋白质:蛋白质是构成一切细胞和组织结构必不可少的成分。
有机物-特点多数有机化合物主要含有碳、氢两种元素,此外也常含有氧、氮、硫、卤素、磷等。
部分有机物来自植物界,但绝大多数是以石油、天然气、煤等作为原料,通过人工合成的方法制得。
和无机物相比,有机物数目众多,可达几百万种。
有机化合物的碳原子的结合能力非常强,互相可以结合成碳链或碳环。
碳原子数量可以是1、2个,也可以是几千、几万个,许多有机高分子化合物甚至可以有几十万个碳原子。
此外,有机化合物中同分异构现象非常普遍,这也是造成有机化合物众多的原因之一。
有机化合物除少数以外,一般都能燃烧。
和无机物相比,它们的热稳定性比较差,有机物结构式电解质受热容易分解。
有机物的熔点较低,一般不超过400℃。
有机物的极性很弱,因此大多不溶于水。
有机物之间的反应,大多是分子间反应,往往需要一定的活化能,因此反应缓慢,往往需要催化剂等手段。
而且有机物的反应比较复杂,在同样条件下,一个化合物往往可以同时进行几个不同的反应,生成不同的产物。
有机物-历史“有机”这历史性名词,可追塑至19世纪,当时被认为有机化合物只能以生物经vis vitalis(life-force 生命力)合成。
此理论基于有机物与“无机”的基本分别,无机物是不会被生命力合成而来。
但后来这理论被推翻,Friedrich W?hler 以氰酸钾及硫酸铵合成尿素(一个有机物)。
一般而言,有机化合物定义为化合物中有碳氢键而无机化合物则没有。
因此碳酸(H2CO3)是无机化合物,但是蚁酸 (HCOOH 第一个脂肪酸)则是有机化合物。
有机物-分类按照碳链结合形式的不同,有机化合物基本可以分为:脂肪族化合物:(或开链族化合物):碳原子和碳原子之间形成一条开放的链,可以是直链也可以带支链;碳环族化合物:碳原子连接成环状脂环族:碳原子和碳原子之间形成一条封闭的环状链,也可以带支链;芳香族:碳原子和碳原子之间形成一条封闭的环状链,但各碳原子之间的结合是单键和双键互相交错的;杂环族:碳原子和碳原子之间形成一条封闭的环状链,但其中某些碳原子被其他元素的原子取代。
大学有机化学名词解释1. 有机化学有机化学是研究有机物的结构、性质、合成方法和反应规律的一门分支学科。
2. 有机物有机物是由碳元素和氢元素以及其他在有机化合物中常见的原子(如氧、氮、硫等)组成的化合物。
有机物在天然界中广泛存在,并具有许多重要的生物和工业应用。
3. 有机化合物有机化合物是由碳原子与其他元素(通常为氢、氧、氮、硫等)形成的化学键而构成的化合物。
有机化合物具有多样的结构和性质,并且在生活和工业中有许多重要的应用。
4. 烃类烃类是一类仅由碳和氢元素构成的有机化合物。
根据其分子结构的不同,烃类可以进一步分为脂烃、烯烃和炔烃等不同类别。
- 脂烃是由碳和氢构成的饱和烃,其中碳原子通过单键连接。
- 烯烃是由碳和氢构成的不饱和烃,其中碳原子之间存在双键。
- 炔烃是由碳和氢构成的不饱和烃,其中碳原子之间存在三键。
5. 功能团功能团是有机化合物分子中具有一定特殊结构和化学性质的部分。
功能团可以决定有机化合物的物理性质和化学反应,常用于对有机化合物进行命名和分类。
常见的功能团包括羟基、醛基、酮基、羧基、酯基、醚基、胺基等。
6. 反应机理反应机理描述了有机反应中化学物质之间的转变和产物生成的步骤和过程。
了解反应机理对于理解有机反应的原理和预测产物具有重要意义。
7. 分子结构有机化合物的分子结构描述了化合物中各个原子的排列方式以及化学键的连接方式。
分子结构对于理解和预测有机化合物的性质和反应行为至关重要。
8. 碳骨架碳骨架是指有机化合物中由碳原子构成的骨架结构。
碳骨架决定了有机化合物的基本结构类型,可以通过修改碳骨架而改变化合物的性质和反应活性。
以上是有机化学中的一些重要名词的解释。
希望对您的学习和研究有所帮助。
有机化学复习总结一.有机化合物的命名1. 能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:1)伞形式:CCOOHOHH 3 2)锯架式:CH 3OH HHOH C 2H 53)纽曼投影式:H H 4)菲舍尔投影式:COOHCH 3OH H5)构象(conformation)(1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是e 取代的椅 式构象。
多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。
立体结构的标记方法1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为E 构型。
CH 3C H C 2H 5CH 3C CH 2H 5Cl(Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯2、 顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH 3C CHCH 3HCH 3CCH HCH 3顺-2-丁烯反-2-丁烯333顺-1,4-二甲基环己烷反-1,4-二甲基环己烷3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
名词解释
(1)有机化合物—碳氢化合物及其衍生物。
(2)键能—形成共价键的过程中体系释放出的能量,或共价键断裂过程中体系所吸收的能量。
(3)极性键—由不相原子形成的键,由于成键原子的电负性不同,其吸引电子的能力不同,使电负性较强原子的一端电子云密度较大,具有部分负电荷,而另一端则电子云密度较小,具有部分正电荷,这种键具有极性,称为极性键。
云对称地分布在两个成键原子之间,这种键没有极性,称为极性键。
(4)官能团—分子中比较活泼而容易发生反应的原子或基团,它常常决定着化合物的主要性质,反映化合物的主要特征。
(5)实验式—表示组成物质的元素原子最简整数比的化学式。
(6)构造式—表示分子构造的化学式。
(7)均裂—成键的一对电子平均分给两个成键原子或基团,这种断裂称均裂。
(8)异裂—成键的一对电子完全为成键原子中的一个原子或基团所占有,形成正、负离子,这种断裂称异裂。
(9)sp2杂化—2s轨道和两个2p轨道杂化。
(10)诱导效应—由于分子内成键原子的电负性不同,而引起分子中电子云密度分布不平均,且这种影响沿分子链静电诱导地传递下去,这种分子内原子间相互影响的电子效应,称为诱导效应。
(11)氢键—当氢原子与电负性很强且原子半径较小的原子(如N,O,F等原子)相连时,电子云偏向电负性较大的原子,使氢原子变成近乎氢正离子状态,此时若与另一个电负性很强的原子相遇,则发生静电吸引作用,使氢原子在两个电负性很强的原子之间形成桥梁,这样形成的键,称为氢键。
(12)Lewis酸—能够接受未共用电子对的分子或离子。
大学有机化学总结有机化学复习总结一、试剂的分类与试剂的酸碱性1、自由(游离)基引发剂在自由基反应中能够产生自由基的试剂叫自由基引发剂(free radical initiator),产生自由基的过程叫链引发。
如: Cl2、Br2是自由基引发剂,此外,过氧化氢、过氧化苯甲酰、偶氮二异丁氰、过硫酸铵等也是常用的自由基引发剂。
少量的自由基引发剂就可引发反应,使反应进行下去。
2、亲电试剂简单地说,对电子具有亲合力的试剂就叫亲电试剂(electrophilic reagent)。
亲电试剂一般都是带正电荷的试剂或具有空的p轨道或d轨道,能够接受电子对的中性分子,如:H,、Cl,、Br,、RCH2,、CH3CO,、NO2,、,SO3H、SO3、BF3、AlCl3等,都是亲电试剂。
在反应过程中,能够接受电子对试剂,就是路易斯酸(Lewis acid),因此,路易斯酸就是亲电试剂或亲电试剂的催化剂。
3、亲核试剂对电子没有亲合力,但对带正电荷或部分正电荷的碳原子具有亲合力的试剂叫亲核试剂(nucleophilic reagent)。
亲核试剂一般是带负电荷的试剂或是带有未共用电子对的中性分子,如:OH,、HS,、CN,、NH2,、RCH2,、RO,、RS,、PhO,、RCOO,、X,、H2O、ROH、ROR、NH3、RNH2等,都是亲核试剂。
在反应过程中,能够给出电子对试剂,就是路易斯碱(Lewis base),因此,路易斯碱也是亲核试剂。
4、试剂的分类标准在离子型反应中,亲电试剂和亲核试剂是一对对立的矛盾。
如:CH3ONa +CH3Br?CH3OCH3 + NaBr的反应中,Na,和,CH3是亲电试剂,而CH3O,和Br,是亲核试剂。
这个反应究竟是亲反应还是亲核反应呢,一般规定,是以在反应是最先与碳原子形成共价键的试剂为判断标准。
在上述反应中,是CH3O,最先与碳原子形成共价键,CH3O,是亲核试剂,因此该反应属于亲核反应,更具体地说是亲核取代反应。
亲核反应有机反应的一类,电负性高的亲核基团向反应底物中的带正电的部分进攻而芳环上亲核取代反应历程使反应发生,这种反应为亲核反应。
与之相对的为。
即在相互作用的两个体系之间,由于一个体系对另一个体系的原子核的吸引所引起的。
这些反应属于离子反应。
反应试剂在反应过程中,对与之相互作用的原子或体系给予或共享其电子对者,称为。
由亲核试剂如HO、:NR3、CN、H2N、…等与有机分子相互作用而发生的,称为亲核取代反应(SN)。
在亲核取代反应中,亲核试剂Nu进攻被作用物中的饱和碳原子,取代此饱和碳原子上的一个原子团L芳环上亲核取代反应历程能量变化。
Nu供给碳原子一对电子,生成新的,碳原子与L之间的共价键破裂,L带着一对电子离去:Nu:+RL─→NuR+:L式中R为烷基。
Nu:和L:都带有孤电子对,它们可以是负离子或中性分子。
由亲核试剂HCN、H2O、丙二酸二乙酯等与世轭不饱和醛或酮进行的称亲核加成反应。
例如共轭不饱和酮与HCN加成,形成氰酮:亲电反应electrophilic reaction亲电反应指缺电子(对电子有亲和力)的试剂进攻另一化合物电子云密度较高(富电子)区域引起的反应。
亲电反应属于(ionic reaction)的一种,是的基本反应之一。
[1]在相互作用的两个体系之间,由于一个体系对另一个体系的电子的吸引所引起的化学反应。
这些反应属于离子反应。
反应试剂在反应过程中,从与之相互作用的原子或体系得到或共享电子对者,称为亲电试剂(E+)。
凡由亲电试剂如HNO3、H2SO4、Cl2、Br2等与有机分子相互作用而发生的取代反应,称为亲电取代反应(SE):E++RX─→RE+X+式中R为烷基。
上述类型的正离子取代反应属于SE类型反应。
例如,CH3:MgBr与溴反应时,溴分子的正电荷部分(相当于上式中的E+)与带着一对电子的甲基反应:CH3:|MgBr+Br+|:Br-─→CH3Br+MgBr2亲电反应在芳香族化合物亲电取代反应中,亲电试剂进攻芳香环,生成σ络合物,然后离去基团变成正离子离开,离去基团在多数情况下为质子:一般,第二步的速率比第一步高(k2》k1,k)。
由亲电试剂进攻所引起的加成反应称为亲电加成反应。
在没有光照和自由基引发的条件下,烯烃与卤素的加成反应是亲电加成反应,例如:CH3CH匉CH2+Br2─→CH3CHBrCH2Br反应在非极性溶剂中进行时,极性物质如极性容器壁,极性的溶质如氯化氢、水等都具有催化作用,使反应速率加快。
加成速率与烯烃的结构密切相关,双键连有给电子基团者加溴就快,连有吸电子基团者加溴就慢。
在大多数情况下,亲电加成反应是反式加成,加成中间体为溴桥正离子,反应是分步进行的:亲电反应反应物亲电反应在亲电反应过程中,从与之相互作用的原子或体系得到或共享电子对的反应物,称为(electrophiles?E);与亲电试剂作用的反应物称为(nucleophile?Nu)。
最常见的亲电试剂是(halohydrocarbon)和(acyl halide),亲电试剂是(Lewis acid),因而亲电试剂的亲电性与其酸性有关,一般而言,酸性强的亲电试剂亲电性强,但二者没有定量关系,特例也有不少。
纽曼投影式纽曼投影式是纽曼(Newman)于1995年提出来的。
它像锯架投影式一样,是表示相邻两个原子连接的原子或原子团之间的空间关系。
画这种投影式是把分子的立体模型(如乙烷)放在眼前,从C-C单键的延长线上去观察,用一个较大的圆圈(也可以不用圆圈)表示C-C单键上的碳原子,前后两个圆圈实际上是重叠的,故纸面上只能画出一个来。
圆圈前面的三个氢原子表示离眼睛较近碳原子上的三个氢原子,圆圈上面的三个氢原子表示离眼睛较远碳原子的三个氢原子。
前面和后面的三个C-H键之间的距离都是相等的,角距为120°。
这样所得乙烷的纽曼投影式如下:(Ⅷ)为乙烷的球棒模型。
由箭头指引的方向去观察得到纽曼投影式(Ⅸ)。
(Ⅹ)为简化的纽曼投影式,虚线表示后面碳原子上的C-H键。
分子轨道理论1. 分子轨道理论在化学键理论中的位置分子轨道理论是现代共价键理论的一个分支。
其与现代共价键理论的重要区别在于,分子轨道理论认为原子轨道组合成分子轨道,电子在分子轨道中填充、运动。
而现代共价键理论则讨论原子轨道,认为电子在原子轨道中运动。
2. 理论要点1) 分子轨道由原子轨道线性组合而成分子轨道的数目与参与组合的原子轨道数目相等。
H2中的两个 H有两个1s,可组合成两个分子轨道。
两个s轨道只能只能“头对头”组合成σ分子轨道,MO和*MO, 能量总和与原来AO(2个)总和相等,σ*的能量比AO低,称为成键轨道,σ比AO高,称为反键轨道。
成键轨道在核间无节面,反键轨道有节面. 当原子沿 x 轴接近时,p x与 p x头对头组合成σP x和σP*x,同时p y和p y,p z和 p z分别肩并肩组合成π*p y , πp y和π*p z , πp z分子轨道,π轨道有通过两核连线的节面,σ轨道没有。
2) 线性组合三原则a) 对称性一致原则对核间连线呈相同的对称性的轨道可组合,除上述讲的 s-s, p-p 之外,还有:若 s 和 p x沿 y 轴接近,对称不一致,不能组成分子轨道b) 能量相近原则H 1s -1312 kJ/mol Na3s - 496 kJ/mol Cl 3p -1251 kJ/mol O 2p -1314 kJ/mol(以上数据按 I1值估算)左面 3 个轨道能量相近,彼此间均可组合, 形成分子, Na 3s 比左面 3 个轨道能量高许多, 不能组合.(不形成共价键, 只为离子键) c) 最大重叠原理在对称性一致、能量相近的基础上,原子轨道重叠越3)分子磁学性质电子自旋产生磁场,分子中有不成对电子时,各单电子平行自旋,磁场加强。
这时物质呈顺磁性。
表现在外磁场中显磁性,在磁天平中增重。
若分子中无成单电子时,电子自旋磁场抵消,物质显抗磁性(逆磁性或反磁性), 表现在于外磁场作用下出现诱导磁矩,与外磁场相排斥,故使磁天平减重. 实验表明, 单质 O2是顺磁性的. 用分子轨道理论解释,见 O2的分子轨道图和分子轨道式:按路易斯理论, 氧气分子电子构型为 :用路易斯理论,不能解释氧气分子无单电子. 用现代价键理论也解释不通, p x-p x成σ键, p y-p y成π键, 单电子全部成对, 形成共价键, 无单电子. 分子轨道理论在解释O2的磁性上非常成功。
N2大,越易形成分子轨道, 或说共价键越强. 3) 分子轨道能级图分子轨道的能量与组成它的原子轨道能量相关,能量由低到高组成分子轨道能级图4) 分子轨道中的电子排布分子中的所有电子属于整个的分子,在分子轨道中依能量由低到高的次序排布,同样遵循能量最低原理,保里原理和洪特规则。
3. 同核双原子分子1) 分子轨道能级图A图适用于 O2, F2分子, B图适用于N2, B2, C2等分子.对于 N, B, C原子, 2s 和 2p 轨道间能量差小, 相互间排斥作用大, 形成分子轨道后, σ2s和σ2Px之间的排斥也大,结果, 出现 B图中σ2Px的能级反比π2Py , π2Pz的能级高的现象. 2) 电子在分子轨道中的排布电子只填充在成键轨道中, 能量比在原子轨道中低. 这个能量差, 就是分子轨道理论中化学键的本质. 可用键级表示分子中键的个数: 键级 = (成键电子数 - 反键电子数)/2H2分子中, 键级 = (2 - 0)/2 = 1, 单键由于填充满了一对成键轨道和反键轨道,故分子的能量与原子单独存在时能量相等. 故 He2不存在,键级为零,He之间无化学键。
He2+的存在用价键理论不好解释,无两个单电子的成对问题。
但用分子轨道理论则认为有半键. 这是分子轨道理论是抗磁性的. 4. 异核双原子分子非键轨道: 无对应的(能量相近, 对称性匹配)的原子轨道, 直接形成的分子轨道. 注意: 非键轨道是分子轨道, 不再属于提供的原子.H 的1s与 F的 1s, 2s 能量差大, 不能形成有效分子轨道. 所以F 的1s, 2s 仍保持原子轨道的能量, 对 HF 的形成不起作用, 称非键轨道, 分别为1σ和 2σ. 当 H 和 F 沿 x 轴接近时, H的 1s 和F 的 2p x对称性相同,能量相近 ( F 的 I1比 H 的 I1大, 故能量高), 组成一对分子轨道 3σ和4σ(反键), 而 2p y和2p z由于对称性不符合, 也形成非键轨道, 即 1π和 2π.较现代价键理论的成功之处。
双烯合成反应双烯合成反应,也称为“狄尔斯(Diels)—(Alder)反应” :共轭二烯烃和某些具有碳碳双键、三键的不饱和化合物进行1,4-加成,生成环状化合物的反应称为双烯合成反应。
获得1950年诺贝尔化学奖。
(1)双烯体是以顺式构象进行反应的,反应条件为光照或加热。
(2)双烯体(共轭二烯)可是连状,也可是环状。
如环戊二烯,环己二烯等。
(3)亲双烯体的双键碳原子上连有吸电子基团时,反应易进行。
常见的亲双烯体有:CH2=CH-CHO CH2=CH-COOH CH2=CH-COCH3 CH2=CH-NO2CH2=CH-CN CH2=CH-COOCH3 CH2=CH-CH2Cl(4)D-A反应的产量高,应用范围广是有机合成的重要方法之一,在理论上和生都占有重要的地位。
双烯合成反应既不是离子性反应,也不是自由基反应,而是不生成活性中间体且又一步完成的协同反应。
当双烯体2号位有推电子基,亲双烯体上有拉电子基,产物以两取代基处在1,4位为主;当双烯体1号位有推电子基,亲双烯体上有拉电子基,产物以两取代基处在邻位为主脂环烃alicyclic hydrocarbon具有脂肪族性质的环烃,分子中含有闭合的碳环,但不含苯环。
中文名称:旋光性英文名称:optical rotation;optical activity定义:当光通过含有某物质的溶液时,使经过此物质的偏振光平面发生旋转的现象。
可通过存在镜像形式的物质显示出来,这是由于物质内存在不对称碳原子或整个分子不对称的结果。
由于这种不对称性,物质对偏振光平面有不同的折射率,因此表现出向左或向右的旋光性。
利用旋光性可以对物质(如某些糖类)进行定性或定量分析。
离去基团leaving group离去基团(或称离去基)在中从一较大分子中脱离的或,是与中应用的。
在亲核取代反应中,被进攻的称为(substrate),而从底物分子中带着一对断裂出去的原子或称为离去基团,常用L表示。
一般讲,底物是提供原子与之形成新键的反应物,而离去基团往往是或。
常见的离去基团有:X-,-OCOR,-OTs,-ONO2,-OH,…。
易接受电子、承受能力强的是好的离去基团。