7.3一些重要的烃类和石油化工
- 格式:docx
- 大小:35.23 KB
- 文档页数:7
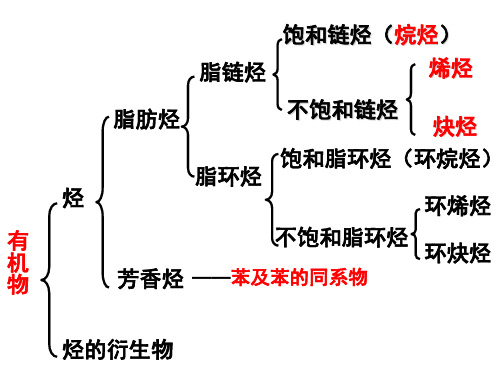



上海市使用的化学教材跟人教版教材纷歧样,而很多老师是人教版或其他版本教材出身,加之教材在教学中的作用不容忽视,因此将初三到高三的教材目录罗列如下:九年级上册第一章化学的魅力第二章空气第三章溶液第四章碳九年级下册第五章酸、碱第六章盐、金属第七章化学与生活一、高中化学教材介绍(上海科学技术出版社)高中一年级第一学期1、打开原子世界的大门1.1 从葡萄干面包原子模型到原子结构的行星模型1.2 原子结构和相对原子质量1.3 揭开原子核外电子运动的面纱2、开发海水中的卤素资源2.1 以食盐为原料的化工产品2.2 海水中的氯2.3 从海水中提取溴和碘3、探索原子构建物质的奇妙3.1 原子间的相互作用3.2 离子键3.3 共价键4、剖析物质变更中的能量变更4.1 物质在溶解过程中有能量变更吗4.2 化学变更中的能量变更高中一年级第二学期5、评说硫、氮的“功”与“过”5.1 从黑火药到酸雨5.2 认识物质的量浓度5.3 硫酸5.4 化学肥料中的主角6、揭示化学反应速率和平衡之谜6.1 化学反应为什么有快有慢6.2 反应物如何可能转酿成生成物6.3 化工生产能否做到又快又多7、探究电解质溶液的性质7.1 电解质的电离7.2 研究电解质在溶液中的化学反应7.3 盐溶液的酸碱性7.4 电解质溶液在通电情况下的变更高中二年级第一学期8、走进精彩纷呈的金属世界8.1 应用广泛的金属资料——钢铁8.2 铝和铝合金的崛起9、初识元素周期律9.1 元素周期律9.2 元素周期表10、学习几种定量测定方法10.1 测定1mol气体的体积10.2 结晶水合物中结晶水含量的测定10.3 酸碱滴定高二年级第二学期11、认识碳氢化合物的多样性11.1 碳氢化合物的宝库——石油11.2 石油化工的龙头——乙烯11.3 煤化工和乙炔11.4 一种特殊的碳氢化合物——苯12、初识生活中的一些含氧有机化合物12.1 杜康酿酒话乙醇12.2 醋和酒香12.3 家庭装潢说甲醛13、检验一些无机化合物13.1 离子的检验13.2 混合物的检验高三年级拓展型课程1、原子结构与元素周期律1.1 原子结构1.2 元素周期律2、化学键和晶体结构2.1 化学键和分子间作用力2.2 晶体3、化学中的平衡3.1 溶解平衡3.2 化学反应中的平衡3.3 电离平衡3.4 水的电离和盐类水解4、离子互换反应和氧化还原反应4.1 离子互换反应4.2 氧化还原反应5、非金属元素5.1 非金属单质5.2 一些非金属化合物5.3 化工生产6、金属元素6.1 金属及其冶炼6.2 一些金属化合物7、烃7.1 烃的分类和同系物7.2 烃的命名和同分异构现象7.3 一些重要的烃类和石油化工8、烃的衍生物8.1 卤代烃8.2 醇和酚8.3 醛8.4 羧酸和酯9、化学实验探究9.1 罕见气体的制备和净化9.2 物质的提纯和分离9.3 物质的检验9.4 定量实验9.5 化学实验方法的探究。

石油化工基础知识石油化工的基础原料石油化工的基础原料有4类:炔烃 (乙炔)、烯烃 (乙烯、丙烯、丁烯和丁二烯)、芳烃(苯、甲苯、二甲苯)及合成气。
由这些基础原料可以制备出各种重要的有机化工产品和合成材料天然气化工以天然气为原料的化学工业简称天然气化工。
其主要内容有:1)天然气制碳黑;2)天然气提取氦气;3)天然气制氢;4)天然气制氨;5)天然气制甲醇;6)天然气制乙炔;7)天然气制氯甲烷;8)天然气制四氯化碳;9)天然气制硝基甲烷;10)天然气制二硫化碳;11)天然气制乙烯;12)天然气制硫磺等。
100×104 t原油加工的化工原料据资料统计,100×104 t原油加工可产出:乙烯15×104 t,丙烯9×104 t,丁二烯2.5×104 t,芳烃8×104 t,汽油9×104 t,燃料油47.5×104 t。
炼油厂的分类可分为4种类型。
1)燃料油型生产汽油、煤油、轻重柴油和锅炉燃料。
2)燃料润滑油型除生产各种燃料油外,还生产各种润滑油。
3)燃料化工型以生产燃料油和化工产品为主。
4)燃料润滑油化工型它是综合型炼厂,既生产各种燃料、化工原料或产品同时又生产润滑油。
原油评价试验当加工一种原油前,先要测定原油的颜色与气味、沸点与馏程、密度、粘度、凝点、闪点、燃点、自燃点、残炭、含硫量等指标,即是原油评价试验。
炼厂的一、二、三次加工装置把原油蒸馏分为几个不同的沸点范围(即馏分)叫一次加工;将一次加工得到的馏分再加工成商品油叫二次加工;将二次加工得到的商品油制取基本有机化工原料的工艺叫三次加工。
一次加工装置;常压蒸馏或常减压蒸馏。
二次加工装置:催化、加氢裂化、延迟焦化、催化重整、烃基化、加氢精制等。
三次加工装置:裂解工艺制取乙烯、芳烃等化工原料。
辛烷值辛烷值是表示汽油在汽油机中燃烧时的抗震性指标。
常以标准异辛烷值规定为100,正庚烷的辛烷值规定为零,这两种标准燃料以不同的体积比混合起来,可得到各种不同的抗震性等级的混合液,在发动机工作相同条件下,与待测燃料进行对比。

化学石油化工知识点总结化学石油化工是一个重要的工业领域,涵盖了许多关键的知识点。
以下是对化学石油化工的一些主要知识点进行总结和拓展:1. 石油及其加工技术:石油是化学石油化工的基础原料,它主要由碳氢化合物组成。
石油加工技术涉及原油分馏、催化裂化、催化重整等过程,以生产出不同种类的石油产品,如汽油、柴油、润滑油等。
2. 化学反应工程:化学反应工程是石油化工过程中最关键的环节之一。
它涉及到反应的选择、反应器的设计、反应条件的控制等方面。
常见的化学反应包括酸碱中和、氧化还原、聚合等。
3. 催化剂:催化剂在化学石油化工中起着至关重要的作用。
它们可以加速化学反应的进行,提高反应速率和选择性。
常见的催化剂有金属催化剂、酸碱催化剂、酶催化剂等。
4. 分离技术:分离技术在石油化工中被广泛应用于提纯和分离混合物。
常用的分离技术包括蒸馏、萃取、吸附、膜分离等。
这些技术可以根据不同物质的物理性质和化学性质来实现分离和纯化。
5. 储运与安全:化学石油化工产品的储运和安全是非常重要的环节。
这涉及到储罐、管道、车辆等的设计和维护,以确保产品的安全运输和储存。
此外,化学石油化工企业还需要遵守相关的安全法规,并采取适当的措施来预防事故和环境污染。
6. 绿色化学石油化工:近年来,绿色化学石油化工成为关注的热点。
绿色化学石油化工致力于开发和应用更环保、可持续的技术和工艺,以减少对环境的影响。
例如,使用可再生能源作为替代能源来源,开发生物基化工产品等。
总之,化学石油化工涉及广泛的知识领域,其中的细节和应用非常繁多。
以上只是对一些主要知识点的概括,希望能为读者提供一个初步了解化学石油化工的框架。
如果想更深入地了解该领域,还需要进一步学习和实践。
高一化学第2节石油和煤、重要的烃山东科技版【本讲教育信息】一. 教学内容:第2节石油和煤、重要的烃教学目的:1. 了解石油的组成,石油产品的广泛用途。
2. 了解加成反应及其不饱和烃的概念。
3. 了解乙烯的物理性质和主要用途,掌握乙烯的化学性质。
4. 了解煤的组成、煤干馏产品的广泛应用。
5. 掌握苯的结构式及其重要的化学性质,了解苯及其同系物在组成、结构性质上的差异。
二. 重点、难点:乙烯及苯的化学性质三. 知识分析石油和煤是复杂的混合物,主要成分都是复杂的有机化合物,并分别被誉为“工业的血液”和“工业的粮食”。
(一)石油的炼制乙烯(1)石油的炼制阅读课本回答下列问题:①石油的主要成分是什么?②什么是石油的分馏?③石油裂化的目的是什么?④石油裂解的目的是什么?(解答:①含有不同数目碳原子的烃。
②将石油加热,沸点低的烃先汽化,蒸气冷凝后变为液体,随着温度的升高,沸点较高的烃再汽化,再冷凝,这样通过加热和冷凝,把石油分成不同沸点的产物叫做石油的分馏。
③提高轻质燃料油特别是汽油的质量。
④使长链烃断裂为乙烯、丙稀等小分子烃。
)(2)乙烯 乙烯是衡量一个国家石油化工发展水平的标志。
物理性质:无色稍有气味的气体,难溶于水,标准状况下密度为1.25g/L ,略小于空气。
其分子式为C 2H 4,结构简式为CH 2=CH 2,是一种平面型分子,是非极性分子,易溶于 有机溶剂。
化学性质:①氧化反应a. 乙烯在空气中燃烧火焰呈淡蓝色,并伴有黑烟。
原因是乙烯分子中含碳量较高。
方程式为:C 2H 4+3O 2→2CO 2+2H 2Ob. 乙烯通入紫色的酸性高锰酸钾溶液,可使其退色。
说明乙烯可被高锰酸钾氧化。
它的化学性质活泼,可利用此反应区别甲烷和乙烯,但不能除去甲烷中混有的乙烯。
原因是:乙烯被酸性高锰酸钾氧化最终生成二氧化碳和水,生成新的杂质。
②加成反应定义:有机物分子中不饱和的碳原子与其他原子或原子团直接结合生成新物质的反应称为加成反应。
7.3一些重要的烃类和石油化工
一、教学目标:
知识与技能:
1.掌握乙烯的分子组成、结构和化学性质,进一步掌握结构与性质的关系。
2.认识乙烯的性质,(燃烧、能被酸性高锰酸钾溶液氧化、能与溴的四氯化碳溶液发生加成反应,并能写出相应的化学方程式。
过程与方法:
1.从生活实际出发,认识乙烯在化工生产中的作用,激发学生的兴趣。
2.展示分子结构模型增加感性认识,强化理论与实际的联系。
情感态度与价值观:
1.通过乙烯的学习,养成良好的思考、分析问题的方法,加强“结构与性质”的认识。
2.通过乙烯应用的学习,激发学生兴趣,积极投身于科学研究。
二、重点难点
教学重点:乙烯的结构与性质的关系
教学难点:从结构上认识乙烯的加成反应
二、教学方法
实验探究、设疑启发、对比归纳等。
三、教具
多媒体、石蜡油、试管、水槽、碎瓷片、石棉网、酒精灯、铁架台、酸性KMnO4溶液、溴水四、教学过程
教学过程设计
校正学生的正误,
还能被听讲、理解并书写有关化学反应方程式
听讲、做笔记
五、板书设计
2.1 乙烯
一、乙烯的结构特征
分子式C
2H
4
电子式:
结构式:结构简式:CH
2=CH
2
二、物理性质
三、化学性质
1、乙烯的氧化反应
(1)乙烯的燃烧
(2)乙烯能使酸性高锰酸钾褪色2、乙烯的加成反应
3、聚合反应(课后练习)。