茶叶中茶多酚的提取与含量测定方案(精选.)
- 格式:doc
- 大小:32.50 KB
- 文档页数:5


茶叶中茶多酚含量测定工作方案一、 紫外分光光度法1. 实验原理在一定PH 条件下,酒石酸铁能与多酚类物质反应形成蓝紫色络合物,该络合物在540nm 波长下具有最大吸光度。
用分光光度法测定其含量2. 仪器试剂A. 酒石酸亚铁溶液:称取1.0g 硫酸亚铁(O H FeSO 247•)和5.0 g 酒石酸钾钠(OH KNa O H C 2614144•),用水溶解并定容至1L (低温保存有效期10天)。
B. PH=7.5 磷酸盐缓冲液1/15mol/L 磷酸氢二钠:称取23.9 g 十二水磷酸氢二钠(O H HPO Na 24212•),加水溶解后定容至IL 。
1/15 mol/L 磷酸二氢钾:称取经110℃烘干2h 的磷酸二氢钾(42PO KH )9.08 g,加水溶解后定容至1L 。
取上述 1/15mol/L 的磷酸氢二钠溶液85mL 和1/15mol/L 的磷酸二氢钾溶液15mL 混合均匀。
3. 工作步骤1) 试样的制备与测定:称取磨碎茶叶试样0.1g(准确至0.0001g) ,置于小烧杯中,加温水30mL ,溶解冷却,注入100mL 容量瓶中,定容、摇匀、过滤,弃去初滤液约20mL ,剩余的滤液为试液【1】。
取试液【1】 2mL于50mL比色管中,加酒石酸铁10mL摇匀,用PH=7.5的磷酸盐缓冲液定容。
取2mL蒸馏水于50mL比色管中,加酒石酸铁10mL摇匀,用PH=7.5的磷酸盐缓冲液定容作为空白对照,于540nm处用1cm比色皿测定吸光度值。
2)标准系列溶液的配制与测定:称取茶多酚纯品0.2500g,加水溶解定容至250mL,混匀,即为每毫升含1mg 茶多酚的标准溶液。
分别称取标准溶液0.0mL、1.0mL、2.0mL、3.0mL、4.0mL于一组50mL比色管中,各加水至10mL,再加酒石酸铁溶液10mL,用PH=7.5的缓冲液定容至刻度,混匀后用1cm比色皿,以试剂空白作参比,于波长540nm处测定吸光度,绘制出标准曲线。

本标准适用于茶叶中茶多酚含量的测定。
在茶叶水浸出物中与亚铁离子产生络合反应的酚性化合物,均称茶多酚。
1 原理茶叶中多酚类物质能与亚铁离子形成紫蓝色络合物。
用分光光度法测定其含量。
2 仪器和用具实验室常规仪器及下列各项:2.1 分析天平:感量0.0001g。
2.2 分光光度仪。
3 试剂和溶液所用试剂应为分析纯(AR),水为蒸馏水。
3.1 酒石酸亚铁溶液:称取1g (准确至0.0001g) 硫酸亚铁(GB 664-77)和5g (准确至0.0001g)酒石酸钾钠(GB 1288-81),用水溶解并定容至1L(溶液应避光,低温保存,有效期一个月)。
3.2 pH7.5磷酸盐缓冲液:3.2.1 1/15M磷酸氢钠: 称取23.377g磷酸氢二钠(GB 1263-77),加水溶解后定容至1L。
3.2.2 1/15M磷酸二氢钾: 称取9.078g磷酸二氢钾(GB 1274-77),加水溶解后定容至1L。
取上述1/15M的磷酸氢二钾溶液85ml和1/15m的磷酸二氢钾溶液15ml混合均匀。
4 操作方法4.1 取样按GB 8302-87《茶取样》的规定取样。
4.2 试样的制备按GB 8303-87《茶磨碎试样的制备及其干物质含量测定》的规定,制备试样。
4.3 测定步骤4.3.1 试液的制备按GB 8305-87《茶水浸出物测定》中3.4.1的规定,制备试液。
4.3.2 测定准确吸取上述(4.3.1)试液1mL,注入25mL的容量瓶中,加水4mL和酒石酸亚铁溶液(3.1)5mL,充分混合,再加pH7.5的缓冲液(3.2)至刻度,用10mm比色杯,在波长540nm处,以试剂空白溶液作参比,测定吸光度(A)。
5 结果计算5.1 计算方法和公式茶叶中茶多酚的含量,以干态质量百分率表示,按下式计算:A×1.957×2 L1茶多酚(%)=──────×─────×100100 L2×M×m式中: L1——试液的总量,mL;L2——测定时的用液量,mL;M——试样的质量,g;m——试样干物质含量百分率,%;A——试样的吸光度;1.957——用10mm比色杯,当吸光度等于0.50时,每毫升茶汤中含茶多酚相当于1.957mg。

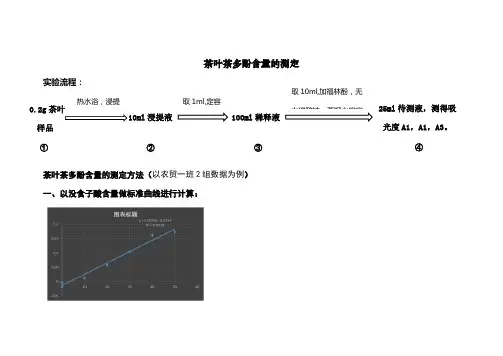
茶叶茶多酚含量的测定茶叶茶多酚含量的测定方法(以农贸一班2组数据为例)一、以没食子酸含量做标准曲线进行计算:上图中的横坐标为每25ml没食子酸标准液中没食子酸的含量,纵坐标为吸光度值。
样品待测液含量对应关系:25ml待测液中茶多酚含量=10ml1/10=0.2g茶叶中茶多酚总含量的1/100。
由对应关系进行公式推导:茶叶样品中茶多酚含量(%)=浸提液中茶多酚的含量/(样品质量*干物质含量)浸提液中茶多酚的含量=1ml中茶多酚含量*10ml=10ml稀释液中茶多酚的含量*10*10ml=25ml待测液中茶多酚的含量*10*10ml茶多酚含量(%)=A*V*d/(L*m*m1*(10^6)),稀释因子d应该为10。
同时由于:A=K*X+b,所以此公式应该调整为:茶多酚含量(%)=[(A-b)*V*d/(L*m*m1*(10^6))]*100A----待测液平均吸光度b----标准曲线公式中的常量,本实验为-0.0134V----浸提液体积本实验为10mld----稀释因子,在以没食子酸含量为横坐标的计算方法中,d=10L----标准曲线斜率m----样品质量,本实验为0.2m1----样品干物质含量,本实验为80%详细过程如下:A1=0.885 A2=0.822 A3=0.784平均光度值A=(A1+A2+A3)/3=0.830将A值带入公式:茶多酚含量(%)= [( A-b)*V*d/(L*m*m1*(10^6))]*100,可以求得茶叶样品中茶多酚的含量=13.5%二、以没食子酸浓度作标准曲线上图中的横坐标为没食子酸标准溶液的浓度,纵坐标吸光度A此时的计算公式推导过程为:茶叶样品中茶多酚含量(%)=0.2g茶叶中茶多酚含量/(0.2*干物质含量)0.2g茶叶中茶多酚的含量为=浸提液浓度*10浸提液浓度=10ml稀释液浓度*10010ml稀释液浓度=25ml待测液浓度*25ml/10ml25ml待测液浓度可以由标准曲线公式:A=L*X+b测得。

茶叶中茶多酚的检测一、原理:茶叶磨碎样中的茶多酚用70%的甲醇在70℃的水浴中提取,福林酚试剂氧化茶多酚中-OH基团并显蓝色,最大吸光度波长λ为765nm,用没食子酸做矫正标准定量茶多酚。
二、仪器分析天平:感量0.001g;水浴:70℃±1℃;离心机:转速3500r/min分光光度计三、试剂本标准所用水均为重蒸馏水,除特殊规定外,所用试剂为分析纯。
1、甲醇2、碳酸钠3、甲醇水溶液(体积比):7+34、福林酚试剂:试剂甲(①4%碳酸钠溶液;②0.2NNAOH溶液;③1%硫酸铜溶液;④2%酒石酸钾钠;(1)将试剂①和②等体积混合;(2)将试剂③和④等体积混合;(3)将(1)和(2)混合溶液按50:1比例混合。
)试剂乙(取10ml1%的乙液于100ml的容量瓶,加水定容)。
(4)将试剂甲和试剂乙按1:1的比例现配成福林酚。
5、将(4)中的福林酚20ml转移到200ml容量瓶中,用水定容并摇匀。
6、7.5%碳酸钠(质量浓度):称取37.50g±0.01g碳酸钠,加适量水溶解,转移至500ml容量瓶中,定容至刻度,摇匀。
7、没食子酸标准储备溶液(1000μg/ml):称取0.110g±0.001g没食子酸(GA,相对分子质量188.14),于100ml容量瓶中溶解并定容至刻度,摇匀(现配)。
8、没食子酸工作液:用转移管分别移取1.0,2.0,3.0,4.0,5.0ml的没食子酸标准储备液溶液于100ml容量瓶中,分别用水定容至刻度,摇匀,浓度分别为10,20,30,40,50μg/ml。
四、操作方法1、供试液的制备母液的制备:称取0.2g(精确到0.0001g,本次实验0.2331g)均匀磨碎的式样于10ml的离心管中,加入在70℃中预热过的70%的甲醇溶液ml,用玻璃棒充分均匀湿润,立即移入70℃水浴中。
浸提10min(隔5min搅拌一次),浸提后冷却至室温,转入离心机在3500r/min转速下离心10min,将上清液转移至10ml容量瓶。

茶多酚的提取及测定实验报告一、实验目的茶多酚是茶叶中多酚类物质的总称,包括黄烷醇类、花色苷类、黄酮类、黄酮醇类和酚酸类等,具有抗氧化、清除自由基、抗菌、抗病毒、降血脂、降血压等多种生理活性和药理作用。
本实验的目的是掌握茶多酚的提取和测定方法,了解茶多酚的性质和应用。
二、实验原理茶多酚易溶于水、乙醇、甲醇、丙酮等有机溶剂,可采用溶剂萃取法进行提取。
常用的提取溶剂有乙醇、乙酸乙酯等。
在酸性条件下,茶多酚与金属离子(如铝离子)形成稳定的络合物,可通过分光光度法进行测定。
三、实验材料与仪器1、实验材料新鲜绿茶(或市售茶叶)2、实验试剂乙醇(95%)、乙酸乙酯、酒石酸亚铁溶液、磷酸缓冲液(pH =75)、蒸馏水3、实验仪器电子天平、恒温水浴锅、旋转蒸发仪、分光光度计、离心机、移液器、容量瓶(100 mL、500 mL)、具塞锥形瓶、移液管、漏斗、滤纸四、实验步骤1、茶多酚的提取(1)称取 10 g 茶叶粉末,放入具塞锥形瓶中,加入 100 mL 70%的乙醇溶液,在70℃恒温水浴锅中浸提1 h,期间每隔15 min 搅拌一次。
(2)提取结束后,冷却至室温,然后用离心机以 4000 r/min 的转速离心 15 min,收集上清液。
(3)将上清液转移至旋转蒸发仪中,在 50℃下减压浓缩至无乙醇味,得到茶多酚粗提液。
2、茶多酚的纯化(1)将茶多酚粗提液用乙酸乙酯进行萃取,萃取次数为 3 次,每次用量为 50 mL。
(2)合并乙酸乙酯萃取液,用蒸馏水洗涤 2 次,每次用量为 50 mL。
(3)将洗涤后的乙酸乙酯萃取液转移至旋转蒸发仪中,在 50℃下减压浓缩至干,得到茶多酚纯品。
3、茶多酚的测定(1)标准曲线的绘制准确称取 01000 g 没食子酸标准品,用蒸馏水溶解并定容至 100 mL,得到 1000 mg/mL 的没食子酸标准储备液。
分别吸取 000 mL、100 mL、200 mL、300 mL、400 mL、500 mL 没食子酸标准储备液于 100 mL 容量瓶中,加入蒸馏水至 50 mL,然后加入 5 mL 酒石酸亚铁溶液和 5mL 磷酸缓冲液(pH = 75),用蒸馏水定容至刻度,摇匀。

绿茶中茶多酚的提取与含量的测定一、摘要茶叶是中华民族传统的保健饮品,茶多酚上茶叶只能感最重要的保健活性成分,其含量与茶业质量有密切关系。
茶多酚是茶叶中三十多种多酚类物质的总称,包括儿茶素、黄酮类、花青素和酚酸等四大类物质。
茶多酚的含量占干物质总量的20%~35%。
而在茶多酚总量中,儿茶素约占70%,它是决定茶叶色、香、味的重要成分。
现代茶叶药理学研究表明,茶多酚对防衰延寿、减少抗癌药物的毒副作用有良好的效果。
此外茶多酚还可去脂减肥,降胆固醇,防止动脉粥样硬化,抗血凝等抵抗心血管系统疾病的作用。
本实验旨在对今后人们科学认识茶与科学饮茶起一定指导作用。
关键词:茶多酚、儿茶素、保健饮品、防衰延寿、去脂减肥。
二、正文1、前言:众所周知茶叶是良好的保健饮品,但是那种成分在起作用却不为众人所知或者知之甚少。
本实验通过对对茶叶的提取与含量测定,可使我在校大学生了解茶多酚和儿茶素的保健活性,加深对绿茶的保健作用的认识,更好的了解绿茶的保健作用。
2、实验目的a、学习用酒石酸亚铁显色法测定茶多酚含量的原理和方法b、掌握分光光度计的使用方法和过滤等实验操作的方法c、通过实验测定了解茶叶中多酚类物质的含量3、实验原理a、多酚类物质包括花青苷、黄酮苷、单宁等,具体又可分为若干种。
多酚类物质含有酚羟基,有的还含有羧基,属于极性有机化合物,常用极性溶剂提取,如甲醇、乙醇、乙酸乙酯、丙酮、水以及由这些溶剂按比例组成的复合溶剂。
b、本实验茶多酚总量的测定方法为较为简单实用的酒石酸亚铁分光光度比色法。
酒石酸亚铁分光光度比色法原理:过量的酒石酸亚铁与提取液中多酚反应生成稳定的紫褐色络合物,溶液颜色的深浅与溶液中多酚含量成正比。
本实验以儿茶素做标准物质测定绿茶中茶多酚含量。
4、实验设备:水浴锅,分光光度计,锥形瓶,容量瓶(3只1000ml、7个50ml),吸管,漏斗,烧杯四个(2个100ml、2个500ml),电子天平,容量瓶,铁架台,滤纸,玻璃棒,5ml 管两只5、实验材料及试剂a、实验材料:茶叶,儿茶素b、试剂的配制:(1)酒石酸亚铁溶液:称取1.00g硫酸亚铁(FeSO4·7H2O)和5.00g酒石酸钾钠(C4H4O6NaK·4H2O),混合后加蒸馏水溶解,定容到1000mL;(2)pH 7.5磷酸盐缓冲液:称取60.20g Na2HPO4·12H2O和5.00g NaH2PO4·12H2O,混合后加蒸馏水溶解,定容到1000mL。

茶叶中茶多酚的提取和测定一,主要仪器、药品及材料仪器: 722 - E可见分光光度计,干燥箱, 电子天平, pH计, 容量瓶, 真空泵, 布氏漏斗。
化学试剂:无水硫酸钠,硫酸亚铁( FeSO4 ·7H2O) ,酒石酸钾(KNaC4H4O6 ·4H2O) ,磷酸氢二钠(Na2HPO4 ·12H2O),磷酸二氢钾(KH2 PO4 ) ,乙酸乙酯。
材料:茶叶二,茶多酚的提取工艺。
采集茶叶→去灰尘,洗干净→晾干→干茶叶→粉碎→90℃接近沸水中搅拌浸提→过滤→乙酸乙酯萃取→得有机相→无水硫酸钠干燥→减压蒸馏→得黄色粉末状茶多酚→称量。
1 预处理。
粉碎干茶叶:将采集来的茶叶洗净、晾干,烘干,最后粉碎。
粉碎的目的是与液体的接触面增大,使提取率增高。
由于试验条件的限制,用剪刀代替粉碎机,将干茶叶剪碎,并且用研钵研细。
干茶叶量为50. 00g。
2 提取。
在众多的提取方法中,选用了溶剂提取法,具体过程是称取经过预处理的干茶叶末30. 00g,加250mL 90℃接近沸水中搅拌浸提,过滤,先后用250mL 的乙酸乙酯萃取两次。
合并两次有机相,再用无水硫酸钠干燥,减压蒸馏除去乙酸乙酯溶剂得黄色粉末状茶多酚。
称量为0. 2945g,提取率为0. 98%。
三,测定1 定性测定。
从外观上看,为黄色粉末状。
物理性能为,易溶于水及乙醇,味苦涩。
2 定量测定方法。
光度法———酒石酸亚铁比色法。
其测定原理是茶多酚类物质能与亚铁离子形成紫蓝色络合物。
用分光光度法测定其含量。
3 茶多酚标准溶液的配制。
称取纯品0.2500g,加水溶解定容至250mL,混匀,即为每毫升含1mg纯品的标准溶液(mg/mL) 。
4 茶多酚的含量。
茶多酚标准曲线的绘制。
分别吸取茶多酚标准溶1.0mL、2. 0mL、3. 0mL、4. 0mL 于4 个50mL 容量瓶中,各加水至10mL,再加酒石酸亚铁10mL,加入pH为7. 5的磷酸缓冲液至刻度,混匀后用1㎝比色皿,以空白试剂作参比,于540nm处测定吸光度(A) ,绘制出标准曲线表1茶多酚标准曲线y = 321. 16x + 0. 003R2 = 1。

设计性实验茶叶中茶多酚的提取与含量测定实验方案新疆农业大学食品科学与药学学院班级:葡工162班姓名:王勇峰学号:220162712指导老师:阿不都热依木茶叶中茶多酚的提取与含量测定一.实验目的及要求1.用无害溶剂从茶叶中提取茶多酚。
2.分离、纯化茶多酚粗品,掌握溶剂提取法提取茶多酚的原理及方法。
3.定量分析茶多酚产品含量。
二.实验原理有机溶剂萃取法:有机溶剂萃取法是传统的提取工艺。
是利用茶叶中不同化合物在不同溶剂中的溶解度不同进行提取分离。
在粗茶叶萃取溶液中,除含有茶多酚以外,还含有咖啡碱、酯质、色素、植物多糖、有机酸、以及悬浮物,且茶多酚含量仅为25%~40% ,所以大多数工艺用乙酸乙酯、氯仿等有机溶剂反复萃取的方法进一步除杂、纯化、精制。
茶水用氯仿萃取可得到水层和有机层,咖啡碱存在于有机层,而茶多酚则存在于水层中,根据萃取及过滤原理,将有机层和水层分别进行浓缩、萃取,即可得到相应粗产物。
三.实验仪器及药品仪器:天平;分析天平;铁架台;抽滤装置;超级恒温水浴槽;长颈漏斗一个;滤纸若干张;分液漏斗一个;100毫升的烧杯(三个);玻璃棒一个;药品:1.乙醇水溶液(50%);2.干茶叶原料;3.氯仿(分析纯);4.Na2SO4溶液馏水四.实验步骤1、温度设定:打开超级恒温水浴电源开关,使温度达到90℃2、称量:称取30克干茶叶,放在100毫升小烧杯中。
3、溶解:用量筒量取40毫升50%乙醇水溶液,倒入小烧杯中,用玻璃棒轻轻搅拌,使干茶叶完全浸润在乙醇溶液中。
4、加热:将干茶叶和乙醇水溶液的混合液置于超级恒温水浴槽中,加热20分钟。
5、过滤:将加热完毕的混合液取出,冷却到室温;用长颈漏斗对混合液进行过滤,滤除茶叶残渣。
再对残渣进行乙醇萃取.6、分离萃取:1)对分液漏斗进行试漏,调整好铁架台高度;2)用量筒量取20毫升氯仿①,置于100毫升小烧杯中;将茶叶滤液倒入分液漏斗中,再将氯仿倒入其中,再倒入少量Na2So4溶液②,轻轻摇匀,使之混合充分,静置,分层,上层应为茶多酚水溶液,呈茶色,下层为氯仿乙醇混合液,为无色。

茶叶中茶多酚的提取工艺及其含量测定一、本文概述本文旨在探讨茶叶中茶多酚的提取工艺及其含量测定方法。
茶多酚是茶叶中的重要成分,具有抗氧化、抗炎、抗癌等多种生物活性,对人体健康具有显著的益处。
因此,研究茶叶中茶多酚的提取工艺和含量测定方法,对于茶叶的品质控制、新产品开发以及茶产业的可持续发展具有重要意义。
本文将首先介绍茶多酚的基本性质及其在茶叶中的分布情况,为后续提取工艺和含量测定方法的研究提供理论基础。
接着,将详细阐述茶多酚的提取工艺,包括提取原料的选择、提取溶剂的选用、提取条件的优化等方面,以期获得高效、环保、经济的提取方法。
在此基础上,本文还将探讨茶多酚的含量测定方法,包括紫外可见光谱法、高效液相色谱法、气相色谱法等常用的分析方法,并对各种方法的优缺点进行比较和评价。
通过本文的研究,旨在为茶叶加工企业、科研机构以及广大茶叶爱好者提供一套科学、实用的茶多酚提取工艺和含量测定方法,为茶叶的品质控制和新产品开发提供技术支持,推动茶产业的健康发展。
二、茶多酚的提取工艺茶多酚(Tea Polyphenols)是茶叶中的重要活性成分,具有多种生物活性,如抗氧化、抗炎、抗癌等。
因此,提取茶多酚的工艺研究对于茶叶深加工和茶多酚的开发利用具有重要意义。
选择品质优良、无污染的茶叶作为提取原料。
通常,绿茶中茶多酚的含量较高,因此绿茶是提取茶多酚的首选。
将选好的茶叶进行粉碎处理,以提高后续提取过程中的传质效率。
茶多酚的提取通常采用有机溶剂提取法,常用的溶剂有乙醇、丙酮、甲醇等。
其中,乙醇因其毒性低、安全性高、提取效果好而被广泛应用。
乙醇的浓度、温度以及提取时间等因素都会影响茶多酚的提取效果。
常用的茶多酚提取方法包括浸提法、回流提取法、超声提取法等。
其中,回流提取法因其提取效率高、操作简便而被广泛应用。
回流提取法是将茶叶粉末与乙醇混合后,在加热条件下进行回流提取,使茶多酚充分溶解在乙醇中。
提取液经过浓缩后,可采用大孔树脂吸附法、柱层析法等方法进行纯化,以去除杂质,提高茶多酚的纯度。
茶叶中茶多酚的萃取和检测及应用一、茶多酚的萃取方法茶多酚是茶叶中的主要活性成分,具有多种生物活性,如抗氧化、抗炎、抗癌等作用。
因此,茶多酚的萃取方法对于茶叶的加工和利用具有重要意义。
1. 水煮法:将茶叶放入开水中煮沸,茶多酚会溶于水中。
这种方法简单易行,适用于家庭茶叶的制备,但茶多酚的得率较低。
2. 乙醇萃取法:将茶叶与乙醇混合浸泡,茶多酚会溶于乙醇中。
乙醇萃取法能够提取茶叶中的茶多酚,并且得率较高。
3. 超临界流体萃取法:利用超临界流体(如二氧化碳)的高温高压性质,将茶叶中的茶多酚提取出来。
这种方法能够提取茶叶中的茶多酚,并且不会破坏茶多酚的活性。
二、茶多酚的检测方法茶多酚的检测方法主要包括色谱法、光谱法和电化学法等。
1. 色谱法:色谱法是目前茶多酚检测的常用方法之一。
其中,高效液相色谱法(HPLC)是最常用的分析技术,它能够快速、准确地测定茶多酚的含量。
2. 光谱法:光谱法包括紫外-可见光谱法和红外光谱法等。
紫外-可见光谱法通过测量茶多酚在紫外-可见光区域的吸光度来确定其含量。
红外光谱法则通过测量茶多酚在红外区域的吸收特征来进行分析。
3. 电化学法:电化学法利用电化学技术对茶多酚进行检测,如循环伏安法、方波伏安法等。
这些方法具有灵敏度高、操作简单等优点。
三、茶多酚的应用茶多酚在食品、医药和化妆品等领域具有广泛的应用价值。
1. 食品领域:茶多酚可以作为天然的食品添加剂,具有抗氧化、抗菌、抗癌等功能。
茶多酚可以用于保鲜剂、防腐剂、色素等方面,提高食品的质量和保健功能。
2. 医药领域:茶多酚具有抗氧化、抗炎、抗癌等多种生物活性,可以用于疾病的预防和治疗。
茶多酚可以制成口服药物、注射剂、外用药膏等形式,用于心血管疾病、肿瘤等疾病的治疗。
3. 化妆品领域:茶多酚具有抗氧化、抗衰老等功效,可以用于化妆品的制备。
茶多酚可以用于面霜、面膜、洗发水等产品中,具有保湿、抗皱、美白等作用。
总结:茶多酚是茶叶中的重要活性成分,具有多种生物活性。
茶叶中茶多酚类物质提取与含量测定系别:牛物医药工稈系班级:食品科学与工程一、目的要求1、了解茶叶中茶多酚及茶多酚的组成及性状;2、掌握溶剂提取法提取茶多酚的原理及方法;3、掌握萃取法分离有机溶剂中的茶多酚的操作方法;二、茶多酚总述1、组成:茶多酚是茶叶中酚类及其衍生物的总称,因此常称为多酚类。
其主要成分是黄烷醇类、羟基-4-黄烷醇类、花色甘类、黄酮醇类和黄酮类。
这些化合物都具有2-苯基苯并吡喃的基本结构,故统称为类黄酮物质。
茶叶中绿原酸、鸡鈉酸、咖啡酸等酚酸类化合物也是茶多酚的组分之一。
在茶多酚各组分之一黄烷醇类为主,黄烷醇类优异儿茶素类物质为主。
2、性状:茶多酚是介于淡黄色至茶褐色之间的无定型粉末,味涩,略有吸湿性,易溶于水,可溶于乙醇、甲醇、乙醚、丙酮、乙酸乙酯,微溶于油脂,不溶于氯仿及苯等有机溶剂。
茶多酚具有较好的耐酸性,在pH<7时较稳定,在pH>7时则不稳定且氧化变色加快,呈红色。
3.茶多酚的提取方法茶多酚提取工艺效果较好的是有机溶剂萃取法、离子沉淀提取法、树脂吸附分离法、超临界二氧化碳萃取法,其次是超声波浸提法、层析法、膜技术。
4.贮存方法:贮存于阴凉通风干燥环境,并与有毒、有气味的物品隔离,避免直接与三价铁离子及碱性物质接触。
三、实验原理有机溶剂萃取法:有机溶剂萃取法是传统的提取工艺。
是利用茶叶中不同化合物在不同溶剂中的溶解度不同进行提取分离。
在粗茶叶萃取溶液中,除含有茶多酚以外,还含有咖啡碱、酯质、色素、植物多糖、有机酸、以及悬浮物,且茶多酚含量仅为25%- 40%,所以大多数工艺用乙酸乙酯、氯仿等有机溶剂反复萃取的方法进一步除杂、纯化、精制。
茶水用氯仿萃取可得到水层和有机层,咖啡碱存在于有机层,而茶多酚则存在于水层中,根据萃取及过滤原理,将有机层和水层分别进行浓缩、萃取,即可得到相应粗产物。
溶剂萃取法一般的工艺路线图所示溶剂萃取法一般的工艺路线本法的优点是:稳定、可靠;缺点是:有效成分的含量和提取 率较低,通过以上工艺获得的茶多酚含量通常仅能达到 50%- 65%四、 仪器和药品仪器:天平;分析天平;铁架台;抽滤装置;超级恒温水浴槽; 长颈漏斗一个;滤纸若干张;分液漏斗一个;100毫升的烧杯(三个); 玻璃棒一个;药品:1. 乙醇水溶液(50%);2. 干茶叶原料;3. 氯仿(分析纯);4. Na2So4溶液馏水,五、 实验步骤1、 温度设定:打开超级恒温水浴电源开关,使温度达到 90 °CI 茶叶 I —— | |乙醇2、称量:称取30克干茶叶,放在100毫升小烧杯中。
;.' 茶叶中茶多酚的含量测定1、实验目的:掌握实验操作的趣味性,了解实验内容在实际生活中的应用,充分理解和掌握茶多酚含量在现实生活中的作用,进一步熟悉茶叶中茶多酚测定的原理及操作。
2、实验原理:茶叶中多酚类物质能与亚铁离子形成紫蓝色络合物。
用分光光度法测定其含量。
3、仪器和用具:分析天平(感量0.0001g). 分光光度仪及实验常用仪器4、试剂和溶液:所用试剂应为分析纯(AR),水为蒸馏水。
在茶叶水浸出物中与亚铁离子产生络合反应的酚性化合物,均称茶多酚。
5、操作方法:秤取5g茶叶加入100mL水煮沸,静止冷却20分钟,加压过滤,量取滤液体积记为V1 酒石酸亚铁溶液:称取1g (准确至0.0001g) 硫酸亚铁和5g (准确至0.0001g)酒石酸钾钠,用水溶解并定容至1L(溶液应避光,低温保存,有效期一个月)。
6、pH7.5磷酸盐缓冲液:磷酸氢钠: 称取23.377g磷酸氢二钠,加水溶解后定容至1L。
磷酸二氢钾:称取9.078g磷酸二氢钾,加水溶解后定容至1L。
取上述磷酸氢二钾溶液85ml和磷酸二氢钾溶液15ml混合均匀。
7、准确称取上述试液1mL ,注入25mL容量瓶中加水4mL和酒石酸亚铁溶液5ml 充分混合,再加入pH=7.5的缓冲溶液至刻度,用10mm比色皿,在波长等于540nm 出,以试液空白溶液做参比溶液,测定吸光度为A.8、茶叶中茶多酚的含量,以干态质量百分率表现,按下式计算:A×1.957×2 V1茶多酚(%)=────────× --------- ×100 结果=1000 1×m式中——滤液体积记为V1 mLm——试样的质量,g;A——试样的吸光度;此次实验测定A=1.957——用10mm比色杯,当吸光度等于0.50时,每毫升茶汤中含茶多酚相当于1.957mg。
注意:a. 应取两次测定的算术平均值作为标准。
同一样品的两次测定值之差,每100g试样不得超过0.5g。
(n=6),方法的灵敏度和准确度均满足实际样品检测的需要。
参考文献:[1]吕刚,王利兵,刘军,等.包装材料中的份类环境雌激素的测定-固相萃取/气相色谱质谱法[J].分析实验室,2008,27(9):73-75[2]卫碧文,缪俊文,于文佳.气相色谱-质谱法分析食品包装材料中双酚A [J].分析实验室,2009,28(1):107-109[3]雅韵,徐晓云,谢孟峡,等.动物组织中己烯雌酚残留的基体固相扩散-气相色谱-质谱分析方法研究[J].分析化学,2003,31(11):1356-1359[4]卫碧文,缪俊文,于文佳.气相色谱-质谱法分析食品包装材料中双酚A [J].分析实验室,2009,28(1):107-109[5]周建科,张前莉,韩康,等.中老年奶粉中双酚A 和乙烯雌酚的反相高效液相色谱测定[J].食品工业科技,2007,28(2):233-234[6]刘宏程,邹艳红,黎其万,等.高效液相色谱分离牛奶中己烯雌酚、己烷雌酚和双烯雌酚[J].分析化学,2008,36(2):245-248[7]彭青枝,潘思轶,刘松.高效液相色谱法测定罐装食品中双酚A [J].中国卫生检验杂志,2010,20(10):2415-2416[8]王瑶,周建华,张鸿雁,等.食品中己烯雌酚的检测方法[J].食品工业科技,2012,33(2):373-375[9]丁红春,李建林,徐逸云,等.婴幼儿奶瓶中迁移双酚A 的高效液相色谱-电喷雾串联质谱检测方法研究[J].化学分析计量,2010,19(5):42-45[10]岳强,于志强,王德超,等.人体尿液中双酚A 与壬基酚的同位素稀释的LC -MS/M 分析[J].分析测试学报,2009,28(7):859-862[11]杜志峰,黄金凤,郭新东,等.动物肌肉组织中己烯雌酚残留量的液相色谱-串联质谱法测定[J].分析测试学报,2007,26(6):823-826[12]闫小峰,孙志文.超高效液相色谱-串联质谱法测定饲料中的己烯雌酚[J].饲料广角,2010(11):38-40收稿日期:2012-12-23茶叶中茶多酚提取及含量测定的研究浦周芳,韩丽琴,曹宏梅(吉林医药学院,吉林吉林132013)摘要:探讨茶多酚的提取条件。
茶叶中多酚类物质的含量测定与分析茶叶是一种广泛被消费的饮品,其独特的香气和味道深受人们喜爱。
而茶叶中多酚类物质的含量则是决定茶叶品质和保健功效的重要指标之一。
本文将介绍茶叶中多酚类物质的测定方法和分析结果。
一、茶叶多酚类物质简介1. 茶叶多酚类物质的种类茶叶中的多酚类物质主要包括儿茶素、黄酮类化合物以及茶多酚等。
其中,儿茶素是茶叶中最主要的成分,占据了茶叶多酚总量的约80%。
儿茶素又可分为儿茶素单体和儿茶素聚合物,其含量和比例会对茶叶的品质和风味产生重要影响。
2. 茶叶多酚类物质的健康功效茶叶中的多酚类物质具有多种保健功效,包括抗氧化、抗炎、降压、降血脂等。
其中,儿茶素作为一种有效的天然抗氧化剂,被广泛研究和应用于预防心脑血管疾病、抗癌等领域。
二、茶叶中多酚类物质的含量测定方法1. Folin-Ciocalteu法Folin-Ciocalteu法是一种经典的多酚类物质总量测定方法。
该方法基于多酚类物质与Folin-Ciocalteu试剂反应生成的蓝色化合物的光吸收特性。
通过比较未知样品的吸光度与已知标准物质的吸光度,可以计算出茶叶中多酚类物质的含量。
2. 高效液相色谱法(HPLC)HPLC是一种精确和高效的多酚类物质测定方法。
该方法通过将茶叶样品经过提取和净化处理后,利用高效液相色谱仪分离多酚类物质,并通过标准曲线计算出茶叶中多酚类物质的含量。
HPLC具有分离效果好、准确度高和灵敏度高的优点。
三、茶叶多酚类物质的分析结果通过上述测定方法,我们可以得到茶叶中多酚类物质的含量结果。
以绿茶为例,其多酚类物质含量一般在10%~30%之间,其中儿茶素单体的含量较高,茶多酚和黄酮类化合物的含量相对较低。
而红茶多酚类物质的含量较绿茶更低,一般在5%~10%之间。
根据茶叶多酚类物质的含量结果,可以对茶叶品质进行初步评估。
高含量的多酚类物质通常意味着茶叶的品质较好,并且具有更多的保健功效。
当然,茶叶的品种、产地、加工工艺等因素也会对多酚类物质的含量产生影响,因此在分析结果时需要综合考虑。
实验三 茶叶中茶多酚含量的测定一、实验目的:1、了解茶叶品质的检测与鉴定方法2、学习茶叶中茶多酚含量的测定方法二、实验原理茶叶磨碎样中的茶多酚用70%的甲醇在70°C 的水浴上提取,福林酚试剂氧化茶多酚中-OH 其团并显蓝色,最大吸收波长为765 nm ,用没食子酸作校正标准定量茶多酚。
三、实验材料1、供试样品 普洱茶、绿茶、白茶。
2、主要试剂 甲醇,无水碳酸钠,福林酚,没食子酸,蒸馏水。
3、仪器设备 恒温水浴锅;电子天平;离心机;分光光度计四、实验方法1、准确称取0.2 g 已磨碎试样,置10 ml 离心管中,加入5 ml 70%甲醇,放入水浴锅(70°C )中,浸提10 min ,冷却后,于4000 r/min 转速下离心10 min ,转移上清液至10 ml 离心管中。
2、待测液:取浸提液1 ml 定容至100 mL ,备测。
以表1浓度测定没食子酸标准液系列的吸光度,以其为纵坐标,浓度为横坐标绘制没食子酸的标准曲线。
表1 没食子酸标准曲线浓度管号 1 2 3 4 5 610 µg/mL 没食子酸标准液 0.0 1.0 2.0 3.0 4.0 5.0 标准没食子酸含量µg 0 10 20 30 40 50 吸光度(A )取待测液10 ml ,分别置于25 ml 带塞比色管中,各加入5.0 ml R 10%福林酚试剂,揺匀,反应3~8 min ,加入4.0 ml 7.5%无水碳酸钠溶液加水定容至刻度,摇匀,放置60 min 后于波长765 nm 处测定吸光度A ,以吸光度为纵坐标,没食子酸含量(µg )为横坐标,制得标准曲线。
五、结果与分析按以下公式计算茶多酚含量:100m 10m L d V A )%(16⨯⨯⨯⨯⨯⨯=茶多酚含式中:A ——样品测试吸光度;V ——样品提取液体积(10 mL );d ——稀释因子(1 mL 稀释成100 mL ,稀释因子为100);L ——没食子酸标准曲线的斜率;m——样品干物质含量(%);m1——样品质量,单位为克(g )。
设计性实验
茶叶中茶多酚的提取与含量测定
实验方案
新疆农业大学食品科学与药学学院
班级:葡工162班
姓名:王勇峰
学号:220162712
指导老师:阿不都热依木
茶叶中茶多酚的提取与含量测定
一.实验目的及要求
1.用无害溶剂从茶叶中提取茶多酚。
2.分离、纯化茶多酚粗品,掌握溶剂提取法提取茶多酚的原理及方法。
3.定量分析茶多酚产品含量。
二.实验原理
有机溶剂萃取法:有机溶剂萃取法是传统的提取工艺。
是利用茶叶中不同化合物在不同溶剂中的溶解度不同进行提取分离。
在粗茶叶萃取溶液中,除含有茶多酚以外,还含有咖啡碱、酯质、色素、植物多糖、有机酸、以及悬浮物,且茶多酚含量仅为25%~40% ,所以大多数工艺用乙酸乙酯、氯仿等有机溶剂反复萃取的方法进一步除杂、纯化、精制。
茶水用氯仿萃取可得到水层和有机层,咖啡碱存在于有机层,而茶多酚则存在于水层中,根据萃取及过滤原理,将有机层和水层分别进行浓缩、萃取,即可得到相应粗产物。
三.实验仪器及药品
仪器:天平;分析天平;铁架台;抽滤装置;超级恒温水浴槽;长颈漏斗一个;滤纸若干张;分液漏斗一个;100毫升的烧杯(三个);玻璃棒一个;药品:
1.乙醇水溶液(50%);
2.干茶叶原料;
3.氯仿(分析纯);
4.Na2SO4溶液馏水
四.实验步骤
1、温度设定:打开超级恒温水浴电源开关,使温度达到90℃
2、称量:称取30克干茶叶,放在100毫升小烧杯中。
3、溶解:用量筒量取40毫升50%乙醇水溶液,倒入小烧杯中,用玻璃棒轻轻搅拌,使干茶叶完全浸润在乙醇溶液中。
4、加热:将干茶叶和乙醇水溶液的混合液置于超级恒温水浴槽中,加热20分钟。
5、过滤:将加热完毕的混合液取出,冷却到室温;
用长颈漏斗对混合液进行过滤,滤除茶叶残渣。
再对残渣进行乙醇萃取.
6、分离萃取:
1)对分液漏斗进行试漏,调整好铁架台高度;
2)用量筒量取20毫升氯仿①,置于100毫升小烧杯中;将茶叶滤液倒入分液漏斗中,再将氯仿倒入其中,再倒入少量Na2So4溶液②,轻轻摇匀,使之混合充分,静置,分层,上层应为茶多酚水溶液,呈茶色,下层为氯仿乙醇混合液,为无色。
3)将下层溶液小心放至小烧杯中,上层溶液从分液漏斗上口倒至100毫升小烧杯中;
7、抽滤浓缩:
(1)安装好减压抽滤装置;
(2)将布氏漏斗里的滤纸用少量茶多酚水溶液润湿,开启抽气阀,一边缓慢倒入液体,一边抽滤。
3)抽滤完毕,关闭抽气阀,干燥得到咖啡碱。
8、萃取:(1)水层用乙酸乙酯萃取得有机层。
(2)重复上步抽滤浓缩步骤,得茶多酚。
9、称量:(1)将布氏漏斗内的滤饼用玻璃棒小心刮出,置于洁净滤纸上;(2)另取一张滤纸将粉末里的水分压干(3)用分析天平称量出茶多酚。
工业做法:
五.数据处理
以计算茶多酚的含量为例:
茶叶中茶多酚的百分含量计算公式为
W=(Mc/M)*100%
式中:Mc是最后提取出的茶多酚的质量,单位为g;
M为最初称取的茶叶原料的质量,单位为g
六.实验分析及注意事项:
1、萃取时要严格控制下层液的流速,太快有可能使上层液损失,使测得的百分含量偏低;
2、最后浓缩抽滤时,抽气阀不要开得太大,否则会使滤纸破损,导致产品损失;
3、浓缩完毕后,要及时称量,否则由于茶多酚具有吸湿性,会使测得的结果偏高。
4.使用的有机溶剂氯仿(CHCl3)有毒,使得产品和操作都不太安全;
最新文件仅供参考已改成word文本。
方便更改。