氧化还原离子方程式书写
- 格式:pptx
- 大小:84.47 KB
- 文档页数:4

新情境下氧化还原反应方程式的书写“四步法”突破新情景下氧化还原方程式的书写[示例] KMnO 4能与热的经硫酸酸化的Na 2C 2O 4反应,生成Mn 2+和CO 2,该反应的离子方程式是______________________________________________________________。
分析 第一步:依题意,锰元素的化合价降低,故KMnO 4是氧化剂,Mn 2+是还原产物;碳元素的化合价升高,故Na 2C 2O 4(碳元素化合价为+3价)是还原剂,CO 2是氧化产物。
第二步:按“氧化剂+还原剂——还原产物+氧化产物”把离子方程式初步写成:MnO -4+C 2O 2-4——Mn2++CO 2↑。
由MnO -4→Mn 2+,锰元素降了5价;由C 2O 2-4→CO 2,碳元素升了1价,1 mol C 2O 2-4共失去2 mol e -,故在C 2O 2-4前配5,在氧化产物CO 2前配10;在MnO -4前配2,在还原产物Mn 2+前配2,即2MnO -4+5C 2O 2-4——2Mn2++10CO 2↑。
第三步:反应在硫酸中进行,故在左边补充H +,右边补充H 2O,2MnO -4+5C 2O 2-4+ H +——2Mn 2++10CO 2↑+ H 2O 。
第四步:依据电荷守恒及H 、O 原子守恒配平如下:2MnO -4+5C 2O 2-4+16H +=====△2Mn 2++10CO 2↑+8H 2O 。
专题训练1.按要求完成下列方程式。
(1)已知在酸性介质中FeSO 4能将+6价铬还原成+3价铬。
写出Cr 2O 2-7与FeSO 4溶液在酸性条件下反应的离子方程式:_________________________________________。
(2)用NaClO —NaOH 溶液氧化AgNO 3,制得高纯度的纳米级Ag 2O 2。
写出该反应的离子方程式:______________________________________________________________。


离子方程式的书写规则离子方程式的书写规则如下:一、离子反应常见类型:1、复分解型离子反应:例:Ag++Cl-=AgCl↓2H++CO32-=CO2↑+H2O2、置换反应型:例:Zn+2H+=Zn2++H2↑Cl2+2I-=2Cl-+I23、盐类水解型:例:NH4++H2O==NH3·H2O+H+CH3COO-+H2O==CH3COOH+0H-4、复杂的氧化还原型:例:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O另外还有生成物中有络合物时的离子反应等。
例1:将少量Cl2通入H2S水溶液中:Cl2+H2S=S↓+2H++2Cl-,将过量Cl2通入H2S水溶液中:4Cl2+H2S+4H2O=10H++SO42-+8Cl-例2:Ca(HCO3)2溶液与适量或过量NaOH溶液作用:①Ca2++2HCO3-+2OH-=CaCO3↓+CO3-+2H2O若与少量NaOH溶液作用,则应写为:②Ca2++HCO3-+OH-=CaCO3↓+H2O 例3:澄清石灰水跟过量NaHCO3溶液作用:同例2①式与少量NaHCO3溶液作用,则同例2②式.例4:向Ca(H2PO4)2溶液中滴加过量的Ca(OH)2溶液:3Ca2++2H2PO4-+4OH-=Ca3(PO4)2↓+4H2O向Ca(H2PO4)2溶液中滴加少量Ca(OH)2溶液:Ca2++H2PO4-+OH-=CaHPO4↓+H2O 例5:向NaHSO4溶液中滴加Ba(OH)2溶液至沉淀恰好完全H++SO42-+Ba2++OH-=BaSO4↓+H2O向NaHSO4溶液中滴加Ba(OH)2溶液至沉淀恰好中和:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O规律:当某电解质的正、负离子完全参加了反应,则在配平的离子方程式中,反应物中该正、负离子的个数比,应与其电解质的组成比相同;当某电解质的正、负离子都参观加了反应,却未完全反应,则在配平的离子方程式中,该正、负离子的个别数比与其电解质组成不相同。
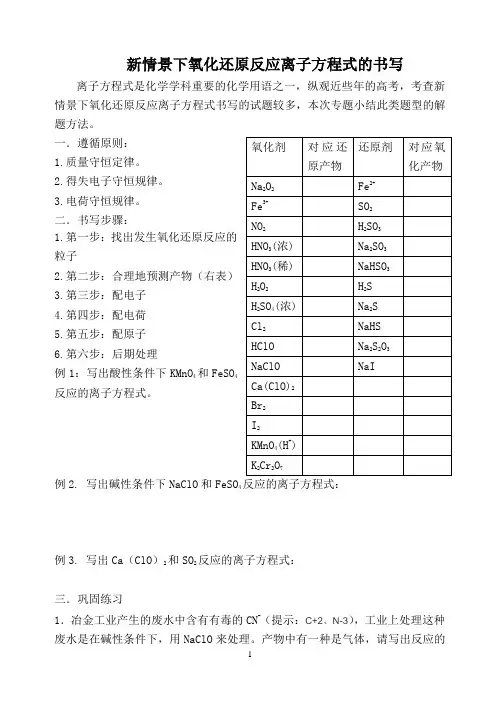
新情景下氧化还原反应离子方程式的书写离子方程式是化学学科重要的化学用语之一,纵观近些年的高考,考查新情景下氧化还原反应离子方程式书写的试题较多,本次专题小结此类题型的解题方法。
一.遵循原则:1.质量守恒定律。
2.得失电子守恒规律。
3.电荷守恒规律。
二.书写步骤:1.第一步:找出发生氧化还原反应的粒子2.第二步:合理地预测产物(右表)3.第三步:配电子4.第四步:配电荷5.第五步:配原子6.第六步:后期处理例1:写出酸性条件下KMnO4和FeSO4反应的离子方程式。
例2. 写出碱性条件下NaClO和FeSO4反应的离子方程式:例3. 写出Ca(ClO)2和SO2反应的离子方程式:三.巩固练习1.冶金工业产生的废水中含有有毒的CN-(提示:C+2、N-3),工业上处理这种废水是在碱性条件下,用NaClO来处理。
产物中有一种是气体,请写出反应的离子方程式 。
2.将实验室FeSO 4溶液与过氧化氢溶液混合,写出其离子方程式 。
3.将SO 2通入酸性KMnO 4溶液,溶液逐渐褪色,生成Mn 2+,同时pH 降低,则该反应的离子方程式是 。
4.若饮用水中ClO 2-的含量超标,可向其中加入适量的Fe 2+将ClO 2-还原成Cl -,写出离子方程式 。
5.用K 2Cr 2O 7可以装配检验司机是否酒后开车的装置。
其反应离子方程式为 ; 6.工业上为了处理含有Cr 2O 72-的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl ,以Fe 为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬的含量已低于排放标准。
请回答下列问题: (1)两极发生反应的电极反应式 阳极:___________________________ 阴极:__________________________ (2)写出Cr 2O 72—变为Cr 3+的离子方程式:____________________________ (3)废水由酸性变为碱性的原因是________________________________ (4)_______(填“能”或“不能”)改用石墨电极,原因是________ ______ 。

新情境下氧化还原反应方程式的书写“四步法”突破新情景下氧化还原方程式的书写[示例] KMnO 4能与热的经硫酸酸化的Na 2C 2O 4反应,生成Mn 2+和CO 2,该反应的离子方程式是______________________________________________________________。
分析 第一步:依题意,锰元素的化合价降低,故KMnO 4是氧化剂,Mn 2+是还原产物;碳元素的化合价升高,故Na 2C 2O 4(碳元素化合价为+3价)是还原剂,CO 2是氧化产物。
第二步:按“氧化剂+还原剂——还原产物+氧化产物”把离子方程式初步写成:MnO -4+C 2O 2-4——Mn 2++CO 2↑。
由MnO -4→Mn 2+,锰元素降了5价;由C 2O 2-4→CO 2,碳元素升了1价,1 mol C 2O 2-4共失去2 mol e -,故在C 2O 2-4前配5,在氧化产物CO 2前配10;在MnO -4前配2,在还原产物Mn 2+前配2,即2MnO -4+5C 2O 2-4——2Mn 2++10CO 2↑。
第三步:反应在硫酸中进行,故在左边补充H +,右边补充H 2O,2MnO -4+5C 2O 2-4+ H +——2Mn 2++10CO 2↑+H 2O 。
第四步:依据电荷守恒及H 、O 原子守恒配平如下:2MnO -4+5C 2O 2-4+16H +=====△2Mn 2++10CO 2↑+8H 2O 。
专题训练1.按要求完成下列方程式。
(1)已知在酸性介质中FeSO 4能将+6价铬还原成+3价铬。
写出Cr 2O 2-7与FeSO 4溶液在酸性条件下反应的离子方程式:_________________________________________。
(2)用NaClO —NaOH 溶液氧化AgNO 3,制得高纯度的纳米级Ag 2O 2。
写出该反应的离子方程式:______________________________________________________________。

一、陌生氧化还原反应方程式的书写方法1.“四步法”书写陌生氧化还原反应方程式第一步:根据元素化合价的升降判断氧化剂、还原剂、氧化产物、还原产物。
第二步:按“氧化剂+还原剂=还原产物+氧化产物”写出方程式,根据得失电子守恒配平上述四种物质。
注意:不属于“氧化剂、还原剂、氧化产物、还原产物”的物质这一步暂不写在方程式中。
第三步:根据电荷守恒或反应物的酸碱性,在方程式左边或右边补充H+、OH-或H2O等。
第四步:根据质量守恒配平反应方程式。
例:实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:软锰矿与过量固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl:用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩溶液,结晶得到深紫色的针状KMnO4晶体。
请回答:(1)软锰矿制备K2MnO4的化学方程式是;(2)KMnO4能与热的经硫酸酸化的Na2C2O4反应,生成Mn2+和CO2,该反应的化学方程式是。
解析:(1)第一步,Mn元素由MnO2中的+4价升高到K2MnO4中的+6价,故MnO2是还原剂,K2MnO4是氧化产物。
Cl元素由KClO3中的+5价降低到KCl中的-1价,故KClO3是氧化剂,KCl是还原产物。
第二步,按“氧化剂+还原剂=还原产物+氧化产物”把化学方程式初步写为:KClO3+3MnO2 KCl+3K2MnO4。
由于Cl元素降6价,Mn元素升2价,所以MnO2、K2MnO4的化学计量数均为3。
第三步,由于反应是在碱性条件下进行,且第一步写出的方程式中右边钾元素物质的量多于左边钾元素的物质的量,故在方程式左边反应物中补充KOH,右边生成物中补充H2O:KClO3+3MnO2+KOHKCl+3K2MnO4+H2O。
第四步,根据K元素守恒,在KOH前面配6;根据H元素守恒在H2O 前面配3。
两边的O元素相等,说明方程式已配平:3MnO2+6KOH+KClO3 3K2MnO4+KCl+3H2O。

氧化还原反应离子方程式书写的必备基础书写氧化还原反应离子方程式时,要熟记常见的元素及其形成的具有强氧化性和强还原性的物质或离子。
(1)涉及的元素:H、Na、Fe、Cu、N、O、S、Cl、Br、I。
(2)元素形成具有强氧化性和强还原性的物质或离子。
①强氧化性物质或离子:H2O2、Na2O2、Fe3+、Fe(OH)3、Fe2O3、Fe3O4、HNO3(浓)、HNO3(稀)、O2、O3、H2SO4(浓)、Cl2、HClO、NaClO、Ca(ClO)2、Br2、I2、KMnO4(H+)、K2Cr2O7(H+);②强还原性物质或离子:Fe2+、FeO、Fe3O4、Fe(OH)2、FeS、FeS2、FeBr2、FeI2、CuS、Cu2S、Cu2O、CuH、SO2、H2SO3、Na2SO3、NaHSO3、H2S、Na2S、NaHS、NaI。
(3)必须掌握的转化关系练习:1、将SO2通入到FeCl3溶液中的离子反应方程式将SO2通入到酸性KMnO4溶液的离子反应方程式将NaNO2溶液中加入酸性KMnO4溶液:将H2S通入到FeCl3溶液中的离子反应方程式将FeCl3溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为__________________________2、向H2O2溶液中滴入酸性FeCl2溶液中的离子反应方程式向H2O2溶液中滴入稀硫酸和KI混合溶液中的离子反应方程式向FeSO4溶液中加入酸性KMnO4溶液的离子反应方程式向FeO中加入稀硝酸的离子反应方程式3、H2C2O4溶液中加入酸性KMnO4溶液的离子反应方程式H2O2与酸性KMnO4溶液混合的离子反应方程式H2O2与酸性K2Cr2O7溶液混合的离子反应方程式4、Fe3O4溶解于稀硝酸的离子反应方程式Fe3O4溶解于氢碘酸的离子反应方程式5、Cu2O溶解于稀H2SO4中发生的离子反应为6、Mg与稀硝酸反应将N元素还原到最低价,则发生的离子反应方程式7、Na2S溶液长期放置有硫析出,原因为_______________________________________(用离子方程式表示)。

氧化还原反应离子方程式的配平
对于一般的氧化还原反应方程式配平的基本步骤是:标变价,列变化,求总数,配系数。
再根据反应的类型找出相应的方法:如歧化型(cl2+naoh→nacl+naclo3+h2o)用逆向配平法;归中型(反歧化型)(ki+kio3+h2so4→i2+k2so4+h2o)用正向配平法等。
氧化还原反应的基本原则是氧化剂得电子总数和还原剂失电子总数相等,即电子守恒原则,表现为化合价降低总数和升高总数相等。
配平三原则:
1、得失电子守恒:氧化剂和还原剂得失电子总数相等,化合价升高总数==化合价降低总数;
2、质量守恒:反应前后原子的种类和个数维持不变;
3.电荷守恒:离子反应前后,所带电荷总数相等。
配平基本方法:化合价滑行法
1、标价态:写出反应物和生成物的化学式,标出有化合价变化的元素的化合价
2、列于变化:列举反应前后元素化合价的变化值。
3、求总数:将化合价升高数和化合价降低数的最小公倍数定为电子转移总数。
依据电子守恒,确定氧化剂、还原剂、氧化产物、还原产物的系数。
4、分体式系数:用观察法配平其他物质的化学计量数,配平后,把单线换成等号。
5、细检查:利用守恒三原则,检查是否配平
任何的水解还原成反应方程式,分体式平时都必须严苛的经过这些步骤,特别就是最后的检查一定必须存有,以保证恰当!
当然,仅仅通过一两个练习就想熟练掌握氧化还原反应的配平是不可能的,一定要多找些例子勤加练习!。

氧化还原反应离子方程式氧化还原反应是化学反应中常见的一种类型,它涉及到物质中电子的转移。
在氧化还原反应中,一种物质失去电子,被氧化为较高的氧化态,而另一种物质获得这些电子,被还原为较低的氧化态。
这个过程中,电子的转移伴随着原子或离子的电荷的变化。
离子方程式是用来描述氧化还原反应中离子的形式的方程式。
它将反应中涉及到的化学物质以离子的形式表示,并用方程式表示它们之间的反应。
离子方程式可以更直观地展示氧化还原反应的电子转移过程。
举个例子来解释氧化还原反应离子方程式。
考虑以下反应:铁(Fe)与氯(Cl2)反应生成氯化铁(FeCl2)。
在这个反应中,铁原子失去了两个电子,而氯原子获得了这两个电子。
因此,我们可以将这个反应写成离子方程式如下:Fe(s) → Fe2+(aq) + 2e-Cl2(g) + 2e- → 2Cl-(aq)在这个离子方程式中,Fe(s)表示固态的铁,Fe2+(aq)表示溶解在水中的两个电荷为+2的铁离子,2e-表示两个电子,Cl2(g)表示气态的氯分子,2Cl-(aq)表示溶解在水中的两个电荷为-1的氯离子。
方程式中的箭头表示电子的转移方向。
离子方程式的写法可以有所不同,具体取决于化学物质的实际状态和反应条件。
例如,如果反应发生在溶液中,那么溶剂也需要考虑在内,离子方程式中会使用(aq)表示溶液中的离子。
此外,离子方程式还可以通过添加系数来平衡反应方程式,使得反应前后的离子数目保持一致。
除了离子方程式,还有一种常用的描述氧化还原反应的方程式是电子方程式。
电子方程式是在离子方程式的基础上简化而来的,它只关注电子的转移过程,不考虑离子的形式。
使用电子方程式时,我们只需要写出电子的转移方向和数量,而不需要写出离子的形式。
总结起来,氧化还原反应离子方程式是用来描述氧化还原反应中离子形式的方程式。
它能够清晰地展示氧化还原反应中电子的转移过程,帮助我们理解反应的电荷变化和物质的氧化还原性质。
通过掌握离子方程式的写法和理解,我们可以更好地理解和分析氧化还原反应,并在化学实验和工业生产中应用这些知识。

中学阶段一些还原性离子的常见氧化还原反应的归纳南江县职业中学唐志强在中学化学的学习过程中,氧化还原是学生普遍感到难学,难于把握。
为了提高学习效率。
在这里,就中学阶段常涉及到的常见还原性离子Fe2+ ,I- ,S2-,SO32-,Br-的一些反应,做简单的归纳。
一Fe2+的一些常见的氧化还原反应:①Fe2++X2=Fe3++2X- (X代表Cl Br)②2Fe2++H2O2 +2H+ =2Fe3++2H2O③3Fe2++NO3-+H+=3Fe3++NO↑+H2O④5Fe2++MnO4-+8H+=5F3++Mn2++4H2O⑤12Fe2++6H2O+3O2=4Fe(OH)3↓+8Fe3+⑥2Fe2++ClO-+2H+=2Fe3+ +Cl-+H2O二I-的常见的氧化还原反应:①2I-+X2=I2+2X-(X代表Cl Br)②2Fe3++2I-=2Fe2++I2③2I-+H2O2+2H+=I2+2H2O④10I-+2MnO4-+16H+=5I2+2Mn2++8H2O⑤2I-+ClO-+2H+=I2+Cl-+H2O⑥6I-+2NO3-+8H+=3I2+2NO↑+4H2O三S2-的常见的氧化还原反应:①S2-+X2=S↓+2X- (X代表Cl Br I)②S2-+H2O2+2H+=S↓+H2O③S2-+2Fe3+=S↓+2Fe2+ 或2S2-+2Fe3+=FeS↓+S↓+Fe2+④3S2-+2NO3-+8H+=3S↓+2NO↑+4H2O⑤5S2-+2MnO4-+16H+=5S↓+2Mn2++8H2O⑥S2-+ClO-+2H+=S↓+Cl-+H2O四SO3-的常见的氧化还原反应:①SO32-+X2+H2O=SO42-+2X- (X代表Cl Br I)②SO32-+2Fe3++H2O=SO42-+2Fe2++2H+③5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O④SO32-+H2O2=SO42-+H2O⑤3SO32-+2NO3-+2H+=3SO42-+2NO↑+H2O⑥2SO32-+O2=2SO42-五常涉及的Fe2+,Br-,I- 还原性的比较的氧化还原反应离子方程式的书写:从上面的反应得知还原性强弱顺序为I- >F2+>Br- :①Cl2+2I-=2Cl-+I2(通入少量氯气于碘化亚铁溶液)②3Cl2+2Fe2++4I-=6Cl-+2Fe3++2I2 (通入过量氯气于碘化亚铁溶液)③Cl2+2Fe2+=Cl-+2Fe3+ (通入少量氯气于FeBr2溶液)④3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2 (通入过量氯气于FeBr2溶液)⑤把等物质的量氯气通入氯化亚铁溶液:分析:设氯气1摩尔,则由氯气变成氯离子需得2摩尔电子,由得失电子守恒可知:FeBr2 也为1摩尔,应该亚铁离子为1摩尔先失去1摩尔电子,然后由Br- 失去1摩尔电子,所以参加反应的Br-也只有1摩尔。

氧化还原反应方程式的书写1.氧化还原反应中实际上包含氧化和还原两个过程;下面是一个还原过程的反应式:NO3-+4H++3e-→NO+2H2O;KMnO4、Na2CO3、Cu2O、Fe2SO43四种物质中的一种物质甲能使上述还原过程发生;1物质甲为,在该反应中作剂;2写出并配平该氧化还原反应的离子方程式:; 1Cu2O,还原剂23Cu2O+14H++2NO3—===6Cu2+++2NO↑+7H2O2.在氧化还原反应中,氧化过程和还原过程是同时发生的;Cu2O-2e-+2H+=2Cu2++H2O是一个氧化过程的反应式,下列五种物质FeSO4、Fe2SO43、CuSO4、Na2CO3、KI中的一种能使上述氧化过程顺利发生;1写出并配平该反应的离子方程式:;2向1中反应后的溶液里,加入酸性高锰酸钾溶液,反应的离子方程式为;2Fe3++Cu2O+2H+=2Fe2++Cu2++H2O5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O3.某反应体系中共有6种物质,KClO3、KCl、HCl、Cl2、ClO2、H2O,请你设计同位素示踪法确定反应的方程式并配平:_2K37ClO3+4HCl=2KCl+Cl2+237ClO2+2H2O4.过二硫酸钾K2S2O8具有强氧化性,可将I-氧化为I2:S2O-28+2I-=2SO-24+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应;试用离子方程式表示Fe3+对上述反应的催化过程:、;2Fe3++2I-=2Fe2++I2、S2O82-+2Fe2+=2SO42-+2Fe3+5.根据事实完成下列反应的化学方程式:1AsH3是一种很强的还原剂,室温下,它能在空气中自燃,其氧化产物为As2O3,该反应的化学方程式为______________________________________________________;2NaNO3与氢碘酸作用,放出NO气体并有单质I2生成____________________;3砷为氮族元素,其氧化物As2O3俗称砒霜,可用马氏试砷法来检验,其原理是将Zn、盐酸和试样混合,若含有砒霜,则生成AsH3气体,这一反应的离子方程式为;2AsH3+3O2=As2O3+3H2O,2NO3—+8H++6I—=2NO+3I2+4H2O6Zn+12H++As2O3=2AsH3+6Zn2++3H2O6.含氰化物有CN-的废水危害大,CN-的含量为L~L就能毒杀鱼类;其处理方法是用氧化法使其转化为低毒的氰酸钾KCNO,氧化剂常用次氯酸盐;而生成的CNO-可进一步降解为能直接排放到空气中的无毒气体;若用NaClO溶液处理NaCN的废液,产生另外两种盐,其化学方程式为;NaClO+NaCN====NaCl+NaCNO7.由稀有气体元素Xe 氙与氧元素形成的一种共价化合物XeO 3极不稳定,易转化为单质而呈强氧化性;将适量的XeO 3投入含Mn 2+的水溶液中,溶液逐渐变为紫红色且pH 不断减小;试写出有关的离子方程式:__________;5XeO 3+6Mn 2++9H 2O=6MnO 4-+5Xe↑+18H +8.氢化亚铜CuH 是一种难溶物质,用CuSO 4溶液和“另一物质”在40°C~50°C 时反应可生成它;CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu +在酸性条件下发生的反应是:2Cu +===Cu 2++Cu;根据以上信息,结合自己所掌握的化学知识,回答下列问题: 1写出CuH 在氯气中燃烧的化学反应方程式:_________________________________;2如果把CuH 溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH 溶解在足量稀硝酸中反应的离子方程式:____________________________________________________;2CuH+3Cl 2═2CuCl 2+2HCl,CuH+3H ++NO 3-=Cu 2++2H 2O+NO↑9.某学生两次分别用2.6 g 锌与硝酸溶液进行反应,两次所用的硝酸溶液中均含有6.3 g 的HNO 3,但浓度不同,均恰好完全反应;又已知第一次实验中有1/5的HNO 3被还原,第二次实验中只有1/10的HNO 3被还原;试写出相应的反应方程式;第一次_________________________________________________________________ 第二次_________________________________________________________________; 4Zn+10HNO3=4ZnNO32+N2O+5H2O4Zn+10HNO3=4ZnNO32+NH4NO3+3H2O 10.亚硝酸HNO 2是一种比醋酸略强的弱酸,很不稳定,易发生自身氧化还原反应而分解;1低温下,将等物质的量的NO 和NO 2通入水中,可制得HNO 2,反应的化学方程式为2NO 既有氧化性又有还原性,其氧化产物或还原产物与溶液的pH 的关系如下表所示: pH 范围 大于7 小于7 产物 NO NO 、N 2O 、N 2中的一种①在碱性条件下,NaNO 2溶液与NaClO 溶液反应的离子方程式为_________________②若HNO 2与氢碘酸反应时按物质的量之比1∶2进行,且I -被氧化成I 2,则该反应的离子方程式为____________________________________________________________3在冷冻的NaNO 2溶液中加入或通入下列物质,不能制得HNO 2的是________填序号. a .稀H 2SO 4 b .稀HClc .CO 2d .SO 2 1NO +NO 2+H 2O===2HNO 22①NO 2—+ClO -===NO3—+Cl - ②2HNO 2+4H ++4I -=I 2+N 2O↑+3H 2O 3cd 11.某反应体系中的物质有:NaOH 、Au 2O 3、Na 2S 4O 6、Na 2S 2O 3、Au 2O 、H 2O;①将Au 2O 3之外的物质分别填如以下空格内,配平后标出电子转移的方向和数目; ②反应中,被还原的元素是,还原剂是;③纺织工业中常用氯气作漂白剂,Na 2S 2O 3可作为漂白后布匹的“脱氯剂”,Na 2S 2O 3和Cl 2反应的产物是H 2SO 4、NaCl 和HC1,,则还原剂与氧化剂物质的量之比为;⑴Au 2O 3+4Na 2S 2O 3+2H 2O==2Na 2S 4O 6+Au 2O+4NaOH ⑵;Na 2S 2O 3⑶⑷1:412.已知:2Fe+3Br2=2FeBr3,Fe2+的还原性大于Br-现有16.8g铁和反应后加入适量水后,通入amolCl2;当a≤时,反应离子方程式为2Fe2++Cl2=2Fe3++2Cl-13.次磷酸H3PO2是一种精细化工产品,具有较强还原性,回答下列问题:⑴H3PO2是一种一元中强酸,写出其电离方程式:①H3PO2中,磷元素的化合价为②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:填化学式③NaH2PO2是正盐还是酸式盐其溶液显性填弱酸性、中性、或者弱碱性2H3PO2的工业制法是:将白磷P4与氢氧化钡溶液反应生成pH3气体和BaH2PO22后者再与硫酸反应,写出白磷与氢氧化钡溶液反应的化学方程式:。
氧化还原型离子方程式的书写技巧氧化还原型离子反应是物质在有自由移动离子的状态(一般情况是溶液)下发生的氧化还原反应。
这类离子反应相对来说比较复杂、抽象。
书写这类离子反应方程式,既要考虑离子反应发生的条件和离子反应方程式的书写规则,也要遵循氧化还原反应的本质和规律,要同时满足得失电子守恒、电荷守恒和质量守恒。
所以,对学生来讲有较大的难度。
氧化还原型离子反应方程式的书写是一个重难知识点,在高考中经常出现,是考查学生综合运用知识能力的一个重要方面。
氧化还原型离子反应方程式的书写技巧分为三步:一、找出发生反应的氧化剂和对应的还原产物、还原剂和对应的氧化产物,根据相应元素反应前后化合价的变化,使化合价升降相等。
常见的氧化剂和对应的还原产物:Cl2---Cl-Fe3+---Fe2+MnO4----Mn2+ClO----Cl- NO3-(H+)---NO2(NO)常见的还原剂和对应的氧化产物:H2S(S2-)---S SO2(SO32-、HSO3−)--- SO42-I----I2 Fe2+--- Fe3+二、根据反应体系的性质,如酸性用H+,碱性用OH-等使反应式电荷守恒。
三、根据质量守恒,观察反应式左右两边,补充有关的物质,如H2O等。
例如:在FeCl3的酸性溶液中通入足量的SO2,发生反应的离子方程式:___________。
解析:按照上述技巧,1、氧化剂是Fe3+、还原产物是Fe2+,还原剂是SO2、氧化产物是SO42- ,根据化合价升降相等,则2Fe3++ SO2→2Fe2++SO42-2、溶液是酸性,用H+使电荷守恒,则2Fe3++ SO2→2Fe2++SO42-+4H+3、根据质量守恒,反应式左边需加2H2O,则2Fe3++ SO2+2H2O→2Fe2++SO42-+4H+答案为:2Fe3++ SO2+2H2O=2Fe2++SO42-+4H+再分析一下近几年高考题中对氧化还原型离子反应方程式书写的考查:【2015年高考全国新课标1卷36(2)】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。
过氧化氢氧化的离子方程式氧化还原反应是指,一种物质在发生化学反应过程中,原本未具有的氧化物和还原物即物质由原来的状态通过改变氧化状态而转变的反应。
通常来说,一般情况下,氧化还原反应离子方程式是表示一种物质在发生化学反应变化的反应方程。
在这一反应中,原来尚未具有的还原物和氧化物在同一反应中互相转化而得到。
氧化还原反应是化学反应中最重要的基本反应之一。
1. 以氢氧化做示例氢氧化反应的离子方程式是:2H⁺ + O₂ → 2H₂O。
离子方程式表明,氢阴离子得以被氧化并且两个氢氧化阴离子被还原成了一分子水。
从化学反应的角度来看,可以说氢阴离子被氧化,同时又是水的还原物。
2. 以氯氧化做示例氯氧化反应的离子方程式是:Cl⁺ + O₂ → ClO₂⁻。
离子方程式表明,氯阳离子得以被氧化,一个氯离子变成了一个氯氧化阴离子。
从化学反应的角度来看,可以说氯阳离子被氧化,同时又是氧化物。
3. 以氢硫化作示例氢硫化反应的离子方程式是:2H⁺ + S → H₂S。
离子方程式表明,氢离子通过与硫离子发生反应,产生一分子氢硫化物。
从化学反应的角度来看,可以说氢离子被还原,同时又是硫的氧化物。
4. 以氯硫化做示例氯硫化反应的离子方程式是:Cl⁺ + S → ClS₂⁻。
离子方程式表明,氯阳离子被硫离子氧化并产生一个氯硫化阴离子。
从化学反应的角度来看,可以说氯阳离子被氧化,同时又是硫的还原物。
5. 综上一般来说,氧化还原反应离子方程式是表示一种物质在发生化学反应变化的反应方程。
在这种反应中,原本未具有的还原物和氧化物,即物质由原来的状态通过改变氧化状态而转变的反应,使得化学反应可以归结为:还原物加氧被氧化,氧化物失氧被还原。