10.3 液液萃取过程的计算
- 格式:ppt
- 大小:3.55 MB
- 文档页数:36







11 液液萃取(溶剂萃取)Liquid-liquid extraction(Solventextraction)11.1 概述一、液液萃取过程:1、液液萃取原理:根据液体混合物中各组分在某溶剂中溶解度的差异,而对液体混合物实施分离的方法,也是重要的单元操作之一。
溶质 A + 萃取剂 S——————〉S+A (B) 萃取相 Extract分层稀释剂 B B + A (S…少量) 萃余相 Raffinate(残液)一般伴随搅拌过程 => 形成两相系统,并造成溶质在两相间的不平衡则萃取的本质:液液两相间的传质过程,即萃取过程是溶质在两个液相之间重新分配的过程,即通过相际传质来达到分离和提纯。
溶剂 extractant(solvent)S 的基本条件:a、S 不能与被分离混合物完全互溶,只能部分互溶;b、溶剂具有选择性,即溶剂对A、B两组分具有不同溶解能力。
即(萃取相内)(萃余相内)最理想情况: B 与 S 完全不互溶 => 如同吸收过程: B 为惰性组分相同:数学描述和计算实际情况:三组分分别出现于两液相内,情况变复杂2 、工业萃取过程:萃取不能完全分离液体混合物,往往须精馏或反萃取对萃取相和萃余相进行分离,而溶剂可循环使用。
实质:将一个难于分离的混合物转变为两个易于分离的混合物举例:稀醋酸水溶液的分离:萃取剂:醋酸乙酯3 、萃取过程的经济性:取决于后继的两个分离过程是否较原液体混合物的直接分离更容易实现( 1 )萃取过程的优势:(与精馏的关系)a、可分离相对挥发度小或形成恒沸物的液体混合物;b、无相变:液体混合物的浓度很低时,精馏过于耗能(须将大量 B 汽化);c、常温操作:当液体混合物中含有热敏性物质时,萃取可避免受热;d、两相流体:与吸附离子交换相比,操作方便。
( 2 )萃取剂的选择——萃取过程的经济性a、分子中至少有一个功能基,可以与被萃取物质结合成萃合物;b、分子中必须有相当长的烃链或芳香环,可使萃取剂和萃合物容易溶解于有机相,一般认为萃取剂的分子量在350-500之间较为合适。
![[精华]液液萃取例](https://uimg.taocdn.com/0256fe16a7c30c22590102020740be1e650ecc31.webp)
液-液萃取实验(1)设备参数萃取塔塔径D=37mm;塔高=1000mmm;塔的有效高度H=750mm(2)实验数据及处理记录频率为10/次时,T煤=27℃,T水=26℃;频率为20/次时,T煤=30℃,T水=28℃;相关物性参数:水的密度1000kg/m3;煤油密度800kg/m3;流量计转子密度7900kg/m3 ;苯甲酸相对分子质量M=122012g/mol.1)转子流量计校正:q==6.805 L/h2)原料煤油浓度的计算:(对频率为10/次时原料举例)苯甲酸浓度C1 X V1=C(NaOH)x V(NaOH) =0.0134X14.35X10-3mol/l煤油的质量=800x10x10-6=8.00g煤油的浓度X1=C1xV1x122.12/8.00kgA/kgB=2.94×10-3 kgA/kgB; y2=0.同理可得其他成分的浓度,结果见上表。
Y与1/(Y E-Y)的数据关系℃计算示例原料煤油浓度C1 =14.80×0.0134/10=0.019832 mol/l煤油密度:0.8000g/cm3 苯甲酸摩尔质量:M=122g/mol 水的密度:1g/ cm310ml煤油质量:m=0.8000×10=8.0000g 25ml水质量:m=1.0000×25=25.0000g原料煤油浓度X1 =0.019832×0.01×122/8.0000=3.024×10-3 kgA/kgB同理可得到其他的浓度。
Y2=0做操作线描点(X1,Y1),(X2,Y2),连接两点即可得到操作线。
在塔底和塔顶浓度范围内,取一系列的Y值,由10次/分操作线方程y=1.046x+0.0019可得一系列对应的X值。
20次/分操作线方程为y=1.0305x+0.0019。
再由10次/分,按25℃平衡方程y=76143x3-476.58x2+1.2614x+3E-06的相应X对应的Y E 值。


实验八 液-液萃取操作实验一、实验目的1.了解液-液萃取设备的结构和特点。
2.熟悉液 液萃取塔的操作。
二、实验原理萃取是分离液体混合物的一种常用操作。
其工作原理是在待分离的混合液中加入与之不互溶(或部分互溶)的萃取剂,形成共存的两个液相,并利用原溶剂与萃取剂对原混合液中各组分的溶解度的差别,使原溶液中的组分得到分离。
1.液-液传质的特点液-液萃取与吸收、精馏同属于相际传质操作过程,它们之间有很多相似之处。
但由于在液-液萃取系统中,两相的密度差和界面张力均较小,因而会影响传质过程中两相的充分混合。
为了强化两相的传质,在液 液萃取时需借助外力将一相强制分散于另一相中(如利用塔盘旋转的转盘塔、利用外加脉冲的脉冲塔等)。
然而两相一旦充分混合,要使它们充分分离也较为困难,因此,通常在萃取塔的顶部和底部都设有扩大的相分离段。
萃取过程中,两相混合与分离的好坏,将直接影响萃取设备的效率。
影响混合和分离的因素有很多,分离效果除了与液体的物性有关外,还与设备结构、外加能量和两相流体的流量等因素有关,以致于很难用数学方程直接求得,所以表示传质好坏的级效率或传质系数的值多用实验直接测定。
研究萃取塔性能和萃取效率时,应注意观察操作现象,实验时应注意了解以下几点:(1)液滴的分散与聚结现象。
(2)塔顶、塔底分离段的分离效果。
(3)萃取塔的液泛现象。
(4)外加能量大小(改变振幅、频率)对操作的影响。
2.液-液萃取塔的计算本实验以水为萃取剂,从煤油中萃取苯甲酸。
水相为萃取相(用字母E 表示,又称连续相、重相)。
煤油相为萃余相(用字母R 表示,又称分散相、轻相)。
在轻相入口处,苯甲酸在煤油中的浓度应保持在0.0015~0.0020(kg 苯甲酸/kg 煤油)之间。
轻相从塔底进入,作为分散相向上流动,经塔顶分离段分离后由塔顶流出;重相由塔顶进入,作为连续相向下流动至塔底经π形管流出。
轻、重两相在塔内呈逆向流动。
在萃取过程中,一部分苯甲酸从萃余相转移至萃取相。
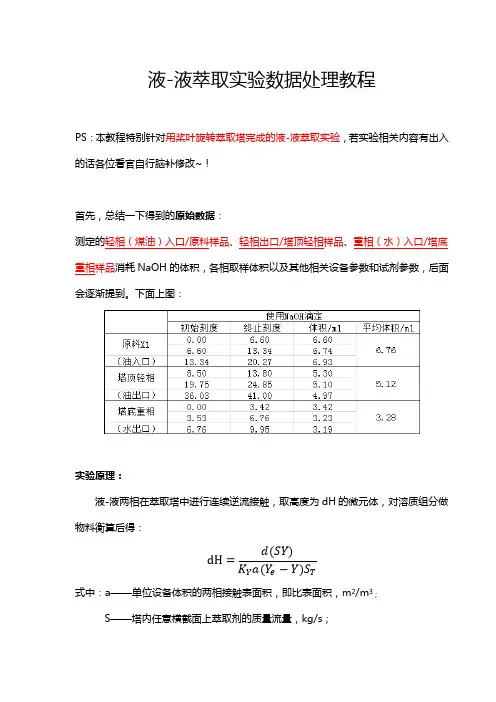
液-液萃取实验数据处理教程PS:本教程特别针对用桨叶旋转萃取塔完成的液-液萃取实验,若实验相关内容有出入的话各位看官自行脑补修改~!首先,总结一下得到的原始数据:测定的轻相(煤油)入口/原料样品、轻相出口/塔顶轻相样品、重相(水)入口/塔底重相样品消耗NaOH的体积,各相取样体积以及其他相关设备参数和试剂参数,后面会逐渐提到。
下面上图:实验原理:液-液两相在萃取塔中进行连续逆流接触,取高度为dH的微元体,对溶质组分做物料衡算后得:dH=d(SY)K Y a(Y e−Y)S T式中:a——单位设备体积的两相接触表面积,即比表面积,m2/m3;S——塔内任意横截面上萃取剂的质量流量,kg/s;K Y ——以(Y e −Y)为推动力的总传质系数,kg/(m 2·s) S T ——塔的横截面积,m 2;Y ——塔内任意横截面上萃取相中溶质组分A 的质量比,kgA/kgB ;Y e ——与塔内任意横截面上萃余相呈平衡的萃取相中溶质的质量比,kgA/kgB 。
对特定条件下的连续逆流萃取操作过程,S K Y aS T基本不变,作常数处理,将上式积分并整理后得:H =H OE N OE式中:H OE ——萃取相的总传质高度,m ;N OE ——萃取相的总传质单元数。
H OE =SK Y aS TN OE=∫dYe Y 1Y 2在Y-X 坐标系中做平衡曲线及操作线,在塔顶及塔底的浓度范围内任取一系列Y 值,可由操作线找出一系列的X 值,再用平衡曲线找出一系列的Y e 值,进而计算出对应的1(Y e −Y)值。
在直角坐标系上,以Y 为横坐标,1(Y e −Y)为纵坐标,绘制曲线,图解积分求传质单元数N OE ,H 为设备参数,进而得到H OE 。
体积总传质系数为:K Y a =S OE T~~~~~~~~~~~~~~~~~~~我是华丽丽的分割线~~~~~~~~~~~~~~~~~~~ 下面就根据实验原理将计算过程及要点展示如下:计算步骤1.根据滴定体积算出苯甲酸在各出入口的浓度(质量浓度)2.做出操作线,取一系列Y值得到一系列X值为纵坐标,绘制曲线3.根据平衡曲线算出Y e,进而以Y为横坐标,1(Y e−Y)4.在上述曲线中图解积分,最后得到相关计算量一、算出苯甲酸在各出入口的浓度(质量浓度)密度等数据大家要按照自己做实验时的温度来取,具体计算过程就略啦~主要就是注意区别溶剂以及计算单位(kgA/kgB)~下面上图:进水就是不含苯甲酸的水~二、操作线按照上述的X、Y对应的值即可得到两组(X,Y)的点,这两个点连线得到的就是操作线,如下图所示:在上述操作线的Y范围内取一系列值,然后算出对应的X值,以小编的数据来说就是取0~0.000212区间中的一系列值~。
12萃取本章学习要求1.熟练掌握萃取过程的原理;部分互溶物系的液-液相平衡关系;萃取过程(包括单级萃取、多级错流萃取和多级逆流萃取)的计算;对于组分B 、S部分互溶体系,要会熟练地利用杠杆规则在三角形相图上迅速准确的进行萃取过程计算;对于组分B、S不互溶体系,则可仿照吸收的计算方法。
2.理解溶剂选择的原则;影响萃取操作的因素;萃取剂和操作条件的合理选择;萃取过程的强化措施。
3.了解萃取操作的经济性;萃取操作的工业应用;液-液萃取设备及选用。
12.1 概述液-液萃取又称溶剂萃取,是向液体混合物中加入适当溶剂(萃取剂),利用原混合物中各组分在溶剂中溶解度的差异,使溶质组分A从原料液转换到溶剂S的过程,它是三十年代用于工业生产的新的液体混合物分离技术。
随着萃取应用领域的扩展,回流萃取,双溶剂萃取,反应萃取,超临界萃取以及液膜分离技术相继问世,使得萃取成为分离液体混合物很有生命力的单元操作之一。
蒸馏和萃取均属分离液体混合物的单元操作,对于一种具体的混合物,要会经济合理化的选择适宜的分离方法。
一般工业萃取过程分为如下三个基本阶段:1.混合过程将一定量的溶剂加入到原料液中,采取措施使之充分混合,以实现溶质由原料向溶剂的转移的过程;2.沉降分层分离出萃取相与萃余相。
3.脱出溶剂获得萃取液与萃余液,回收的萃取剂循环使用。
萃取过程可在逐级接触式或微分接触式设备中进行,可连续操作也可分批进行。
12.2液液相平衡12.2.1三角形相图根据组分间的互溶度,三元混合体系可分为两类:(1)Ⅰ类物系组分A、B及A、S分别完全互溶,组分B、S部分互溶或完全不互溶;(2)Ⅱ类物系组分A、S及组成B、S形成两对部分互溶体系本章重点讨论Ⅰ类物系连续操作的逐级接触萃取过程。
12.2.1三元体系的相平衡关系萃取过程以相平衡为极限。
相平衡关系是进行萃取过程计算和分析过程影响因素的基本依据之一。
对于组分B、S部分互溶物系,相的组成、相平衡关系和萃取过程的计算,采用等腰三角形相图最为方便。
化学萃取计算公式详解化学萃取是一种常用的化学分离技术,通过溶剂的选择和合理的操作条件,可以有效地提取目标物质。
在化学萃取过程中,需要对萃取效果进行评估和计算。
本文将详细介绍化学萃取的计算公式,并对其进行详细解析。
1. 萃取率。
萃取率是评价化学萃取效果的重要指标,它表示目标物质在溶剂中的提取率。
萃取率的计算公式如下:\[E = \frac{C_2V_2}{C_1V_1} \times 100\%\]其中,E表示萃取率,\(C_1\)和\(V_1\)分别表示原液中目标物质的浓度和体积,\(C_2\)和\(V_2\)分别表示萃取液中目标物质的浓度和体积。
2. 分配系数。
分配系数是描述溶质在两种不同相(通常是水相和有机相)之间分配的程度的指标。
分配系数的计算公式如下:\[K_d = \frac{C_o}{C_w}\]其中,\(K_d\)表示分配系数,\(C_o\)表示有机相中溶质的浓度,\(C_w\)表示水相中溶质的浓度。
3. 萃取平衡常数。
萃取平衡常数是描述化学萃取过程中平衡状态的指标,它反映了溶质在两相间的分布情况。
萃取平衡常数的计算公式如下:\[K_e = \frac{C_2}{C_1}\]其中,\(K_e\)表示萃取平衡常数,\(C_1\)和\(C_2\)分别表示水相和有机相中溶质的浓度。
4. 萃取效率。
萃取效率是评价化学萃取过程中能量利用的指标,它表示单位能量下提取的目标物质量。
萃取效率的计算公式如下:\[EE = \frac{m}{W} \times 100\%\]其中,EE表示萃取效率,m表示提取的目标物质质量,W表示消耗的能量。
5. 萃取选择性。
萃取选择性是描述化学萃取过程中对不同物质的选择性的指标,它反映了不同物质在萃取过程中的分布情况。
萃取选择性的计算公式如下:\[S = \frac{K_d(A)}{K_d(B)}\]其中,S表示萃取选择性,\(K_d(A)\)和\(K_d(B)\)分别表示不同物质在两相间的分配系数。
实验十二、液-液萃取实验实验十二液-液萃取实验一、实验目的二、基本原理三、实验流程三、设备参数四、实验步骤五、实验报告要求六、思考题实验目的1.了解液-液萃取设备的结构和特点;2.掌握萃取塔的操作方法;3.观察萃取塔内两相流动现象;基本原理萃取是利用液体混合物中各组分对某一溶剂的溶解度存在一定的差异来分离液体混合物的一种过程。
液-液萃取过程实质上并没有直接完成分离任务,而是将一种难于分离的混合物转变为两个易于分离的混合物。
因而,萃取过程在经济上是否优越还取决于后继的两个分离过程是否较原混合液直接分离更容易实现。
实验流程调速电机转子流量计Π型管往复振动筛板塔煤油贮槽曲柄连杆机构水高位槽煤油高位槽水相出口油相出口接自来水排放口设备参数萃取塔塔径为35mm,有效高度1.10m,内装20块塔板;转子流量计LZB-4 1.6~16l/hLZB-4 1~10l/hSTS 直流调速电源实验步骤确定外加能量对萃取效果的影响⑴打开水阀门,向水高位槽中注水;⑵将苯甲酸与煤油以一定比例混合,加到煤油贮槽,再用泵送至高位槽;⑶先在塔中灌满连续相――水,再开启分散相――煤油,待分散相在塔顶凝聚一定厚度的液层后,调节连续相的界面于一定的高度;⑷采用数字显示pH计测定水槽中水的pH值;⑸采用数字显示pH计,测定不同频率(可通过电压调节)或不同振幅(可通过曲柄连杆机构调节)下的水相出口pH值(一种操作条件下稳定五分钟后再取样测量)。
观察液泛现象固定连续相或分散相流量,加大分散相或连续相流量,实验报告要求1.根据所学内容及实验情况,描述实验中的萃取过程并写出影响萃取传质过程的主要因素。
2.描述在实验所用的萃取设备内两相的流动及传质情况。
实验思考题1.在萃取过程中选择连续相及分散相的原则是什么?2.本实验为什么不宜用水作为分散相,倘若用水作分散相,操作步骤是什么样的?两相分层分离段应设在塔顶还是塔底?3.重相出口为什么采用Π形管,Π形管的高度是怎么确定的?。