九年级化学图像专题
- 格式:doc
- 大小:1.45 MB
- 文档页数:2


平凡者工作室著版权所有,仅供内部使用解题关键: 一看:横、纵坐标的含义;二看:化学反应中的折点 的含义:一般认为每一折点代表一个反应的开始或结束; 三看:理解曲线的变化或趋势。
即图像是上升,下降,还是平直。
一般规律:①反应快慢:看倾斜角度(只有时间图像才能说反应快慢); ②产物质量:看图像纵坐标最大值;由完全反应掉反应物质量决定; ③反应起始时间:若反应条件为加热(高温),开始时间大于零。
催化剂能改变反应所需时间但不影响生成物质量。
类型一:金属与酸反应图像产生艮的质矍 I 酸过量或恰好反应) (金囑过垦或拾好反应)要求图像 足量的金属与等质量的酸反应: 金属过量,酸不足• 金属活动性:A > B 若A 和B 化合价相同,Ar (A ) > Ar (B )贝9 m (A ) > m (B ) I 0反应时间 足量的酸与等质量的金属反应: 酸过量,金属不足• 金属活动性:A > B 若A 和B 化合价相同,消耗等 质量的金属,贝Ar (A )> Ar (B ) c 的质盘或炼祝反直时间酸的质亘 酸的相对尙了质量十刼甘于中的H 不数 (1)纵坐标是H 2质量或体积,横坐标是时间的图像 要求 图像 金属与酸反应: fHi 的质屋或体祝 若A 和B 化合价相同,消耗等 L A 质量的金属,贝Ar (A )v Ar (B)0 霞的质楚 金属与酸反应: 的质星或体积 若A 和B 化合价相同,消耗等A /Z 质量的金属,贝 AAr (A )v Ar (B )------------ k°金属质量(2)纵坐标是H 质量或体积,横坐标是金属质量或酸质量图像 类型二:化学反应中反应物的质量或生成物的质量变化 要 反应物有剩余:起 反应物无剩 生成物的质量 求 始不为零,终点不 余:起始不为变化:不断增为零零 葬,终点为零 加,结束不变图■卩4臼拎|讪,黑像U丄o时何石19 时何k 0 时何&密闭容器中,总质量或某元素质量,反应 前后质量变化类型三:反应条件对反应影响要求图像加入催化剂结束不影响 生成物质量,只影响反 应快慢丄俸化制类型四:复分解反应中的图像沉淀沉淀 质I. 加入A 某物质量加入 某期质矍加热或高温,对反应物 的质量变化影响。

初中化学图像习题专题以及联系及其详细答案用函数图像表示一些化学(物理)现象发生的过程具有形象、直观、简洁的特点。
通过对图像试题的分析,能较好地考查学生抽象、概括、分析判断能力,培养良好的思维品质。
图像题是中考及化学竞赛中必不可少的一类题,涉及的内容主要包括质量守恒定律的应用;pH的变化;导电情况的分析;沉淀量与气体量关系计算;跨学科知识应用;溶液有关问题等等。
以用直角坐标系表示的曲线变化图形式出现的最多。
【方法点拨】解答曲线题关键要抓住曲线的起点、转折点、终点,由图像表示的意义与学科知识结合起来,并从中发现变化规律和趋势,把握了事物变化的规律就找到了解决问题的突破口。
一、固体物质的溶解度图像例1、现有A、B、C三种物质的溶解度曲线如图1所示。
已知在20℃~30℃间,A与B有相同的溶解度;在70℃时A、C溶解度相同。
(1)请在溶解度曲线中标出物质的标号;(2)在10℃时,三种物质的溶解度由大到小的顺序为_____;(3)在50℃时,三种物质的质量均为85g,分别放入100g水中形成溶液,其中__的溶液为饱和溶液,___的溶液为不饱和溶液;(4)要从A和B的混合物中提纯A,可采用____方法。
[解析]溶解度是初中化学的重要知识点,用纵坐标表示溶解度,横坐标表示温度,根据某一固体物质在不同温度时在水里的溶解度,可画出该物质的溶解度随温度变化的图像-溶解度曲线,这类图像题主要考查学生对溶解度曲线意义的了解,通过观察溶解度曲线可获得以下信息:①同种物质在不同温度下的溶解度;②不同种物质在同一温度下的溶解度;③同种物质的溶解度如何受温度变化的影响;④两种物质溶解度曲线相交点的意义。
教师指导学生学会发现和利用这些基础知识后,这类题不难得出正确答案。
参考答案:(1)略;(2)由大到小C、B、A;(3)A、B;C (4)降温结晶。
二、溶质的质量分数的图像例2、在一定温度下,向一定量的氯化钠稀溶液中不断加入氯化钠固体,并搅拌,在此过程中溶液里溶质的质量分数(w)与加入氯化钠质量(m)的变化关系如图2所示,其中图像正确的是()[解析]溶质的质量分数是溶液组成的一种表示方法。
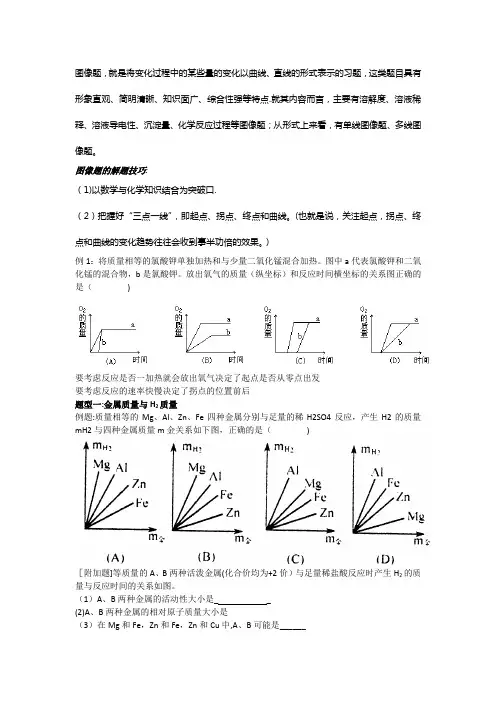
图像题,就是将变化过程中的某些量的变化以曲线、直线的形式表示的习题,这类题目具有形象直观、简明清晰、知识面广、综合性强等特点.就其内容而言,主要有溶解度、溶液稀释、溶液导电性、沉淀量、化学反应过程等图像题;从形式上来看,有单线图像题、多线图像题。
图像题的解题技巧:(1)以数学与化学知识结合为突破口.(2)把握好“三点一线”,即起点、拐点、终点和曲线。
(也就是说,关注起点,拐点、终点和曲线的变化趋势往往会收到事半功倍的效果。
)例1:将质量相等的氯酸钾单独加热和与少量二氧化锰混合加热。
图中a代表氯酸钾和二氧化锰的混合物,b是氯酸钾。
放出氧气的质量(纵坐标)和反应时间横坐标的关系图正确的是()要考虑反应是否一加热就会放出氧气决定了起点是否从零点出发要考虑反应的速率快慢决定了拐点的位置前后题型一:金属质量与H2质量例题:质量相等的Mg、Al、Zn、Fe四种金属分别与足量的稀H2SO4反应,产生H2的质量mH2与四种金属质量m金关系如下图,正确的是()[附加题]等质量的A、B两种活泼金属(化合价均为+2价)与足量稀盐酸反应时产生H2的质量与反应时间的关系如图。
(1)A、B两种金属的活动性大小是_ _(2)A、B两种金属的相对原子质量大小是(3)在Mg和Fe,Zn和Fe,Zn和Cu中,A、B可能是______题型二:有关溶液中溶质质量分数的图象题例题:有一杯食盐溶液,加水稀释,若以质量分数a%为纵坐标,以溶液的体积v为横坐标,则下图正确的是()练习1:m克KNO3的不饱和溶液,恒温蒸发水分直至有少量晶体析出。
在此过程中,能表示溶质的质量分数a%与时间t的变化关系的是( )练习2: 现有一杯接近饱和的食盐溶液,在恒温及溶剂(水)质量不变的条件下,为了达到饱和,不断向其中加入固体NaCl质量m,下图能表示加入的固体质量m与质量分数a%的关系的是()题型三:有关溶液的pH值与溶液的关系例题:将一定浓度的硫酸加水稀释,所得溶液的pH值与加水量m关系相符的图像是( )变形:1、向碱溶液中加水稀释2、向酸溶液中加碱溶液3、向碱溶液中加酸溶液练习: 向100克20%的氢氧化钠溶液中缓缓加入100克20%的盐酸溶液,所得溶液的pH值与加盐酸溶液的质量m关系相符的图象是()题型四:物质导电性与加入溶液量的关系例题:向一定量10%的硫酸溶液中,不断加入10%的氢氧化钡溶液,其导电能力的变化与加入氢氧化钡溶液量m的关系符合的图像是()题型五:有关质量守恒定律的图象题 例题:一定质量的木炭与过量氧气在密闭容器内加热使其充分反应。

专题08 图像题(讲练)【要点梳理】一、有关体积变化的图像——电解水水通电生成氢气和氧气的体积比为2:1。
注意是体积比不是质量比。
二、有关质量变化的图像1.化学反应中反应物的质量变化图像:图1图2分析:随着反应的进行,反应物质量不断减小,若反应物有剩余,则图像如图1所示;若反应物没有剩余,则图像如图2所示。
2.化学反应中生成物的质量变化(1)一种物质和另一种物质的反应图像:图3图4分析:图3,随着反应的进行,生成物的质量不断增加,当反应结束时,生成物的质量达到最大;之后,生成物质量将不再随加入物质质量(或时间)发生变化。
举例:红磷燃烧生成物的变化。
图4,反应时加入催化剂,反应的速率或反应的总时间会发生变化,但生成物的质量不发生变化。
举例:分解过氧化氢制氧气有无催化剂的变化图像。
(2)一种物质和两种物质的反应图像:图5图6分析:一种物质和两种物质发生化学反应时,首先判断反应发生的先后顺序,然后判断生成物的质量,先发生反应的生成物曲线通常从原点开始(如图5所示);后发生反应的生成物曲线通常从原点后开始(如图6所示)。
举例:向部分变质的氢氧化钠溶液中滴加稀盐酸,生成气体的坐标曲线(如图6所示),因为稀盐酸先和NaOH发生中和反应,当NaOH完全消耗完后,稀盐酸再与碳酸钠反应才有气体生成。
(3)化学反应中物质总质量(含元素种类)的变化化学反应中物质总质量(或元素种类)不变(如图7、图8所示)图像:图7图8三、溶质质量分数的变化曲线物质溶解时,溶质质量分数的变化。
图像:图9图10分析:图1,在一定温度下,向某不饱和溶液中继续加入某溶质,该溶质的质量分数随着溶质的增加而增大,当溶液达到饱和时,溶质质量分数不变。
图2,溶液稀释时,溶质的质量不变,而溶液的总质量不断增加,所以溶质质量分数不断减小。
四、pH变化曲线1.酸碱中和反应中的pH曲线图像:图11图12分析:图1,碱入酸,滴定前,溶液的pH<7,此时溶液呈酸性;当酸碱恰好完全反应时,溶液的pH=7;随着碱的继续加入,溶液的pH>7,溶液呈碱性。


图像题(一)1、a、b两支试管,b试管内有少量二氧化锰,现同时在两支试管内滴加等量的浓度相同的过氧化氢溶液,能正确表示a、b两支试管放出的氧气的质量纵坐标与反应时间横坐标关系的图是()A.B.C.D.2.已知FeCl3也可以做H2O2分解的催化剂,现向装有一定量的H2O2溶液的试管中滴入适量的FeCl3溶液,充分反应忽略水的挥发。
下列图象正确的是()A.B. C.D.3.下列图像能正确反映对应变化关系的是()A.用等质量、等浓度的双氧水制取氧气B.加热高锰酸钾制取氧气C.将水通电电解一段时间D.向一定量的过氧化氢溶液中加入二氧化锰4.两份质量相同的氯酸钾,其中一份中加入少量二氧化锰,分别同时加热,放出氧气的质量m与加热时间t 的关系图像正确的是()a为加热纯净氯酸钾的曲线,b为加热加有二氧化锰的氯酸钾的曲线A. B. C. D.5.今有A、B两质量相等的固体,其中A为纯氯酸钾,B是氯酸钾和二氧化锰的混合物,在酒精灯上同时加热,均完全反应,得到的气体质量与加热时间关系图象正确的是()A. B. C. D.6.在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前后及t 1、t 2时各物质质量如图所示。
下列说法中不正确的是()A.该反应为化合反应B.丙可能为该反应的催化剂C.该反应中,乙、丁的质量变化之比为7:5D.该反应中,甲、乙的相对分子质量之比为2:77.某同学误将少量KMnO 4当成MnO 2加入KClO 3中加热制取氧气,部分物质质量随时间变化如图所示。
下列关于该过程的说法中正确的是()A.t 2时刻,O 2开始产生B.t 1时刻,KMnO 4开始分解C.c 一定是代表氧气的质量D.对氯酸钾起催化作用的是高锰酸钾8.质量相等的两份固体,然后分别放在酒精灯上均匀受热,放出氧气的质量m 随反应时间t 变化的函数图象如图,a 为纯净的氯酸钾,b 为加入了高锰酸钾的氯酸钾,正确的是()A. B. C. D.9.下列4个图象能正确反映对应变化关系是()A.过量红磷测定空气中氧气含量 B.用酒精灯加热一定量KMnO 4固体C.加热氯酸钾和MnO 2取氧气 D.向盛有一定量H 2O 2溶液的烧杯中加入MnO 2A.生成氧气的质量B.固体中二氧化锰的质量C.固体中氧元素的质量D.固体中钾元素的质量分数。


中考化学图象题的解法和技巧图像是研究和处理化学问题的一种方法和手段。
化学试题中常运用图像信息表示化学过程或相关的变化规律,称之为图像题,它以化学中的基本概念、基本理论、元素化合物和化学实验等知识为载体,精心设计问题的一种信息处理与分析的试题。
这类题目具有形象直观、简明清晰、知识面广、综合性强等特点。
图像题要求学生能从文字、表格、图象中提取能解决问题的有用信息,能较好地考查学生抽象、概括、观察、分析判断能力和信息提取能力。
图像题是初中化学教学的重要部分,是每年中考的必考内容,在省、市各层次的考试中,出现频率都非常高。
专题归纳一、图像题的内容从内容上来说,出现在质量守恒、金属与酸、盐溶液的反应、溶液的性质、酸碱盐之间的反应、微粒间的变化、反应速率等。
给出的题目一般有坐标、图表、分子原子模型等,知识面广,知识的联系强,近三年中考中常作为综合题出现。
二、解题方法分析已知条件,读懂题目中有限的文字信息,对整个函数图象进行多角度认真分析。
1. 直角坐标系题:解题要点在于解题时要求学生首先弄清楚横坐标和纵坐标到底是什么,理解起点、终点、转折点的含义,然后根据所学知识分析概念、图象、数值三者之间的关系。
起点一般有三种情况:起点从原点开始;起点开始于y轴;起点开始于x轴。
变化趋势可分为三种:变大、变小、不变型。
终点可分为:接近某个值或等于某个值。
2.表格型题:解题要点在于通过审题,获取有用信息,然后对表格中数据进行比较分析,依据物质的性质、变化规律进行解答。
(1)起点开始于y轴的图象一般是当横坐标所表示的量为零时,其纵坐标所表示的量不为零。
如向不饱和溶液中加入溶质,其溶质质量的变化图象。
(2)起点开始于x轴的图象一般是当横坐标所表示的量达到一定程度时,其纵坐标所表示的量才开始变化。
如条件为加热的反应其生成物(纵坐标)随时间(横坐标)的变化图象。
(3)pH图象和溶解度曲线均为曲线图象,不要画成直线。
二、主要题型1.金属与酸反应图象题。

完整版)九年级化学图像专题
中物质浓度变化的图像
要求纵坐标是物质浓度,横坐标是时间的图像。
一般规律:
①溶液中某物质浓度随时间的增加而减小,说明该物质参与了反应。
②溶液中某物质浓度随时间的增加而增大,说明该物质是反应生成物。
③溶液中某物质浓度在一段时间内先增加后减小,说明该物质是反应中间体。
④溶液中某物质浓度在一段时间内保持不变,说明该物质不参与反应。
图像中的横纵坐标含义需要注意,化学反应中的折点代表反应的开始或结束。
在分析图像时,需要理解曲线的变化趋势,包括上升、下降或平直。
根据图像的倾斜角度和纵坐标最大值可以判断反应的快慢和产物质量,而加热或高温对反应起始时间和生成物质量有影响。
催化剂能够改变反应所需时间但不影
响生成物质量。
在金属与酸反应的图像中,足量金属与等质量酸反应时,金属过量则酸不足,反之亦然。
根据金属的活动性和化合价可以判断金属的质量变化。
在反应条件对反应影响的图像中,催化剂只影响反应快慢,加热或高温只影响反应物质量变化,而不影响生成物质量。
复分解反应中的图像符合B 或D图,向一混合溶液中加入另一溶液,过一会才产生沉淀或气体。
在溶液中物质浓度变化的图像中,可以根据物质浓度随时间的变化趋势判断该物质是否参与反应,是反应生成物还是反应中间体,或者不参与反应。

九年级化学中考总复习-专题突破第4讲图像题复习要求:1.了解常见的图像题型和解题思路;2.通过例题讲解、练习提高图像题的分析解题能力。
复习重点、难点:1.图像题分析、解题能力的培养。
复习过程:一、考点归纳整理:图像题常见题型:(一)金属与酸反应类型1.等质量的金属与足量的酸反应,氢气质量与反应时间的关系:(1)反应速率由快到慢_________________________________;(2)金属活动性由强到弱_________________________________;(3)产生氢气由多到少_________________________。
2.足量的金属与等质量的酸反应,氢气质量与反应时间的关系:3.等质量的金属与足量的酸反应,氢气质量与酸的质量的关系:(二)溶液酸碱度的变化1.溶液酸碱性的改变:(1)酸性溶液加水稀释,酸性______,pH_______,逐渐趋近7;(2)碱性溶液加水稀释,碱性性______,pH_______,逐渐趋近7;(3)碱性溶液中加酸,溶液由____性(pH___7)到____性(pH ___7)到___性(pH___7);(4)酸性溶液中加碱,溶液由____性(pH___7)到____性(pH ___7)到___性(pH___7)。
2.中和反应图像的意义:如图是氢氧化钠和稀盐酸中和反应的pH变化图,横坐标表示的是加入_______溶液的质量,当加入该溶液的质量为a时,溶液中的溶质为_________,当加入该溶液的质量为b 时,表示_______________________,溶液中的溶质为_________,当加入该溶液的质量为c 时,溶液中的溶质为_________。
(三)反应速率与时间的关系1.常见影响化学反应速率的几个因素:(1)温度,一般温度越______,反应越快;(2)反应物浓度,一般反应物浓度越____,反应越快;(3)反应物的接触面积,反应物接触面积越_____,反应越快;(4)催化剂,一般催化剂可以________化学反应速率。
题型复习(一)图像图表题1.把等质量的X 、Y 、Z 、M 四种金属分别加入到同体积、同浓度的足量稀盐酸中,再把X 加入到Z(NO 3)2溶液中,M 加入到YNO 3溶液中。
反应关系如图所示。
据此判断四种金属的活动性顺序为( )A .Z >X >M >YB .X >Z >M >YC .X >Z >Y >MD .Y >M >Z >X2 )3.向一定量黄铜(铜锌合金)粉末中逐滴加入稀硫酸,下列图像能正确表示对应变化关系的是( )4.向一定质量AgNO 3和Cu(NO 3)2的混合溶液中加入过量的Zn 粉,溶液质量随反应时间变化的情况如图所示。
下列说法正确的是( )A .取A 点溶液,滴加稀盐酸,无白色沉淀B .图标上B ~C 段质量增加的原因是Zn 与Cu(NO 3)2溶液反应 C .B 点时溶液中金属离子有Zn 2+、Cu 2+,金属单质有Zn 、Cu 、AgD .C 点和D 点溶质种类不同,金属单质种类也不同5.已知:2KClO 3=====MnO 2△2KCl +3O 2↑,如图表示一定质量的KClO 3和MnO 2固体混合物受热过程中,某变量y 随时间的变化趋势,纵坐标表示的是( )A .固体中氧元素的质量B .生成O 2的质量C .固体中MnO 2的质量D .固体中钾元素的质量分数6.往200gFeCl 3和CuCl 2的混合溶液中加入铁粉。
已知反应的先后顺序和化学方程式分别为:2FeCl 3+Fe==3FeCl 2;CuCl 2+Fe==FeCl 2+Cu 图为加入铁粉的质量与反应后剩余固体质量关系。
则下列说法不正确的是( )A .B 点后溶液的颜色为蓝色 B .D 点对应纵坐标为6.4C .该200 g 溶液中的CuCl 2 质量分数为6.75%D .取DE 两点间的剩余固体加入盐酸,均有气泡产生7.下列四个坐标示意图分别表示四个实验过程中的某些变化情况,其中错误的是( )A .加热一定量碳铵(NH 4HCO 3)的实验,试管中固体的质量变化B .等质量的镁条和铁丝分别与足量的稀硫酸反应,产生气体的质量变化C .向一定量的二氧化锰固体中加入一定量的过氧化氢溶液,二氧化锰的质量变化D .将水通电一段时间,相同状况下产生气体的体积变化8.下图为某化学反应的微观模拟示意图,下列说法中,不正确的是( )A .该反应不属于置换反应B .图示中x 的数值为3C .反应前后氢元素的化合价发生了改变D .反应中甲、丙两物质的质量比为2∶79.向烧杯中逐滴加入X 溶液至过量(图甲),生成沉淀或气体的质量与加入X 溶液的质量关系符合图乙的是( )10.将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀盐酸的质量变化曲线如图所示: (1)在滴加的过程中,烧杯中溶液的pH 逐渐________(填“增大”“减小”或“不变”)。
中考化学图像型计算题专题复习一、溶液的质量的计算1. (6分)在一烧杯中盛有一定质量的MgCOa 体,向其中滴加溶质的质量分数为 10%的HSO 溶液,至恰好完全反应。
得到102g 不饱和溶液。
向所得溶液中逐滴滴 人溶质质量分数为10 %的NaO 溶液,产生沉淀的质量与所滴入NaOl 溶液的质量关 系曲线如图所示。
请根据题意回答下列问题:(1)在滴入稀硫酸时,观察到的明显实验现象是⑵ 当滴入NaO 溶液至图中A 点时,烧杯中溶液里含有的溶质是(写化学式)O(3)当滴入10%的NaOl 溶液80g 时(即B 点),试通过计算,求此时所得不饱和 溶液的质量。
(计算结果精确至0.1g )产f 80滴入NaOH 溶液的质量/g2. (6分)在一烧杯中盛有42.2gCaCO 和CaCb 的粉 末状混合物,向其中188.8g 水,使混合物中 的可溶物完全溶解。
然后再向其中逐滴加如 溶质的质量分数为10%勺稀盐酸,烧杯中难 溶固体物质的质量与所滴入稀盐酸的质量关 系曲线如图所示。
请根据题意回答下列问题: ⑴在滴入稀盐酸的过程中,观察到的明显现 象是: ① ________________________ ② ____________________________ 。
⑵当滴入10%勺稀盐酸至图中A 点时,烧杯中溶液里含有的溶质是(写化学 式) 。
⑶当滴入10%勺稀盐酸146g 时(即B 点),试通过计算,求此时烧杯中所得 不饱和溶液的质量。
(计算结果精确到0.1g )产生沉淀的质量g!、B 073g146g滴入稀盐酸的质量/gB0 463、(7分)在一烧杯中盛有一定质量的金属镁,向其中加入足量的稀硫酸,至恰好完全反应,在一定温度下得到 30g MgSO 的不饱和溶液。
向所得溶液中逐滴滴入溶质 质量分数为10%勺NaOH 溶液,溶液的总质量 与滴入NaOH 溶液的质量的质量关系曲线如 图所示。
请根据题意回答下列问题: ⑴写出在整个实验过程中观察到的一项实验 现象: _____________________ 。