华师大版-科学-八年级上册-6.1 构成物质的微粒 同步自测
- 格式:doc
- 大小:96.50 KB
- 文档页数:4

1第六章物质的构成1构成物质的微粒有2、 分子是保质物质 ___________ 的最小粒子,原子是 ____________ 中的最小粒子.分子、原子和离子都是构成 ___________ 的粒子. 3、 在化学反应中,原子得到电子形成 离子,原子失去电子形成离子,离子是原子 ___________ 或___________ 的产物.4、1911年著名物理学家卢瑟福等人为探索原子的内部结构进行了 下面的实验.他们用一束带正电的、质量比电子大得多的高速运 动的a 粒子轰击金箔,发现:① 大多数a 粒子能穿透金箔而不改变原来的运动方向; ② 一小部分a 粒子改变了原来的运动方向; ③ 有极少数a 粒子被弹了回来. 根据以上实验现象能得出关于金箔中 Au 原子结构的一些结论,试写出其中的三点:② ________________________________________________________________ ③ ________________________________________________________________ 5、下列属于离子直接构成的物质是 _____________________________ 。
6、 “遥看不是雪,唯有暗香来“说明分子在永不停息做无规则运动,”大风起兮尘飞扬“ ________ (填“能”或“不能”)说明分子在做无规则运动。
7、 装满液体的容器难以被压缩说明 _______________________ ;水由液态变成气态的过程中体 积变大,说明 _________________ ;(①、分子体积变大;②、分子间间距变大)蔗糖块放入水 中一段时间消失了说明 。
8、下列微粒中,构成原子的有,构成原子核的有 ,带电的粒子有 ;在原子中,核电何数- 数- 数- 序数; ①质子②离子③中子④电子⑤分子⑥原子9、Na 原子失去一个电子成为带一个正电荷的 Na 离子,他们(填”属于①、NaCI ②、CO ③、KI④、H 2O ⑤ CuSQ ⑥NaOH 起子运动轨迹示意图成的物质化学式有;宇宙含量最多的元素是;地核中含量最多的元“或”不属于“)冋一种兀素的粒子,原因是因为他们的相同。

最新精选华师大版科学八年级上册第6章物质的构成1 构成物质的微粒习题精选八十五第1题【单选题】以下说法中正确的是( )A、分子的运动是匀速直线运动B、扩散现象只能在气体中进行C、固体分子总是保持静止状态的D、分子之间同时存在着引力和斥力【答案】:【解析】:第2题【单选题】“超临界水”(H2O)因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的状态,用“○”表示氢原子,“”表示氧原子,下列模型能表示“超临界水”分子的是( )A、B、C、D、【答案】:【解析】:第3题【单选题】为了揭开原子内部结构的奥秘,1911年著名物理学家卢瑟福等人做了一个著名的“卢瑟福实验”:用一束带正电的质量比电子大很多的高速运动的α粒子轰击金箔,结果是大多数α粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,甚至有极少数的α粒子被反弹了回来。
通过这一实验现象不能够获得的结论是( )A、原子核质量较大B、原子核体积很小C、核外电子带有负电荷D、原子核带有正电荷【答案】:【解析】:第4题【单选题】下列电离方程式正确的是( )A、Al2(SO4)3=Al^3^++有误B、H2SO4=2H^++有误C、Ba(OH)2=Ba^2^++(OH^-)2D、Na2CO3=2Na^++CO3-【答案】:【解析】:第5题【单选题】用分子、原子的观点分析下列生活中的现象,其解释不合理的是( )A、50ml水与50ml酒精混合后,总体积小于100ml—分子间有间隔B、八月桂花飘香—分子在不停地运动C、1滴水中约含1.67×10^21个水分子—分子很小D、水结成冰—分子停止运动【答案】:【解析】:第6题【单选题】关于扩散现象,下列说法错误的是( )A、温度越高,扩散进行得越快B、扩散现象是由物质分子无规则运动产生的C、扩散现象在气体、液体和固体中都能发生D、在太空中,扩散现象将消失【答案】:【解析】:第7题【单选题】下列事例中,哪一个事不能表明物体的分子在不停地做无规则的运动( )A、刮风时尘土飞扬B、在皮肤上擦点酒精,立即就能闻到酒精的味道C、在墙角堆煤,过一段时间,墙表面及其内部靠近表面的一浅层都变黑了D、衣箱中的卫生球变小了,衣服上充满了卫生球的气味【答案】:【解析】:第8题【填空题】(1)请用化学符号填空:①2个双氧水分子______;②3个氢氧根离子______;③标出BaO中Ba元素的化合价______;(2)如图表示在一定条件下,物质转化过程的围观示意图,请根据图形信息回答问题:①CO分子中C、O元素的质量比为______;②O^2^﹣核外电子数为______;③该过程的化学反应方程式为______【答案】:【解析】:第9题【填空题】模型类型:一个模型可以是一幅______ 、一张______ 或______ 图像,也可以是一个复杂的______ 或______ 的示意。

第6章测试卷一、选择题(每题2分,共40分)1.下列各组元素中,元素符号的第一个字母相同的一组是() A.氯、碳、钙、铜B.氢、汞、铁、银C.钠、镁、氧、氮D.锰、硫、锌、钡2.下列符号中,既可用来表示一种物质,又可用来表示一种元素,还可用来表示一个原子的是()A.H B.O C.He D.CO3.作为相对原子质量基准的1个碳-12原子的质量为1.993×10-26 kg,某种氢原子1个原子的质量为3.348×10-27 kg,则该氢原子的相对原子质量约为() A.1 B.2 C.3 D.44.科学家用有机分子和球形笼状分子,首次制成了“纳米车”(如图)。
“纳米车”底盘和轮轴由一种有机分子构成,而轮轴末端是四个球形笼状的C60分子制成的轮子。
“纳米车”可以用来运输单个的有机分子,生产复杂的材料或药物。
下列有关“纳米车”的说法不正确的是()(第4题)A.C60是一种新型的非金属单质B.“纳米车”是混合物C.“纳米车”运输单个的有机分子的过程肉眼可见D.“纳米车”研制成功说明人类操纵分子技术又进入一个新的阶段5.当你打开试卷时,可能会闻到一些油墨的气味,这主要是因为构成物质的微粒()A.质量很小B.在不断运动C.体积很小D.之间有空隙6.下列各组物质中,都由分子构成的一组是()A.金和金刚石B.水和氨气C.汞和氯化钠D.干冰和硫酸铜7.在我们身边的物质中,属于单质的是()A.水B.食盐C.氧气 D.空气8.白枇杷汁多、味甜,口感好,含锌、铁、钙、硒等。
这里的锌、铁、钙、硒是指()A.原子B.分子C.元素 D.离子9.由同种元素组成的物质一定不是()A.纯净物B.单质C.化合物D.混合物10.有一些物质,它们中的一些原子集团常作为一个整体参加反应,下列物质中含有原子集团的是()A.NaCl B.NaNO3C.CaCl2D.KCl11.元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,其中X、Y、Z代表三种不同的元素。
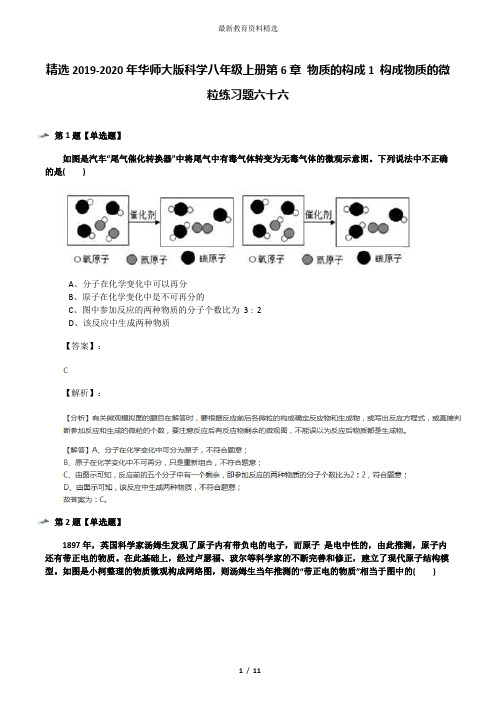
精选2019-2020年华师大版科学八年级上册第6章物质的构成1 构成物质的微粒练习题六十六第1题【单选题】如图是汽车“尾气催化转换器”中将尾气中有毒气体转变为无毒气体的微观示意图。
下列说法中不正确的是( )A、分子在化学变化中可以再分B、原子在化学变化中是不可再分的C、图中参加反应的两种物质的分子个数比为3∶2D、该反应中生成两种物质【答案】:【解析】:第2题【单选题】1897年,英国科学家汤姆生发现了原子内有带负电的电子,而原子是电中性的,由此推测,原子内还有带正电的物质。
在此基础上,经过卢瑟福、玻尔等科学家的不断完善和修正,建立了现代原子结构模型。
如图是小柯整理的物质微观构成网络图,则汤姆生当年推测的“带正电的物质”相当于图中的( )A、甲B、乙C、丙D、丁【答案】:【解析】:第3题【单选题】对于下列问题的微观解释中,错误的是( )?A、一滴水中大约有1.67×10<sup style="line-height: 22px;">21个水分子,说明水分子很小B、墙内开花墙外可闻到花香,说明分子在不断运动C、6000L氧气在加压的情况下可装入容积为40L的钢瓶中,说明氧分子数目减少了D、一氧化碳和二氧化碳具有不同的化学性质,说明它们的分子构成不同【答案】:【解析】:第4题【单选题】下列说法正确的是( )A、“破镜难重圆”是因为固体分子间只存在着排斥力B、原子核内质子所带的正电荷数与中子所带的负电荷数相等,所以通常物体不带电C、在空调房间吸烟时,会看到烟雾在空中弥漫,这是分子的无规则运动D、宇宙大爆炸理论认为宇宙诞生于大爆炸,爆炸引起宇宙膨胀【答案】:【解析】:第5题【单选题】如图所示是餐桌上常见的美食,其中所包含的物理知识正确的是( )A、蒸饺﹣﹣刚蒸熟的饺子冒“白气”是汽化现象B、牛肉面﹣﹣挑面时香气四溢说明分子在做无规则运动C、回锅肉﹣﹣炒肉时是通过做功的方式使肉和菜的内能增加D、玉米排骨汤﹣﹣当汤沸腾以后,把炖汤的火调小是为了降低汤的温度【答案】:【解析】:第6题【单选题】下列说法中正确的是( )A、在天文学中,用“光年”作为时间单位B、太阳是宇宙的中心,地球是太阳的一颗行星C、夸克是由比其更小的质子和中子构成的D、质子带正电,中子不带电,它们是由更小的粒子夸克组成的【答案】:【解析】:第7题【单选题】将一根细线松松地系在一个铁丝框架的相对的两边上。

八年级科学上册第六章物质的构成第1节构成物质的微粒同步练习(扫描版,无答案)(新版)华东师大版
编辑整理:
尊敬的读者朋友们:
这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(八年级科学上册第六章物质的构成第1节构成物质的微粒同步练习(扫描版,无答案)(新版)华东师大版)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为八年级科学上册第六章物质的构成第1节构成物质的微粒同步练习(扫描版,无答案)(新版)华东师大版的全部内容。
构成物质的微粒。

华师大版八上科学单元同步训练卷二十八(第1节构成物质的微粒)(I)卷一、选择题 (共20题;共41分)1. (2分)关于物质的组成,下列说法中错误的是()A . 原子是由原子核和核外电子组成B . 物质是由大量分子组成的C . 原子核由质子和中子组成D . 质子带负电,电子带正电2. (2分)下列关于分子和原子的说法,错误的是()A . 分子和原子都可以构成物质B . 由分子构成的物质,分子是保持其化学性质的最小粒子C . 在化学变化中,分子可以分成原子,原子又可以结合成新的分子D . 分子和原子之间都有间隔,分子之间间隔较大,原子之间间隔较小3. (2分)氧气在一定条件下变成淡蓝色液体,此过程中发生变化的是()A . 氧分子的体积B . 氧分子的间隔C . 氧气的化学性质D . 构成氧分子的原子4. (2分)物质是由原子、分子、离子等粒子构成的,有一粒子,其原子核内有16个质子、16个中子,原子核外有18个电子,该粒子是()A . 原子B . 阳离子C . 阴离子D . 分子5. (2分)有科学家研究发现,氧气可通过高能真空紫外线照射二氧化碳直接产生,该化学反应模型如图所示。
关于该反应的说法错误的是()A . 属于分解反应B . 反应中的最小微粒是分子C . 符合质量守恒定律D . 为制取氧气提供了新的方法6. (2分)一氧化碳和二氧化碳的化学性质不同的主要原因是()A . 分子的构成不同B . 密度不同C . 生成它们的反应条件不同D . 用途不同7. (2分)下列各图是气体微粒的示意图,图中“空心圆”和“实心圆”分别表示两种不同的原子,那么其中表示同种分子的是()A .B .C .D .8. (2分)下列微观示意图中和分别表示氢原子和氧原子,下列说法正确的是()A . 参加反应的是两种物质B . 反应物和生成物中只有一种单质C . 化学变化中原子可分D . 化学变化前后原子种类不变9. (2分)(2014·台州)汤姆生最早发现了原子中存在一种带负电荷的粒子,证明了原子是可以再分的。
第6章物质的构成6.1构成物质的微粒(一)[学生用书A52]1.下列微粒中不能构成物质的是(B)A.原子B.电子C.离子D.分子2.下列各组物质中,都是由分子构成的是(A) A.水、氢气B.铁、氧气C.氯化钠、铜D.氯化钠、水3.下列物质的分子模型可用“”表示的是(C) A.氮分子B.氯分子C.氯化氢分子D.甲烷分子4.下列物质中不是由原子直接构成的物质是(B) A.金刚石B.二氧化碳C.氦气D.铁5.原子和分子的根本区别是(B)A.大小不同B.在化学反应中能否再分C.能否保持物质的物理性质D.能否直接构成物质6.若用“”表示氢原子,用“”表示氧原子,则保持水的化学性质的粒子可表示为(C)A B C D7.下列关于分子、原子、离子的叙述错误的是(B)A.分子、原子、离子都可以构成物质B.分子都是由离子构成的C.原子呈电中性D.离子可以带正电荷和负电荷8.下列说法错误的是(D)A.原子不显电性B.在化学变化中能否再分是原子和分子的本质区别C.原子的质量主要集中在原子核上D.所有原子的原子核都含有中子和质子9.下列物质由离子构成的是(B)A.二氧化碳B.氯化钾C.铜D.氧气10.如图是分子结构模型示意图(图中“”“”分别表示两种不同的原子),其中表示两种物质混合的是(A)11.原子不是构成物质的最小微粒,它还能再分,原子是由带正电荷的__原子核__和带负电荷的__核外电子__构成的。
原子核在原子中所占的体积__极小__,核外电子在核外空间做__高速运动__。
通过实验,科学家们最终发现,原子核是由更小的两种粒子——__质子__和__中子__构成。
12.在原子中,核电荷数=__质子数__=__核外电子数__。
原子核和核外电子所带的电量大小相等,电性相反,因而原子呈电__中性__。
13.科学研究证实,物质是由微粒构成的,例如,铁是由铁原子构成的。
请你填写构成下列物质的具体微粒名称。
(1)家中铝合金窗户中的铝是由__铝原子__构成的。
第6章物质的构成__6.1__构成物质的微粒(一)__[学生用书A52]1.下列粒子微粒中不能构成物质的是(B)A.原子B.电子C.离子D.分子2.下列各组物质中,都是由分子构成的是(A)A.水、氢气B.铁、氧气C.氯化钠、铜D.氯化钠、水3.下列物质的分子模型可用“”表示的是(C)A.氮分子B.氯分子C.氯化氢分子D.甲烷分子4.下列物质中不是由原子直接构成的物质是(B)A.金刚石B.二氧化碳C.氦气D.铁5.原子和分子的根本区别是(B)A.大小不同B.在化学反应中能否再分C.能否保持物质的物理性质D.能否直接构成物质6.若用“”表示氢原子,用“”表示氧原子,则保持水的化学性质的粒子可表示为(C)7.下列关于分子、原子、离子的叙述错误的是(B)A.分子、原子、离子都可以构成物质B.分子都是由离子构成的C.原子呈电中性D.离子可以带正电荷和负电荷8.下列说法错误的是(D)A.原子不显电性B.在化学变化中能否再分是原子和分子的本质区别C.原子的质量主要集中在原子核上D.所有原子的原子核都含有中子和质子9.下列物质中,由带正、负电荷的离子构成的是(B)A.二氧化碳B.氯化钠晶体C.氢气D.银10.下图是分子结构模型示意图(图中“○”“●”表示两种不同的原子),其中表示两种物质混合的是(A)11.原子不是构成物质的最小微粒,它还能再分,原子是由带正电荷的__原子核__和带负电荷的__核外电子__构成的。
原子核在原子中所占的体积__极小__,核外电子在核外空间做__高速运动__。
通过实验,科学家们最终发现,原子核是由更小的两种粒子——__质子__和__中子__构成。
12.在原子中,核电荷数=__质子数__=__核外电子数__。
原子核和核外电子所带的电量大小相等,电性相反,因而原子呈电__中性__。
13.科学研究证实,物质是由微粒构成的,例如,铁是由铁原子构成的。
请你填写构成下列物质的具体微粒名称。
(1)家中铝合金窗户中的铝是由__铝原子__构成的。
第6章 物质的构成 复习检测卷[时间:90分钟 分值:120分]一、选择题(每小题2分,共40分)1.科学家合成了一种新型的氧分子,化学式为O 4,下列有关O 4的说法正确的是( C )A .O 4是一种化合物B .O 4是一种混合物C .O 4是一种单质D .O 4是一种氧化物2.碳-12是指含6个中子的碳原子。
下列有关氧-16和氧-18两种氧原子的说法正确的是( A )A .质子数相同B .质量相同C .电子数不相同D .16和18表示原子个数3.下列说法正确的是( A )A .由分子构成的物质在发生化学变化时,分子种类改变,原子种类不变B .离子是带电的原子或原子团,所以带电的微粒一定是离子C .构成固体物质的微粒都是静止不动的D .不同的氢原子属于不同的元素4.下列化学符号与表述的意义相符的是( C )A .Cl 2:2个氯原子B .Fe 2+:1个铁离子带2个单位的正电荷C .H 2O 2-1 :过氧化氢中氧元素显-1价D .NO 2:二氧化氮由1个氮原子和1个氧分子构成5”分别表示不同元素的原子,则其中表示单质的是( A )A. B. C. D.6.小金建立的有关物质宏观组成和微观构成的思维导图如图所示,其中“▲”处应填入的是(A)A.原子B.中子C.电子D.质子7.下列四种物质:①KClO3;②Cl2;③HCl;④HClO。
按氯元素的化合价由低到高的顺序排列的是(D)A.①②④③B.②③④①C.③②①④D.③②④①8.认真分析测定相对原子质量的示意图,推断A原子的相对原子质量约为(B)A.12B.16C.5D.109.下列关于晶体和非晶体的说法,正确的是(B)A.晶体和非晶体在熔化时都要吸热,且温度都保持不变B.晶体内部的物质微粒有规则地排列,而非晶体内部的物质微粒不规则地排列C.晶体内部的物质微粒是静止的,而非晶体内部的物质微粒是不停地运动的D.金刚石是晶体,石墨是非晶体10.以下关于纸上层析的叙述,错误的是(D)A.纸上层析法适用于分离和检验化学性质十分相近的分子或离子B.由于滤纸对被分离物质中各组分的吸附能力不同,使得相同时间内各组分在纸上移动的距离不同C.纸上层析法是利用试样中各种离子随展开剂在滤纸上展开的速度不同而形成不同位置的色斑D.为了看到色斑,只有有色离子的检验才可以用纸上层析法11.下列关于粗盐提纯的说法正确的是(C)A.用托盘天平准确称得11.25 g食盐B.粗盐经过溶解、过滤、蒸发、结晶后得到纯净的氯化钠C.当蒸发到有大量固体析出时,停止加热,利用余热将液体蒸干D.在粗盐提纯实验中还需要用到烧瓶和石棉网12.用微粒的观念学习科学有助于更好地认识物质的构成,下列有关说法错误的是(D )A.分子、原子、离子都是构成物质的微粒B.分子是由原子构成的,但分子不一定比原子大C.同一元素的原子和离子可以相互转化D.同一种原子只能构成一种分子13.下图为元素周期表的一部分,根据三种元素的相关信息,下列说法不正确的是(D )A.三种元素位于元素周期表的同一周期B.三种元素均属于非金属元素C.硫原子的质子数为16D.磷元素的相对原子质量为30.97 g14.正确使用化学用语是重要的科学学科素养。
6.1构成物质的微粒1.如图所示,向盛水的烧杯中放入一小粒品红,一段时间后,烧杯中形成红色溶液,此实验能说明:①分子处于不断运动之中②分子大,原子小③分子可再分,原子不能再分④分子之间有间隔()A.①②B.②③C.①③D.①④2.为了解释水电解的微观变化,小丽做了许多分子、原子模型,其中能表示水分子模型的是()A.B.C.D.3.卢瑟福的α粒子轰击金箔实验推翻了汤姆生在1903年提出的原子结构模型,为建立现代原子理论打下了基础。
如图线条中,可能是α粒子(带正电)在该实验中的运动轨迹的是()A.a b c d B.a b c C.b c d D.a d4.同种元素的原子和离子一定相同的是()A.质子数B.电子数C.最外层电子数D.电子层数5.下列结构示意图,表示阳离子的是()A.B.C.D.6.R2﹣离子核外共有n个电子,则R原子核内质子数为()A.n+2B.n﹣2C.n D.2n7.令X、Y、Z和R分别代表四种元素.若a X m+、b Y n+、c Z n﹣、d R m﹣四种离子的电子层结构相同(令a、b、c、d分别为四种元素的核电荷数),则下列关系正确的是()A.a﹣c=m﹣n B.a﹣b=n﹣m C.c﹣d=m+n D.b﹣d=n+m8.镭具有放射性,镭原子会分裂,变成一个质子数为86、中子数为136的氡原子和一个具有2个中子、2个电子的氦原子,并放出放射能.试推断镭原子的核电荷数与相对原子质量分别为()A.88,138B.86,140C.88,226D.84,1689.某工业盐酸中含有H+、Fe3+、Cl﹣,H+和Cl﹣的个数比为91:94,Cl﹣和Fe3+的个数比为()A.1:94B.3:94C.94:1D.94:3二.解答题(共3小题)10.初中化学学习中,我们初步认识了物质的微观结构.(1)氯化钠、金刚石、干冰三种物质中,由离子构成的物质是.(2)是某粒子的结构示意图,该粒子在化学反应中容易电子(填“得到”或“失去”),变成(填“阳”或“阴”)离子.(3)如图是CO与O2反应的微观示意图.反应前后没有发生变化的粒子是.(填序号)11.模型是联系宏观与微观的桥梁。
6.1构成物质的微粒同步自测
班级姓名得分
一、选择题
1.分子、原子和离子都是构成物质的粒子,下列物质由离子构成的是()A.汞 B.石墨 C.水 D.氯化钠
2.下列物质是由原子直接构成的是()
A.蒸馏水、二氧化碳 B.铁、干冰
C.氯化钠、氢气 D.铜或铝等
3.下列关于原子的说法中,正确的是()
A.原子不显电性,说明原子内的电子数等于中子数
B.原子是最小的粒子
C.原子的质量主要集中在原子核上
D.原子不能直接构成物质
4.下列关于原子的叙述正确的是()
①一切原子都是由质子、中子和电子构成的②原子在不停地运动③原子是化学变化中的最小拉子
④原子由原子核和核外电子构成⑤原子中不存在电荷,因而原子不带电。
A.②③④ B.①②④ C.①③⑤ D.①②③④⑤
5.对分子、原子、离子的下列认识,其中正确的是()
A.氢原子是最小的微粒,不可再分
B.镁原子的质子数大于镁离子的质子数
C.当液态水变成冰,水分子间不存在间隔
D.分子、原子、离子都可以直接构成物质
6.下面是4位同学对分子、原子、离子的认识,其中正确的是( )。
7.原子和分子的根本区别是()
A.大小不同 B.能否直接构成宏观物质
C.能否保持物质的化学性质 D.在化学反应中能否再分
8.保持二氧化碳化学性质的最小粒子是()
A.二氧化碳分子
B.碳原子和氧原子
C.碳分子和氧分子
D.碳原子
9.对分子、原子、离子的下列认识,其中正确的是()
A.氢原子是最小的微粒,不可再分
B.氧原子的质子数等于氧离子的质子数
C.当液态水变成冰,水分子间不存在间隔
D.只有分子可以直接构成物质
10.从分子的角度解释下列现象,错误的是()
A.汽油挥发--分子体积变大 B.花香四溢--分子不断运动
C.氢气燃烧--分子发生改变 D.一滴水约有1.67×1021个水分子-分子很小
二、填空题
11.在原子中,原子核所带______与核外______所带的______相等,______相反,因此整个原子______电性。
12.构成物质的微粒有______,其中______是保持物质化学性质的一种微粒,______是化学变化的最小微粒。
13.试用分子的有关性质解释下列问题,将序号填在横线上:
①分子的体积和质量都非常小②分子总是在不停地运动③分子间有一定的间隔④同种物质的
分子,化学性质相同
A.春天的校园,四处飘香______;
B.物质的“三态”变化______;
C.一滴水中含有数以亿计个水分子______;
D.水蒸发变成水蒸气后,化学性质不变______。
14.我们学过的微粒有许多如分子、离子、质子等,根据题目要求,具体填在空格上。
(1)铁是由______构成的.氯化钠是由_______和_______构成的。
(2)加热氧化汞时,______先分裂成______和______,再结合成新分子,从而说明化学变化中的最小粒子是______;
(3)显示电中性的微粒有______;带正电荷的微粒有______;带负电荷的微粒有______。
(各写一个)
15.水的三态发生变化,其实是构成水的间的发生了变化,而且这种变化与有关。
16.美国科学家将铅和氪的原子核对撞,获得了一种质子数为118.中子数为175的超重原子,该原子核内的中子数与核外电子数之差是。
和。
液态物质中,分子运动比较自由,粒子间的作用力比固体。
因此液体没有确定的形状,但具有。
气态物质中,分子间距大,所以容易被。
参考答案
1. D 汞和石墨都是原子构成的,水由水分子构成,氯化钠是由离子构成的。
3.C A.
原子不显电性,由于原子核所带的电量和核外电子所带的电量相等,电性相反,所以整个原子不显电性,故A错误;B.在化学变化中原子是最小的粒子,而不能说原子是最小的粒子,故B错误;
C.原子由原子核和核外电子构成,电子的质量很小可以忽略,所以原子的质量主要集中在原子核
上,故C正确;D.原子可以直接构成物质,例如金属铁就是由铁原子直接构成的。
4. A 有的原子核中没有中子,例如氢原子中没有中子所以①说法错误;原子和分子都时刻在不断
运动,所以②说法正确;在化学变化中分子分成原子,原子再重新组合成新的分子,所以说原子是化学变化中的最小粒子,所以③说法正确;原子由原子核和核外电子构成,所以④说法正确;
原子核中的质子带正电荷,核外电子带负电荷,所以⑤说法错误。
5. D A.氢原子尽管很小,但还可以再分,氢原子可由质子和电子构成,故A错误; B.原子在变
为离子时,变化的是核外电子,而质子数不变,故B错误; C.当液态水变成冰,说明水分子之间有间隔且间隔变小,故C错误; D.根据常见物质的构成,如水由分子构成,铁由原子构成,氯化钠由离子构成,则分子、原子、离子都可以直接构成物质。
6.B 分子、原子、离子都是构成物质的基本粒子,离子带电,但分子和原子不带电。
原子是化学变
化中的最小粒子,但分子在化学变化中可以再分,而离子可以得失电子变为原子。
分子是保持物质化学性质的最小粒子(由分子构成的物质)。
由原子构成的物质和由离子构成的物质,分别由构成它的原子或离子保持其化学性质。
8. A
分子构成的物质由分子保持化学性质,由原子构成的物质,胡子保持化学性质,离子构成的由离子保持化学性质,所以保持二氧化碳化学性质的最小粒子分子。
9.B A.氢原子是最小的微粒,不可再分,错误。
原子是最小粒子,只是在化学变化中这一前提条
件下,离开此前提,原子并不是最小的,它还可以分成质子、中子和电子;B.氧原子的质子数等于氧离子的质子数,正确,因为它们属于同种元素,质子数相同。
尽管他们的核外电子数不同,
但这并不影响元素种类;C.当液态水变成冰,水分子间不存在间隔,错误。
物质的分子间都有间隔,不论该物质处于何状态。
只是固体物质的分子间隔比液体或气体分子间隔小而已;D.分子、原子、离子都可以直接构成物质。
11. 正
电荷;电子;电量;电性;不显
12. 分子、原子和离子;分子;原子。
13. A ②;B ③;C ①;D ④.
14. (1)铁原子.钠离子、氯离子(2)氧化汞,氧原子、汞原子,原子(3)分子或原子;
质子或原子核;电子
15.水分子间隙温度
17.运动增大
18.固态液态气态变小体积形状小流动性压缩。