二氧化硅及硅酸的性质
- 格式:pptx
- 大小:2.78 MB
- 文档页数:33

硅和二氧化硅的结构-概述说明以及解释1.引言1.1 概述概述:硅是一个非金属元素,属于周期表中的第14族,原子序数为14,化学符号为Si。
它在自然界中广泛存在于矽酸盐和硅氧石等化合物中。
硅具有良好的导电性和光伏特性,因此在半导体器件、太阳能电池等领域有着广泛的应用。
同时,由硅与氧元素形成的化合物二氧化硅,也就是常说的硅石英,是一种重要的无机化合物,具有稳定的结构和优良的物理化学性质。
本文将探讨硅和二氧化硅的结构特点,以及它们在科学研究和工业应用中的意义。
1.2 文章结构本文主要分为引言、正文和结论三部分。
在引言部分中,我们将对硅和二氧化硅的重要性进行概述,介绍本文的目的和意义,以及文章的整体结构安排。
在正文部分,我们将首先深入探讨硅的结构,包括其原子结构、物理性质和化学性质,以便读者了解硅的基本特性。
接着,我们将详细讨论二氧化硅的结构,包括其分子结构、结晶结构以及在不同应用领域中的应用情况。
最后,在结论部分,我们将总结硅和二氧化硅的结构特点,探讨它们在科学研究和工业应用中的重要性,同时展望未来的研究方向,为读者提供对这一领域的更深入了解和思考。
1.3 目的本文旨在深入探讨硅和二氧化硅的结构特点,分析其原子、分子和结晶结构,探讨其物理性质和化学性质。
通过对硅和二氧化硅结构的详细描述和分析,旨在帮助读者更深入地理解这两种物质在科学研究和工业应用中的重要性和价值。
同时,本文还将展望硅和二氧化硅在未来可能的研究方向,为相关领域的科研工作者提供一定的参考和启示。
通过本文的阐述,希望能够激发更多对硅和二氧化硅结构的研究和探索,推动相关领域的发展和进步。
2.正文2.1 硅的结构硅是地球上最丰富的元素之一,它的原子序数为14,电子排布为2, 8, 4。
在周期表中,硅位于第三周期、14族元素。
硅的原子结构具有四个价电子,因此每个硅原子可以形成四个共价键。
硅原子通过共价键形成硅晶体,硅晶体的晶格结构为菱面体结构。
硅的物理性质表现为高硬度、高熔点、高电阻率等特点。



考点13 硅和二氧化硅【考点定位】本考点考查硅和二氧化硅的性质与应用,明确二氧化硅是酸性氧化物,但能溶于HF酸的特殊性、硅的半导体性质及二氧化硅作光导纤维的应用。
【精确解读】1.硅的物理性质和化学性质:(1)物理性质:晶体硅是灰黑色,有金属光泽,硬而脆的固体,它的结构类似金刚石,具有较高的沸点和熔点,硬度也很大,它的导电性介于导体和绝缘体之间,是良好的半导体材料.(2)化学性质:化学性质不活泼①常温下,除与氟气、氢氟酸及强碱溶液反应外,与其他物质不反应Si+2F2═SiF4、Si+4HF═SiF4↑+2H2↑、Si+2NaOH+H2O═Na2SiO3+2H2↑;②在加热条件下,能与氧气、氯气等少数非金属单质化合Si+O2△SiO2、Si+2Cl2△4;(4)制备:在电炉里用碳还原二氧化硅先制得粗硅SiO2+2C 高温Si+2CO↑,将制得的粗硅,再与Cl2反应后,蒸馏出SiCl4,然后用H2还原SiCl4可得到纯硅.有关的反应为:Si+2Cl2△SiCl4,SiCl4+2H2高温Si+4HCl;2.硅的用途:高纯硅可作半导体材料,制造集成电路、晶体管、硅整流器等半导体器件,还可以制造太阳能电池.硅的合金用途也很广,如含硅4%的钢具有良好的导磁性,可用来制造变压器的铁芯;含硅15%左右的钢具有良好的耐酸性,可用来制造耐酸设备.3.二氧化硅的物理性质和化学性质:(1)物理性质:无色透明或白色粉末,原子晶体,熔沸点都很高,坚硬难熔,不溶于水,天然的二氧化硅俗称硅石,是构成岩石的成分之一.(2)化学性质:常温下性质不活泼;①不与水反应,不能跟酸(氢氟酸除外)发生反应.SiO2+4HF═SiF4↑+2H2O(氢氟酸不能盛放在玻璃容器中);②具有酸性氧化物的性质,能跟碱性氧化物或强碱反应,SiO2+2NaOH═Na2SiO3+H2O (实验室中盛放碱液的试剂瓶用橡胶塞而不用玻璃塞的原因)CaO+SiO 2高温CaSiO 3、Na 2CO 3+SiO 2高温Na 2SiO 3+CO 2↑(制玻璃)③具有弱氧化性 SiO 2+2C高温Si+2CO↑、SiO 2+2Mg高温Si+2MgO↑,SiO 2+3C高温SiC(金刚砂)+2CO↑;(3)二氧化硅的用途:①光导纤维的主要原料;②石英的主要成分是SiO 2,纯净的石英可用来制造石英玻璃;③玛瑙石含有有色杂质的石英晶体,可用于制造精密仪器轴承,耐磨器皿和装饰品。

第1课时二氧化硅和硅酸[学习目标定位] 1.了解硅在自然界中的存在形式,硅酸盐产品的组成和重要用途。
2.了解二氧化硅的结构、性质和用途。
3.了解硅酸的制备、性质和应用。
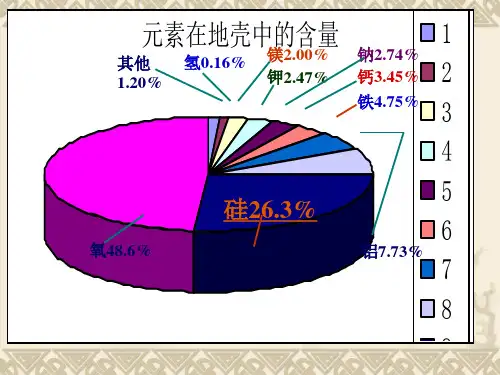
一二氧化硅1.硅元素在地壳中的含量是26.3%,仅次于氧。
硅元素在自然界中主要以氧化物及硅酸盐的形式存在,原因是硅是一种亲氧元素。
2.硅的氧化物为二氧化硅,俗名为硅石,天然二氧化硅分为结晶形(如方石类、水晶等)和无定形(如硅藻土)。
根据日常生活中的实例描述二氧化硅的物理性质:坚硬固体、不溶于水、熔点高。
3.列表比较二氧化碳和二氧化硅的性质。
CO2+H2O H2CO3归纳总结二氧化硅的结构与性质(1)二氧化硅与二氧化碳的物理性质差异较大的原因是物质晶体结构不同。
二氧化硅晶体结构如图:二氧化硅晶体是由Si原子和O原子按1∶2的比例所组成的立体网状结构的晶体。
(2)二氧化硅的化学性质有稳定性强,与水、一般酸不反应,能与氢氟酸反应,能与碱、碱性氧化物反应。
1.下列叙述中,正确的是()A.自然界中存在大量的单质硅B.石英、水晶、硅石的主要成分都是二氧化硅C.二氧化硅的化学性质活泼,能跟酸或碱溶液发生化学反应D.自然界中硅元素都存在于石英中答案B解析自然界中硅元素含量很高,但都以化合态形式存在,A项错误;硅元素是亲氧元素,主要以氧化物和硅酸盐的形式存在,D项错误;二氧化硅的性质稳定,C项错误。
2.由MgO、Al2O3、SiO2、Fe2O3组成的混合粉末。
现取两份该混合粉末试样进行实验。
(1)将一份混合粉末溶于过量的盐酸,得到沉淀X和滤液Y,沉淀X为________,滤液Y中含有的阳离子主要是______________,向滤液Y中加入过量NaOH溶液,得到的沉淀是____________________。
(2)将另一份混合粉末溶于过量NaOH溶液,发生反应的离子方程式为_________________。
答案(1)SiO2Al3+、Mg2+、Fe3+、H+Mg(OH)2、Fe(OH)3(2)SiO2+2OH-===SiO2-3+H2O、Al2O3+2OH-===2AlO-2+H2O二硅酸1.硅酸的制备:按表中实验操作要求完成实验,并将观察到的实验现象及有关结论填入表中:2.写出上述实验中反应的化学方程式。


二氧化硅与偏硅酸
二氧化硅是一种无机物,化学式为SiO₂,是一种酸性氧化物,对应水化物为硅酸。
它不溶于水,也不与水起化学反应,是一种酸性氧化物,只能和碱类物质反应,从而生成盐和水。
偏硅酸是一种二元酸,化学式为H2SiO3。
它在高温下不稳定,容易分解为二氧化硅和水。
在低温下稳定,但在水中几乎不溶。
偏硅酸可以与碱类物质反应生成硅酸盐和水,如偏硅酸钠、偏硅酸镁等。
在特定条件下,二氧化硅与水会部分生成偏硅酸和硅酸。
这过程较为复杂,与特定溶液的酸碱性及浓度有关。
总的来说,二氧化硅与偏硅酸是两种不同的物质,但它们之间存在一定的联系。
如需更多信息,建议查阅相关文献或咨询化学专家。


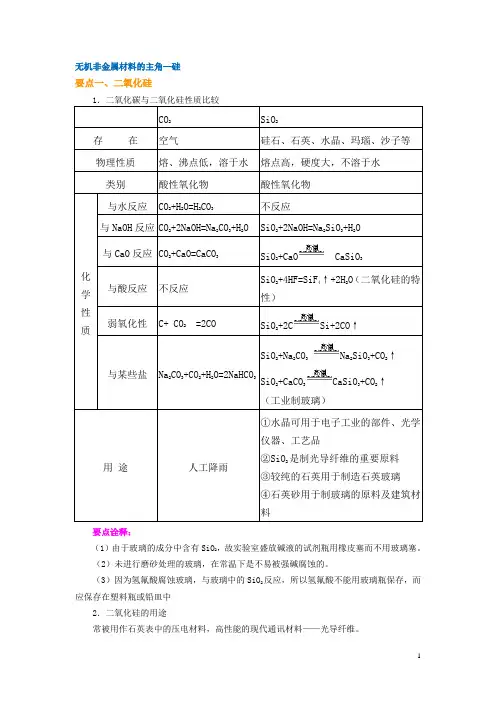
无机非金属材料的主角—硅要点一、二氧化硅NaCaSiO要点诠释:(1)由于玻璃的成分中含有SiO2,故实验室盛放碱液的试剂瓶用橡皮塞而不用玻璃塞。
(2)未进行磨砂处理的玻璃,在常温下是不易被强碱腐蚀的。
(3)因为氢氟酸腐蚀玻璃,与玻璃中的SiO2反应,所以氢氟酸不能用玻璃瓶保存,而应保存在塑料瓶或铅皿中2.二氧化硅的用途常被用作石英表中的压电材料,高性能的现代通讯材料——光导纤维。
3.二氧化硅的结构特点在SiO2晶体中,每个Si周围结合4个O,Si在中心,O在4个顶角;许多这样的四面体又通过顶角的O相连接,每个O为两个四面体所共有,即每个O与2个Si相结合。
实际上,SiO2晶体是由Si和O按1∶2的比例所组成的立体网状结构的晶体。
由结构可知,二氧化硅的化学性质很稳定。
要点二、硅酸1.硅酸的性质硅酸是一种白色胶状物质,不溶于水,能形成胶体。
硅酸经干燥脱水形成硅酸干凝胶——“硅胶”。
硅酸的酸性很弱,比碳酸的酸性还弱,在与碱反应时只能与强碱反应。
如:H2SiO3+2NaOH=Na2SiO3+2H2O。
硅酸的热稳定性很差,受热分解为SiO2和H2O。
2.硅酸的制取由于SiO2不溶于水,所以硅酸是通过可溶性硅酸盐与其他酸反应制得的。
Na2SiO3+2HCl=H2SiO3↓+2NaCl,Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3(证明酸性:H2CO3>H2SiO3)。
要点三、硅酸盐1.硅酸盐是由硅、氧和金属元素组成的化合物的总称。
一般不溶于水,稳定性高。
它是构成岩石和土壤的主要成分,硅酸盐的种类很多,结构也很复杂,通常用氧化物的形式来表示其组成。
例如:硅酸钠Na2SiO3(Na2O·SiO2),高岭石Al2Si2O5(OH)4(Al2O3·2SiO2·2H2O)。
书写顺序为:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水。
注意事项:(1)氧化物之间以“·”隔开;(2)计量数配置出现分数应化为整数。
硅及其化合物硅元素在地壳中的含量排第二,在自然界中没有游离态的硅,只有以化合态存在的硅,常见的是二氧化硅、硅酸盐等。
硅原子最外层有4个电子,既不易失去电子又不易得到电子,主要形成四价的化合物。
1、单质硅(Si):⑴物理性质:有金属光泽的灰黑色固体,熔点高,硬度大。
⑵化学性质:①常温下化学性质不活泼,只能跟F2、HF和NaOH溶液反应。
Si+2F2=SiF4Si+4HF=SiF4↑+2H2↑Si+2NaOH+H2O=Na2SiO3+2H2↑②在高温条件下,单质硅能与O2和Cl2等非金属单质反应。
Si+O2高温SiO2Si+2Cl2高温SiCl4⑶用途:太阳能电池、计算机芯片以及半导体材料等。
⑷硅的制备:工业上,用C在高温下还原SiO2可制得粗硅。
SiO2+2C=Si(粗)+2CO↑ Si(粗)+2Cl2=SiCl4SiCl4+2H2=Si(纯)+4HCl2、二氧化硅(SiO2):⑴SiO2的空间结构:立体网状结构,SiO2直接由原子构成,不存在单个SiO2分子。
⑵物理性质:熔点高,硬度大,不溶于水。
⑶化学性质:SiO2常温下化学性质很不活泼,不与水、酸反应(氢氟酸除外),能与强碱溶液、氢氟酸反应,高温条件下可以与碱性氧化物反应:①与强碱反应:SiO2+2NaOH=Na2SiO3+H2O(生成的硅酸钠具有粘性,所以不能用带磨口玻璃塞试剂瓶存放NaOH溶液和Na2SiO3溶液,避免Na2SiO3将瓶塞和试剂瓶粘住,打不开,应用橡皮塞)。
②与氢氟酸反应[SiO2的特性]:SiO2+4HF=SiF4↑+2H2O(利用此反应,氢氟酸能雕刻玻璃;氢氟酸不能用玻璃试剂瓶存放,应用塑料瓶)。
③高温下与碱性氧化物反应:SiO2+CaO 高温CaSiO3⑷用途:光导纤维、玛瑙饰物、石英坩埚、水晶镜片、石英钟、仪器轴承、玻璃和建筑材料等。
3、硅酸(H2SiO3):⑴物理性质:不溶于水的白色胶状物,能形成硅胶,吸附水分能力强。
硅及其化合物知识总结1.硅单质(Si)(1)存在:硅是一种亲氧元素,在自然界中以化合态存在,在地壳中的含量仅次于氧。
(2)物理性质:晶体硅是灰黑色固体,硬度大,熔、沸点高,具有金属光泽。
(3)化学性质:常温下能与F 2、HF 、NaOH 反应;加热时能与H 2化合生成不稳定的氢化物SiH 4,还能与Cl 2、O 2化合分别生成SiCl 4、SiO 2。
涉及的化学方程式如下:2:Si +O 2=====△SiO 22:Si +2F 2===SiF 42:Si +2Cl 2=====△SiCl 4②与氢氟酸反应:Si +4HF===SiF 4↑+2H 2↑。
③与NaOH 溶液反应:Si +2NaOH +H 2O===Na 2SiO 3+2H 2↑(4)用途:①良好的半导体材料;②太阳能电池;③计算机芯片。
(5)高纯硅的制备①SiO 2+2C=====高温Si(粗)+2CO ↑(1800~2000℃)②③2.二氧化硅(SiO 2)(1)存在与形态SiO 2的存在形态有结晶形和无定形两大类。
自然界中的二氧化硅,存在于沙子、水晶、玛瑙,石英等中。
(2)结构SiO 2是由Si 原子和O 原子按个数比1∶2直接构成的立体网状结构的晶体。
(3)二氧化硅与二氧化碳都是酸性氧化物,二者的性质与用途比较性质与用途二氧化硅二氧化碳物理性质硬度大,熔、沸点高,不溶于水熔、沸点低,可溶于水化学性质与水反应不反应CO 2+H 2OH 2CO 3与酸反应(只与HF 反应)氢氟酸用于刻蚀玻璃:SiO 2+4HF===SiF 4↑+2H 2O不反应与碱反应(如NaOH)SiO 2+2NaOH===Na 2SiO 3+H 2O(盛碱液的试剂瓶不能用玻璃塞)CO 2+2NaOH===Na 2CO 3+H 2O 或CO 2+NaOH===NaHCO 3与盐反应(如Na 2CO 3)SiO 2+Na 2CO 3=====高温Na 2SiO 3+CO 2↑CO 2+Na 2CO 3+H 2O===2NaHCO 3与碱性氧化物反应与CaO 反应:SiO 2+CaO=====高温CaSiO 3与Na 2O 反应:CO 2+Na 2O===Na 2CO 3与碳反应2C +SiO 2=====高温Si +2CO ↑C +CO 2=====高温2CO 主要用途制光学仪器、石英玻璃;水晶和玛瑙可制作饰品;常用来制造通讯材料——光导纤维;以SiO 2为主要成分的沙子是基本的建筑材料化工原料、灭火剂;干冰用作制冷剂,人工降雨3.硅酸(H 2SiO 3)(1)物理性质:难溶于水的白色胶状物质。
硅酸的性质1、基本信息化学品名称:硅酸(H2SiO3) 英文名称:Silicic acid CAS NO:7699-41-4分子量:78.09958 密度:2.1~2.3 g/cm3 性状:硅酸为玻璃状无色透明的不规则颗粒,不溶于酸(氢氟酸除外),溶于苛性碱溶液。
和硅胶相比含有较多羟基,是一种高纯试剂硅胶。
加热到150℃分解为二氧化硅。
与氢氟酸激烈反应并分解。
化学性质:1、弱酸性Na2SiO3+CO2+H2O==Na2CO3+H2SiO3↓ 可说明酸性H2SiO3<H2CO3,又可说明Na2SiO3溶液应密封保存。
2、不稳定性H2SiO3==加热==H2O+SiO22、生产方法硅酸结构式制备:盐酸和硅酸钠反应可生成硅酸(酸性强于硅酸的酸和硅酸盐)反应方程式:Na2SiO3+2HCl==2NaCl+H2SiO3↓ (强酸换弱酸)电离平衡常数K1=2.2*10-10(30℃)注意:硅酸是原硅酸脱水而生成的,原硅酸是Si(OH)4,或写成H4SiO4,硅酸是H2SiO3硅酸盐酸和Na2SiO3溶液起反应时生成白色胶状沉淀,这种白色胶状物沉淀叫做硅酸(H2SiO3)工业上采用硫酸法。
即将硅酸钠与硫酸反应生成硅溶胶,经凝聚、洗涤、干燥和浓盐酸浸泡,再经洗涤、干燥而得。
3、应用领域用于气体及蒸汽的吸附,油脂、蜡的脱色,催化剂及其载体的制备。
用于生产钨丝的溶剂,分析化学上的化学试剂、接触剂和色谱分离的吸附剂,制造硅胶和硅酸盐的原料。
在分析化学中能将不溶性氟化物如氟化钙、氟化铝转化为可溶性溶液,进行氟的测定。
编辑本段硅酸盐所谓硅酸盐指的是硅、氧与其它化学元素(主要是铝、铁、钙、镁、钾、钠等)结合而成的化合物的总称。
它在地壳中分布极广,是构成多数岩石(如花岗岩)和土壤的主要成分。
由于其结构上的特点,种类繁多(硅酸盐矿物的基本结构是硅――氧四面体;在这种四面体内,硅原子占据中心,四个氧原子占据四角。
这些四面体,依着四面体,依着不同的配合,形成了各类的硅酸盐)。
二氧化硅制硅酸二氧化硅是日常生活所熟悉的一种矿物质,也是一种非金属非金属化合物,其具有众多独特性能,而硅酸是以二氧化硅为原料制备的一种碱性水溶液,在化学反应中可以起到控制反应中化学反应速率的作用,而且其应用范围也极其广泛。
一、二氧化硅的性质二氧化硅是由二氧化硅分子组成的无机化合物,其分子表面具有圆柱形晶体结构,每个二氧化硅分子中都有一个硅原子与两个氧原子键合而成,它的分子式为SiO2,通常形成白色粉末状的无机物质,它的熔点约为1710℃,比重为2.195-2.653,溶解性较差,在水中不易溶解,但可以溶解在硝酸、硫酸、盐酸等强酸和盐中,也可以溶解在有限的硫酸锌溶液中,并具有良好的化学稳定性,不容易被氧化、水解或分解,被看做是最基本的硅酸盐,也是工业应用最多的硅酸盐之一。
二、硅酸的制备硅酸可以以二氧化硅为原料,采用两种不同的方法进行制备。
1.吸湿剂吸收空气中的水分,然后在此时加入有机酸,经由醇和醋酸来分解合成硅酸,可以制成较稳定的混合溶液;2.二氧化硅和强酸,如硝酸和硫酸,经加热分解合成硅酸,当反应温度较高时,可以制得硅酸晶体;在实际过程中,制备硅酸时,必须同时温控和控制反应时间,以免硅酸中的某些成分被氧化或水解,从而影响制备的硅酸的质量。
三、硅酸的应用硅酸的应用大致可分为工业和生活两个领域,诸如陶瓷,洗衣粉,金属材料,精密仪器,制药原料,人造晶体,锂离子电池,肥皂,汽车刹车油等,其应用都极其广泛。
1.陶瓷行业,硅酸是制作高温耐火性陶瓷材料的重要原料,可制作出多种耐火性陶瓷器皿;2.洗衣粉行业,硅酸可以提供洗涤服务,可抑制污渍,具有良好的洗涤效果,还可以保护衣物色彩,因此,大部分洗衣粉都会加入硅酸;3.金属行业,硅酸可以抑制金属材料的腐蚀性,还可以维护金属材料的表面光泽;4.制药行业,硅酸可以改善药物的生物利用率,保护药物的安全性,还可以抑制药物的氧化性,有效抑菌;5.汽车刹车液行业,硅酸可以防止刹车液的氧化,保护刹车液的性能,还可以有效抑制碳烟沉积;6.人造晶体行业,硅酸可以作为重要的辅助剂,在熔融中起到促进熔融的作用,减少熔融粘块,提高晶体结晶的效果。