无机化学 铂系元素及其化合物 PPT课件
- 格式:ppt
- 大小:1.24 MB
- 文档页数:10





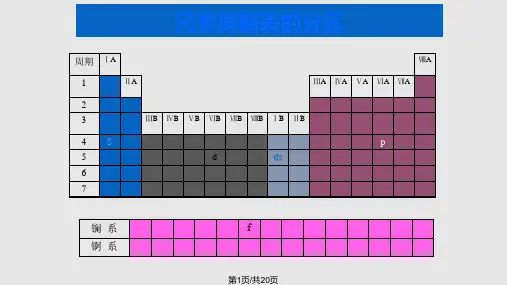


铂系元素铂系元素5周期Ru Rh Pd 价电子构型4d75s1 4d85s1 4d10稳定氧化数+4 +3 +2 最高氧化数+8 +6 +4 6周期Os Ir Pt 价电子构型4f145d66s2 4f145d76s2 4f145d96s1 稳定氧化数+8 +3、+4 +2、+4 最高氧化数+8 +6 +6 以单质状态存在,最重要的有铂矿、锇铱矿。
大多数能吸收气体, 其中钯吸氢能力最大(溶解氢的体积比为1:700) 有催化性能如 Pt-Rh 合金或Pt-Ru-Pd 合金为氨氧化制硝酸的催化剂高的化学稳定性铂系元素的单质Ru 、Rh 、Ir 、OsPd 、Pt不溶解 反应高温 不反应 溶解常温 王水非金属(氧、硫、氯等) 3Pt+4HNO 3+18HCl =3H 2[PtCl 6]+4NO+8H 2O铂金之美•因"铂"由"金"和"白"两字组合,颜色又为银白色,故亦称“白金”。
色泽银白,金属光泽,硬度4~4.5, 相对密度为21.45。
熔点高,为1773℃。
富延展性,可拉成很细的铂丝,轧成极薄的铂箔。
化学性质极稳定,不溶於强酸强缄,在空气中不氧化。
广泛用於珠宝首饰业和化学工业中,用以制造高级化学器皿、铂金坩锅以及加速化学反应速度的催化剂等。
Pd的储氢功能•钯单质有极强的吸氢能力。
•Graham在1866年报道,钯在从红热逐渐冷却时能够吸收多达935倍于其自身体积的氢。
•钯即使吸收了大量的氢也不会丧失其延展性,这在所有金属里都是独一无二的。
Pt和Pd的重要化合物1氯铂酸及其盐氯铂酸Pt + 4HNO3 + 18HCl = 3H2[PtCl6] + 4NO↑+ 8H2O PtCl4 + 2HCl = H2[PtCl6]Pt (OH)4 + 6HCl = H2[PtCl6] + 4H2O铂酸盐Pt (OH)4 + 2NaOH = Na2[Pt(OH)6]PtCl4 + 2NH4Cl = (NH4)2[PtCl6]PtCl4 + 2KCl = K2[PtCl6] (黄色)K2[PtCl6] +2KBr = 2KCl + K2[PtBr6] (深红) K2[PtCl6] +2KI = 2KCl + K2[PtI6] (黑色)Pt 和Pd 的重要化合物2 氯钯酸及其盐氯钯酸 H 2[PdCl 6]只存在于溶液中,若将其溶液蒸干,可得H 2[PdCl 6]或PdCl 2。
