器械包装操作流程图
- 格式:doc
- 大小:45.00 KB
- 文档页数:5


灭菌物品装放时应注意哪些要点消毒供应中心是对整个医院所使用器械进行消毒的地方,是相对重要的地方。
它可以有效确保治疗工具的无菌性,确保使用安全,下面我们就详细了解一下,在消毒供应中心中灭菌物品该如何包装和存放:一、包装:1、设备和布料应装在不同的房间里。
2、包装工应首先检查包装的质量,在光照下检查准备是否良好,并使用干净、干燥(纺织类)的包装布,不得有损伤。
3、封隔器应重新检查设备的型号、规格、数量,拆下的设备应进行组装,检查内容是否完整,只有确保设备齐全后才能包装。
4、盆、碗和其他用具应分开包装。
如剪刀和钳子等轴向器械不能完全锁定。
打开有盖的容器,用吸湿布、纱布或医用吸水纸将堆放的容器隔开;将官腔内物品盘绕放置,保持官腔通畅;对精细器械等采取防护措施。
5、细菌物品的包装采用封闭式包装,用双层包装材料分两次包装。
密封包装,如采用纸袋、纸塑袋等材料,可采用单层包装设备。
6、包装质量:仪表包装重量不超过7kg,敷料包装重量不超过5kg。
灭菌包装的体积不得超过30cm×30cm×50cm。
7、包装后,每个包装上应贴上灭菌化学指示物。
封闭包装应采用专用胶带,胶带长度应与灭菌包装的体积和重量相适应,松紧适度。
包装应严密,保持封口完整。
在高危险品的灭菌包装中还应放置化学指示卡。
8、灭菌物品的包装标签应标明物品名称、包装机等,灭菌前应注明灭菌批次、灭菌日期和有效期,标识应具有可追溯性。
二、规范手术器械包装过程1、专用设备的包装流程图和照片专用设备的包装流程图和照片,将相关设备的名称、设备的数量、设备的类型,合适的包装方法、有规律的包装顺序进行专用设备单独标记和命名,这样一来有利于供应中心护士能够尽早熟悉消毒供应中心内的布局。
2、手术器械和手术敷料的独立包装为避免超重和不符合规则的包装,请分开包装手术器械和手术敷料。
在外科手术包装之前,请根据外科器械包装卡再次确认设备的类型和数量,并使用无纺布将包装封闭,可实行需要两层包装的材料分两次进行包装。

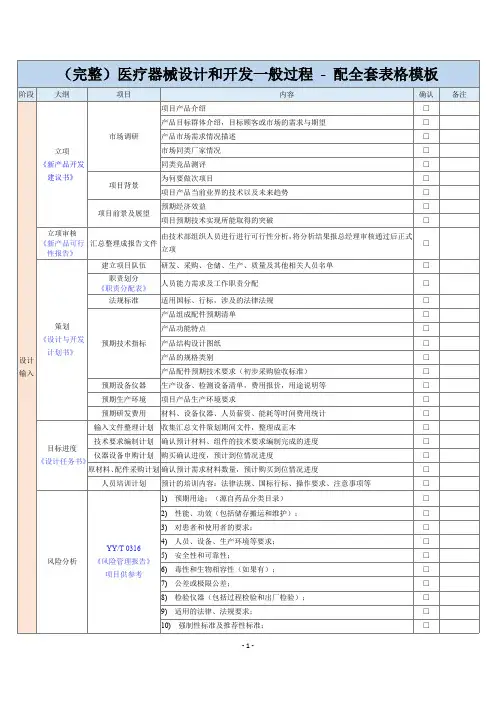
项目建议书表单编号:提出部门建议人项目名称型号规格销售对象建议日期基本要求(包括主要功能、性能、结构、外观包装、技术参数说明等):市场预测分析(包括市场现状、目标顾客或市场的需求与期望):同类厂家情况、同类竞品测评:项目前景及展望:总经理批示:签名:日期:新产品可行性报告表单编号:项目名称(中文):项目申请人:项目编号:项目概述:(产品简述、预计研发周期等)国标、行标、现有技术标准,涉及的法律法规:现有设备和拟定须添置的新机器或设施:现有人员配备和预期需增加人员:原材料、配件等技术标准和市场行情:此项目的潜在困难、挑战及解决方案:设计与开发计划书项目编号:项目名称:项目组长:项目计划表表单编号:项目名称项目编号RZ/YF-02-002新产品可行性报告F-YF-01-02-002设计完成时间项目产品设计输入F-YF-04-02-002预计试产时间项目组长主要开发人员产品工作原理及预期用途:资源配备需增购生产设备:需增购检测设备:经费预算:原材料、配件确认预计材料:技术要求:项目小组组建:项目小组成员:需增加人员:预期生产、检测环境:法律、法规、国标、行标、操作要求:附件职责分配表表单编号:设计开发阶段的划分及主要内容负责人主要部门完成期限新产品立项市场可行性调研报告评估和规划阶段新产品可行性报告设计和开发输入阶段产品结构方案设计风险分析设计和开发输入评审设计和开发输出阶段产品图样工艺文件检验规程包装图样设计设计和开发输出评审设计转换阶段样品试制设计验证阶段样品检测型式检验试制小结设计确认阶段临床评价设计更改产品注册阶段产品注册产品批量生产、投放市场产品的改进和投产,上市后的风险管理评审会议职责说明:1.设计评审的目的:发现潜在的不确定因素,或者已经知道的不足,然后采取措施,跟踪和解决这些问题,使评审对象最后具有能力满足要求。
a)设计输入的评审资料:应包括但不限于市场调研报告、新产品可行性报告、产品评估报告、涉及的法律法规。



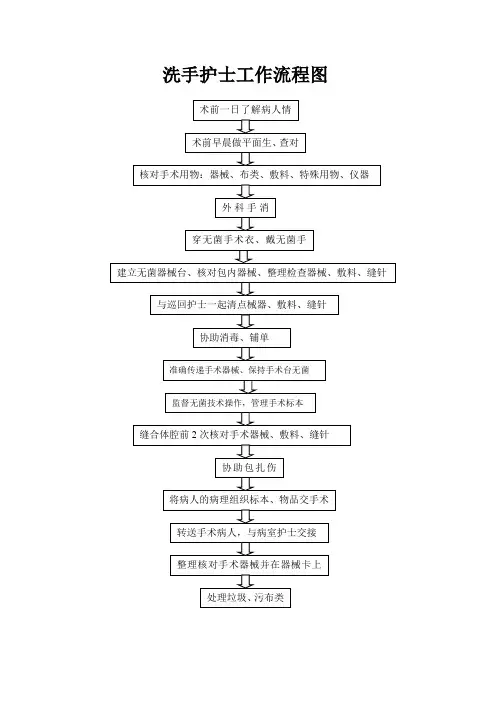
洗手护士工作流程图巡回护士工作流程图留置针穿刺操作流程图外科手消毒操作流程图穿无菌衣、戴无菌手套操作流程图手术器械清点流程图手术中取血、输血流程图腹腔镜操作流程图高频电刀操作流程图手术室医疗回收处理流程图内镜器械清洗流程图内镜器械包装流程图过氧化氢等离子体低温灭菌器操作流程图手术中缺失物品查找流程1、洗手护士、巡回护士2次核对后确认发生手术物品缺失事件。
2、通知手术医生、麻醉师暂停手术。
3、根据缺失物品类别及发现缺失时段,估计物品可能遗留的区域,分区域查找,洗手护士查找无菌区,手术医生探查切口,巡回护士查找手术间。
4、未及时发现则报告护士长,由其主持全方位查找。
(1)查找手术间内敷料单褶皱内、地面、垃圾桶、料料筐、标本袋、吸引器瓶。
(2)查找与手术间相通的辅助间、刷手间、器械间、准备间,外走廊(3)如缝针等金属器械,可显影敷料缺失寻查:①电话通知放射进行照X片。
②X线结果显示若在切口内,手术医生探查取出;未在切口内,关闭切口,在其它区域继续查找。
(5)手术医生探查、体腔。
(6)与曾进入手术室的相关手术的员、麻醉师沟通,是否取用或将其带出手术间。
5、巡回护士在手术护理记录单上书写事件发生经过及物品未在切口骨的证实结果,由手术医生签字。
6、发现但查找超过30分钟或最终未发现缺失物品的,填写工作缺陷报告单,详细记录事件发生、查找的过程、时间、结果等作为后期责任认定依据。
7、手术室统一保存工作缺陷报告单。
手术中缺失物品查找流程图手术护理不良事件报告及处理流程1判断手术护理不良事件:手术病人识别错误、手术部位错误、手术病人跌倒、用药错误、输血及输液意外、手术病人约束意外、意外针刺伤、管道意外脱落、药物不良反应、其他需要报告的意外事例。
2发生手术护理不良事件后,当事人应第一时间报告护士长;护士长了解情况后立即报告护理部主任,严重不良事件由护理部主任报告相关主管部门,如分管护理院长、医务科。
3妥善保管不良事件的各种记录、检验报告,对造成不良事件的药物、储血袋,输液瓶、器具等,医患双方共同封存并签字。

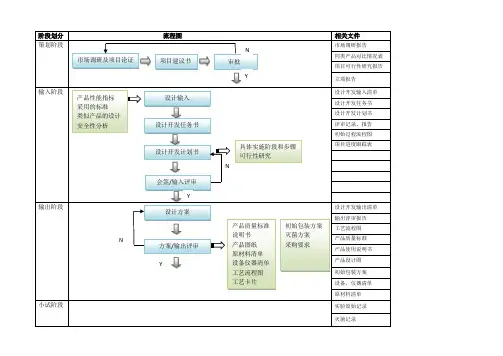
医疗器械项目开发设计流程图详图精品文档-可编辑
阶段划分
策划阶段
市场调研及项目论证
产品性能指标
采用的标准
类似产品的设计
安全性分析
流程图
XXX
项目建议书审批
XXX
设计输入
相关质量记录
市场调研报告
同类产品对比情况表项目可行性研究报告立项报告
设计开发输入清单设计开发任务书
设计开发计划书
作业文件
记录操作规程
工艺流程
产品质量标准
使用说明书
安全防护规定
输入阶段
设计开发任务书
具体实施阶段和步骤
可行性研究
XXX
会签/输入评审
XXX
评审记录、报告
初始过程流程图
项目进度跟踪表
设计开发输出清单
输出评审报告
设计开发计划书
输出阶段
设计方案
产品格量尺度说明书
产品图纸
原材料清单设备仪器清单工艺流程图初始包装方案灭菌方案
采购要求
合格证、
装箱单
工艺流程图
产品质量标准产品使用说明书产品设计图
初始包装方案设备、仪器清单原材料清单XXX
方案/输出评审XXX
小试阶段
尝试原始记录
精品文档-可编辑小样研制
加速老化测试包装运输测试性能检测
内毒素测定
重要性能测试
小试评审
XXX
中试阶段
软件:试产方案
岗位操作规程
包装、灭菌工艺
硬件:人员
原辅料
生产、检验设备
灭菌记录尝试室管理制度
尝试室生物平安规章制度
尝试室样品管理制度
配液等实验标准操作规程不合格品管理规程
不合格品销毁管理规定。

腹腔镜器械的使用流程(以胆囊手术为例)术前准备:1、术前擦拭并检查腹腔镜仪器及二氧化碳钢瓶,并调试到正常状态备用。
2、病人取平卧位,右上肢开通液路、外展固定;左上肢邦袖带,襁褓约束法固定(以利术者操作)3、备电刀脚踏,必要时备温盐水。
4、器械护士备敷料包×1 中单包×1 开胶洞巾×1手术衣包×1 LC器械×1 大开胶器械(防中转开胶用)腹腔镜专用器械×1套→由器护从消毒机中无菌技术取出5、备一次性物品:保护套×2、11#刀×1、7×10敷贴×3或4、钛夹×1、50ml注射器×1、吸引器×1(不带头)、其余同常规手术术中:1、开机程序○1摄像机:接通电源→连接摄像头→开机→连接手术台上的腹腔镜镜子→拉下保护套○2冷光源:接通电源→开机→连接冷光源线到镜子上→拉下保护套→开灯→据医生使用要求,调节亮度(一般调至光源1/3即可,防止产热过大)○3气腹机:接通电源→开机→打开CO2气瓶开关、自检、待显示屏上均显示“O”为止→设定流量(一般10—18升/分)与压力(一般12—14mmHg)→按T(低流量)开关,充气至0.6—0.7时再按H,术中当压力超过预设界限时,即停止充气。
(注意:流量、压力预设后有记忆功能,再次开机,仍会出现上次的数字,请按医生要求调节)○4高频电刀:要使用脚踏板的,同我院使用方法一致。
2、建立气腹后,调体位,头高脚低并左倾10—15O(即头高右高)→目的是充分暴露。
3、术中密切观泵气胶机上所显示的腹腔压力,如有异常及时通知医生,予以处理。
4、铺单:中单一块铺于右侧腋下至骼骨。
其余同常规。
5、依次固定吸引器,电凝主导线,冷光源导线,二氧化碳连接管。
6、开台次序:消毒(递弯钳夹碘棉)、布巾钳×2、11#尖刀×1↓气胶针(通气)、干碘棉(擦镜头刀)2/月、妇科用干盐水板球↓分离钳、平齿钳/爪钳↓电凝钩、棒、剪刀↓钛夹钳切下↓胆囊递尖刀、大弯钳、扩大切口、取出胆表式用无齿卵圆钳取尽结石后取出,或用粉碎器粉碎后,置于无菌标本袋(可用无菌手套制作)取出↓递平头吸引器、温盐水冲洗、检查腹腔清点↓器械小物件(尤其是上皮帽)关腹、碘棉消毒、敷贴、缝针(关气)7、术毕,撤下各导线,并关仪器、拔掉开关,做好使用记录。
腹腔镜器械的使用流程(以胆囊手术为例)术前准备:1、术前擦拭并检查腹腔镜仪器及二氧化碳钢瓶,并调试到正常状态备用。
2、病人取平卧位,右上肢开通液路、外展固定;左上肢邦袖带,襁褓约束法固定(以利术者操作)3、备电刀脚踏,必要时备温盐水。
4、器械护士备敷料包×1 中单包×1 开胶洞巾×1手术衣包×1 LC器械×1 大开胶器械(防中转开胶用)腹腔镜专用器械×1套→由器护从消毒机中无菌技术取出5、备一次性物品:保护套×2、11#刀×1、7×10敷贴×3或4、钛夹×1、50ml注射器×1、吸引器×1(不带头)、其余同常规手术术中:1、开机程序○1摄像机:接通电源→连接摄像头→开机→连接手术台上的腹腔镜镜子→拉下保护套○2冷光源:接通电源→开机→连接冷光源线到镜子上→拉下保护套→开灯→据医生使用要求,调节亮度(一般调至光源1/3即可,防止产热过大)○3气腹机:接通电源→开机→打开CO2气瓶开关、自检、待显示屏上均显示“O”为止→设定流量(一般10—18升/分)与压力(一般12—14mmHg)→按T(低流量)开关,充气至0.6—0.7时再按H,术中当压力超过预设界限时,即停止充气。
(注意:流量、压力预设后有记忆功能,再次开机,仍会出现上次的数字,请按医生要求调节)○4高频电刀:要使用脚踏板的,同我院使用方法一致。
2、建立气腹后,调体位,头高脚低并左倾10—15O(即头高右高)→目的是充分暴露。
3、术中密切观泵气胶机上所显示的腹腔压力,如有异常及时通知医生,予以处理。
4、铺单:中单一块铺于右侧腋下至骼骨。
其余同常规。
5、依次固定吸引器,电凝主导线,冷光源导线,二氧化碳连接管。
6、开台次序:消毒(递弯钳夹碘棉)、布巾钳×2、11#尖刀×1↓气胶针(通气)、干碘棉(擦镜头刀)2/月、妇科用干盐水板球↓分离钳、平齿钳/爪钳↓电凝钩、棒、剪刀↓钛夹钳切下↓胆囊递尖刀、大弯钳、扩大切口、取出胆表式用无齿卵圆钳取尽结石后取出,或用粉碎器粉碎后,置于无菌标本袋(可用无菌手套制作)取出↓递平头吸引器、温盐水冲洗、检查腹腔清点↓器械小物件(尤其是上皮帽)关腹、碘棉消毒、敷贴、缝针(关气)7、术毕,撤下各导线,并关仪器、拔掉开关,做好使用记录。
医疗器械公司流程图医疗器械公司流程图是公司运营的重要部分,它涵盖了公司的各个运营环节,从产品研发到生产、销售及售后服务。
一个标准的医疗器械公司流程图包括研发流程、生产流程、销售流程和售后服务流程等。
一、研发流程1、需求分析:了解市场需求,明确产品目标用户和需求。
2、概念开发:基于需求分析,进行产品概念设计。
3、详细设计:进行产品详细设计,包括功能设计、结构设计、材料选择等。
4、原型制造与测试:制造产品原型,进行各项性能测试,确保产品满足设计要求。
5、改进与优化:根据测试结果进行产品改进和优化。
6、准备生产:完成产品定型,准备进入批量生产。
二、生产流程1、采购:根据产品需求,采购所需原材料和零部件。
2、生产计划:制定生产计划,安排生产顺序。
3、生产制造:按照产品设计和工艺要求,进行产品制造。
4、质量检测:对成品进行质量检测,确保产品符合相关标准和设计要求。
5、包装与运输:对合格产品进行包装,安排运输,确保产品按时交付。
三、销售流程1、市场调研:了解市场需求,分析竞争对手,明确自身优势。
2、产品定价:根据产品成本、市场需求和竞争状况,制定合理的产品价格。
3、销售策略:制定销售策略,包括促销活动、渠道选择等。
4、客户沟通:与客户进行沟通,了解客户需求,提供解决方案。
5、订单处理:处理客户订单,包括订单确认、发货等。
6、售后服务:提供售后服务,解决客户问题,提高客户满意度。
四、售后服务流程1、问题接收:接收客户反馈的问题和需求。
2、问题处理:对问题进行分类处理,安排相应部门解决。
3、问题反馈:及时向客户反馈处理结果,确保客户满意度。
4、产品维修:对出现故障的产品进行维修或更换。
5、定期回访:定期对客户进行回访,了解产品使用情况,收集反馈意见。
6、产品升级:根据市场需求和客户反馈,对产品进行升级改进。
医疗器械公司流程图的制定需要考虑多方面因素,包括市场需求、产品质量、生产成本、客户需求等。
通过对流程图的梳理和优化,可以提高公司的运营效率和市场竞争力。
分类消毒干燥检查包装灭菌储存回收清洗发放附1供应室工作附2穿脱防护服流程穿法脱法穿胶鞋脱手套穿第一层手套穿衣结衣领带结好腰带穿第二层手套戴防护面罩进行清洗工作脱防护面罩洗手解开腰带脱防护衣脱胶鞋洗手附3氯消净消毒液使用指引穿好防护桶内加水至指示线(5L)500mg/L有效氯加氯消净1包(20g)1600mg/L有效氯或氯消净1包/水1.5L指示卡监测有效氯浓度浸泡30-45分钟或抹洗注意事项:1.按说明书使用,配制时注意做好个人防护安全。
2.应现配现用,放置于阴凉处。
3.每天使用前指示卡监测有效氯浓度。
4.物品上有大量有机物时应先冲洗后浸泡,减少拮抗作用。
附4器械清洗消毒操作流回收1.封闭包装2.特殊病原体感染器械器具应双层封闭包装并标明疾病名称单独回收处理。
清洗冲洗洗涤漂洗终末漂洗1.在流动水下冲洗。
2.管腔类高压水枪清洗。
3.打开器械轴节并拆开零件。
1.多酶液浸泡后刷洗或擦洗(鲁沃夫多酶清洗剂按1:270稀释,浸泡2-5分钟,室温水即可)。
2.管腔器械应注满多酶液浸泡。
3.超声清洗(时间宜3-5分钟)。
1.在流动水下冲洗或刷洗。
2.管腔器械用高压冲洗。
用软水、纯化水或蒸馏水消毒湿热消毒75%乙醇消毒化学消毒剂1.水温80℃,时间≥10分钟。
2.水温90℃,时间≥1分钟。
浸泡时间>10分钟500mg/L含氯消毒剂浸泡消毒、冲洗或按消毒技术规范及产品说明书要求执行。
干燥1.首先干燥设备进行干燥,金属15-20分钟,70-90℃;塑胶30-40分钟,65-75℃。
2.不耐热物品应使用消毒的低纤维絮布进行干燥处理。
3.管腔类器械应使用高压气枪或95%乙醇进行干燥。
4.禁止使用自然干燥法进行干燥。
检查保养1.目测或者使用带光源放大镜进行检查,检查不合格的应返回重新处理。
2.带电源的应进行绝缘性检查。
3.生锈的器械进行除锈处理(鲁沃夫除锈剂按1:7稀释,浸泡2-10分钟,水温50-80℃)、清洗。
4.使用水溶性润滑剂润滑(鲁沃夫润滑剂1:10稀释,浸泡1-2分钟,室温即可)。