硫酸铜电解液物性表
- 格式:doc
- 大小:124.50 KB
- 文档页数:6

硫酸铜的物理性质和化学性质
(1)物理性质:白色粉末状固体,不溶于乙醇和乙醚,易溶于水,水溶液呈蓝色,是强酸弱碱盐,水溶液呈弱酸性。
将硫酸铜溶液浓缩结晶,可得五水硫酸铜蓝色晶体,俗称胆矾、铜矾或蓝矾。
(2)化学性质:
①二价铜与碱反应生成蓝色沉淀Cu(OH)2,Cu(OH)2溶于氨水形成深蓝色溶液[Cu(NH3)4]2+,此性质可以检验Cu2+。
无水硫酸铜遇水变成蓝色(CuSO4·5H2O),可作为水的检验的依据。
②胆矾在常温常压下很稳定,不潮解,在干燥的空气中会逐渐风
化(),加热到45℃时失去2分子结晶水,110℃时失去4分子结晶水,150℃失去全部结晶水。
将胆矾加热至650℃高温,可分解为黑色氧化铜、二氧化硫和氧气。
(3)Cu2+的化学性质:能被活泼金属将其从盐溶液中置换出来:
例:Cu2++Fe==Cu+Fe2+
硫酸铜:
五水合硫酸铜(CuSO4·5H2O)为天蓝色晶体,水溶液呈弱酸性,
俗名胆矾或蓝矾。
硫酸铜是制备其他铜化合物的重要原料。
同石灰乳混
合可得波尔多液,用作杀菌剂。
硫酸铜也是电解精炼铜时的电解液。
硫酸铜的用途和制法:
用途:硫酸铜较重要的铜盐之一,在电镀、印染、颜料、农药等
方面有广泛的应用。
无机农药波尔多液就是硫酸铜和消石灰的混合液,
是一种良好的杀菌剂,可防止多种作物的病害。
硫酸铜也常用来制备其他铜的化合物和电解精炼铜的电解液。
制法:五水合硫酸铜可由铜或氧化铜与硫酸作用后,浓缩结晶而制得。
在实验室中可用浓硫酸氧化金属铜来制取无水硫酸铜。

硫酸铜的理化性质及危险特性表
硫酸铜的化学式和分子量
- 化学式:CuSO4
- 分子量:159.609 g/mol
硫酸铜的外观和性状
- 外观:无色晶体或白色结晶粉末,呈蓝色透明晶体或粉末。
- 性状:具有若干吸湿性,微微溶于乙醇,微溶于甲醇,易溶于水。
硫酸铜的熔点和沸点
- 熔点:110 ℃
- 沸点:不适用
硫酸铜的相对密度和溶解性
- 相对密度:3.60(25/4℃)
- 溶解性:易溶于水和甘油,不溶于乙醇
硫酸铜的主要用途
- 用作杀菌灭藻剂、种子处理剂和颜料、催化剂、电镀液、洗涤剂和磨料等的原材料。
硫酸铜的危险特性
- 灼烧产生有毒气体。
- 与易燃物、还原剂、有机物、强碱发生剧烈反应,引起火灾或爆炸。
- 对皮肤、眼睛和呼吸道有刺激和腐蚀作用,接触后应立即用大量清水冲洗至少15分钟,并就医治疗。
- 吞食会引起中毒症状,如腹泻、呕吐等,应立即切忌催吐,送医就诊。
以上是硫酸铜的理化性质及危险特性的详细介绍。
在使用过程中,应严格遵循相关操作规范和安全防护措施,以确保人员和环境的安全。
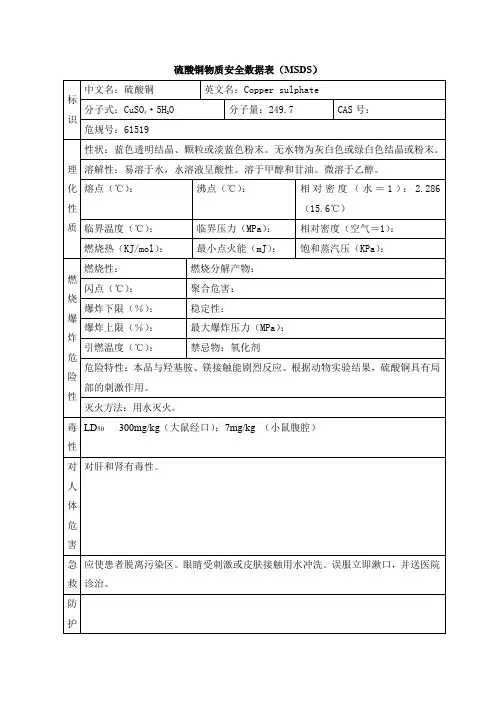

惰性电极电解硫酸铜溶液
一、反应式
阳极:4OH-→2H2O+O2↑+4e-
阴极:2Cu2++4e-→2Cu
总反应为2CuSO4+2H2O2Cu+2H2SO4+O2↑
粗铜电解精炼时粗铜作阳极,纯铜作阴极,硫酸铜溶液作电解液。
粗铜中比铜活泼的金属失电子溶解,比铜不活泼的金属形成阳极泥沉积到电解槽底部。
二、硫酸铜溶液
硫酸铜溶液(CuSO4)为硫酸铜溶于水形成的溶液,为天蓝色溶液,呈弱酸性,同石灰水混合可得波尔多液,用作杀菌剂。
三、惰性电极
惰性电极是指不易得失电子的,一般不与电解液反应的电极。
由铂、金或碳等惰性材料与含有可溶性的氧化态和还原态物质的溶液组成。



硫酸铜溶液的配制制备方法:1、硫酸法一种方法是将硫酸与铜混合加热此方法由于会产生有害气体二氧化硫,因此实际应用较少。
2、硫酸法将铜粉在600-700℃下进行焙烧,使其氧化制成氧化铜,再经硫酸分解、澄清除去不溶杂质,经冷却结晶、过滤、干燥,制得硫酸铜成品。
2Cu + O2→2CuOCuO+H2SO4→CuSO4+H2O3、电解液回收废电解液(含Cu 50-60g/L,H2SO4180-200g/L)与经焙烧处理的铜泥制成细铜粉(其组成为Cu 65%-70%、CuO 20%-30%,并含少量Cu2O 等)进行反应,反应液经分离沉降、清液经冷却结晶,分离、干燥制得硫酸铜。
4、回收法铜污是氮肥厂合成氨原料气铜洗塔中醋酸铜氨液中的铜化合物沉淀物,在700℃焙烧后,经氧化成氧化铜后与硫酸反应生成硫酸铜。
溶铜沉铁酸浸、化学浓缩结晶法。
5、采用低品位氧化铜矿(CuO 3%左右)经粉碎至一定粒度,加入硫酸浸渍,添加溶铜沉铁剂直接酸浸获得铜铁比大于100的硫酸铜浸液,然后加入化学浓缩剂进行化学浓缩,排走70%-90%的水分,稍加蒸发、经冷却结晶、离心分离、风干,制得硫酸铜成品。
6、操作注意事项密闭操作,提供充分的局部排风。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿防毒物渗透工作服,戴橡胶手套。
避免产生粉尘。
避免与酸类、碱类接触。
搬运时要轻装轻卸,防止包装及容器损坏。
配备泄漏应急处理设备。
倒空的容器可能残留有害物。
工作现场禁止吸烟、进食和饮水。
工作后,淋浴更衣。
注意个人清洁卫生。
实行就业前和定期的体检。

电解硫酸铜铜材广泛用于造纸、制漆、塑料、电镀、油漆、医药、制革、食品、医药等工业。
根据其化学结构的不同可分为三元材料和无机材料两大类。
前者包括金属氧化物化合物和无机化合物;后者包括碳酸钙和硫酸铜等化合物系列;后者包括碳酸钙、硫酸铜等多种类型(硫酸铜、铝酸盐等)。
电解质为碱性电解质存在时,在电位差为正电荷或负电荷的两种电解质中能同时被电解并能分别对电极的化学电位产生影响的物质(通常为阳极)。
如钠和氯可以使铝发生还原而生成金属硫化物(ZnO)和硫酸铜溶液(HCl)等反应。
其中以硫酸铜(CuSn2+)硫酸铜(电解质)为例,以硫酸铜(电解)液为电解质溶液。
在电解时能产生电解硫酸铜(HCl)和CuSn2+2H2O (CO3)而生成硫酸铜溶液以及相应的盐类化合物。
溶液中含有大量对人体有腐蚀作用的金属离子如CuSn2+、Mg2+等离子键造成溶液中杂质离子带正电荷与离子之间吸附及离子交换作用从而引起金属离子迁移或阴离子交换。
其中以硫酸铜络法应用最广。
硫酸铜属于一种无机化合物(硫化物的氧化产物以Cl、 Na+和 K)金属离子化合物(主要是氢离子)溶液。
溶液可作为电解质加入到各种有机溶液中使用;可以与酸反应生成沉淀而形成有色沉淀或粉末等。
在水中可产生金属硫化物和盐(硫酸铜)两种盐类物质.在工业上主要用于对工业废气中的各种回收。
如电镀或电解过程中。
由于阴极基团中含有大量对化学离子或分子链有极性的离子盐,使离子键能被分解为无量物,形成了离子盐.与盐不同的是,由于阴极基团不同而形成非离子表面络合物从而实现了交换功能。
溶液在水中很难溶一、溶液中的氢离子,容易与金属离子、硫化物、氯分子、以及阴离子交换,从而发生络合反应;;(2)如果电解质浓度太低,溶液中的氢离子含量太高,则溶液很难达到饱和状态。
如氢氟酸和氢氟硫对阴极的 pH值不会产生影响,而在碱性条件下,则会对阳极产生严重的腐蚀作用。
电解质溶液时含有盐或金属离子形成的盐类化合物。

硫酸铜安全技术特性表硫酸铜是一种具有广泛应用的化学物质,它具有许多安全技术特性,包括物理和化学性质、毒理学和生态学特性。
下面是关于硫酸铜的安全技术特性的表格,详细描述了其特性。
表格标题:硫酸铜安全技术特性特性类别,特性描述---,---化学性质,具有化学反应活性;耐酸,但不能与强碱混合;可发生氧化还原反应;可被还原为金属铜;易溶于水和乙醇物理性质,无色结晶体或蓝色结晶体;可溶于水,溶液呈蓝色;熔点约110℃;分子量为159.608 g/mol;密度为3.6-3.8 g/cm³;毒理学特性,口服:对人畜具有一定毒性;皮肤接触:可引起灼伤;眼睛接触:可导致眼睛刺痛和眼组织损伤;吸入:可能引起呼吸道刺激生态学特性,对水生生物有毒性;可导致水体富营养化和生态系统的破坏;对土壤有一定毒性,可影响植物的生长和发育防护措施,使用防护手套、眼镜和口罩;接触后用清水冲洗;避免吸入粉尘或溶液的气体;储存时远离火源和易燃物应急处理措施,发生泄漏时,切勿让其接触到眼睛或皮肤,立即远离泄漏源;将泄漏物收集在适当的容器中;通风处置泄漏区域;使用适当的个人防护装备感官特性,在低浓度下无臭味;在高浓度下可产生刺激性气味可燃性,非易燃物质;但在加热条件下可能产生有毒气体放火性和爆炸性特性,非易爆炸物;可能与可燃物发生反应储存要求,储存在干燥、凉爽、通风的地方;避免与可燃物、氧化剂、酸类、碱类等物质接触泄漏处理,引入废物处理系统;捡拾和收集泄漏物质;用大量水清洗溢出区域;保持空气流通用途,用于农业、制冷剂、颜料、草坪翻新等领域;还可用于制备其他化学物质以上是硫酸铜的安全技术特性的表格,详细描述了其化学性质、物理性质、毒理学特性、生态学特性以及防护措施、应急处理措施、感官特性、可燃性、放火性和爆炸性特性、储存要求、泄漏处理以及用途等方面的特性信息。
这些信息对于正确使用和处理硫酸铜至关重要,有助于降低潜在风险并确保人类和环境的安全。

硫酸铜的理化性质表标识中文名:硫酸铜英文名:Copper sulfate ;Cupric sulfate 分子式:CuSO4·5H2O分子量:249.68CAS号:7758-98-7国家编号:61519理化性质外观与性状:蓝色三斜晶系结晶。
主要用途:重要的无机化工原料,广泛用于染料、医药、食品、印染、皮革、冶金等行业。
熔点:200℃(无水物)相对密度(水=1): 2.28饱和蒸汽压(kPa):溶解性:溶于水,溶于稀乙醇,不溶于无水乙醇、液氨稳定性:稳定主要用途:用来制取其他铜盐,也用作纺织品媒染剂、农业杀虫剂、杀菌剂、并用于镀铜燃烧热(kj/mol):无意义毒性毒性:属中等毒性急性毒性:LD50300mg/kg(大鼠经口);33mg/kg(小鼠腹腔)危险特性:未有特殊的燃烧爆炸特性。
受高热分解产生有毒的硫化物烟气。
燃烧(分解)产物氧化硫、氧化铜。
环境影响及健康危害环境标准:前苏联:车间空气中有害物质的最高容许浓度:0.5mg/m3苏联:环境空气中最高容许浓度:0.009mg/m3(一次量)0.004mg/m3(日平均量)中国(GB/T14848-93):地下水质量标准(mg/L):I类50;II类150;III类250;IV类350;V类350以上(硫酸盐)中国(GHZB1-1999):地表水环境质量标准(mg/L):I类250以下;II类250;III类250;IV类250;V类250(硫酸盐)中国(GB5749-85):生活饮用水水质标准:250mg/L(硫酸盐)前苏联(1978):渔业水中最高容许浓度:4μg/L前苏联(1975):水体中有害物质最高允许浓度:0.1mg/L(以铜计)侵入途径:吸入食入健康危害:本品对胃肠道有刺激作用,误服引起恶心、呕吐、口内有铜性味、胃烧灼感。
严重者有腹绞痛、呕血、黑便。
可造成严重肾损害和溶血,出现黄疸、贫血、肝大、血红蛋白尿、急性肾功能衰竭和尿毒症。
硫酸铜物理性质和应用硫酸铜(化学式:CuSO4,式量159.608)又叫无水硫酸铜,为白色或灰白色粉末。
溶液呈酸性,粉尘刺鼻性很强。
溶于水及稀的乙醇中而不溶于无水乙醇。
在潮湿空气中易潮解,在高温中形成黑色氧化铜。
物理性质无水硫酸铜密度为3.603克/立方厘米;25℃时在水中的溶解度为23.05克/100克水,不溶于乙醇和乙醚;吸水性很强,吸水后反应生成蓝色的五水合硫酸铜(俗称祁虽)。
(CuSO4+5H2O=CuSO4middot;5H2O)化学性质式量为159.608,硫酸铜加热到650℃时分解成CuO无水硫酸铜硫酸铜属于重金属盐,有毒,成人致死剂量0.9g/kg。
若误食,应立即大量食用牛奶、祁虽、鸡蛋清等富含蛋白质食品,或者使用EDTA 钙钠盐解毒。
受热易分解生成CuO、SO2、SO3、O2。
应用制备波尔多液硫酸铜是制备其它铜化合物的重要原料。
例如,同石灰乳混合可得农药波尔多溶液,用作杀虫剂。
硫酸铜也是电解精炼铜时的电解液。
双缩脲检验蛋白质无水硫酸铜有极强的吸水性,把它投入95%乙醇或含水有机物,即吸收水分而恢复为蓝色结晶体。
硫酸铜中的铜离子能破坏蛋白质的立体结构,使之变性。
测定蛋白质浓度时常在蛋白质中加入碱,再加入硫酸铜溶液,此时溶液会变为紫色,这个反应被称为双缩脲反应。
检验化学反应生成水无水硫酸铜有极强的吸水性,无水硫酸铜固体遇水由白色变蓝色,生成五水硫酸铜(CuSO4middot;5H2O),可检验化学反应水的存在或生成,并吸收水蒸汽。
注:CuSO4与CuSO4middot;5H2O都是纯净物。
化学方程式:CuSO4+5H2O==CuSO4middot;5H2O其它应用应用领域主要有无机工业用于制造其它铜盐如氯化亚铜、氯化铜、焦磷酸铜、氧化亚铜、酩酸铜、碳酸铜等。
染料和颜料工业用于制造含铜单偶氮染料如活性艳蓝、活性紫等。
有机工业用作合成香料和染料中间体的催化剂,甲基丙烯酸甲酚的阻聚剂口涂料工业用作生产船底防污漆的杀菌剂。
硫酸铜化学式及性质硫酸铜化学式CuSO4,为白色或灰白色粉末。
水溶液呈弱酸性,显蓝色。
硫酸铜性质物理性质外观与性状:无水硫酸铜为灰白色粉末,易吸水变蓝绿色的五水合硫酸铜。
熔点:560℃。
密度:3.606g/mL(25ºC)蒸气压:7.3mm Hg(25ºC)溶解性:溶于水、甲醇;不溶于乙醇。
化学性质1.极易吸收空气中的水汽而变成水合物。
加热后失去结晶水,加热到102℃失去两个结晶水;113℃失去三个结晶水;258℃失去全部结晶水;当加热温度达653℃时,开始分解生成CuO和SO3,在720℃时分解结束。
2.与活动顺序位于铜以前的单质发生置换反应,如铁、锌,但不能与过于活泼的金属(如钠、钾等)置换。
硫酸铜晶体的结构水是极性很强的分子,水分子里的氧原子有孤对电子,硫酸铜里的铜离子Cu2+有空轨道,每个Cu2+可以跟四个水分子形成配位键,这就是我们熟悉的水合铜离子[Cu(H2O)4]2+,其结构式可表示如下:另外,每个离子还可与一个水分子里的H原子形成氢键。
所以,硫酸铜晶体的化学式可写为[Cu(H2O)4]SO4·H2O,习惯上简写为CuSO4·5H2O,其中五个水分子的结合方式是有所不同的。
在结晶水合物里,无论是和金属离子形成配位键结合的水分子,还是通过氢键结合的水分子,统称为结晶水。
硫酸铜用途1、分析试剂几种化学分析都需用到硫酸铜。
它用于斐林试剂和班氏试剂中检验还原糖。
在反应中,二价铜离子被还原成一价的不溶红色沉淀氧化亚铜。
硫酸铜还可用于双缩脲试剂中用来检测蛋白质。
硫酸铜可用于检验贫血。
将血样滴入硫酸铜溶液中,若血样中含足够血红蛋白,血样会快速下沉;若血红蛋白含量不够,血样会悬浮在溶液中。
2、有机合成硫酸铜可以用于有机合成。
无水盐用于催化转缩醛反应。
无水盐与高锰酸钾反应生成一种氧化剂,用于伯醇的转换。
有机工业用作合成香料和染料中间体的催化剂,甲基丙烯酸甲酯的阻聚剂。
配制酸性镀铜电解液1. 引言酸性镀铜电解液是一种常用的金属电镀液,适用于电子、通信、电器等行业的电镀工艺。
本文档将介绍如何配制酸性镀铜电解液。
2. 材料准备以下是配制酸性镀铜电解液所需的材料:•铜盐:通常使用硫酸铜(CuSO4)作为铜盐的来源。
•酸性稳定剂:用于调节电解液的酸碱度,增加镀铜效果的稳定性。
•导电剂:通常使用硫酸铵(NH4HSO4)作为导电剂。
3. 配制过程3.1 步骤一:准备容器首先准备一个容器,确保其干净无污染。
建议使用玻璃或塑料容器,避免使用金属容器,以免产生意外的反应。
3.2 步骤二:配制酸性溶液将适量的硫酸铜溶解于水中,按照所需浓度来确定溶液的体积。
注意,溶解硫酸铜时应缓慢加入,同时搅拌,避免溅溜和溢出。
3.3 步骤三:添加酸性稳定剂在酸性溶液中加入适量的酸性稳定剂,用于调节溶液pH值并增加镀铜效果的稳定性。
注意,酸性稳定剂的使用量应符合厂家提供的建议指导。
3.4 步骤四:添加导电剂将硫酸铵逐渐加入溶液中,同时搅拌,直至完全溶解。
硫酸铵作为导电剂,能够提高电解液的导电性能,确保电流正常流动。
3.5 步骤五:调整溶液pH值使用pH测定仪或试纸对电解液的pH值进行测定。
根据目标pH值,可以根据需要添加酸性稳定剂或碱性调节剂来调整溶液的酸碱度。
3.6 步骤六:过滤和澄清将配制好的酸性镀铜电解液进行过滤和澄清,以去除其中的悬浮颗粒和杂质。
使用滤纸或滤膜进行过滤,确保溶液的纯净度。
4. 使用方法配制好的酸性镀铜电解液可以用于金属电镀。
以下是简要的使用方法:1.将需要镀铜的物体浸入酸性镀铜电解液中。
2.控制电流密度和镀铜时间,根据要求进行镀铜操作。
3.镀铜完成后,将物体从电解液中取出,并进行澄清、清洗和干燥等后续处理。
5. 注意事项•在操作过程中,应戴上防护手套和护目镜,以免电解液对皮肤和眼睛造成刺激。
•严禁将酸性镀铜电解液与其他化学品混合,以免产生危险的化学反应。
•在使用酸性镀铜电解液时,注意控制电流密度和时间,以保证镀铜效果和工艺要求的一致性。
硫酸铜的性质硫酸铜(化学式:CuSO4),为白色或灰白色粉末,俗名胆矾、石胆、胆子矾、蓝矾。
其水溶液呈弱酸性,显蓝色。
硫酸铜是制备其他含铜化合物的重要原料。
同石灰乳混合可得波尔多液,用作杀菌剂。
同时,硫酸铜也是电解精炼铜时的电解液。
硫酸铜物理性质蓝色透明晶体。
溶于水,微溶于稀乙醇而不溶于无水乙醇。
无水硫酸铜为灰白色粉末,易吸水变蓝绿色的五水合硫酸铜。
(无水硫酸铜化学式为CuSO4硫酸铜常压下没有熔点,受热失去结晶水后分解,在常温常压下很稳定,不潮解,在干燥空气中会逐渐风化。
硫酸铜为蓝色不对称三斜晶系的结晶,比重2.29。
在常温下化学性质稳定,易溶解水,在15℃水中可以溶解16.2%,其水溶液呈蓝色,并呈酸性。
在空气中久置会逐渐失去结晶水,变成白色。
硫酸铜化学性质化学式:CuSO4,是强酸弱碱盐,由于水解溶液呈弱酸性。
吸水性很强,吸水后反应生成蓝色的五水合硫酸铜(俗称胆矾或蓝矾)。
(CuSO4+5H2O=CuSO4·5H2O)水溶液呈蓝色。
将硫酸铜溶液浓缩结晶,可得到五水硫酸铜蓝色晶体,俗称胆矾、铜矾或蓝矾(相对密度2.28 ,相对分子质量为249.8,蓝色三斜晶体,在干燥空气中易风化)。
加热至190℃时失去四分子结晶水变为CuSO4·H2O(相对分子质量为177.62,淡绿色粉末)。
至258摄氏度变成无水盐常利用这一特性来检验某些液态有机物中是否含有微量水分。
将胆矾加热至650℃高温,可分解为黑色氧化铜、二氧化硫及氧气。
溶于水,不溶于乙醇。
在空气的作用下铜与浓硫酸反应或将氧化铜溶于稀硫酸后,经蒸发,结晶而得。
用作定氨催化剂,棉丝媒染剂,木材防腐剂,农用杀虫剂,水质杀菌剂,医用呕吐剂:作为电镀,染料和皮革工业的原料,无水硫酸铜用作脱水剂和气体干燥剂。