新生儿呼吸窘迫综合征诊疗指南
- 格式:doc
- 大小:20.00 KB
- 文档页数:6

首都儿科研究所附属儿童医院新生儿呼吸窘迫综合症临床路径一、新生儿呼吸窘迫综合症临床路径标准住院流程(一)适用对象第一诊断为新生儿呼吸窘迫综合症,又称新生儿肺透明膜病(HMD)(ICD-10:P22.002)。
(二)诊断依据。
根据《临床诊疗指南-小儿内科分册》(中华医学会编著,人民卫生出版社),《诸福棠实用儿科学(第七版)》(人民卫生出版社)1. 病史:早产儿或糖尿病母亲婴儿及剖宫产儿。
生后1-3小时出现呼吸困难。
进行性加重并伴呼气性呻吟,吸气性三凹,青紫,严重者呼吸减慢,节律不整.呼吸暂停。
由于严重缺氧和酸中毒。
患儿可出现反应迟钝,肌张力低下,体温不升,心功能衰竭,休克等。
病情于24-48小时达顶峰。
死亡多发生于生后3天内,3天后病情可逐渐恢复。
2. 体征:呼气性呻吟,吸气性三凹,青紫,两肺呼吸音减弱。
严重者呼吸减慢,节律不整.呼吸暂停。
3. 辅助检查:1) X线表现:有持征性改变,分四级。
I级:两肺细小颗粒网状阴影,分布较均匀,心影清楚,支气管充气征不明显。
Ⅱ级:两肺见较大密集的粒网状阴影,胸廓小,呈钟形,肺透光度减低,可见支气管充气征。
Ⅲ级:全肺透光度丧失,呈磨玻璃样,横膈及心影模糊,支气管充气征明显。
Ⅳ级:全肺野一致性密度增高,完全变白,膈面和心影看不见,支气管充气征不明显。
2) 泡沫稳定试验:对怀疑可能发生的病人生后3分钟之内取胃液0.5-1ml,加等量95%酒精,用力振荡15秒钟,静立15分钟后观察试管内泡沫多少。
(-)无泡沫。
(+)试管液面周边1/3有小泡沫。
(++)试管液面周边>1/3至整个管周有一层泡沫。
(+++)试管周边有泡沫层。
(-)支持HMD诊断,(+)或(++)可疑、(+++)可排除HMD。
(三)治疗方案的选择。
根据《临床诊疗指南-小儿内科分册》(中华医学会编著,人民卫生出版社),《诸福棠实用儿科学(第七版)》(人民卫生出版社)1. 支持治疗及护理:应按早产儿加强护理。

新生儿呼吸窘迫综合征诊疗指南【NRDS诊断标准】(一).具有发病的高危因素:母孕期患有糖尿病、胆汁淤积、宫内感染、早产、胎膜早破超过24小时、宫内窘迫、剖宫产、产时窒息等。
(二).具有NRDS临床症状及体征症状:生后6小时内发生进行性加重的呼吸急促(>60/分)。
体征:(1)、发绀、鼻扇、吸气性三凹征和明显的呼气呻吟;(2)、严重时呼吸浅快,呼吸节律不整、呼吸暂停及四肢松弛;(3)、听诊可闻及双肺呼吸音减低。
(三)具有典型的胸部X线检查特征胸片特征性改变是判断NRDS严重程度的重要指标之一,但不是早期诊断的必须条件之一。
NRDS胸片特征性改变包括:Ⅰ级:双肺透光度降低,呈毛玻璃样改变。
Ⅱ级:双肺透光度降低,见明显支气管充气征,心影及肋膈角清楚。
Ⅲ级:双肺透光度明显降低,见明显支气管充气征,心影及肋膈角模糊。
Ⅳ级:全肺透光度严重降低,呈“白肺”样改变。
(四)、辅助检查1、如果可能,应在生后1小时内抽取胃液做泡沫震荡实验。
2、在使用肺表面活性物质(PS)治疗前及治疗后检测血气分析3、尽快完成胸片检查,并在使用PS后6-12小时进行复查,必要时增加复查次数。
4、严重病例应当完善心脏彩超检查,以明确有无肺动脉高压及动脉导管未必。
5、积极完善血糖、乳酸、电解质、肝肾功等检测,了解患儿机体内环境状态。
【NRDS治疗】(一)、PS的应用1、胎龄<28周的早产儿都应接受表面活性物质预防性治疗(生后15 min内)。
2、如果新生儿在产房内需接受气管插管,或母亲未接受产前皮质激素治疗,则对胎龄>28周~<30周的新生儿应预防性使用表面活性物质对已患RDS或RDS高危的新生儿应尽早给予PS,以降低死亡率及肺气漏。
3.在有RDS进展的证据时,如持续需氧、需要机械通气或CPAP 6 cm H2O需氧浓度>50% ,应给与第二或第三剂表面活性物质。
4、对需从CPAP改为机械通气治疗的RDS患儿,应给与第二剂PS。
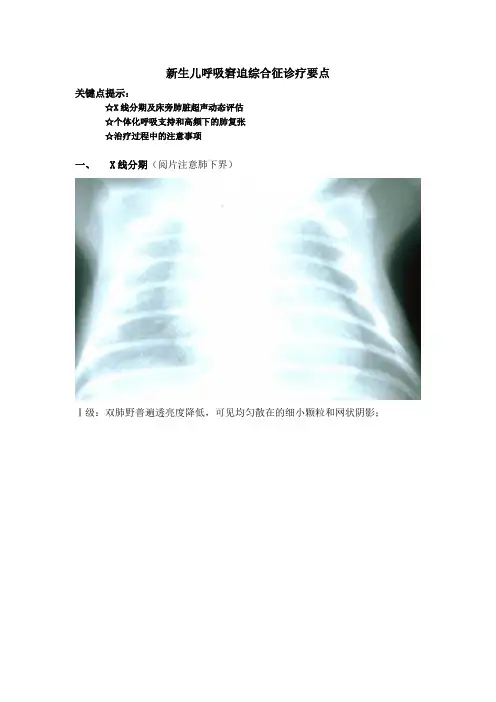
新生儿呼吸窘迫综合征诊疗要点关键点提示:☆X线分期及床旁肺脏超声动态评估☆个体化呼吸支持和高频下的肺复张☆治疗过程中的注意事项一、X线分期(阅片注意肺下界)Ⅰ级:双肺野普遍透亮度降低,可见均匀散在的细小颗粒和网状阴影;Ⅱ级:可见支气管充气征,延伸至肺野中外带;Ⅲ级:心缘、膈缘模糊;Ⅳ级:整个肺野呈白肺,支气管充气征更加明显。
床旁肺脏超声:超声诊断标志为肺实变,多以背部为著,但病程早期可仅发现弥漫B线,需动态评估以与湿肺相鉴别(湿肺诊断应谨慎)。
二、个体化呼吸支持1、无创呼吸支持由弱至强:加温加湿高流量吸氧(HFNC)、持续气道正压通气(CPAP)、双水平气道正压通气(BIPAP)、经鼻间歇正压通气(NIPPV)、(1)对于所有RDS高危新生儿(如胎龄<30周而无需机械通气),应生后立即开始 CPAP,直到临床情况好转、平稳,建议酌情呼吸支持至矫正32周。
(2)起始PEEP压力至少6cmH2O,FiO230-40%,然后根据临床表现、TcSO2、胸片肺下界位置(第8-10肋为宜)和灌注情况调节。
(3)对CPAP失败病例,可以考虑使用INSURE技术。
(4)加温加湿高流量吸氧(HFNC)可用于撤离呼吸机后备选方法,尤其是避免长期CPAP鼻粘膜损伤的主要替代治疗。
<1kg的流量2-4L/min(kg*2),较大体重可流量4-8L/min。
2、肺表面活性物质替代治疗(2小时内开始使用):(1)应使用天然制备的PS。
(2)以下情况应在产房开始使用PS:未接受产前激素治疗的超早产儿或者需要气管插管复苏的患儿。
(3)推荐方案:胎龄<26周的吸入氧浓度(FiO2)>0.3,胎龄>26周的FiO2>0.4时应进行治疗。
(4)剂量:首剂200 mg/kg,酌情重复给药,一般不超过3次,间隔6-12小时,剂量100-120 mg/kg。
3、机械通气(1)尽可能缩短机械通气用时间,选择以潮气量为目标的通气模式,可缩短机械通气时间,降低BPD和IVH。


2024新生儿呼吸窘迫综合征及其护理新生儿呼吸窘迫综合征(Respiratory Distress Syndrome,RDS)是一种常见的新生儿疾病,通常发生在早产儿或肺部未充分成熟的足月儿身上。
RDS 主要是由于胎儿肺部表面活性物质不足或者肺部未充分发育引起的,这会导致肺部出现弹性度降低、通气障碍以及肺部积液等症状,严重影响新生儿的呼吸功能和生存率。
针对RDS,临床常见的护理措施主要包括以下几方面:1.治疗性呼吸支持:对于呼吸困难的新生儿,常规给予氧疗、呼吸机辅助通气或者光合作用治疗,以保障新生儿的正常呼吸功能。
呼吸机通气需要根据新生儿的肺功能情况进行调整,避免氧中毒和肺损伤。
2.营养支持:对于呼吸窘迫综合征的新生儿,保证充足的营养摄入也非常重要。
护士需要根据新生儿的生长发育情况,及时调整配方奶粉或者母乳喂养方式,确保新生儿获得足够的热量和营养支持。
3.胸部理疗:对于呼吸窘迫综合征的新生儿,胸部理疗是非常重要的护理措施。
轻拍、振荡和按摩等技术可以帮助清除肺部分泌物,提高肺活量,促进氧气交换,改善新生儿的呼吸功能。
4.保温护理:新生儿呼吸窘迫综合征的患者由于肺部功能不全,呼吸负荷较大,易消耗大量能量,导致体温下降。
因此,保持新生儿的体温稳定非常关键,护士需要加强保暖护理,注意环境温度和新生儿的衣物覆盖,避免发生低体温现象。
5.监测和观察:护士需要密切观察新生儿的病情变化,包括心率、血氧饱和度、呼吸频率等指标的监测,及时发现并处理新生儿的不适症状。
同时,定期进行临床评估和检查,及时调整治疗措施。
6.家属支持:新生儿呼吸窘迫综合征的治疗过程对家属来说也是一个巨大的挑战,护士需要与家属进行沟通和协作,解释病情和治疗措施,提供心理支持,帮助家属正确应对疾病,增强信心和毅力。
综上所述,新生儿呼吸窘迫综合征是一种常见的新生儿疾病,需要采取综合性的护理措施。
护理人员要关注患儿的呼吸支持、营养支持、胸部理疗、保温护理、监测和观察以及家属支持等方面,全面照顾患儿的身心健康,提高患儿的生存率和生活质量。

新生儿科临床诊疗指南目录新生儿窒息与缺氧缺血性损伤 (1)新生儿呼吸窘迫综合征 (4)早产儿管理 (8)新生儿高胆红素血症 (14)新生儿感染性肺炎 (17)新生儿败血症 (20)新生儿窒息与缺氧缺血性损伤【概述】新生儿窒息是指由于产前、产时或产后的各种疾病使新生儿出生后不能建立正常呼吸,引起缺氧并导致全身多脏器损害,是围产期新生儿死亡和致残的主要原因之一。
【诊断】1、新生儿窒息(1)出生后1min内Apgar评分为国际上对新生儿窒息的一种通用的评判方法(表1-1)。
8~10分者基本正常,4~7分为轻度窒息,0~3分为重度窒息。
若出生后1min内评分≥8分,而数分钟降至7分以下亦属窒息。
表1-1新生儿Apgar评分表体征0分1分2分皮肤颜色青紫或苍白身体红、四肢青紫全身红心率(次/分) 无<100 >100 弹足底或插管反应无反应有些动作如皱眉哭、喷嚏肌张力松弛四肢略屈曲四肢活动呼吸无慢、不规则正常、哭声响(2)脐动脉血或胎儿头皮血PH值<7.00也可作为新生儿窒息的诊断依据。
2、缺氧缺血性器官损害(1)缺氧缺血性脑病(HIE):患儿有严重的宫内窘迫或出生时重度窒息史(Apgar评分1分钟≤3分钟,并持续至5分钟时仍≤5分),出生后不久出现神经系统症状,并持续至24h小时以上,即可诊断为HIE。
根据病情可分为轻、中、重三度(表1-2)。
表1-2 HIE的临床分度项目轻度中度重度意识过度兴奋嗜睡、迟钝昏迷肌张力正常减低松软或肌张力増高原始反射稍活跃减弱消失惊厥无通常伴有多见或持续中枢性呼吸衰竭无无或轻度常有瞳孔改变无无或缩小不对称、扩大或光反应消失前囟张力正常正常或稍饱满饱满、紧张病程及预后兴奋症状在24h内最明显3d逐渐消失,预后好大多在一周末症状消失,10d后仍不消失者可能有后遗症病死率高、多在1周内死亡,存活者症状可持续数周,多有后遗症3、围产期缺氧缺血对其他器官系统的损害见表1-3。


完整版)新生儿呼吸窘迫综合征诊疗规范新生儿呼吸窘迫综合征(NRDS)是由于肺表面活性物质缺乏引起的,主要发生在胎龄<35周的早产儿,但晚期早产儿或足月儿也有可能发病。
该病的病理特征是肺透明膜,也被称为肺透明膜病(HMD)。
诊断方面,对早产儿、剖宫产新生儿、糖尿病母亲新生儿要随时注意可能发生RDS。
临床表现方面,早产儿出生后不久就会出现呼吸困难,先是呼吸增快、急促、鼻扇,呼吸60次/分以上,然后出现呼气性,吸气时出现三凹征,至生后6小时症状已非常明显。
病情会逐渐加重,继而出现呼吸不规则、呼吸暂停、发绀、呼吸衰竭。
听诊双肺呼吸音减低。
血气PaO2下降,PaCO2升高,BE负值增加,生后24-48小时病情最重,病死率高,能生存3天以上者肺成熟度增加,可逐渐恢复。
但不少患儿并发肺部感染或PDA,病情可再度加重,轻度病例可仅有呼吸困难、,而发绀不明显。
剖宫产新生儿发生RDS多见于足月儿或晚期早产儿,可在1-72小时发生呼吸困难,有些患儿先后有湿肺表现,呼吸困难逐渐加重,然后发生RDS。
X线检查方面,对发生呼吸困难的新生儿应立即进行胸片检查,随着病情进展需动态随访胸片。
根据病情程度可将胸片改变分为4级,分别为Ⅰ级、Ⅱ级、Ⅲ级和Ⅳ级。
鉴别诊断方面,GBS(B族溶血性链球菌)感染和重度湿肺需与RDS进行鉴别。
治疗方面,肺表面活性物质(PS)治疗是一种有效的方法,应及时使用。
治疗时机要早期给药,一旦出现呼吸困难、,胸片提示RDS,立即给药,不要等到胸片出现严重RDS改变。
给药剂量:固尔苏一般每次使用100mg/kg左右。
对于严重病例,剂量可增加至100-200mg/kg。
XXX一般每次使用70mg/kg左右,首次可在40-100mg/kg。
给药次数:轻度病例一般只需要给药一次。
但应根据病情需要决定给药次数。
如果FIO2>0.4或MAP>8cmH2O才能维持正常血气,应重复给药。
持续气道正压呼吸(CPAP):轻度或早期RDS应尽早使用CPAP。



2019版欧洲共识指南:新生儿呼吸窘迫综合征的防治(全文)一、简介新生儿呼吸窘迫综合征(RDS )是早产儿的重要疾病,随着近年治疗手段的不断成熟,小胎龄早产儿存活率逐渐增高,但是支气管肺发育不良(BPD )发病率仍然较高。
欧洲RDS防治指南2007年首次发布,2010 年、2013年和2016年进行了更新,指南中包含现代新生儿重症监护中临床医生可使用的所有资源和经验,获得欧洲丿用研究学会的大力支持。
由于月市表面活性物质(PS)和持续气道正压通气(CPAP )的早期使用,典型的胸部X线表现如毛玻璃样改变和支气管充气征目前已很难看到,临床医生主要通过评估患儿病程早期呼吸做功和吸入氧浓度(FiO2)判断是否需要给予PS治疗。
2017年欧洲有8 156例RDS资料上传到美国Vermont Oxford新生儿协作网,数据显示RDS发病率在出生fl台龄28周早产儿为80% ,胎龄24周则高达90%。
55%的极低出生体重(VLBW )婴儿接受PS治疗。
欧洲VLBW 婴儿慢性月市疾病/BPD发生率约为18%。
RDS的防治目标是通过干预尽可能提高新生儿存活率,同时最大程度减少潜在不良反应,包括BPD。
许多用于预防和治疗RDS的策略和方法已经过临床试验并被纳入到更新的系统评价中。
本指南对截止到2018年底发表的文献证据进行严格审查后,对先前发表的4版指南进行更新,采用与既往指南相似的格式总结防治策略,列出循证推荐,使用GRADE等级反映每个推荐意见的证据支持力度。
证据质量和推荐强度见表1。
1 .妊娠<28~30周、存在早产风险的孕妇均应转诊到具有诊治RDS 经验的围产中心(C1 )。
2 .理想情况下,对妊娠34周内存在早产风险的孕妇至少在分娩前24 h 给予单疗程产前激素治疗(A1 )。
3 .妊娠<32周再次出现早产征象,且距第1个疗程产前激素治疗超过1 ~2周者,可重复给予1个疗程激素治疗(A2 )。
4 •妊娠<32周,紧急分娩前应给予硫酸镁(MgSO4 )治疗(A2 )。
新生儿呼吸窘迫综合征诊疗指南
【NRDS诊断标准】
(一).具有发病的高危因素:母孕期患有糖尿病、胆汁淤积、宫内感染、早产、胎膜早破超过24小时、宫内窘迫、剖宫产、产时窒息等。
(二).具有NRDS临床症状及体征
症状:生后6小时内发生进行性加重的呼吸急促(>60/分)。
体征:
(1)、发绀、鼻扇、吸气性三凹征和明显的呼气呻吟;
(2)、严重时呼吸浅快,呼吸节律不整、呼吸暂停及四肢松弛;
(3)、听诊可闻及双肺呼吸音减低。
(三)具有典型的胸部X线检查特征
胸片特征性改变是判断NRDS严重程度的重要指标之一,但不是早期诊断的必须条件之一。
NRDS胸片特征性改变包括:
Ⅰ级:双肺透光度降低,呈毛玻璃样改变。
Ⅱ级:双肺透光度降低,见明显支气管充气征,心影及肋膈角清楚。
Ⅲ级:双肺透光度明显降低,见明显支气管充气征,心
影及肋膈角模糊。
Ⅳ级:全肺透光度严重降低,呈“白肺”样改变。
(四)、辅助检查
1、如果可能,应在生后1小时内抽取胃液做泡沫震荡实验。
2、在使用肺表面活性物质(PS)治疗前及治疗后检测血气分析
3、尽快完成胸片检查,并在使用PS后6-12小时进行复查,必要时增加复查次数。
4、严重病例应当完善心脏彩超检查,以明确有无肺动脉高压及动脉导管未必。
5、积极完善血糖、乳酸、电解质、肝肾功等检测,了解患儿机体内环境状态。
【NRDS治疗】
(一)、PS的应用
1、胎龄<28周的早产儿都应接受表面活性物质预防性治疗(生后15 min内)。
2、如果新生儿在产房内需接受气管插管,或母亲未接受产前皮质激素治疗,则对胎龄>28周~<30周的新生儿应预防性使用表面活性物质
对已患RDS或RDS高危的新生儿应尽早给予PS,以降低死亡率及肺气漏。
3.在有RDS进展的证据时,如持续需氧、需要机械通气或CPAP 6 cm H2O需氧浓度>50% ,应给与第二或第三剂表面活性物质。
4、对需从CPAP改为机械通气治疗的RDS患儿,应给与第二剂PS。
5、在有可能的条件下,给药后立即(或早期)拔除气管插管改为CPAP,能缩短机械通气时间,从而有利于患儿稳定。
PS:剂量100~200mg/kg,肺灌洗液中提取的天然制剂较好,生后2~4h (12~24h内)应用,由气管内给药可维持8~15小时,(2~4次)。
6~12h重复,最多应用4次,除800g以下,一般给药1~2次即可。
滴入或气雾法。
制剂:天然;半合成;人工合成。
固尔苏,意大利生产,通用名:猪肺表面活性物质poractantalfa,别名:猪肺磷脂;
(二)、机械通气治疗
1、机械通气策略:
(1)呼吸衰竭的NRDS患儿应使用机械通气提高存活率。
(2)低碳酸血症会增加BPD和脑室周围白质软化的危险性,应尽可能避免。
(3)应经常调整呼吸机参数。
从而获得最佳肺容量。
(4)应尽可能缩短机械通气使用时间,减少肺损伤
(5)优先考虑使用CPAP或NIPPV,避免或减少气管插管和机械通气时间。
(6) 采用同步和潮气量控制的常频通气模式,及积极的撤机方案能缩短机械通气时间。
(7) 撤机后可以接受pH>7.22的中等程度的高碳酸血症。
2、CPAP的应用:
(1)对所有存在RDS高危因素的患儿,如胎龄<30周不是必须使用机械通气者都应使用CPAP,直到临床状况被进一步评估。
(2)PEEP至少要保证在5cmH2O的压力。
(3)为了减少机械通气的使用,对RDS患儿应早期使用CPAP和PS。
CPAP:压力5~10cmH2O;
3、人工呼吸器:
用CPAP后PaO2仍≤50mmHg(6.67kPa), PaCO2≥60mmHg(8kPa)或频发呼吸暂停或体重<1500g。
吸气峰压20~25cmH2O(1.96~2.45 kPa),呼气末正压4~5cmH2O(0.39~0.49kPa),氧浓度开始6生后第1天即可使用全静脉营养。
0%~80%,以后渐减至40%,呼吸率30~40次/min,吸:呼=1:1~2。
(三)、败血症的防治
1、RDS患儿应常规使用抗生素,直到排除败血症。
2、治疗过程中需要考虑到真菌感染可能性。
(四)、支持疗法
为使RDS患儿达到最好的治疗效果,适合的支持疗法是必要的,包括维持正常体温、合理的液体疗法、良好的营养支持、治疗动脉导管开放及稳定循环功能维持合适的血压和组织灌注。
1.体温控制:体温维持在36.5~37.2℃
2.液体和营养治疗
①置于湿化暖箱中的大多数患儿,静脉补液量从
70~80ml/(kg·d)开始;
②早产儿液体和电解质疗法应个体化处理,生后5d
允许体重每天下降2.5%~4%(总共15%);
③生后数天限制补钠,尿量增多后逐渐增加补钠,
需要小心监测液体平衡和电解质水平;
④生后第1天即可使用全静脉营养;
⑤生后第1天,如果无特殊情况即可开始微量肠道
喂养。
3.组织灌注的维持
定期监测血压,维持正常的组织灌注,必要时使用血管活性药物。
4.PDA的治疗
如果有指征(出现PDA早期表现如低血压,特别是舒张压降低,和脉压差增大),可使用药物关闭动脉导管。
【预防】
产前预防,地塞米松6mg肌注q12h×4应于临产24h以前使用。
产后预防,表面活性剂的应用,生后15~30min给药。
【医患沟通】
1、费用问题:机械通气,PS的应用费用昂贵等;
2、疗程及转归,生后头3天为危险期,疗程较长;
3、并发症:早产儿视网膜病(ROP),支气管肺发育不良(BPD),机械通气相关性肺炎(V AP)等。