第一章原料气的制取习题及答案
- 格式:doc
- 大小:1.58 MB
- 文档页数:8

2020年中考化学实验专题复习专题二气体的制取一、单选题(共3题;共6分)1.下列实验操作正确的是( )A. 检验二氧化碳B. 倾倒液体C. 量取液体D. 稀释浓硫酸2.实验室用锌粒和稀硫酸制取氢气,下列实验操作正确的是()A. 稀释硫酸B. 装入锌粒C. 制备氢气D. 收集氢气3.下列实验方案能达到实验目的是()A. AB. BC. CD. D二、实验探究题(共5题;共52分)4.请结合下列实验常用装置,回答有关问题。
(1)图中标有字母的仪器的名称:a________。
(2)实验室用高锰酸钾制取氧气,反应的化学方程式是________。
(3)实验室制取氢气,反应的化学方程式是________。
(4)实验室制取二氧化碳的反应方程式为________;如果用E装置收集该气体,则气体从________端进入(填“b”或“c”),若要用E装置验证二氧化碳能否与水反应,瓶中需装________,且气体从________端进入(填“b”或“c”)。
(5)实验室常用装置C代替装置B制取气体,该装置的优点是________,下列反应适用于该装置的是________(填序号)。
a.大理石和稀盐酸b.锌粒与稀硫酸c.过氧化氢溶液与二氧化锰粉末5.请结合下列实验装置,回答问题:(1)仪器①的名称是________。
(2)若用A 装置制氧气,完全反应后,试管中剩余的固体药品是________。
(3)实验室用双氧水制氧气的发生装置应选择________装置(填上图装置字母),化学方程式为:________。
研究显示O2的体积分数大于36%时可使带火星的木条复燃,因此,氧气验满时采用带火星的木条复燃的方法________(填“可靠”或“不可靠”),为了收集一瓶较纯净的氧气最好选择________装置(填上图装置字母)。
(4)图F 所示的装置可以替代启普发生器制取二氧化碳。
I、该装置右侧放的药品是________,左侧放的药品是________。

习题一、填空题1、德士古气化炉是一种以进料的的气化装置,该炉有两种不同的炉型,根据粗煤气采用的冷却方法不同,可分为和。
2、目前常用的气化炉有、、、。
3、煤气发生炉可根据使用气化剂和煤气热值不同,一般可以分为、、、。
4、气化的基本过程包括、、、等几个过程。
5、煤的气化是指利用进行多相反应产生、、的过程。
6、对于移动床气化炉而言,炉内料层可分为六个层带,自上而下分别为、、、、、。
7、合成氨过程中,要求半水煤气的组成满足:。
8、根据自控水平及维护炉内工作状况稳定的原则,一般循环时间为。
9、在间歇制气过程中,要求在正常生产条件下,吹出物量不应超过总入炉燃料量的,一般生产1 m3的半水煤气,约消耗的空气。
10、烃类蒸汽转化催化剂中,活性组分是,但其以形式存在于催化剂中,因此在使用时必须先用或进行。
二、判断题1、以空气为气化剂生产的煤气叫做水煤气,其组成中含有大量的H2和CO,发热量很高,可作为燃料。
()2、煤中灰分高,有利于气化生产,气化率高。
()3、在气化过程中,煤的粒度越小,气化率越高。
()4、经常使用及长时间停炉的煤气发生炉可直接点火,可以不经烘炉直接投入生产运行。
()5、如果生产中没有及时给煤,炉内料层高度下降,煤气出口温度会带上升。
()6、如果气化炉卸炉不充分,不会影响出口煤气温度。
()7、从发生炉出来的粗煤气温度很高,带有大量的热量同时带有大量的固体杂质。
()8、煤气中的硫主要以SO2、硫醇形式存在。
()9、水碳比越高,越有利于甲烷的蒸汽转化。
()10、压力越高,越有利于甲烷的蒸汽转化。
()11、提高转化温度,有利于甲烷的蒸汽转化,同时可抑制析碳反应的进行。
()12、二段转化过程中,要求催化剂中镍含量要高。
()13、烃类蒸汽转化催化剂的永久性毒物主要是硫化物及砷化物。
()三、名词解释1、空气煤气2、水煤气3、混合煤气4、半水煤气5、水蒸气分解率6、循环时间7、水碳比8、空间速率四、简答题1、原料气制取的途径是什么2、简述煤气化的原理。
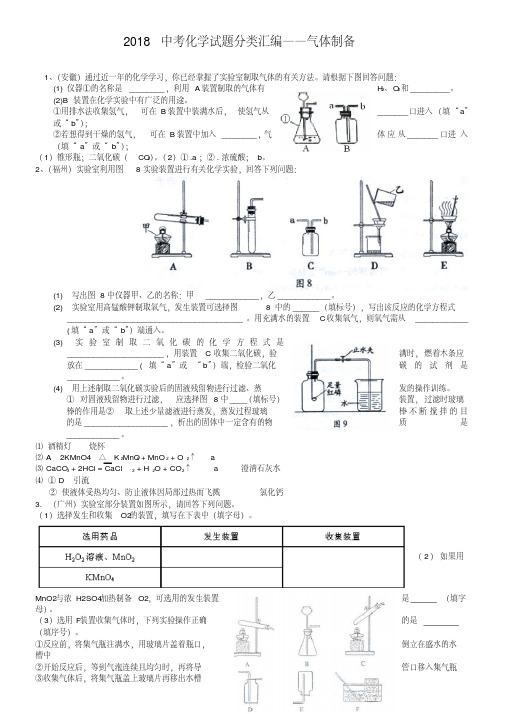
2018中考化学试题分类汇编——气体制备1、(安徽)通过近一年的化学学习,你已经掌握了实验室制取气体的有关方法。
请根据下图回答问题:(1)仪器①的名称是________,利用A装置制取的气体有H2、O2和_________。
(2)B装置在化学实验中有广泛的用途。
①用排水法收集氢气,可在B装置中装满水后,使氢气从_______口进入(填“a”或“b”);②若想得到干燥的氢气,可在B装置中加入________,气体应从_______口进入(填“a”或“b”);(1)锥形瓶;二氧化碳(CO2)。
(2)①.a;②.浓硫酸;b。
2、(福州)实验室利用图8实验装置进行有关化学实验,回答下列问题:(1) 写出图8中仪器甲、乙的名称:甲____________,乙____________。
(2) 实验室用高锰酸钾制取氧气,发生装置可选择图8中的______(填标号),写出该反应的化学方程式________________________________________。
用充满水的装置C收集氧气,则氧气需从____________ (填“a”或“b”)端通入。
(3) 实验室制取二氧化碳的化学方程式是______________________,用装置C收集二氧化碳,验满时,燃着木条应放在____________ (填“a”或“b”)端,检验二氧化碳的试剂是____________。
(4) 用上述制取二氧化碳实验后的固液残留物进行过滤、蒸发的操作训练。
①对固液残留物进行过滤,应选择图8中____(填标号)装置,过滤时玻璃棒的作用是②取上述少量滤液进行蒸发,蒸发过程玻璃棒不断搅拌的目的是___________________,析出的固体中一定含有的物质是____________。
⑴酒精灯烧杯⑵ A 2KMnO4 △ K2MnO4 + MnO2 + O2↑ a⑶ CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ a 澄清石灰水⑷① D 引流②使液体受热均匀、防止液体因局部过热而飞溅氯化钙3. (广州)实验室部分装置如图所示,请回答下列问题。

专题17 气体的制取1.(2017江苏苏州中考)(题文)实验室常用块状大理石和稀盐酸制取CO2气体。
(1)写出实验室制取CO2的化学方裎式:_______________。
(2)若用如图所示装置(固定装置省略)制CO2。
连接好装置后,需检查装置的气密性。
具体操作方法是:先_______________(填字母,下同),后_______________若导管口有气泡,放手后导管内上升一段稳定的水柱,则气密性良好。
A.用手捂住试管B.将导管一端浸入水中(3)实验窒收集CO2可用的方法是_______(填字母)。
A.排水法B.向下排空气法C.向上排空气法(4)实验室常用澄清石灰水检验CO2,写出反应的化学方程式:____________________。
(5)某些大理石中含少量硫化物,使制得的CO2中混有H2S气体。
欲获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下:查阅资料:I.H2S能与NaOH等碱溶液、CuSO4溶液反应。
Ⅱ.CO2中混有的HCl气体可用饱和NaHCO3溶液吸收。
①装置甲中所盛试剂应选用_______(填字母)。
A.浓硫酸B.NaOH溶液C.澄清石灰水D.CuSO4溶液②装置丙的作用是____________。
【答案】CaCO3+2HCl CaCl2+H2O+CO2↑ B A C CO2+Ca(OH)2CaCO3↓+ H2O D 除去CO2中的水蒸气或干燥CO2【解析】(1)大理石的主要成分是碳酸钙,和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)在连接好装置后,将导管一端伸入水中,用手捂住试管,若导管口有气泡冒出,且松手后导管内形成一段水柱,则气密性良好;(3)二氧化碳的密度比空气大且能溶于水,所以可用向上排空气法收集;(4)检验二氧化碳气体用澄清的石灰水,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;(5)①乙装置中的碳酸氢钠溶液是用来除去二氧化碳中混有的氯化氢气体的,则装置甲中所盛试剂是用来除硫化氢气体的,且不与氯化氢反应,所以是硫酸铜溶液;②甲装置中的硫酸铜溶液除去了二氧化碳中混有的硫化氢气体,乙装置中的碳酸氢钠溶液除去了二氧化碳中混有的氯化氢气体,则装置丙是用浓硫酸来吸收二氧化碳中的水蒸气进行干燥。


2019-2019高考化学复习常见气体的制取专题训练(带答案)气体的制取是高考化学必需积累的内容。
下面是常见气体的制取专题训练,请考生刚好检测。
1.下图是制取和收集某气体的试验装置,可用于()A.加热NaHCO3制CO2B.用Cu与稀硝酸反应制NOC.用NH4Cl与浓NaOH溶液反应制NH3D.用Zn和稀硝酸反应制H2【答案】B2.用如右图所示装置进行下列试验,能达到试验目的的是()A.瓶中盛适量浓H2SO4,从B口进气来干燥SO2B.从B口进气,用排空气法收集CO2C.瓶中盛满水,从B口进气,用排水法收集NO2D.瓶中装满水,A口连接导管并伸入量筒中,从B口进气,用排水法测量生成H2的体积【答案】D【解析】浓H2SO4与SO2不反应,可能用浓H2SO4干燥SO2,但进气方向错误,应从A口进;CO2的密度比空气大,应选择向上排空气法收集,因此应从A口进气;NO2与水反应,不能用排水法收集。
3.试验室制取下列气体时,下列尾气处理方法不正确的是()A.制Cl2的尾气:可用NaOH溶液汲取B.制NH3的尾气:可用H2SO4溶液汲取C.制SO2的尾气:可用酸性KMnO4溶液汲取D.制NO2的尾气:可用水汲取【答案】D【解析】NO2与水发生反应:3NO2+H2O===2HNO3+NO,反应生成的NO仍是大气污染物且不溶于水,不符合尾气处理要求。
4.下列试验装置图正确的是()【答案】B【解析】A项中温度计的水银球没有插入液面以下;C项中反应装置无加热仪器,错误;D项中导管不应插入液面以下,错误。
5.(2019保定联考)试验室中制取、洗气并收集气体的装置如下图所示。
仅用此该装置和表中供应的物质完成相关试验,最合理的选项是()选项 a中的液体 b中的固体 c中液体 A 浓盐酸 MnO2 饱和食盐水 B 浓氨水生石灰浓H2SO4 C 浓硫酸 Cu片 NaOH溶液 D 稀HNO3 Cu片 H2O 【答案】D【解析】浓盐酸与MnO2在加热的条件下才能反应,A项不合理;NH3不能用浓硫酸干燥,且氨气极易溶于水,B项不合理;浓硫酸与铜常温下不反应,C项也不合理;稀硝酸与铜反应制NO,NO难溶于水,且水能将NO2重新转化为NO,合理。
合成氨工艺——原料气的制备综述系别:化学与材料工程系课程名称无机化工工艺学班级:姓名:学号:日期:汽转化法、固体燃料气化法、一氧化碳变换。
气态烃类转化、固体燃料气化和重质烃类转化。
其中以天然气为原料的气态烃类转化过程经济效益最高。
关键字:原料气;气态烃蒸汽转化法;固体燃料气化法;一氧化碳变换;引言:制取合成氨的原料气的气态烃主要有天然气,此外还有炼厂气、油田气、焦炉气及裂解气等。
天然气蕴藏在地下多孔层岩石中,是一种多组分的混合气体,主要成分是烷烃,其中甲烷占绝大多数(含量在90%以上),另有少量的乙烷、丙烷和丁烷,一般还含有硫化氢、二氧化碳、氮和水分,以及微量的惰性气体,如氦和氩等。
天然气相对密度0.65,比空气轻,具有无色、无味、无毒的特性。
在800℃高温、一定压力及催化剂作用下,天然气中烷烃和水蒸气发生化学反应,可得到含有H2、CO、CO2、N2、CH4的转化气。
法、固体燃料气化法、一氧化碳变换。
气态烃类转化、固体燃料气化和重质烃类转化。
其中以天然气为原料的气态烃类转化过程经济效益最高。
对天然气为原料生产合成氨的装置,大中型规模多采用前者,而小型合成氨厂则采用后者。
天然气中主要成份为甲烷,还含有乙烷、丙烷及其他少量烯烃等,其中也有极少量的S等对催化剂有害的元素,转化前必须先脱硫。
1、气态烃类转化法气态烃类转化法以轻质烃为原料生产原料气。
有操作连续、工程投资省、能量消耗低等优点。
甲烷制备原料气主要反应主反应:()()()() ()()()()gHgCOgOHCOgHgCOgOHCH222224g3g+=++=+副反应:()()() ()()()()()()()sgsg2sg22224CgOHgHCOCgCOCOgHCCH+=++=+=烃类蒸汽转化法应用最多的是加压两段催化转化法。
甲烷蒸汽转化反应包含反应很多,但经物理化学中判断独立反应数的方法可得出其独立反应数为3个。
甲烷蒸汽转化的生产方式为二段转化,采用二段转化的原因是转化率高必须转化温度高,全部用很高温度,设备和过程控制都不利,设备费用和操作费用都高。
中考化学复习常见气体的制取习题及答案学问点复习以及相应的练习可以关心同学们更好的以及,下面是我给大家带来的中考化学复习常见气体的制取习题及答案,盼望能够关心到大家!中考化学复习常见气体的制取习题及答案一、单项选择题1.(2021泰安)试验室制取气体选择收集(方法)时,下列气体性质不需考虑的是( )A.密度B.可燃性C.溶解性D.能否与水反应2.(2021扬州)下列气体中可用向下排气法收集的是( )A.H2B.N2C.O2D.SO23.(2021湖州)下图所示的装置有许多用途,下列使用方法不正确的是( )第3题图A.排水法收集氧气时,由a口进气B.排空气法收集氢气时,由b口进气C.排水法收集氢气时,由b口进气D.排空气法收集二氧化碳时,由a口进气4.(2021威海)以下是试验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )A.试验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②B.试验室收集氧气和二氧化碳均可使用装置③,气体从导管b 进入C.试验室干燥氯气和二氧化碳均可使用装置④,气体从导管a 进入D.试验室收集的氯气和二氧化碳,均可如图⑤临时存放二、选择填充题5.(2021江西)下列物质用于试验室制取气体,可以直接采纳右图所示装置的是( )第5题图A.用氯酸钾的二氧化锰制取氧气B.用锌粒和稀硫酸制取氢气C.用过氧化氢溶液和二氧化锰制取氧气D.________________________________6.(2021安徽改编)试验室可通过加热高锰酸钾固体制取氧气,下列试验操作正确的是( )A.组装好装置后,检查装置的气密性B.加入药品后,直接将酒精灯火焰对准药品加热C.水槽中有气泡冒出时,马上收集气体D.试验结束时,__________________________(填“先熄灭酒精灯再移出导管”或“先移出导管后熄灭酒精灯”)三、试验与探究题7.(2021云南)依据下图所示的试验装置回答问题。
气体制备真题及答案解析气体制备是化学实验中常见的一项内容,通过不同的化学反应或方法,可以得到各种不同性质的气体。
本文将通过几个常见的气体制备真题,以及对其答案的解析,来帮助读者更好地理解气体制备的原理和方法。
1. 【真题】如何制备氧气?【答案解析】制备氧气的方法很多,最常见的方法是通过加热过氧化氢(H2O2)来产生氧气。
反应方程式如下:2H2O2(aq)→ 2H2O(l)+ O2(g)在实验中,可以使用实验室常用的实验器材:胶塞烧瓶。
首先,将一定量的过氧化氢溶液加入烧瓶中,并在烧瓶口插入玻璃导管,将导管的另一端浸入水中。
然后,轻轻加热胶塞烧瓶,过氧化氢会分解产生氧气,并通过导管冒出水面。
2. 【真题】请描述制备氮气的方法及其原理。
【答案解析】制备氮气的一种方法是通过加热氨合成硝酸(NH4NO3),反应方程式如下:NH4NO3(s)→ N2(g)+ 2H2O(g)该反应是放热反应,因此通过加热固体氨合成硝酸,可以产生氮气和水。
在实验中,可以使用试剂瓶装有氨合成硝酸,然后加热试剂瓶,观察到氮气从口中冒出。
另一种常见的制备氮气的方法是通过液氮的升华得到。
液氮在室温下很容易蒸发,蒸发的气体就是氮气。
实验中,可以使用液氮倒入一个封闭的容器中,等待液氮升华为气体,就可以制备氮气。
3. 【真题】请解释制备氯气的原理及方法。
【答案解析】制备氯气的方法之一是通过盐酸与漂白粉(含二氧化氯)的反应得到。
反应方程式如下:Ca(ClO)2(s)+ 2HCl(aq)→ CaCl2(aq)+ Cl2(g)+ H2O (l)这是一个氧化还原反应,其中盐酸起到了氧化剂的作用,漂白粉中的二氧化氯则起到了被氧化的作用。
在实验中,首先需要在实验室通风良好的条件下操作。
将适量的盐酸倒入试剂瓶中,然后加入适量的漂白粉,观察到产生氯气的气泡。
另外,制备氯气还可以使用电解法。
将食盐溶解在水中,然后使用氯化钠溶液作为电解液,通过电解将氯化钠分解为氯气和氢气。
第一章合成氨原料气的制备1.固体燃料气化:是指用氧或含氧气化剂对固体燃料(指煤和焦炭)进行热加工,使其转化为可燃性气体的过程,简称为“造气”。
气化所得到的可燃性气体称为煤气,进行气化反应的设备称为煤气发生炉。
2.煤气种类:空气煤气:是以空气作为气化剂所制得的煤气。
其成分主要为氮和二氧化碳。
水煤气:系以水蒸气为气化剂制得的煤气,主要成分为氢气和一氧化碳,两者含量之和可达到85%左右。
混合煤气:以空气相水蒸气同时作为气化剂所制得的煤气,其配比量以维持反应能够自热进行为原则。
半水煤气:以适量空气(或富氧空气)与水蒸气作为气化剂,所得气体的组成符合(co十H2)/N z=3.1—3.2(摩尔比)以能满足生产合成氨对氢氧比的要求。
3.间歇式制取半水煤气的工作循环(1)吹风阶段由煤气发生炉底部送入空气,提高燃料层温度,吹风气放空。
(2)上吹制气阶段水蒸气由炉底送入,经灰渣层预热、进入气化层进行气化反应,生成的煤气送入气柜。
随着反应的进行,燃料层下部温度下降,上部升高,造成煤气带走的显热增加。
因此,操作一段时间后需更换气流方向。
(3)下吹制气阶段水蒸气自上而下通过燃料层进行气化反应。
煤气由炉底引出,经回收热量后送入气柜。
由于煤气下行时经过灰渣层温度下降,从而减少了煤气带走的显热损失,燃料层温度均衡。
(4)二次上改阶段水蒸气自炉底送入,煤气炉底部的煤气排净,气作好安全准备。
目的是要将存在于为下一循环吹入空(5)空气吹净阶段目的是要回收存在于煤气炉上部及管道中残余的煤气,此部分吹风气亦应加以回收,作为半水煤气中N2的来源。
制气工艺条件:提高燃料层温度的方法,增加吹风速度,延长吹风时间(降低含CO量)5.烃类蒸气转化法是以气态烃和石脑油为原料生产合成氨最经济的方法。
具有不用氧气、投资省和能耗低的优点。
原理:烃类蒸气转化系将烃类与蒸汽的混合物流经管式炉管内催化剂床层,管外加燃料供热,使管内大部分烃类转化为H2、co和coB。
习题一、填空题1、德士古气化炉是一种以进料的的气化装置,该炉有两种不同的炉型,根据粗煤气采用的冷却方法不同,可分为和。
2、目前常用的气化炉有、、、。
3、煤气发生炉可根据使用气化剂和煤气热值不同,一般可以分为、、、。
4、气化的基本过程包括、、、等几个过程。
5、煤的气化是指利用进行多相反应产生、、的过程。
6、对于移动床气化炉而言,炉内料层可分为六个层带,自上而下分别为、、、、、。
7、合成氨过程中,要求半水煤气的组成满足:。
、8、根据自控水平及维护炉内工作状况稳定的原则,一般循环时间为。
9、在间歇制气过程中,要求在正常生产条件下,吹出物量不应超过总入炉燃料量的,一般生产1 m3的半水煤气,约消耗的空气。
10、烃类蒸汽转化催化剂中,活性组分是,但其以形式存在于催化剂中,因此在使用时必须先用或进行。
二、判断题1、以空气为气化剂生产的煤气叫做水煤气,其组成中含有大量的H2和CO,发热量很高,可作为燃料。
()2、煤中灰分高,有利于气化生产,气化率高。
()3、在气化过程中,煤的粒度越小,气化率越高。
()4、经常使用及长时间停炉的煤气发生炉可直接点火,可以不经烘炉直接投入生产运行。
()5、如果生产中没有及时给煤,炉内料层高度下降,煤气出口温度会带上升。
()6、如果气化炉卸炉不充分,不会影响出口煤气温度。
()~7、从发生炉出来的粗煤气温度很高,带有大量的热量同时带有大量的固体杂质。
()8、煤气中的硫主要以SO2、硫醇形式存在。
()9、水碳比越高,越有利于甲烷的蒸汽转化。
()10、压力越高,越有利于甲烷的蒸汽转化。
()11、提高转化温度,有利于甲烷的蒸汽转化,同时可抑制析碳反应的进行。
()12、二段转化过程中,要求催化剂中镍含量要高。
()13、烃类蒸汽转化催化剂的永久性毒物主要是硫化物及砷化物。
()三、名词解释1、空气煤气2、水煤气>3、混合煤气4、半水煤气5、水蒸气分解率6、循环时间7、水碳比8、空间速率四、简答题1、原料气制取的途径是什么2、简述煤气化的原理。
3、制取半水煤气的工业方法有哪些】4、半水煤气生产特点是什么5、间歇式制半水煤气的工作循环有那几个阶段6、目前常用的气化炉形式有什么形式的7、气化用煤分为哪几类各有什么特点8、析碳反应的危害有哪些9、工业生产中一般采取什么措施防止炭黑生成10、石脑油蒸汽转化工艺和甲烷蒸汽转化工艺有什么不同之处五、论述题1、论煤质中水分含量对气化的影响。
2、论F-T合成反应的影响因素。
|3、论煤的粒度对气化过程的影响。
4、流程分析:①上述工艺流程图中1、2、4、5分别是什么设备有什么作用②该工艺流程属于间歇式生产煤气还是连续化法生产③简述工艺流程。
5、流程分析:"①设备1、2的名称是什么各起什么作用②二段转化炉内发生的主要反应有哪些③简述工艺流程。
习题答案"一、填空题1、水煤浆加压气流床淬冷型全热回收型2、移动床、流化床、气流床、熔融床3、空气煤气、混合煤气、水煤气、半水煤气4、煤的干燥、煤的干馏、煤的热解、煤的反应5、煤或半焦与气化剂碳的氧化物、氢气、甲烷6、空气层、干燥层、干馏层、还原层、氧化层、灰渣层7、n(CO+H2)/n(N2)=、9、4% -1.05m310、镍氧化镍氢气一氧化碳还原二、判断题~1、×2、3、×4、×5、√6、√7、√8、×9、√10、×11、×12、×13、×三、名词解释1、空气煤气:以空气为气化剂生成的煤气。
主要成分:N2,CO,CO2,H2。
2、水煤气:以水蒸气为气化剂生成的煤气。
主要成分:H2,CO,CO2,N2。
3、混合煤气:以空气和适量水蒸气的混合物为气化剂生成的煤气。
主要成分:N2,CO,H2,CO2。
4、半水煤气:以水蒸气加适量的空气或富氧空气为气化剂生成的煤气。
主要成分: H 2,CO ,N 2,CO 2。
5、%100⨯=分解前的水蒸汽量水蒸气分解量水蒸气分解率 6、循环时间:每一工作循环所需要的时间,成为循环时间。
包括五个阶段:吹风阶段、一次上吹、下吹、二次上吹、空气吹净阶段。
7、水碳比:是指进口气体中水蒸气与烃原料中所含碳的摩尔比。
:8、空间速率:单位体积催化剂每小时处理的气量,建成空速。
四、简答题1、答:现在工业上采用天然气、炼厂气、石脑油、焦炉气、重油、焦炭和煤生产合成氨,其在高温下与水蒸气作用,制取粗原料气时都可用下式表示,CnHm+nH 2O(g)=nCO+(n+m/2)H 2(H>0)或C+H 2O=CO+H 2()按供热方式的不同,制取粗原料气有下述三种不同方法:外部供热的蒸汽转化法,内部蓄热的间歇操作法,自热反应的部分氧化法。
2、答:以空气为气化剂时,碳与氧之间的反应为:C+O 2=CO 2,C+1/2O 2=CO,C+CO 2=2CO,CO+1/2O 2=CO 2以水蒸气为气化剂时,碳与水蒸气的反应为C+H 2O=CO+H 2,C+2H 2O=CO 2+2H 2通过有关计算知道,下温度高于900℃,水蒸气与碳反应的平衡产物中,含有等量的H2及CO ,其他组分含量接近于零,随着温度的降低,H 2O 、CO 2及甲烷等平衡含量逐渐增加。
3、答:以水蒸气为气化剂的蒸汽转化法:按气化性质分,以纯氧或富氧(有时也同时加入水蒸气)空气作为气化剂的部分氧化法,按气化炉床层形式分,固定床、流化床、气流床和熔床,按排渣的形态分,固体排渣式和液体排渣式。
4、答:(CO+H 2)与N 2的比例为~以空气为气化剂时,,得含N 2的吹风气。
以水蒸气为气化剂时得到含H2的水煤气,以前者反应热为后者提供反应所需要的热,并能维持系统的自热平衡的话,得不到合格的半水煤气;为维持自热平衡,并得到合格的半水煤气,必须采用以下方法,间歇制气法,富氧空气(纯氧)气化法,外热法三种制取工业半水煤气。
}5、答:五个阶段,按气体流向:吹风阶段,吹入空气,提高燃料层的温度,吹风气放空;一次上吹制气阶段,自下而上吹入水蒸气进行气化反应,燃料层下部温度下降,上部升高;下吹制气阶段,水蒸气自上而下进行反应,使燃料层温度趋于均衡;二次上吹制气阶段,使底部下吹煤气排净,为吹入空气做准备;空气吹净阶段,此部分吹风气加以回收,作为半水煤气中氮的主要来源。
6、答:移动床气化炉、流化床气化炉、气流床气化炉、熔融床气化炉。
7、答:气化用煤分为四类:(1)气化时不黏结也不产生焦油,代表性原料有无烟煤、半焦、贫煤等。
(2)气化时黏结并产生焦油,代表性原料油弱黏结性煤和不黏结性煤。
(3)气化时不黏结但产生焦油,代表性原料有褐煤。
(4)气化时不黏结产生大量甲烷,代表性原料有泥炭。
8、答:因为炭黑覆盖在催化剂表面,不仅堵塞微孔,降低催化剂活性,还会影响传热,使一段转化炉炉管局部过热而缩短使用寿命。
甚至还会使催化剂破碎而增大床曾阻力,影响生产能力。
9、答:(1)实际水碳比大于理论水碳比,这是不会有炭黑生成的前提。
(2)选用活性好、热稳定性好的催化剂,避免进入动力学可能析炭区。
|(3)防止原料气和水蒸气带入有害物质,保证催化剂具有良好的活性。
(4)选择适宜的操作条件。
10:、答:①石脑油需先气化,再以气态形式与水蒸气在镍催化剂作用下进行转化反应;②石脑油在蒸汽转化前需进行严格脱硫;③转化过程必须采用抗析碳的催化剂。
五、论述题1、答:(1)煤中水分的存在形式有:内在水、外在水、化合水。
(2)常压气化:水分含量过高,煤料未经充分干燥就进入干馏层,影响干馏的正常进行,而没有彻底干馏的煤进入气化阶段后,又会降低汽化段的温度,使得甲烷的生成,CO2和H2O的还原反应速率降低,降低煤气产率和气化率。
(3)加压气化:适量的水分有好处,因为水分高,挥发分也高,在干馏阶段半焦的气孔率也较大,当进入气化层时,气化速率快,生成的煤气质量好。
(4)炉型不同对气化用煤的水分含量也不同。
固定床水分含量要求在8-10%,而流化床和气流床要求较低,水分含量要求小于5%。
—2、答:(1)原料气组成:①的高低影响合成反应速率的快慢。
CO和H2含量高合成反应速率快,但放热量多易引起床层超温,且成本高,故要求含量在80-85%之间。
②V(H2)/V(CO)的体积比影响反应进行的方向。
V(H2)/V(CO)比值高有利于饱和烃、轻产物及甲烷的生成;V(H2)/V(CO)比值低有利于烯烃、重产物及氧化物的生成。
③提高合成气中的V(H2)/V(CO)和反应压力可提高利用率。
(2)反应温度F-T合成反应温度主要取决于合成时所选用的催化剂。
每一种催化剂都有合适的温度范围,如钴催化剂合适的温度范围为170-210℃。
(3)反应压力反应压力不仅影响催化剂的活性和寿命,而且也影响产物的组成与产率。
(4)空间速度对于不同催化剂和不同合成方法,都有最适宜的空间速度范围。
3、答:(1)粒度大小与比表面间的关系煤的粒度越小,其比表面积越大。
气流通过床层的流通截面增大,气流速度增大。
(2)粒度大小与传热间的关系煤的粒度越大,传热越慢,煤粒内外的温差越大,粒内焦油蒸汽的扩散和停留时间增加,焦油的热分解加剧,影响焦油的产率。
(3)粒度大小与生产能力间的关系煤的粒度太小,当气化速度较大时,小颗粒的煤有可能被带出气化炉外,从而使气化炉的气化效率降低。
(4)粒度大小对各项气化指标的影响通常情况下,煤的粒度太小,煤耗高,水蒸气和氧气的消耗量增加,气化炉的生产能力下降。
4、 答:① 1:煤气发生炉,主要用于生产煤气;2:燃烧室,回收热量;4:废热锅炉,回收余热;5:洗涤塔,洗涤煤气并进行降温。
②该流程属于间歇式生产半水煤气工艺流程。
④ 固体燃料由加料机从煤气发生炉1顶部间歇加入炉内。
吹风时,空气经鼓风机加压之下而上通过煤气发生炉,吹风气经燃烧室2及废热锅炉4回收热量后由烟囱放空。
燃烧室中加入二次空气,将吹风气中可燃气体燃烧使室内的格子蓄热砖温度升高。
蒸汽上吹制气时,煤气经燃烧室及废热锅炉回收余热后,再经洗气箱3及洗涤塔5进入气柜。
下吹制气时,蒸汽从燃烧室顶部进入,经预热后进入煤气发生炉自上而下流经燃料层。
由于煤气温度较低,直接经洗气箱和洗涤塔进入气柜。
二次上吹时,气体流向与上吹响铜。
空气吹净时,气体经燃烧室、废热锅炉、洗气箱和洗涤塔进入气柜。
燃料气化后,灰渣经螺旋炉箅由刮刀刮入灰箱,定期排出炉外。
5、①1:钴钼加氢反应器,将有机硫转化为硫化氢;2:脱硫槽:将硫化氢脱除。
②二段转化过程中催化剂床层顶部发生的反应为:2222H +O =2H O(g) 222CO+O =2CO ;催化剂床层中部发生的主要反应为:422CH +H O=CO+3H 422CH +CO =2CO+2H 222CO+H O=CO +H ③原料天然气经压缩机加压到后,配入%%的氢于一段转化炉对流段3盘管加热至400℃,进入钴钼加氢反应器1进行加氢反应,将有机硫转化为硫化氢,然后进入氧化锌脱硫槽2脱除硫化氢,然后配入中压蒸汽,使水碳比达左右,进入对流段盘管加热到500-520,送入辐射段4顶部原料气总管,再分配进入各转化管。