抗癌新药Ibrance(palbociclib)使用说明
- 格式:docx
- 大小:34.13 KB
- 文档页数:2

Home·Pfizer’s Potential Mega-Blockbuster Breast Cancer Drug 辉瑞口服乳腺癌药物帕博西尼(palbociclib)Pfizer’s PotentialMega-Blockbuster Breast Cancer Drug 辉瑞口服乳腺癌药物帕博西尼(palbociclib)2015年9月5日辉瑞公司的口服乳腺癌药物帕博西尼(palbociclib, Ibrance, 帕博西林)能否成为重磅炸弹产品?帕博西尼(Palbociclib)是近来备受关注的也是辉瑞最重要试验药物之一,2015年2月3日FDA提前批准辉瑞CDK4/6双抑制剂Palbociclib (商品名Ibrance)作为一线药物治疗ER阳性、HER2阴性乳腺癌,比原定4月13日的PDUFA日期提前两个多月。
分析人士预计,palbociclib每年销售额最高可达到30亿-50亿美元之多。
在一项2期临床研究中,使晚期乳腺癌患者的无进展生存期(PFS)平均增加一倍,但对患者总生存期(OS)未显示有统计学意义上的明显改善。
据研究人员2014年4月在圣地亚哥举行的美国癌症研究协会会议上发布的最新数据显示,雌激素受体阳性转移性乳腺癌患者在合并使用Palbociclib与抗雌激素药物来曲唑时,其PFS平均为20.2个月,相比之下,单独使用来曲唑的患者其PFS平均为10.2个月。
辉瑞公司决定在今年第三季度根据乳腺癌试验药物Palbociclib的2期临床试验结果即向美国食品药监局(FDA)申请上市批准,Palbociclib(又名PD-0332991)最早进入人们视野的是在2012年圣安东尼奥乳腺癌会议上(SABCS),一经发布就引起行业广泛关注。
Palbociclib是一种口服的细胞周期素依赖性激酶4、6的抑制药物,主要通过调节细胞周期发挥作用。
Palbociclib主要通过抑制CDK4/6活性来阻止细胞由G1期到S期进而抑制DNA的合成。

帕博西尼(Ibrance,Palbociclib)FDA官方说明书1 适应症和用途IBRANCE是适用与来曲唑联用对有雌激素受体(ER)-阳性,人表皮生长因子受体2(HER2)-阴性晚期乳癌绝经后妇女作为初始基于内分泌治疗对其转移疾病的治疗。
这个适应症是根据无进展生存(PFS)在加速批准下被批准的[见临床研究(14)]。
对此适应症的继续批准可能取决于在验证性试验中临床获益的证明和描述。
2 剂量和给药方法2.1 一般给药信息IBRANCE的推荐剂量是一粒125 mg胶囊口服服用每天一次共21天,接着不用治疗7天组成一个28天完整疗程。
IBRANCE应与食物服用[见临床药理学(12.3)]与来曲唑2.5 mg每天一次联用连续28-天疗程自始至终给予。
应鼓励患者在每天接近相同时间服用他们的剂量。
如患者呕吐或丢失一剂,在那天不应服用另外剂量。
在寻常的时间服用下一次处方剂量。
IBRANCE胶囊应被整吞(在吞咽前不要咀嚼,压碎或打开胶囊)。
如破碎,压碎或不完整时不应摄入胶囊。
2.2 剂量调整建议根据个体安全性和耐受性调整IBRANCE剂量[见警告和注意事项(5)]。
某些不良反应的处理[见警告和注意事项(5)]可能需要暂时中断剂量/延迟和/或减低剂量,或永久终止如同表1,2和3提供每种剂量减低计划[见警告和注意事项(5),不良反应(6)和临床研究(14)]。
见制造商处方资料对共同给药产品,来曲唑,在毒性事件中剂量调整指导原则和其他相关安全性资料或禁忌证。
为与强CYP3A抑制剂使用剂量调整避免强CYP3A抑制剂的同时使用和考虑没有或小CYP3A抑制作用另外同时药物。
如患者必须用强CYP3A抑制剂共同给药,减低IBRANC剂量至75 mg每天一次。
如强抑制剂被终止,增加IBRANCE剂量(抑制剂的3–5个半衰期后)至强CYP3A抑制剂使用前剂量[见药物相互作用(7.1)和临床药理学(12.3)]。
3 剂型和规格125 mg胶囊:不透明硬明胶胶囊,大小0,有焦糖帽和体,帽上用白墨汁印,体上“PBC 125”。

核准日期:哌柏西利胶囊说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:哌柏西利胶囊商品名称:爱博新® / IBRANCE®英文名称:Palbociclib Capsules汉语拼音:Paiboxili Jiaonang【成份】本品主要成份为哌柏西利其化学名称为:6-乙酰基-8-环戊基-5-甲基-2-[[5-(1-哌嗪基)-2-吡啶基]氨基]吡啶[2,3-d]嘧啶-7(8H)-酮化学结构式:分子式:C24H29N7O2分子量:447.53辅料名称:微晶纤维素、单水乳糖、羧甲基淀粉钠、胶态二氧化硅、硬脂酸镁【性状】本品为胶囊剂,内容物为类白色至黄色粉末。
【适应症】本品适用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性乳腺癌,应与芳香化酶抑制剂联合使用作为绝经后女性患者的初始内分泌治疗。
【规格】(1) 75 mg; (2) 100 mg; (3) 125 mg【用法用量】应由具抗癌药物使用经验的医生开始并监督本品治疗。
推荐剂量哌柏西利的推荐剂量为125 mg,每天一次,连续服用21 天,之后停药7 天(3/1 给药方案),28 天为一个治疗周期。
治疗应当持续进行,除非患者不再有临床获益或出现不可接受的毒性。
当与来曲唑联用时,来曲唑的推荐剂量为 2.5 mg,口服,每天一次,在整个28 天治疗周期连续服药。
具体请参见来曲唑批准的说明书。
给药方法口服。
应与食物同服,最好随餐服药以确保哌柏西利暴露量一致(见【药代动力学】)。
哌柏西利不得与葡萄柚或葡萄柚汁同服(见【药物相互作用】)。
哌柏西利胶囊应整粒吞服(吞服前不得咀嚼、压碎或打开胶囊)。
如果胶囊出现破损、裂纹或其他不完整的情况,则不得服用。
应鼓励患者在每天大约相同的时间服药。
如果患者呕吐或者漏服,当天不得补服。
应照常进行下次服药。
剂量调整建议根据个体安全性和耐受性调整哌柏西利的剂量。
出现某些不良反应时可能需要暂时中断/延迟给药和/或减低剂量,或永久停药来进行控制,请参照表1、2 和 3 中提供的方案进行剂量调整(见【注意事项】和【不良反应】)。

辉瑞(Pfizer)突破性乳腺癌药物 Ibrance获 FDA 批准
辉瑞宣布美国FDA批准IBRANCE® (palbociclib) 125mg扩大适应症,治疗转移性乳腺癌。
现在IBRANCE也被批准联合阿斯利康(AZ)内分泌药物Faslodex(fulvestrant,氟维司群)治疗用于接受内分泌治疗后病情进展的激素受体阳性(HR +),人表皮生长因子受体2阴性(HER2)和晚期或转移性乳腺癌。
辉瑞IBRANCE的补充新药申请(sNDA) 经过审查,基于临床3期的结果,授予突破性治疗指定和优先审查资格。
2015年2月获得第一次批准,适应症是联合诺华的Femara(letrozole,来曲唑)治疗HR +,HER2和晚期或转移性乳腺癌。
这次基于无进展生存期获得加速批准,后续的批准是基于临床3期的数据。
IBRANCE是全球上市的FDA首个批准的CDK4/6 抑制剂。
辉瑞肿瘤科,全球总裁和总经理Liz Barrett说'今天的消息给患有转移性乳腺癌的妇女更多的机会。
因为一年以前,全美医师已经接受了在一线药里,它作为一个标准治疗。
IBRANCE扩展批准有一强有力的证据支持,并强调辉瑞继续致力于研究转移性乳腺癌。
辉瑞为提出IBRANCE这样的创新疗法而自豪。
”
临床3期招募521位患者。
IBRANCE的警告和注意事项包括中性粒细胞减少、肺栓塞和胚胎胎儿毒性。
相关阅读:
Pfizer Receives Expanded FDA Approval For IBRANCE (palbociclib) In HR+, HER2- Metastatic Breast Cancer。
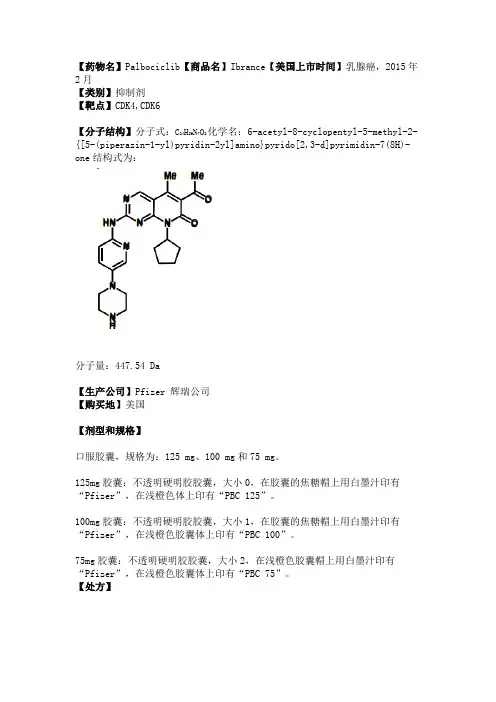
【药物名】Palbociclib【商品名】Ibrance【美国上市时间】乳腺癌,2015年2月【类别】抑制剂【靶点】CDK4,CDK6【分子结构】分子式:C24H29N7O2化学名:6-acetyl-8-cyclopentyl-5-methyl-2-{[5-(piperazin-1-yl)pyridin-2yl]amino}pyrido[2,3-d]pyrimidin-7(8H)-one结构式为:分子量:447.54 Da【生产公司】Pfizer 辉瑞公司【购买地】美国【剂型和规格】口服胶囊,规格为:125 mg、100 mg和75 mg。
125mg胶囊:不透明硬明胶胶囊,大小0,在胶囊的焦糖帽上用白墨汁印有“Pfizer”,在浅橙色体上印有“PBC 125”。
100mg胶囊:不透明硬明胶胶囊,大小1,在胶囊的焦糖帽上用白墨汁印有“Pfizer”,在浅橙色胶囊体上印有“PBC 100”。
75mg胶囊:不透明硬明胶胶囊,大小2,在浅橙色胶囊帽上用白墨汁印有“Pfizer”,在浅橙色胶囊体上印有“PBC 75”。
【处方】Palbociclib是一种黄色至橙色粉有pKa为7.4(第二哌嗪氮)和3.9(吡啶氮)。
在或低于pH 4,Palbociclib行为如同高溶解度化合物。
高于pH 4,药物物质溶解度显著减低。
无活性成分:微晶纤维素,一水乳糖,羟基乙酸淀粉钠,胶体二氧化硅,硬脂酸镁,和硬明胶胶囊壳。
浅橙色,浅橙色/焦糖和焦糖不透明胶囊壳含明胶,红色氧化钛,黄色氧化铁,和二氧化钛;和印刷油墨含虫胶,二氧化钛,氢氧化铵,丙二醇和二甲基硅油。
【作用机理】Palbociclib是一种周期蛋白-依赖激酶(CDK)4和6的抑制剂。
周期蛋白D1和CDK4/6是导致细胞增殖信号通路的下游。
在体外,Palbociclib雌激素受体(ER)-阳性乳癌细胞株通过阻断细胞从细胞周期G1进入S期的进展减低细胞增殖。
用palbociclib和抗雌激素的联合处理与单独各个药物处理比较,乳癌细胞株导致视网膜母细胞瘤蛋白(Rb)磷酸化的减低导致减低E2F表达和信号和阻止增加生长。

一、概述卵巢癌是一种高度恶性的妇科肿瘤,其发病率位居女性生殖系统恶性肿瘤的第二位。
卵巢癌的治疗方法主要包括手术、化疗、放疗、靶向治疗和免疫治疗等。
帕博西尼(Pazopanib)是一种多靶点抗血管生成药物,近年来在卵巢癌的治疗中取得了显著的疗效。
本文将详细介绍卵巢癌帕博西尼治疗方案。
二、帕博西尼的作用机制帕博西尼是一种口服的小分子多靶点抗血管生成药物,主要通过抑制血管内皮生长因子(VEGF)受体2(VEGFR2)的活性,阻断肿瘤血管生成,从而抑制肿瘤生长和转移。
此外,帕博西尼还能抑制其他与肿瘤生长和转移相关的信号通路,如血小板衍生生长因子受体(PDGFR)、成纤维细胞生长因子受体(FGFR)等。
三、帕博西尼治疗方案1. 适应症帕博西尼主要用于以下情况:(1)晚期卵巢癌患者,经一线化疗后疾病进展或复发。
(2)晚期卵巢癌患者,一线化疗期间或治疗后病情稳定,但无手术指征。
2. 用法用量帕博西尼口服,每日一次,每次750mg,餐后服用。
患者应根据医生的建议调整剂量,并在治疗过程中定期复查肝肾功能。
3. 治疗周期帕博西尼的治疗周期为21天,即连续服用帕博西尼21天,休息7天,然后重复上述过程。
4. 联合治疗帕博西尼可与其他化疗药物联合使用,以提高疗效。
以下是一些常见的联合治疗方案:(1)帕博西尼+卡铂+紫杉醇:适用于晚期卵巢癌患者的一线治疗。
(2)帕博西尼+顺铂+长春瑞宾:适用于晚期卵巢癌患者的二线治疗。
5. 不良反应及处理帕博西尼的不良反应主要包括:(1)高血压:帕博西尼可引起血压升高,患者需定期监测血压,必要时调整剂量或使用降压药物。
(2)手足综合症:表现为手足麻木、疼痛、肿胀等症状,可使用抗过敏药物、冷敷等方法缓解。
(3)皮疹:帕博西尼可引起皮疹,可使用抗过敏药物、外用激素等治疗。
(4)肝肾功能损害:帕博西尼可引起肝肾功能损害,患者需定期复查肝肾功能,必要时调整剂量或停药。
四、疗效评估帕博西尼在卵巢癌治疗中的疗效主要体现在以下几个方面:1. 提高无进展生存期(PFS):帕博西尼可显著提高晚期卵巢癌患者的无进展生存期。

核准日期:哌柏西利胶囊说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:哌柏西利胶囊商品名称:爱博新® / IBRANCE®英文名称:Palbociclib Capsules汉语拼音:Paiboxili Jiaonang【成份】本品主要成份为哌柏西利其化学名称为:6-乙酰基-8-环戊基-5-甲基-2-[[5-(1-哌嗪基)-2-吡啶基]氨基]吡啶[2,3-d]嘧啶-7(8H)-酮化学结构式:分子式:C24H29N7O2分子量:447.53辅料名称:微晶纤维素、单水乳糖、羧甲基淀粉钠、胶态二氧化硅、硬脂酸镁【性状】本品为胶囊剂,内容物为类白色至黄色粉末。
【适应症】本品适用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性乳腺癌,应与芳香化酶抑制剂联合使用作为绝经后女性患者的初始内分泌治疗。
【规格】(1) 75 mg; (2) 100 mg; (3) 125 mg【用法用量】应由具抗癌药物使用经验的医生开始并监督本品治疗。
推荐剂量哌柏西利的推荐剂量为125 mg,每天一次,连续服用21 天,之后停药7 天(3/1 给药方案),28 天为一个治疗周期。
治疗应当持续进行,除非患者不再有临床获益或出现不可接受的毒性。
当与来曲唑联用时,来曲唑的推荐剂量为 2.5 mg,口服,每天一次,在整个28 天治疗周期连续服药。
具体请参见来曲唑批准的说明书。
给药方法口服。
应与食物同服,最好随餐服药以确保哌柏西利暴露量一致(见【药代动力学】)。
哌柏西利不得与葡萄柚或葡萄柚汁同服(见【药物相互作用】)。
哌柏西利胶囊应整粒吞服(吞服前不得咀嚼、压碎或打开胶囊)。
如果胶囊出现破损、裂纹或其他不完整的情况,则不得服用。
应鼓励患者在每天大约相同的时间服药。
如果患者呕吐或者漏服,当天不得补服。
应照常进行下次服药。
剂量调整建议根据个体安全性和耐受性调整哌柏西利的剂量。
出现某些不良反应时可能需要暂时中断/延迟给药和/或减低剂量,或永久停药来进行控制,请参照表1、2 和 3 中提供的方案进行剂量调整(见【注意事项】和【不良反应】)。

博来霉素化疗方案博来霉素(Bortezomib)是一种肿瘤治疗药物,属于蛋白酶体抑制剂,常用于治疗多发性骨髓瘤等癌症。
本文将详细介绍博来霉素化疗方案的具体内容和使用方法,以及它在癌症治疗中的作用和效果。
一、药物简介博来霉素是一种特定的蛋白酶体抑制剂,可通过抑制细胞中负责蛋白质降解的酶体功能,进而干扰癌细胞的生存和增殖能力。
由于博来霉素的作用机制与传统化疗药物不同,它被广泛应用于治疗多发性骨髓瘤和其他一些血液系统肿瘤。
二、化疗方案博来霉素化疗方案通常是结合其他药物进行联合治疗,以达到更好的治疗效果。
下面是一种常见的使用博来霉素的化疗方案:1. 药物组合:博来霉素常与鸦片酮(Dexamethasone)和环孢素A (Cyclophosphamide)联合使用。
2. 用药途径:博来霉素可通过静脉注射或皮下注射的方式给药,具体剂量应根据医生的建议来确定。
3. 用药周期:博来霉素的化疗方案通常是按照一定的周期进行治疗,每个周期可持续4-6周。
在这个周期内,博来霉素剂量和给药频率会根据患者的具体情况进行调整,以达到最佳的治疗效果。
4. 用药时间:博来霉素的化疗方案通常需要连续几个周期进行治疗,具体的疗程时间也会根据患者的反应和病情来调整。
三、治疗效果博来霉素化疗方案在治疗多发性骨髓瘤等癌症中已经被广泛应用,并取得了一定的疗效。
博来霉素通过抑制癌细胞内的蛋白质降解酶体,可以有效减少癌细胞的生存和增殖能力。
此外,博来霉素还能够促进早期凋亡(细胞死亡)和抑制肿瘤血管生长,从而达到治疗肿瘤的效果。
尽管博来霉素化疗方案在治疗癌症中取得了一定的成功,但是它仍然可能引起一些治疗相关的不良反应。
常见的不良反应包括血小板减少、贫血、感染等。
因此,在使用博来霉素进行治疗时,医生会根据患者的具体情况和需要进行详细评估和护理。
总结:博来霉素化疗方案是一种常用于治疗多发性骨髓瘤和其他血液系统肿瘤的方案。
它通过抑制蛋白质降解酶体的功能,有效干扰癌细胞的生存和增殖能力。


阿布昔替尼化学结构-概述说明以及解释1.引言1.1 概述阿布昔替尼(Abemaciclib)是一种新型的抗癌药物,属于一类被称为“CDK4/6抑制剂”的药物。
CDK4和CDK6是细胞周期调节蛋白激酶,它们在细胞生长和增殖中起着重要的调控作用。
阿布昔替尼的化学结构与其他CDK4/6抑制剂有所不同,这使得它具有独特的药理特性和潜在的药效。
阿布昔替尼的化学结构中包含苯并三唑环和吡嗪环,并与CDK4/6结合,从而阻止其与细胞周期相关的底物结合,进而抑制肿瘤细胞的增殖。
与传统的化疗药物相比,阿布昔替尼能够更准确地靶向肿瘤细胞,并且对正常细胞的毒副作用较小。
这使得阿布昔替尼成为治疗某些癌症类型的有前景的药物。
阿布昔替尼的合成方法是通过有机合成化学反应来合成的。
具体来说,它是通过苯并三唑和吡嗪为原料,经过多步反应合成而成。
这种合成方法具有高效、高选择性和可控性的特点,能够在合成过程中控制反应的条件和操作,从而得到高纯度和高产率的阿布昔替尼。
目前,阿布昔替尼已经在临床试验中显示出良好的治疗效果,特别适用于乳腺癌、胰腺癌和肾透明细胞癌等恶性肿瘤的治疗。
它可以作为单药使用,也可与其他抗癌药物联合使用,以增强疗效。
在医药领域的前景中,阿布昔替尼被认为是一种具有重要且广泛应用的药物。
随着对其作用机制的深入研究和临床试验的不断推进,阿布昔替尼有望成为治疗多种癌症的首选药物之一。
未来,可以预见,阿布昔替尼的化学结构还有很大的发展潜力。
通过对其结构进行改造和修饰,可以进一步提高其抗肿瘤活性和药物代谢特性,使其更适合临床应用。
因此,对阿布昔替尼化学结构的研究和展望具有重要意义,并且值得进一步深入探索。
1.2文章结构文章结构本文分为引言、正文和结论三个部分。
引言部分主要是对阿布昔替尼的背景和重要性进行概述。
通过引入相关背景知识和对阿布昔替尼的简要介绍,让读者对接下来的内容有一个整体的认识。
正文部分是整篇文章的核心部分,主要包括阿布昔替尼的化学结构及特点、阿布昔替尼的合成方法和阿布昔替尼的应用领域三个方面的内容。

乳腺癌用药哌柏西利 palbociclib
制剂与规格:胶囊:75mg、100mg、125mg
适应证:本品适用于激素受体(HR)阳性、HER2阴性的局部晚期或转移性乳腺癌:(1)与芳香化酶抑制剂联合使用,作为绝经后女性患者的初始内分泌治疗。
鉴于芳香化酶抑制剂的作用机制,绝经前/围绝经期女性接受哌柏西利与芳香化酶抑制剂联合治疗时,必须进行卵巢切除或使用促黄体生成激素释放激素(LHRH)激动剂抑制卵巢功能。
(2)与氟维司群联合使用治疗内分泌治疗后进展的转移性乳腺癌女性患者。
哌柏西利联合氟维司群用于绝经前/围绝经期女性,需要与LHRH激动剂联合用药。
(3)男性乳腺癌:2019年4月4日,FDA批准了美国哌柏西利HR阳性、HER2阴性晚期男性乳腺癌的适应证。
合理用药要点:
1.在接受哌柏西利治疗前,应在有资质的病理实验室进行检测证实HR阳性、HER2阴性患者方可使用。
HR阳性的定义为雌激素受体免疫组化染色显示超过1%的肿瘤细胞核染色阳性。
HER2阴性的定义为IHCO-1+或FISH阴性。
2.本品起始剂量是125mg/d,4周为一个用药周期:服药3周后需停药1周。
应与食物同服,不得与葡萄柚或葡萄柚汁同服,最好随餐服药以确保哌柏西利暴露量一致。
1。
处方信息要点---------------------- 警告和注意事项 --------------------------这些要点并未包含安全和有效使用 IBRANCE 所需的所有信息。
请参见 IBRANCE 的完整处方信息。
• 血液方面:可能发生中性粒细胞减少症。
在IBRANCE 治疗开始前、每个周期开始时以及前两个周期的第 14 天监测全血细胞计数。
(5.1) IBRANCE ®(Palbociclib )口服胶囊 美国首次批准时间:2015 年 • 感染:监测体征和症状并酌情暂停给药。
(5.2)------------------------ 适应症及用法 ------------------------------------•胚胎-胎仔毒性:可导致胎仔伤害。
向患者告知对胎儿的毒性并使用有效避孕措施。
(5.4, 8.1, 8.3)IBRANCE 是一种激酶抑制剂,适用于与来曲唑联合用药,治疗雌激素受体(ER )阳性、人体表皮生长因子受体 2(HER2)阴性的晚期乳腺癌绝经后女性患者,以作为针对转移性疾病的初始内分泌疗法。
该适应症根据无进展生存期(PFS )获得加速批准。
该适应症的继续批准可能取决于在一项验证性试验中的临床获益验证和描述。
(1)--------------------------- 不良反应 -----------------------------最常见的不良反应(发生率 ≥10%)包括中性粒细胞减少症、白细胞减少症、疲劳、贫血、上呼吸道感染、恶心、口腔炎、脱发、腹泻、血小板减少症、食欲减退、呕吐、衰弱、周围神经病变和鼻衄。
(6) -------------------- 用法用量 -------------------------------------------如要报告疑似不良反应,请通过以下方式联系辉瑞公司:与来曲唑合用时,IBRANCE 胶囊与食物同服。
Ibrance(palbociclib)使用说明书2015年第一版批准日期:2015年2月3日;公司:PfizerInc.加速批准,突破性治疗指定和优先审评FDA药品评价和研究中心血液学和肿瘤产品室主任说:“palbociclib添加至来曲唑对被诊断有转移乳癌妇女提供一种新颖治疗选择,”“FDA承诺通过我们的加快批准监管加快癌症药物的上市批准。
”完整处方资料。
IBRANCE人表皮生剂量和给药方法?IBRANCE胶囊是与食物与来曲唑联用口服。
(2)?⑴推荐开始剂量:125mg每天一次与食物服用共21天接着7天不治疗。
(2.1)?⑵建议根据个体安全性和耐受性中断和/或剂量减低给药。
(2.2)?剂型和规格胶囊:125mg,100mg,和75mg(3)?禁忌证无(4)?警告和注意事项⑴血液学:可能发生中性粒细胞减少。
监视完全血细胞计数IBRANCE治疗开始前和在每个疗程开始,以及在头两个疗程第14天,和当临床指示时。
(5.1)?(5.4,8.1,不良反应CYP3ACYP3ACYP3A底物:有狭窄治疗指数敏感CYP3A4底物当与IBRANCE同时给予时剂量可能需要减低。
(7.3)?完整处方资料1适应证和用途?IBRANCE是适用与来曲唑联用对有雌激素受体(ER)-阳性,人表皮生长因子受体2(HER2)-阴性晚期乳癌绝经后妇女作为初始基于内分泌治疗对其转移疾病的治疗.? 这个适应证是根据无进展生存(PFS)在加速批准下被批准的[见临床研究(14)]。
对此适应证的继续批准可能取决于在验证性试验中临床获益的证明和描述。
2剂量和给药方法?2.1一般给药信息?IBRANCE疗7与来曲唑剂量。
2.2/或减低剂(5),不良反应(6)和临床研究(14)]。
见制造商处方资料对共同给药产品,来曲唑,在毒性事件中剂量调整指导原则和其他相关安全性资料或禁忌证。
为与强避免强如抑制3125mg“PBC125”100mg体上75mg“PBC75”。
收藏贴!乳腺癌靶向药物:帕博西尼Ibrance(palbociclib)显奇效全球肿瘤医生网 second_opinion全球肿瘤医生网,国内最专业的综合抗癌网站,肿瘤国内顶尖专家会诊、国际顶尖专家会诊、国际癌症中心就医、出国就医、顶尖癌症基因检测个性化治疗平台。
癌症治疗进展可能令人沮丧, 然而在加州大学洛杉矶分校(UCLA)肿瘤学家Richard Finn报告说,在乳腺癌的标准治疗中增加一种名为帕博西尼Ibrance(palbociclib)的药物,较来曲唑可使乳腺癌患者无进展生存期,从平均10个月增加到20个月。
因为其良好的治疗效果,2015年4月16日,辉瑞(Pfizer)突破性乳腺癌药物Ibrance (palbociclib)在2015年2月凭借一项II期研究的无进展生存期(PFS)数据获得了FDA的加速批准,用作乳腺癌的一线治疗。
IBRANCE(palbociclib) capsules 帕博西尼IBRANCE(palbociclib) capsules 帕博西尼, palbociclib是一种实验性、口服、靶向性制剂,能够选择性抑制细胞周期蛋白依赖性激酶4和6(CDK4/6),恢复细胞周期控制,阻断肿瘤细胞增殖。
细胞周期失控是癌症的一个标志性特征,CDK4/6在许多癌症中均过度活跃,导致细胞增殖失控。
CDK4/6是细胞周期的关键调节因子,能够触发细胞周期从生长期(G1期)向DNA复制期(S1期)转变。
在雌激素受体阳性(ER+)乳腺癌中,CDK4/6的过度活跃非常频繁,而CDK4/6是ER信号的关键下游靶标。
临床前数据表明,CDK4/6和ER 信号双重抑制具有协同作用,并能够抑制G1期ER+乳腺癌细胞的生长。
IBRANCE是一种口服胶囊,一般与来曲唑联用。
推荐剂量:125mg每天一次与食物服用共21天接着7天不治疗。
FDA于2013年4月授予palbociclib治疗晚期或转移性ER+/HER2-乳腺癌的突破性疗法认定。
乳腺癌用药哌柏西利 palbociclib制剂与规格:胶囊:75mg、100mg、125mg适应证:本品适用于激素受体(HR)阳性、HER2阴性的局部晚期或转移性乳腺癌:(1)与芳香化酶抑制剂联合使用,作为绝经后女性患者的初始内分泌治疗。
鉴于芳香化酶抑制剂的作用机制,绝经前/围绝经期女性接受哌柏西利与芳香化酶抑制剂联合治疗时,必须进行卵巢切除或使用促黄体生成激素释放激素(LHRH)激动剂抑制卵巢功能。
(2)与氟维司群联合使用治疗内分泌治疗后进展的转移性乳腺癌女性患者。
哌柏西利联合氟维司群用于绝经前/围绝经期女性,需要与LHRH激动剂联合用药。
(3)男性乳腺癌:2019年4月4日,FDA批准了美国哌柏西利HR阳性、HER2阴性晚期男性乳腺癌的适应证。
合理用药要点:1.在接受哌柏西利治疗前,应在有资质的病理实验室进行检测证实HR阳性、HER2阴性患者方可使用。
HR阳性的定义为雌激素受体免疫组化染色显示超过1%的肿瘤细胞核染色阳性。
HER2阴性的定义为IHCO-1+或FISH阴性。
12.本品起始剂量是125mg/d,4周为一个用药周期:服药3周后需停药1周。
应与食物同服,不得与葡萄柚或葡萄柚汁同服,最好随餐服药以确保哌柏西利暴露量一致。
3.常见副作用为骨髓抑制,因此建议在使用本品前行血常规检查,在中性粒细胞绝对计数≥1.0×109/L且血小板计数≥50×109/L时开始接受治疗。
在第15天检测血常规,中性粒细胞绝对计数0.5×109/L至≤1.0×109/L时,可以继续服药至21天。
如果第15天中性粒细胞绝对计数≤0.5×109/L 时,需暂停服用哌柏西利,直至恢复至≥1.0×109/L,再以降低一个剂量级开始下一疗程治疗。
如果下个疗程前一天检测血常规,中性粒细胞恢复至≥1.0×109/L,可以原剂量开始下一疗程,但如果延迟恢复,则需要降低一个剂量级开始下一疗程。
乳腺癌特效药Ibrance(Palbociclib)显示积极疗效!【药品导读】Ibrance(Palbociclib)获得了FDA突破性疗法认定以及优先审批资格,经加速审批之后获批上市,用于联合来曲唑作为内分泌治疗为基础的初始方案用于治疗ER /HER2-绝经后晚期乳腺癌。
目前该药已获香港各大医院引进。
商品名:Ibrance药品名:Palbociclib中文名:帕博西尼性状:胶囊剂量:125 mg,100 mg,75 mg咨询方:港安健康国际医疗适应症:用于激素受体(HR)阳性,人表皮生长因子受体2(EFGR2)阴性的进展性或转移性乳腺癌,联用于以下两种情况:1.与芳香酶抑制剂联合用于绝经后乳腺癌患者的首次内分泌基础治疗;2.与氟维司群联合用于内分泌治疗后进展的乳腺癌患者。
Ibrance药物说明Ibrance是一种细胞周期蛋白依赖性激酶4和6(D-CDK4/6)的抑制剂。
周期蛋白D1和CDK4/6是细胞增殖信号通路的下游物质。
体外试验表明,Ibrance通过阻断细胞从细胞周期G1进入S期,以减低雌激素受体(ER)阳性乳腺癌细胞株的增殖。
与单独各个药物比较,Ibrance和抗雌激素药物联用可降低癌细胞株的视网膜母细胞瘤蛋白(Rb)磷酸化,从而减低E2F表达,阻止其生长。
在体外试验表明,Ibrance和抗雌激素药物联用可加速ER阳性乳腺癌细胞株衰老,在停药后6天仍有效果。
体内研究用一种ER阳性乳腺癌异种移植动物模型显示Ibrance和来曲唑(Letrozole)联合可抑制Rb磷酸化,从而抑制肿瘤生长。
Ibrance药物试验数据PALOMA-1试验达到了其主要研究重点,证实了IBRANCE 联合来曲唑治疗 ER /HER2- 初治的局部晚期或转移性乳腺癌患者较单药来曲唑延长了患者 PFS。
接受 IBRANCE 联合来曲唑治疗实质性的改善了患者的 PFS,联合组患者中位 PFS 为 20.2 月(95% CI: 13.8, 27.5),接受来曲唑单药治疗患者PFS 为10.2 月(95% CI: 5.7, 12.6)(HR=0.488 [95% CI: 0.319, 0.748])。
第一个乳腺癌免疫治疗药物Ibrance(palbociclib)胶囊剂被美国FDA加速批准。
FDA药品评价和研究中心血液学和肿瘤产品室主任Richard Pazdur医学博士说:“palbociclib添加至来曲唑对被诊断有转移乳癌妇女提供一种新颖治疗选择,”“FDA承诺通过我们的加快批准监管加快癌症药物的上市批准。
”
Ibrance(palbociclib)胶囊剂,供口服使
用。
美国最初批准:2015年
【适应症和用法】
Ibrance是组合表示与来曲唑治疗绝经后
妇女的雌激素受体(ER)阳性,人表皮生长因
子受体2(HER2)阴性晚期乳腺癌作为初始内
分泌为基础的治疗对于其转移性疾病治疗中
的激酶抑制剂。
这个指示下基于无进展生存期
(PFS)加速审批核准。
继续批准该适应症可
能是在验证和临床获益说明队伍的验证试验。
【用法用量】
Ibrance胶囊口服与食物中来曲唑的组合。
推荐起始剂量:125毫克,每天一次与食物一起服用21天,随后7天假治疗。
中断给药和/或减量是基于个人的安全性和耐受性建议。
【剂型和规格】
胶囊:125毫克,100毫克和75毫克。
【警告和注意事项】
血液系统:白细胞减少,可能会发生。
监测全血细胞计数前两个周期的开始Ibrance疗法中,并在每个周期的开始之前,以及在第14天,并作为临床指征。
感染:用于监控的症状和体征,并扣留剂量适当。
胚胎胎儿毒性:可引起胎儿造成伤害。
提醒潜在风险的患者胎儿,并使用有效的避孕措施。
【不良反应】
最常见的不良反应(发生率≥10%)为白细胞减少,白细胞减少,乏力,贫血,上呼吸道感染,恶心,口腔炎,脱发,腹泻,血小板减少症,食欲下降,呕吐,无力,周围神经病变,和鼻出血。
【药物相互作用】
CYP3A抑制剂:避免同时使用Ibrance具有较强CYP3A酶抑制剂。
如果不能避免的强抑制剂,降低Ibrance剂量。
CYP3A诱导剂:避免同时使用Ibrance具有较强的和中度CYP3A诱导剂。
CYP3A的底物:敏感CYP3A4底物具有窄治疗指数的剂量可能需要降低与Ibrance同时给予时。
【好e友Pharmacy】转载编辑
好e友Pharmacy提供专科药物、处方药物、非处方药物、药物配置、药物注射以及各类非住院患者的药物分发、咨询、配送等各项服务。
美国是医药分开的国家,药房全部实行严格的处方药与非处方药分类管理。
对处方药的销售,必须凭美国医生(电子/纸质)处方。
如今国内患者可以依托科技,实现远程的病历交互,由美国医生根据患者病情开具电子处方,以正规渠道在美国药房购买到处方药。