工业分析化学第九章气体分析
- 格式:ppt
- 大小:3.45 MB
- 文档页数:72

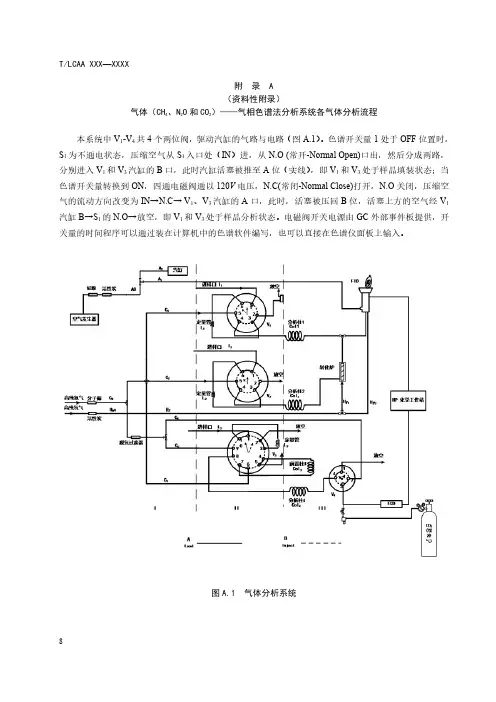
T/LCAA XXX—XXXX8附录A(资料性附录)气体(CH4、N2O和CO2)——气相色谱法分析系统各气体分析流程本系统中V1-V4共4个两位阀,驱动汽缸的气路与电路(图A.1)。
色谱开关量1处于OFF位置时,S1为不通电状态,压缩空气从S1入口处(IN)进,从N.O(常开-Normal Open)口出,然后分成两路,分别进入V1和V3汽缸的B口,此时汽缸活塞被推至A位(实线),即V1和V3处于样品填装状态;当色谱开关量转换到ON,四通电磁阀通以120V电压,N.C(常闭-Normal Close)打开,N.O关闭,压缩空气的流动方向改变为IN→N.C→V1、V3汽缸的A口,此时,活塞被压回B位,活塞上方的空气经V1汽缸B→S1的N.O→放空,即V1和V3处于样品分析状态。
电磁阀开关电源由GC外部事件板提供,开关量的时间程序可以通过装在计算机中的色谱软件编写,也可以直接在色谱仪面板上输入。
图A.1气体分析系统T/LCAA XXX —XXXX9A.1甲烷(CH 4)分析流程如图A.1,首先使六通阀1(V 1)处于样品装填位置(A 位),此时V 1的阀孔2→3、4→5、6→1两两相通。
用注射器将样气从进样口(I 1)推入V 1,样气经V 1阀孔1→6充满定量管L 1,经V 1阀孔3→2,最终经浮子流量计(FL)放空。
转动V 1使其切换到样品分析位置(B 位),此时V 1的阀孔1→2、3→4、5→6两两相通。
载气C 1从V 1的5→6通过L 1再经3→4将样品注入色谱柱1(Col 1)。
气体样品中的CH 4在Col 1中与其它成分分离后进入FID 检测。
A.2二氧化碳(CO 2)分析流程如图A.1,气体样品中CO 2进样、分离、检测的整个过程与CH 4相似,I 2、V 2、Col 2组成了CO 2分析气路,C 2为该气路的载气,最终将CO 2成分推入镍触媒转化器,在375℃高温下被H 2还原定量转化成CH 4后被FID 检测。


化工气体知识点总结大全一、概述化工气体是指化学工业生产、储存和使用中的气态物质,主要包括工业气体、燃料气体和工艺气体。
化工气体在化学工业生产中扮演着重要的角色,广泛用于各种化学反应、氧化和还原过程、燃烧和气体分离等过程中。
本文将介绍化工气体的相关知识点,包括气体的性质、制备、应用以及安全等方面的内容。
二、气体的性质1. 气体的物理性质气体是一种没有固定形状和容积的物质,具有很强的流动性和膨胀性。
气体的压力、体积、温度和物质的量之间存在着一定的关系,这就是气体状态方程。
气体的物理性质受压力、温度和物质的量的影响很大,而且气态分子自由度高,分子之间的距离大,相互作用弱。
2. 气体的化学性质气体在化学反应中往往表现出原子性和离子性特点。
气体分子之间没有明显的相互作用,分子直径较小,气化度大,活动度高。
气体可以很容易地与其他物质发生化学反应,参与氧化、还原、酸碱中和等过程。
3. 气体的密度气体的密度一般比固态和液态物质的密度小得多,与压力和温度有一定的关系。
气态分子之间的相互作用力较小,密度较低。
在标准状态下(1大气压,0℃),1摩尔气体体积为22.4升,即摩尔体积。
4. 气体的溶解性气体与液体和固体可相溶。
气体的溶解度随压力的增加而增加,随温度的升高而减小。
气体的溶解度与压力成正比,与温度成反比。
5. 气体的导电性气体在电场中可以产生电离现象,形成等离子体。
气体的导电性与气体种类和压力有关,低压下气体的导电性通常较弱。
气体放电和等离子体的形成是气体在化学工业中的重要应用。
三、气体的制备1. 物理方法物理方法主要包括压缩、液化和分馏三种。
压缩和液化是通过增加气体分子之间的相互作用力使气体凝聚成液体,然后通过分馏抽取气体。
2. 化学方法化学方法主要包括化学反应和化学分解两种。
化学反应是通过反应生成气体,然后通过吸附或干燥等步骤进行气体的分离和提纯。
化学分解是通过加热或加入催化剂使一种物质分解生成气体。
3. 生物方法生物方法主要是利用生物生产气体,例如利用微生物菌落代谢产生气体。







气体分析操作规程(最新版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的安全管理制度,如通用安全、交通运输、矿山安全、石油化工、建筑安全、机械安全、电力安全、其他安全等等制度,想了解不同制度格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, this shop provides you with various types of safety management systems, such as general safety, transportation, mine safety, petrochemical, construction safety, machinery safety, electrical safety, other safety, etc. systems, I want to know the format and writing of different systems ,stay tuned!气体分析操作规程(1)使用前先充足电,方法:打开仪器电源,把充电电池的残余电用光后,把仪器的电源线接到220伏交流源上即开始充电,保持该状态8小时,即可;(2)使用时检查仪器过滤器是否需要更换,抽气泵是否为抽气状态负压;(3)把仪器带到空气清新的地方,打开电源,进行自校;(4)自校完成后,根据实际情况选择燃料种类,仪器调零;(5)把取样管放入所需需测量的气体中,开始测量;(6)待读数变化较稳时记下读数。
第一章气体分析概论第一节气体分析的基本概念一、气体分析的定义和目的1.1气体分析的定义所谓气体分析就是确定气体中某些成分是什么和是多少的分析活动,包括对各种空间、不同状态和不同组成条件下气体成分的分析。
本书所称气体分析特指对作业场所中与生产安全、劳动卫生和消防安全有关的气体成分的全部分析活动,属于专业性气体分析。
1.2 气体分析的目的安全和消防工程中的气体分析活动的基本目的是通过监视了解作业场所空气中有害成分的含量,为实现安全生产和预防火灾、扑灭火灾的科学决策与及时采取措施提供科学依据。
气体分析的目的因对象的不同而有区别,包括广义气体分析和安全与消防工程特定的气体分析,一般可以归纳为下列几个方面:1) 为实现和谐与稳定服务:为保护生态环境、保护人民群众健康、保障劳动者安全与健康,消除或降低安全事故与火灾损失提供技术支撑。
2) 为安全管理服务:通过对生产场所和生产过程中空气和气体成分的监督与系统调控,进行安全和消防预警,规避风险,降低事故概率。
3) 为制定目标服务:气体分析可以为制定环境保护、生态文明、安全生产和清洁生产等提出量化、可考核的科学目标和指标。
4) 为执行法规服务:气体分析是监督检查和调查取证的重要手段,其成果能够直接为确定状态、判断责任、确定原因、推断过程提供依据。
5)为发展科学技术服务:通过气体分析,可以发现在环保、安全、消防等方面的差距和问题,能够推动、发展创新。
6)为宣传教育服务:气体分析的成果可以用于宣传法规政策、公开信息、普及环境保护、安全生产和消防工作科学知识。
7) 为相关行政许可服务,现场气体分析成果,为有关管理部门审批安全和消防生产许可提供依据。
1.3 气体分析中的定性分析与定量分析气体分析的基本任务或基本职能是对目标空气中的一些关心组分进行定性和定量的测定。
所谓关心组分是指那些已知威胁安全生产、损害作业者健康、导致火灾、影响消防安全的气体中的组成部分;所谓定性分析,本意是要回答空气中某组分是什么物质的问题,在安全和消防工程的气体分析中,定性分析的任务是确定某组分是否达到限定的浓度,关心是否超限,不很关心低于限定浓度的具体数值,一般称为检出。