2018年高考真题全国1卷化学(附答案解析)
- 格式:pdf
- 大小:672.25 KB
- 文档页数:17

2018年普通高等学校招生全国统一考试理科数学注意事项:1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其它答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
一、选择题:本题共12小题,每小题5分,共60分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1.设1i2i 1iz -=++,则||z = A .0B .12C .1D .22.已知集合{}220A x x x =-->,则A =RA .{}12x x -<< B .{}12x x -≤≤ C .}{}{|1|2x x x x <->D .}{}{|1|2x x x x ≤-≥3.某地区经过一年的新农村建设,农村的经济收入增加了一倍,实现翻番,为更好地了解该地区农村的经济收入变化情况,统计了该地区新农村建设前后农村的经济收入构成比例,得到如下饼图:建设前经济收入构成比例 建设后经济收入构成比例则下面结论中不正确的是A .新农村建设后,种植收入减少B .新农村建设后,其他收入增加了一倍以上C .新农村建设后,养殖收入增加了一倍D .新农村建设后,养殖收入与第三产业收入的总和超过了经济收入的一半 4.设n S 为等差数列{}n a 的前n 项和,若3243S S S =+,12a =,则=5a A .12- B .10-C .10D .125.设函数32()(1)f x x a x ax =+-+,若()f x 为奇函数,则曲线()y f x =在点(0,0)处的切线方程为 A .2y x =-B .y x =-C .2y x =D .y x =6.在ABC △中,AD 为BC 边上的中线,E 为AD 的中点,则EB = A .3144AB AC - B .1344AB AC - C .3144AB AC + D .1344AB AC + 7.某圆柱的高为2,底面周长为16,其三视图如图.圆柱表面上的点M 在正视图上的对应点为A ,圆柱表面上的点N 在左视图上的对应点为B ,则在此圆柱侧面上,从M 到N 的路径中,最短路径的长度为 A .172 B .52C .3D .28.设抛物线C :y 2=4x 的焦点为F ,过点(–2,0)且斜率为23的直线与C 交于M ,N 两点,则FM FN ⋅= A .5B .6C .7D .89.已知函数e 0()ln 0x x f x x x ⎧≤=⎨>⎩,,,,()()g x f x x a =++.若g (x )存在2个零点,则a 的取值范围是 A .[–1,0)B .[0,+∞)C .[–1,+∞)D .[1,+∞)10.下图来自古希腊数学家希波克拉底所研究的几何图形.此图由三个半圆构成,三个半圆的直径分别为直角三角形ABC 的斜边BC ,直角边AB ,AC .△ABC 的三边所围成的区域记为I ,黑色部分记为II ,其余部分记为III .在整个图形中随机取一点,此点取自I ,II ,I II 的概率分别记为p 1,p 2,p 3,则A .p 1=p 2B .p 1=p 3C .p 2=p 3D .p 1=p 2+p 311.已知双曲线C :2213x y -=,O 为坐标原点,F 为C 的右焦点,过F的直线与C 的两条渐近线的交点分别为M 、N .若△OMN 为直角三角形,则|MN |=A .32B .3C .23D .412.已知正方体的棱长为1,每条棱所在直线与平面α所成的角相等,则α截此正方体所得截面面积的最大值为 A .334B .233C .324D .32二、填空题:本题共4小题,每小题5分,共20分。
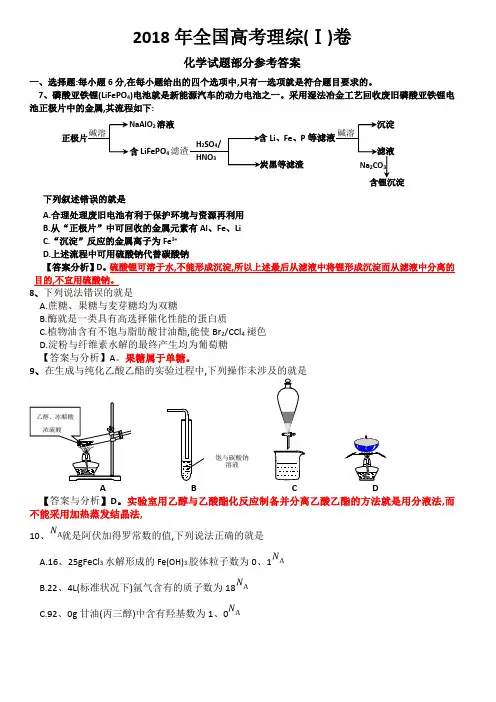
2018年全国高考理综(Ⅰ)卷化学试题部分参考答案一、选择题:每小题6分,在每小题给出的四个选项中,只有一选项就是符合题目要求的。
7、磷酸亚铁锂(LiFePO 4)电池就是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误..的就是 A.合理处理废旧电池有利于保护环境与资源再利用 B.从“正极片”中可回收的金属元素有Al 、Fe 、Li C.“沉淀”反应的金属离子为Fe 3+ D.上述流程中可用硫酸钠代替碳酸钠【答案分析】D 。
硫酸锂可溶于水,不能形成沉淀,所以上述最后从滤液中将锂形成沉淀而从滤液中分离的目的,不宜用硫酸钠。
8、下列说法错误的就是A.蔗糖、果糖与麦芽糖均为双糖B.酶就是一类具有高选择催化性能的蛋白质C.植物油含有不饱与脂肪酸甘油酯,能使Br 2/CCl 4褪色D.淀粉与纤维素水解的最终产生均为葡萄糖 【答案与分析】A 。
果糖属于单糖。
9、在生成与纯化乙酸乙酯的实验过程中,A B C D【答案与分析】D 。
实验室用乙醇与乙酸酯化反应制备并分离乙酸乙酯的方法就是用分液法,而不能采用加热蒸发结晶法, 10、就是阿伏加得罗常数的值,下列说法正确的就是A.16、25gFeCl 3水解形成的Fe(OH)3胶体粒子数为0、1B.22、4L(标准状况下)氩气含有的质子数为18C.92、0g 甘油(丙三醇)中含有羟基数为1、0饱与碳酸钠 溶液乙醇、冰醋酸 浓硫酸正极片碱溶2溶液 LiFePO 4滤渣H 2SO 4/ HNO 3含Li 、Fe 、P 炭黑等滤渣碱溶沉淀 滤液 Na 2CO 3 含锂沉淀D.1、0molCH4与Cl2在光照下反应生成CH3Cl分子数为1、0【答案与分析】B。
盐类水解的程度就是很小的,A不对;隋性气体属于单原子分子,1mol的氩气在标准状况下所占的体积为22、4L,所含的电子数与质子数相等,均为18mol,B正确;1mol甘油(丙三醇)中含有3的羟基,C错误;CH4与CL2在光照的条件下反应生成的产物中含有CH3Cl、CH2Cl2、CHCl3及CCl4,则生成物中含有的CH3Cl少于1mol,D不对。

2018 年全国高考理综 (Ⅰ)卷化学试题部分参考答案一、选择题:每小题 6 分,在每小题给出的四个选项中,只有一选项是符合题目要求的。
7.磷酸亚铁锂( LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:NaAlO2 溶液沉淀正极片碱溶含 Li、Fe、P 等滤液碱溶含 4滤渣H2SO4/滤液LiFePOHNO3 Na2CO3炭黑等滤渣含锂沉淀下列叙述错误的是..A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、 Fe、 LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠【答案分析】 D。
硫酸锂可溶于水,不能形成沉淀,所以上述最后从滤液中将锂形成沉淀而从滤液中分离的目的,不宜用硫酸钠。
8.下列说法错误的是A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含有不饱和脂肪酸甘油酯,能使Br2/CCl4褪色D.淀粉和纤维素水解的最终产生均为葡萄糖【答案与分析】 A。
果糖属于单糖。
9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是乙醇、冰醋酸浓硫酸饱和碳酸钠溶液A B C D【答案与分析】D。
实验室用乙醇与乙酸酯化反应制备并分离乙酸乙酯的方法是用分液法,而不能采用加热蒸发结晶法,10.??A是阿伏加得罗常数的值,下列说法正确的是A. 16.25gFeCl3 水解形成的 Fe(OH)3胶体粒子数为 0.1??AB. 22.4L(标准状况下)氩气含有的质子数为18??AC . 92.0g 甘油(丙三醇)中含有羟基数为 1.0??A. 4 与 Cl2 在光照下反应生成 3 分子数为1.0??A D 1.0molCH CH Cl 【答案与分析】 B 。
盐类水解的程度是很小的, A 不对;隋性气体属于单原子分子,1mol 的氩气 在标准状况下所占的体积为22.4L ,所含的电子数和质子数相等,均为 18mol ,B 正确; 1mol 甘油 (丙三醇)中含有 3?? 的羟基, C 错误;CH 4 与 CL2在光照的条件下反应生成的产物中含有 CH3、 ?? ClCH 2Cl 2 、CHCl 及 CCl ,则生成物中含有的 CH 少于 , D 不对。

2018年全国普通高等学校招生统一考试上海化学试卷考生注意:1.本试卷满分150分,考试时间120分钟。
2.本考试设试卷和答题纸两部分,试卷包括试卷和答题要求;所有答案必须凃或写在答题纸上;做在试卷上一律不得分。
3.答题前,考试务必将答题纸上用钢笔或圆珠笔在答题纸正面清楚地填写姓名、准考证号,并将核后的条形码贴在指定位置上,在答题纸反面清楚地填写姓名。
4.答题纸与试卷在试卷编号上是一一对应的,答题时应特别注意,不能错位。
相对原子质量:H-1 C-12 O-8 Na-23 S-32 Ca-40 Fe-56 Ni-59 Cu-64Br-80 Ba-137一、选择题<本题共10分,每小题2分,每题只有一个正确选项)1.2018年4月24日,东航首次成功进行了由地沟油生产的生物航空燃油的验证飞行。
能区别地沟油<加工过的餐饮废弃油)与矿物油<汽油、煤油、柴油等)的方法是A.点燃,能燃烧的是矿物油B.测定沸点,有固定沸点的是矿物油C.加入水中,浮在水面上的是地沟油D.加入足量氢氧化钠溶液共热,不分层的是地沟油【答案】D【解读】地沟油的主要成分是油脂,在氢氧化钠溶液可水解而不分层,矿物油的主要成分是烃的混合物,不溶于水,氢氧化钠溶液,他们都能燃烧,密度比水小、没有固定的沸点,因此,选D2.氰酸铵<NH4OCN)与尿素[CO(NH2>2]A.都是共价化合物B.都是离子化合物C.互为同分异构体D.互为同素异形体【答案】C【解读】氰酸铵是离子化合物,尿素是共价化合物,他们的分子式相同,结构不同,是同分异构体的关系,因此选C3.230Th和232Th是钍的两种同位素,232Th可以转化成233U。
下列有关Th的说法正确的是A. Th 元素的质量数是232B. Th 元素的相对原子质量是231C. 232Th 转换成233U是化学变化D. 230Th和232Th的化学性质相同【答案】D【解读】232Th 230Th的质量分别是232,230 A项错误,元素的相对原子质量是由各种同位素的相对原子质量取得的平均值,B项错误同位素的物理性质可以不同,但化学性质几乎相同,D项正确,化学变化是生成新物质的变化,原子不变,而C项的原子发生变化错误。
的贡献为1。
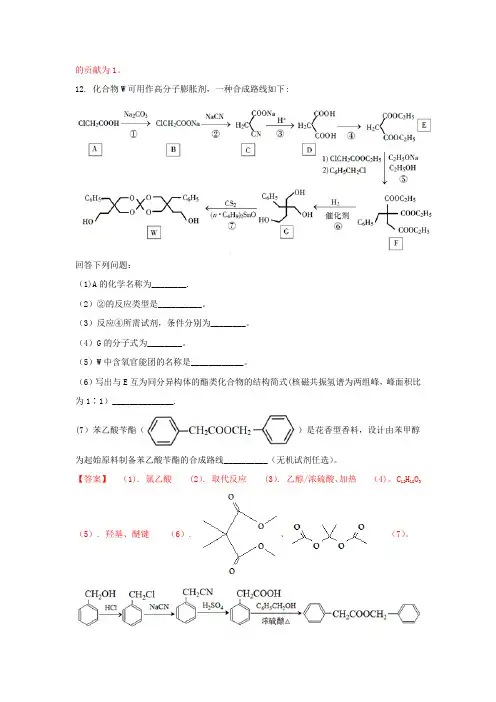
12. 化合物W可用作高分子膨胀剂,一种合成路线如下:回答下列问题:(1)A的化学名称为________.(2)②的反应类型是__________。
(3)反应④所需试剂,条件分别为________。
(4)G的分子式为________。
(5)W中含氧官能团的名称是____________。
(6)写出与E互为同分异构体的酯类化合物的结构简式(核磁共振氢谱为两组峰,峰面积比为1∶1)______________.(7)苯乙酸苄酯()是花香型香料,设计由苯甲醇为起始原料制备苯乙酸苄酯的合成路线__________(无机试剂任选)。
【答案】(1). 氯乙酸 (2). 取代反应 (3). 乙醇/浓硫酸、加热(4)。
C12H18O3(5). 羟基、醚键(6). 、(7)。
【解析】分析:A是氯乙酸与碳酸钠反应生成氯乙酸钠,氯乙酸钠与NaCN发生取代反应生成C,C水解又引入1个羧基.D与乙醇发生酯化反应生成E,E发生取代反应生成F,在催化剂作用下F与氢气发生加成反应将酯基均转化为醇羟基,2分子G发生羟基的脱水反应成环,据此解答.详解:(1)根据A的结构简式可知A是氯乙酸;(2)反应②中氯原子被-CN取代,属于取代反应。
(3)反应④是酯化反应,所需试剂和条件分别是乙醇/浓硫酸、加热;(4)根据G的键线式可知其分子式为C12H18O3;(5)根据W的结构简式可知分子中含有的官能团是醚键和羟基;(6)属于酯类,说明含有酯基。
核磁共振氢谱为两组峰,峰面积比为1:1,说明氢原子分为两类,各是6个氢原子,因此符合条件的有机物结构简式为或;(7)根据已知信息结合逆推法可知合成苯乙酸卞酯的路线图为。
点睛:本题考查有机物的推断和合成,涉及官能团的性质、有机物反应类型、同分异构体的书写、合成路线设计等知识,利用已经掌握的知识来考查有机合成与推断、反应条件的选择、物质的结构简式、化学方程式、同分异构体的书写的知识。
考查学生对知识的掌握程度、自学能力、接受新知识、新信息的能力;考查了学生应用所学知识进行必要的分析来解决实际问题的能力。

高考真题——实验题1.【2018全国卷I-26】醋酸亚铬[(CH3COO)2Cr·H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。
一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。
实验装置如图所示,回答下列问题:(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是,仪器a的名称是。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开K1、K2,关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为。
②同时c中有气体产生,该气体的作用是。
(3)打开K3,关闭K1和K2。
c中亮蓝色溶液流入d,其原因是;d中析出砖红色沉淀,为使沉淀充分析出并分离,需采用的操作是__________ 、___________、洗涤、干燥。
(4)指出装置d可能存在的缺点。
2.【2017全国卷I-26】凯氏定氮法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量。
已知:NH3+H3BO3=NH3·H3BO3;NH3·H3BO3+HCl= NH4Cl+ H3BO3。
回答下列问题:(1)a的作用是________________________________________。
(2)b中放入少量碎瓷片的目的是_________________。
f的名称是______________。
(3)清洗仪器:g中加蒸馏水:打开k1,关闭k2、k3,加热b,蒸气充满管路:停止加热,关闭k1,g中蒸馏水倒吸进入c,原因是___________________________________;打开k2放掉水,重复操作2~3次。
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂。
铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭k3,d中保留少量水。

1.【2018新课标1卷】焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。
回答下列问题:(1)生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。
写出该过程的化学方程式__________。
(2)利用烟道气中的SO2生产Na2S2O5的工艺为:①pH=4.1时,Ⅰ中为__________溶液(写化学式)。
②工艺中加入Na2CO3固体、并再次充入SO2的目的是__________。
(3)制备Na2S2O5也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。
阳极的电极反应式为_____________。
电解后,__________室的NaHSO3浓度增加。
将该室溶液进行结晶脱水,可得到Na2S2O5。
(4)Na2S2O5可用作食品的抗氧化剂。
在测定某葡萄酒中Na2S2O5残留量时,取50.00 mL葡萄酒样品,用0.01000 mol·L−1的碘标准液滴定至终点,消耗10.00 mL。
滴定反应的离子方程式为_____________,该样品中Na2S2O5的残留量为____________g·L−1(以SO2计)。
【答案】 2NaHSO3=Na2S2O5+H2O NaHSO3得到NaHSO3过饱和溶液 2H2O-4e-=4H++O2↑ a S2O52-+2I2+3H2O=2SO42-+4I-+6H+ 0.128【解析】分析:(1)根据原子守恒书写方程式;(2)①根据溶液显酸性判断产物;②要制备焦亚硫酸钠,需要制备亚硫酸氢钠过饱和溶液,据此判断;(3)根据阳极氢氧根放电,阴极氢离子放电,结合阳离子交换膜的作用解答;(4)焦亚硫酸钠与单质碘发生氧化还原反应,据此书写方程式;根据方程式计算残留量。
详解:(1)亚硫酸氢钠过饱和溶液脱水生成焦亚硫酸钠,根据原子守恒可知反应的方程式为2NaHSO3=Na2S2O5+H2O;(2)①碳酸钠饱和溶液吸收SO2后的溶液显酸性,说明生成物是酸式盐,即Ⅰ中为NaHSO3;②要制备焦亚硫酸钠,需要制备亚硫酸氢钠过饱和溶液,因此工艺中加入碳酸钠固体、并再次充入二氧化硫的目的是得到NaHSO3过饱和溶液;点睛:本题以焦亚硫酸钠的制备、应用为载体考查学生对流程的分析、电解原理的应用以及定量分析等,题目难度中等。

2018年普通高等学校招生全国统一考试(北京卷)化学能力测试可能用到的相对原子质量: H1 C12 N14 O166.下列我国科技成果所涉及物质的应用中,发生的不是 ..化学变化的是7.我国科研人员提出了由 CO 2 和 CH 4 转化为高附加值产品 CH 3COOH 的催化反应历程。
该历程示意图如下。
矚慫润厲钐瘗睞枥庑赖。
列说法不.正.确.的是A .生成 CH 3COOH 总反应的原子利用率为 100%B . CH 4→ CH 3COOH 过程中,有C ―H 键发生断裂 C .① → ②放出能量并形成了 C ―C 键D .该催化剂可有效提高反应物的平衡转化率 8.下列化学用语对事实的表述不正确...的是18 18A .硬脂酸与乙醇的酯化反应: C 17H 35COOH+C 2H 518OHC 17H 35COOC 2H 5+H 218O聞創沟燴鐺險爱氇谴净。
-1B .常温时, 0.1mol L ·-1 氨水的 pH=11.1C .由 Na 和 C1 形成离子键的过程:A .甲醇低温所制氢B .氘、氚用作 “人造太阳C .偏二甲肼用作发射 “天D .开采可燃冰, 将其作NH 3·H 2O +OHD.电解精炼铜的阴极反应: Cu2+ +2e-Cu 9.下列实验中的颜色变化,与氧化还原反应无关的是A B C D实验NaOH 溶液滴入石蕊溶液滴入氯Na2S 溶液滴入热铜丝插入稀硝FeSO4 溶液中水中AgCl 浊液中酸中现象产生白色沉淀,溶液变红,随后沉淀由白色逐渐产生无色气体,随后变为红褐色迅速褪色变为黑色随后变为红棕色10.一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料。
其结构片段如下图列关于该高分子的说法正确的是A.完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境B.完全水解产物的单个分子中,含有官能团―COOH 或― NH2C.氢键对该高分子的性能没有影响实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2 溶液做对比实验,④产生白色沉淀多。

绝密★启封(qǐ fēnɡ)并使用完毕前2018年普通高等学校(gāoděngxuéxiào)招生全国统一考试理科综合能力(nénglì)测试化学(huàxué)(北京(běi jīnɡ)卷)本试卷共16页,共300分。
考试时长150分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16第一部分(选择题)1. 下列我国科技成果所涉及物质的应用中,发生的不是..化学变化的是()2. 我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。
该历程示意图如下。
下列说法不正确...的是()A. 生成CH3COOH总反应的原子利用率为100%B. CH4→CH3COOH过程中,有C―H键发生断裂C. ①→②放出能量并形成了C―C键D. 该催化剂可有效提高反应物的平衡转化率3. 下列化学用语对事实的表述不正确...的是()A. 硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH C17H35COOC2H5+H218OB. 常温时,0.1 mol·L-1氨水的pH=11.1:NH3·H2O+OH−C. 由Na和C1形成离子键的过程:D. 电解精炼铜的阴极(yīnjí)反应:Cu2+ +2e −Cu4. 下列实验中的颜色(yánsè)变化,与氧化还原反应(fǎnyìng)无关的是()A B C D实验NaOH溶液滴入FeSO4溶液中石蕊溶液滴入氯水中Na2S溶液滴入AgCl浊液中热铜丝插入稀硝酸中现象产生白色沉淀,随后变为红褐色溶液变红,随后迅速褪色沉淀由白色逐渐变为黑色产生无色气体,随后变为红棕色5. 一种芳纶纤维的拉伸(lā shēn)强度比钢丝还高,广泛用作防护材料。

2018年普通高等学校招生全国统一考试(北京卷)理综化学试题6.下列我国科技成果所涉及物质的应用中,发生的不是..化学变化的是7.我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。
该历程示意图如下。
下列说法不正确...的是A.生成CH3COOH总反应的原子利用率为100% B.CH4→CH3COOH过程中,有C-H键发生断裂C.①→②放出能量并形成了C-C键D.该催化剂可有效提高反应物的平衡转化率8.下列化学用语对事实的表述不正确...的是A.硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH C17H35COOC2H5+H218ONH+OH−B.常温时,0.1 mol·L-1氨水的pH=11.1:NH3·H2O+4C.由Na和C1形成离子键的过程:D.电解精炼铜的阴极反应:Cu2+ +2e−Cu9.下列实验中的颜色变化,与氧化还原反应无关的是10.一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料。
其结构片段如下图下列关于该高分子的说法正确的是A .完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境B .完全水解产物的单个分子中,含有官能团―COOH 或―NH 2C .氢键对该高分子的性能没有影响D .结构简式为:11.测定0.1 mol·L -1 Na 2SO 3溶液先升温再降温过程中的pH ,数据如下。
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl 2溶液做对比实验,④产生白色沉淀多。
下列说法不正确...的是 A .Na 2SO 3溶液中存在水解平衡:23SO -+H 2O3HSO -+OH − B .④的pH 与①不同,是由于23SO -浓度减小造成的C .①→③的过程中,温度和浓度对水解平衡移动方向的影响一致D .①与④的K w 值相等12.验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl 溶液)。

2018年高考化学真题分类汇编专题1 常用化学计量(必修1)Ⅰ—阿伏伽德罗常数和物质的量1。
[2018全国卷Ⅰ—10]N A是阿伏加德罗常数的值.下列说法正确的是A。
16.25gFeCl3水解形成的Fe(OH)3胶体粒子数为0。
1N AB。
22。
4L(标准状况)氩气含有的质子数为18N AC。
92。
0g甘油(丙三醇)中含有羟基数为1。
0 N AD。
1.0molCH4与Cl2在光照下反应生成的CH3Cl分子数为1.0 N A【答案】B【解析】A。
16.25g氯化铁的物质的量是16.25g÷162.5g/mol=0。
1mol,由于氯化铁水解生成氢氧化铁胶体时,只有部分水解,且氢氧化铁胶粒是分子的集合体,因此水解生成的Fe(OH)3胶体粒子数远小于0。
1 N A,A错误;B。
标准状况下22.4L氩气的物质的量是1mol,氩气分子是单原子分子,氩原子中有18个质子,故。
标准状况下22。
4L氩气的含有的质子数是18 N A,B正确;C。
丙三醇是三元醇,分子中含有3个羟基,92.0g丙三醇的物质的量是1mol,其中含有羟基数是3 N A,C错误;D.甲烷与氯气在光照条件下发生取代反应生成的卤代烃有四种,因此生成的CH3Cl分子数小于1。
0 N A,D错误。
【考点】水解平衡;胶体、气体摩尔体积、阿伏加德罗常数、羟基的概念;丙三醇的结构;甲烷的取代反应。
2。
[2018全国卷Ⅱ—11]N A代表阿伏加德罗常数的值.下列说法正确的是A. 常温常压下,124 g P4中所含P-P键数目为4N AB。
100 mL 1mol·L−1FeCl3溶液中所含Fe3+的数目为0.1N AC. 标准状况下,11。
2 L甲烷和乙烯混合物中含氢原子数目为2N AD。
密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2N A【答案】C【解析】A.由于白磷(P4)是正四面体结构,分子中含有6个P-P键。
2018年高考全国1卷答案目录语文2-3数学(文、理)4-16英语16-18文综19-25理综26-32语文答案1.D 2.A 3.B 4.B5.①文人的气质:喜欢丁香花,情趣不俗;时常深情,甜蜜地回忆战斗生活,文雅浪漫;用大义与真情感化青年,智慧过人;②军人的冷峻:遭严剂拷打而不屈服,意志坚定;笑对即将到来的死亡,从容淡定;充满母爱又不忘大义,理智沉稳。
6.①既能表现当代人对赵一曼女士的尊敬之情,又能表现赵一曼精神的当下意义,使主题内蕴更深刻;②可以拉开时间距离,更加全面地认识英雄,使人物形象更加立体;③灵活使用文献档案,与小说叙述相互印证,使艺术描写更真实。
7.D 8.C9.第一问:①《人民日报》侧重介绍我国在量子通信研究方面的巨大成就,彰显中国速度与中国创造;②《自然》杂志侧重介绍潘建伟研究团队在量子通信领域的奉献,强调个人能力和经费投入;③《读卖新闻》以“墨子号”为例,侧重介绍中国实验设施先进,突出投入之大和发展之快给日本带来压力。
第二问:三家媒体的定位和出发点不同,因此对同一事件报道的侧重点不同。
10.C 11.C 12.B 14.B13.(1)诸葛诞凭借寿春反叛,魏帝出征,鲁芝率领荆州文武官兵作为先锋(2)皇上因为鲁芝清廉忠诚行为端正,一向没有私宅,让士兵为他建造五十间房屋。
15.①意为凛冽的寒风终将过去,和煦的春风拂绿枯柳,缀满嫩绿的柳条好像轻烟笼罩一般摇曳多姿;②表达了诗人虽感叹不遇于时,但不甘沉沦的乐观、自勉之情。
16.(1)温故而知新可以为师矣(2)好古文六艺经传皆通习之(3)羽扇纶巾樯橹灰飞烟灭三、语言文字运用17.B 18.C 19.B20.示例:①“堵住”改为“堵塞”;②“管子”改为“管道”:③“换掉”改为“更换”:④“打算”改为“计划”;⑥“正遇上”改为“正值”理科数学答案123456789101112C B A BD A B D C A B A13.6 14.63- 15.16 16. 17.(12分)解:(1)在ABD △中,由正弦定理得sin sin BD ABA ADB=∠∠.由题设知,52sin 45sin ADB =︒∠,所以sin 5ADB ∠=.由题设知,90ADB ∠<︒,所以cos ADB ∠==(2)由题设及(1)知,cos sin 5BDC ADB ∠=∠=. 在BCD △中,由余弦定理得2222cos BC BD DC BD DC BDC =+-⋅⋅⋅∠258255=+-⨯⨯ 25=.所以5BC =.18.(12分)解:(1)由已知可得,BF ⊥PF ,BF ⊥EF ,所以BF ⊥平面PEF .又BF ⊂平面ABFD ,所以平面PEF ⊥平面ABFD .(2)作PH ⊥EF ,垂足为H .由(1)得,PH ⊥平面ABFD .以H 为坐标原点,HF 的方向为y 轴正方向,||BF为单位长,建立如图所示的空间直角坐标系H −xyz.由(1)可得,DE ⊥PE .又DP =2,DE =1,所以PE又PF =1,EF =2,故PE ⊥PF .可得32PH EH ==.则33(0,0,0),(1,,0),(1,22H P D DP --=HP = 为平面ABFD 的法向量.设DP 与平面ABFD 所成角为θ,则3sin ||||||HP DP HP DP θ⋅===⋅所以DP 与平面ABFD19.(12分)解:(1)由已知得(1,0)F ,l 的方程为x =1.由已知可得,点A 的坐标为(1,)2或(1,2-. 所以AM的方程为2y x =-+2y x =. (2)当l 与x 轴重合时,0OMA OMB ∠=∠=︒.当l 与x 轴垂直时,OM 为AB 的垂直平分线,所以OMA OMB ∠=∠.当l 与x 轴不重合也不垂直时,设l 的方程为(1)(0)y k x k =-≠,1221(,),(,)A y x y x B ,则12x x <<,直线MA ,MB 的斜率之和为212122MA MB x x y yk k +=+--. 由1122,y k k x y k x k =-=-得121212(23()42)(2)MA MB x x x x k k x x kk k -+++=--.将(1)y k x =-代入2212x y +=得 2222(21)4220k x k x k +-+-=.所以,21221222422,2121x x x k k k x k -+==++.则3131322244128423()4021k k k k kk k k k x x x x --++-++==+. 从而0MA MB k k +=,故MA ,MB 的倾斜角互补,所以OMA OMB ∠=∠.综上,OMA OMB ∠=∠.20.(12分)解:(1)20件产品中恰有2件不合格品的概率为221820()C (1)f p p p =-.因此2182172172020()C [2(1)18(1)]2C (1)(110)f p p p p p p p p '=---=--.令()0f p '=,得0.1p =.当(0,0.1)p ∈时,()0f p '>;当(0.1,1)p ∈时,()0f p '<.所以()f p 的最大值点为00.1p =.(2)由(1)知,0.1p =.(i )令Y 表示余下的180件产品中的不合格品件数,依题意知(180,0.1)Y B :,20225X Y =⨯+,即4025X Y =+.所以(4025)4025490EX E Y EY =+=+=.(ii )如果对余下的产品作检验,则这一箱产品所需要的检验费为400元.由于400EX >,故应该对余下的产品作检验.21.(12分)解:(1)()f x 的定义域为(0,)+∞,22211()1a x ax f x x x x-+'=--+=-. (i )若2a ≤,则()0f x '≤,当且仅当2a =,1x =时()0f x '=,所以()f x 在(0,)+∞单调递减.(ii )若2a >,令()0f x '=得,x =或x =当(0,(,)22a a x ∈+∞U 时,()0f x '<;当(22a a x ∈时,()0f x '>.所以()f x 在)+∞单调递减,在单调递增.(2)由(1)知,()f x 存在两个极值点当且仅当2a >.由于()f x 的两个极值点12,x x 满足210x ax -+=,所以121x x =,不妨设12x x <,则21x >.由于12121221212121222()()ln ln ln ln 2ln 11221f x f x x x x x x a a a x x x x x x x x x x ----=--+=-+=-+----,所以1212()()2f x f x a x x -<--等价于22212ln 0x x x -+<.设函数1()2ln g x x x x=-+,由(1)知,()g x 在(0,)+∞单调递减,又(1)0g =,从而当(1,)x ∈+∞时,()0g x <.所以22212ln 0x x x -+<,即1212()()2f x f x a x x -<--. 22.[选修4-4:坐标系与参数方程](10分)【解析】(1)由cos x ρθ=,sin y ρθ=得2C 的直角坐标方程为22(1)4x y ++=.(2)由(1)知2C 是圆心为(1,0)A -,半径为2的圆.由题设知,1C 是过点(0,2)B 且关于y 轴对称的两条射线.记y 轴右边的射线为1l ,y轴左边的射线为2l .由于B 在圆2C 的外面,故1C 与2C 有且仅有三个公共点等价于1l 与2C 只有一个公共点且2l 与2C 有两个公共点,或2l 与2C 只有一个公共点且1l 与2C 有两个公共点.当1l 与2C 只有一个公共点时,A 到1l 所在直线的距离为2,所以2=,故43k =-或0k =.经检验,当0k =时,1l 与2C 没有公共点;当43k =-时,1l 与2C 只有一个公共点,2l 与2C 有两个公共点.当2l 与2C 只有一个公共点时,A 到2l 所在直线的距离为22=,故0k =或43k =. 经检验,当0k =时,1l 与2C 没有公共点;当43k =时,2l 与2C 没有公共点. 综上,所求1C 的方程为4||23y x =-+. 23.【解析】(1)当1a =时,()|1||1|f x x x =+--,即2,1,()2,11,2, 1.x f x x x x -≤-⎧⎪=-<<⎨⎪≥⎩故不等式()1f x >的解集为1{|}2x x >.(2)当(0,1)x ∈时|1||1|x ax x +-->成立等价于当(0,1)x ∈时|1|1ax -<成立.若0a ≤,则当(0,1)x ∈时|1|1ax -≥;若0a >,|1|1ax -<的解集为20x a <<,所以21a≥,故02a <≤. 综上,a 的取值范围为(0,2].文科数学答案1.A2.C3.A4.C5.B6.D7.A 8.B 9.B 10.C 11.B 12.D二、填空题13.-7 14.6 15. 三、解答题17.解:(1)由条件可得a n +1=2(1)n n a n+. 将n =1代入得,a 2=4a 1,而a 1=1,所以,a 2=4.将n =2代入得,a 3=3a 2,所以,a 3=12.从而b 1=1,b 2=2,b 3=4.(2){b n }是首项为1,公比为2的等比数列.由条件可得121n na a n n+=+,即b n +1=2b n ,又b 1=1,所以{b n }是首项为1,公比为2的等比数列.(3)由(2)可得12n n a n-=,所以a n =n ·2n -1. 18.解:(1)由已知可得,BAC ∠=90°,BA AC ⊥.又BA ⊥AD ,所以AB ⊥平面ACD .又AB ⊂平面ABC ,所以平面ACD ⊥平面ABC .(2)由已知可得,DC =CM =AB =3,DA =又23BP DQ DA ==,所以BP =. 作QE ⊥AC ,垂足为E ,则QE = 13DC . 由已知及(1)可得DC ⊥平面ABC ,所以QE ⊥平面ABC ,QE =1.因此,三棱锥Q ABP -的体积为11113451332Q ABP ABP V QE S -=⨯⨯=⨯⨯⨯⨯︒=△. 19.解:(1)(2)根据以上数据,该家庭使用节水龙头后50天日用水量小于0.35m 3的频率为 0.2×0.1+1×0.1+2.6×0.1+2×0.05=0.48,因此该家庭使用节水龙头后日用水量小于0.35m 3的概率的估计值为0.48. (3)该家庭未使用节水龙头50天日用水量的平均数为11(0.0510.1530.2520.3540.4590.55260.655)0.4850x =⨯+⨯+⨯+⨯+⨯+⨯+⨯=. 该家庭使用了节水龙头后50天日用水量的平均数为21(0.0510.1550.25130.35100.45160.555)0.3550x =⨯+⨯+⨯+⨯+⨯+⨯=. 估计使用节水龙头后,一年可节省水3(0.480.35)36547.45(m )-⨯=.20.解:(1)当l 与x 轴垂直时,l 的方程为x =2,可得M 的坐标为(2,2)或(2,–2).所以直线BM 的方程为y =112x +或112y x =--. (2)当l 与x 轴垂直时,AB 为MN 的垂直平分线,所以∠ABM =∠ABN .当l 与x 轴不垂直时,设l 的方程为(2)(0)y k x k =-≠,M (x 1,y 1),N (x 2,y 2),则x 1>0,x 2>0.由2(2)2y k x y x=-⎧⎨=⎩,得ky 2–2y –4k =0,可知y 1+y 2=2k ,y 1y 2=–4. 直线BM ,BN 的斜率之和为1221121212122()22(2)(2)BM BN y y x y x y y y k k x x x x ++++=+=++++.① 将112y x k =+,222y x k=+及y 1+y 2,y 1y 2的表达式代入①式分子,可得 121221121224()882()0y y k y y x y x y y y k k ++-++++===. 所以k BM +k BN =0,可知BM ,BN 的倾斜角互补,所以∠ABM +∠ABN .综上,∠ABM =∠ABN .21.解:(1)f (x )的定义域为(0)+∞,,f ′(x )=a e x –1x. 由题设知,f ′(2)=0,所以a =212e . 从而f (x )=21e ln 12e x x --,f ′(x )=211e 2e x x-. 当0<x <2时,f ′(x )<0;当x >2时,f ′(x )>0.所以f (x )在(0,2)单调递减,在(2,+∞)单调递增.(2)当a ≥1e 时,f (x )≥e ln 1exx --. 设g (x )=e ln 1e x x --,则e 1()e x g x x'=-. 当0<x <1时,g ′(x )<0;当x >1时,g ′(x )>0.所以x =1是g (x )的最小值点. 故当x >0时,g (x )≥g (1)=0. 因此,当1ea ≥时,()0f x ≥. 22.[选修4-4:坐标系与参数方程](10分)解:(1)由cos x ρθ=,sin y ρθ=得2C 的直角坐标方程为22(1)4x y ++=.(2)由(1)知2C 是圆心为(1,0)A -,半径为2的圆.由题设知,1C 是过点(0,2)B 且关于y 轴对称的两条射线.记y 轴右边的射线为1l ,y 轴左边的射线为2l .由于B 在圆2C 的外面,故1C 与2C 有且仅有三个公共点等价于1l 与2C 只有一个公共点且2l 与2C 有两个公共点,或2l 与2C 只有一个公共点且1l 与2C 有两个公共点.当1l 与2C 只有一个公共点时,A 到1l 所在直线的距离为2,2=,故43k =-或0k =.经检验,当0k =时,1l 与2C 没有公共点;当43k =-时,1l 与2C 只有一个公共点,2l 与2C 有两个公共点.当2l 与2C 只有一个公共点时,A 到2l 所在直线的距离为22=,故0k =或43k =. 经检验,当0k =时,1l 与2C 没有公共点;当43k =时,2l 与2C 没有公共点. 综上,所求1C 的方程为4||23y x =-+. 23.[选修4-5:不等式选讲](10分)解:(1)当1a =时,()|1||1|f x x x =+--,即2,1,()2,11,2, 1.x f x x x x -≤-⎧⎪=-<<⎨⎪≥⎩故不等式()1f x >的解集为1{|}2x x >. (2)当(0,1)x ∈时|1||1|x ax x +-->成立等价于当(0,1)x ∈时|1|1ax -<成立.若0a ≤,则当(0,1)x ∈时|1|1ax -≥;若0a >,|1|1ax -<的解集为20x a <<,所以21a≥,故02a <≤. 综上,a 的取值范围为(0,2].英语答案1-5 BCCBA6-10BABCC11-15ABAAC16-20BCBCA21-25ADDBC26-30CDBCB31-35CADBA36-40BADGF41-45BCADD46-50CBDCB51-55CACBA56-60DBADA61.longer 62.to see 63.dying 64.is 65.than 66.that \which 67.causes68.strength 69.energetic 70.it \runningDuring my last winter holiday, I went tothe ∧countryside with my father to visit my grandparents. I find founda change there. The first time I went there, they were living in a small house with dogs, ducks, and another other animals. Last winter when I went here thereagain, they had a big separate house to raise dozens of chicken chickens. They also had a small pond which in where∧或 they raised fish. My grandpa said last summer they earned quite a lot by sell selling the fish. I felt happily happythat their life had improved. At the end of our trip, I told my father that I planned to return for every two years,but andhe agreed.文综答案1.C 2.D 3.B 4.C 5.D6.A 7.A 8.D 9.B 10.B11.A 12.A 13.A 14.B 15.B16.A 17.D 18.C 19.D 20.D21.C 22.B 23.C 24.C 25.D26.A 27.B 28.C 29.C 30.A31.D 32.D 33.A 34.B 35.A二、非选择题:共160分。
2018年北京市高考化学试卷一、选择题(共7小题,每小题6分,共42分.每题只有一个正确选项)1.(6.00分)下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是()A.甲醇低温所制氢气用于新能源汽车B.氘、氚用作“人造太阳”核聚变燃料C.偏二甲肼用作发射“天宫二号”的火箭燃料D.开采可燃冰,将其作为能源使用A.A B.B C.C D.D2.(6.00分)我国科研人员提出了由CO2和CH4转化为高附加值产品 CH3COOH的催化反应历程。
该历程示意图如下。
下列说法不正确的是()A.生成CH3COOH总反应的原子利用率为100%B.CH4→CH3COOH过程中,有C﹣H键发生断裂C.①→②放出能量并形成了C﹣C键D.该催化剂可有效提高反应物的平衡转化率3.(6.00分)下列化学用语对事实的表述不正确的是()A.硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH C17H35COOC2H5+H218OB.常温时,0.1mol•L﹣1氨水的pH=11.1:NH3•H2O⇌NH4++OH﹣C.由Na和Cl 形成离子键的过程:→D.电解精炼铜的阴极反应:Cu2++2e﹣═Cu4.(6.00分)下列实验中的颜色变化,与氧化还原反应无关的是()A B C D 实验NaOH溶液滴入FeSO4溶液中石蕊溶液滴入氯水中Na2S溶液滴入AgC1浊液中热铜丝插入稀硝酸中现象产生白色沉淀,随后变为红褐色溶液变红,随后迅速褪色沉淀由白色逐渐变为黑色产生无色气体,随后变为红棕色A.A B.B C.C D.D5.(6.00分)一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料,其结构片段如下图。
下列关于该高分子的说法正确的是()A.完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境B.完全水解产物的单个分子中,含有官能团一COOH或一NH2C.氢键对该高分子的性能没有影响D .结构简式为:6.(6.00分)测定0.1mol•L﹣1 Na2SO3溶液先升温再降温过程中的pH,数据如下:时刻①②③④温度/℃25 30 40 25 pH 9.66 9.52 9.37 9.25实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。
2018年全国统一高考化学试卷(新课标Ⅰ)一、选择题(共7小题,每小题6分,满分42分)1.(6分)磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是()A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+ D.上述流程中可用硫酸钠代替碳酸钠2.(6分)下列说法错误的是()A.蔗糖、果糖和麦芽糖均为双糖 B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖3.(6分)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是()A.B. C.D.4.(6分)N A是阿伏加德罗常数的值,下列说法正确的是()A.16.25gFeCl3,水解形成的Fe(OH)3为胶体粒子数为0.1N AB.22.4L(标准状况)氩气含有的质子数为18N AC.92.0g甘油(丙三醇)中含有羟基数为1.0N AD.1.0molCH4与Cl2在光照下生成CH3Cl的分子数为1.0N A5.(6分)环之间共用一个碳原子的化合物称为螺环化合物,螺(2,2)戊烷()是最单的一种,下列关于该化合物的说法错误的是()A.与环戊烯互为同分异构体 B.二氯化物超过两种C.所有碳原子均处同一平面 D.生成1molC5H12,至少需要2molH26.(6分)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20.W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化台物可与浓硫酸反应,其生成物可腐蚀玻璃。
下列说法正确的是()A.常温常压下X的单质为气态 B.Z的氢化物为离子化合物C.Y和Z形成的化合物的水溶液呈碱性 D.W与Y具有相同的最高化合价7.(6分)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。
2018年天津高考试卷化学试题与答案及解释绝密★启用前2018年普通高等学校招生全国统一考试(天津卷)理科综合化学部分理科综合共300分,考试用时150分钟。
化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷两部分,第Ⅰ卷1至2页,第Ⅱ卷3至6页,共100分。
答卷前,考生务必将自己的姓名、准考证号填写在答题卡上,并在规定位置粘贴考试用条码。
答卷时,考生务必将答案涂写在答题卡上,答在试卷上的无效。
考试结束后,将本试卷和答题卡一并交回。
祝各位考生考试顺利!第Ⅰ卷注意事项:1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
2.本卷共6题,每题6分,共36分。
在每题给出的四个选项中,只有一项是最符合题目要求的。
以下数据供解题时参考:相对原子质量:H 1 C 12 N 14 O 161. 以下是中华民族为人类文明进步做出巨大贡献的几个事例,运用化学知识对其进行的分析不合理的是A. 四千余年前用谷物酿造出酒和醋,酿造过程中只发生水解反应B. 商代后期铸造出工艺精湛的后(司)母戊鼎,该鼎属于铜合金制品C. 汉代烧制出“明如镜、声如磬”的瓷器,其主要原料为黏士D. 屠呦呦用乙醚从青蒿中提取出对治疗疟疾有特效的青蒿素,该过程包括萃取操作【答案与解释】A。
谷物中多含有淀粉,可以经过发酵制酒与醋,过程所发生的化学变化有:第一:淀粉在酒曲酶的作用下水解生成葡萄糖,第二步:葡萄糖在厌氧茵的作用下发生分解生成乙醇和二氧化碳(实质发生了氧化还原反应),A论述错误;商代铸造的用于象征至高无上的权力的司母戊鼎的主要成分是:铜84.77%、锡11.64%、铅27.9%,B观点正确;“明如镜,声如磬q i n g”是形容古代江西景德镇官窑生产的精美瓷器。
由于只有用江西景德镇优质高岭士(即黏士)才能烧制出如此精美的瓷器,固有“明如镜,声如馨”之美誉,C正确;菁蒿素是利用乙醚等有机溶剂从复合花序植物黄花蒿茎叶中提取的有过氧基团的倍半萜内酯药物,其原理就是利用萃取原理,D正确。
2018年高考真题——化学平衡及应用全国1卷28.(15分)采用N 2O 5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。
回答下列问题:(1)1840年 Devil 用干燥的氯气通过干燥的硝酸银,得到N 2O 5,该反应的氧化产物是一种气体,其分子式为_______。
(2)F. Daniels 等曾利用测压法在刚性反应器中研究了25℃时N 2O 5(g )分解反应:其中NO 2二聚为N 2O 4的反应迅速达到平衡。
体系总压强p 随时间t 的变化如下表所示(t =∞时,N 2O 5(g )完全分解):t /min0 40 80 160 260 1300 1700 ∞ p /kPa35.840.342.545.949.261.262.363.1①已知:2N 2O 5(g )2N 2O 4(g )+O 2(g )ΔH 1=−4.4 kJ ·mol −12NO 2(g ) N 2O 4(g ) ΔH 2=−55.3 kJ ·mol −1则反应N 2O 5(g )=2NO 2(g )+12O 2(g )的ΔH =_______ kJ ·mol −1。
②研究表明,N 2O 5(g )分解的反应速率v =2×10−3×25N O p (kPa ·min −1)。
t =62 min 时,测得体系中2O p =2.9 kPa ,则此时的25N O p =________ kPa ,v =_______ kPa ·min −1。
③若提高反应温度至35℃,则N 2O 5(g )完全分解后体系压强p ∞(35℃)____63.1 kPa (填“大于”“等于”或“小于”),原因是________。
④25℃时N 2O 4(g )2NO 2(g )反应的平衡常数K p =_______kPa (K p 为以分压表示的平衡常数,结果保留1位小数)。