实验一 土壤脲酶活性测定
- 格式:ppt
- 大小:89.00 KB
- 文档页数:7

土壤脲酶的测定方法(改良靛酚蓝比色法)一、原理以尿素为底物,经培养后根据脲酶酶促产物--氨(忽略硝化过程造成的氨氮损失)在碱性介质中与苯酚、次氯酸钠作用生成蓝色的靛酚。
该生成物数量与氨浓度成正比。
后即称为靛酚蓝比色法,其结果精确性较高,重现性较好,在脲酶活性测定中的应用最为广泛。
二、试剂1)甲苯1ml/ps注:甲苯易挥发,要在通风条件好的地方操作。
2)5%尿素:称取5g尿素,用水溶至100ml。
10ml/ps3)柠檬酸盐缓冲液(PH6.7):184g柠檬酸和147.5g氢氧化钾(KOH)溶于蒸馏水。
将两溶液合并,用1mol/LNaOH将PH调至6.7,用水稀释定容至1000ml。
20ml/ps注:柠檬酸和氢氧化钾混合时大量放热,需小心缓慢混合,冷却后定容。
4)苯酚钠溶液(1.35mol/L):62.5g苯酚溶于少量乙醇,加2ml甲醇和18.5ml丙酮,用乙醇稀释至100ml(A液),存于冰箱中;27gNaOH溶于100ml水(B液)。
将A、B溶液保存在冰箱中。
使用前将A液、B液各20ml混合,用蒸馏水稀释至100ml。
4ml/ps注:实际配比为:125g苯酚+4ml甲醇+37ml丙酮+25ml乙醇,混合溶解为A液。
54g氢氧化钠溶解为B液,冷却后备用。
A+B,定容至1000ml即得苯酚钠溶液。
苯酚有毒,常温下凝固,不宜称取,需小心。
5)次氯酸钠溶液:用水稀释试剂,至活性氯的浓度为0.9%,溶液稳定。
3ml/ps注:一般次氯酸钠溶液瓶上标注为活性≥5.5%,163.64ml次氯酸钠定容至1000ml。
6)氮的标准溶液:精确称取0.4717g硫酸铵溶于水并稀释至500ml,得到1ml含有0.2mg 氮的标准液;再将此液稀释10倍(吸取5ml标准液定容至100ml)制成氮的工作液(0.01mg/ml)。
二、器材50ml三角瓶,50ml容量瓶,漏斗,25ml试管,定量滤纸,振荡器,分光光度器四、操作步骤1)称取5g过1mm筛的风干土样于50ml三角瓶中,加1ml甲苯,振荡均匀,盖好;注:实际称取2g土。

土壤脲酶的测定方法(苯酚钠—次氯酸钠比色法)土壤脲酶的测定方法(苯酚钠—次氯酸钠比色法)一、原理脲酶存在于大多数细菌、真菌和高等植物里。
它是一种酰胺酶作用是极为专性的,它仅能水解尿素,水解的最终产物是氨和二氧化碳、水。
土壤脲酶活性,与土壤的微生物数量、有机物质含量、全氮和速效磷含量呈正相关。
根际土壤脲酶活性较高,中性土壤脲酶活性大于碱性土壤。
人们常用土壤脲酶活性表征土壤的氮素状况。
土壤中脲酶活性的测定是以脲(尿素)为基质经酶促反应后测定生成的氨量,也可以通过测定未水解的脲(尿素)量来求得。
本方法以脲(尿素)为基质,根据酶促产物氨与苯酚—次氯酸钠作用生成蓝色的靛酚,来分析脲酶活性。
二、试剂1)甲苯2)10%脲(尿素):称取10g脲(尿素),用水溶至100ml。
3)柠檬酸盐缓冲液(PH6.7):184g柠檬酸和147.5g氢氧化钾(KOH)溶于蒸馏水。
将两溶液合并,用1mol/LNaOH将PH调至6.7,用水稀释定容至1000ml。
4)苯酚钠溶液(1.35mol/L):62.5g苯酚溶于少量乙醇,加2ml甲醇和18.5ml丙酮,用乙醇稀释至100ml(A液),存于冰箱中;27gNaOH溶于100ml水(B液)。
将A、B溶液保存在4℃冰箱中。
使用前将A液、B液各20ml混合,用蒸馏水稀释至100ml。
5)次氯酸钠溶液:用水稀释试剂,至活性氯的浓度为0.9%,溶液稳定。
取10%的次氯酸钠溶液9ml,用蒸馏水定容到100ml。
6)氮的标准溶液:精确称取0.4717g硫酸铵溶于水并稀释至1000ml,得到1ml含有0.1mg氮的标准液;再将此液稀释10倍(吸取10ml标准液定容至100ml)制成氮的工作液(0.01mg/ml)。
标准曲线制作:在测定样品吸光值之前,分别取0、1、3、5、7、9、11、13ml氮工作液,移于50ml容量瓶中,然后补加蒸馏水至20ml。
再加入4ml苯酚钠溶液和3ml次氯酸钠溶液,随加随摇匀。

土壤脲酶活性测定(NH4+释放量法)脲酶是酰胺水解酶的一种,在自然界中分布广泛,植物、动物和微生物细胞中均含有此酶。
土壤中的脲酶主要来源于微生物和植物。
脲酶催化尿素的水解反应:在反应过程中,氨基甲酸盐是中间产物。
脲酶还能够催化羟基脲、二羟基脲、半卡巴脲等化合物的水解。
脲酶含有镍,分子量在151,000 Da~480,00 Da之间。
能够抑制脲酶活性的化合物有含硼化合物、尿素衍生物、甲醛、原子量大于50的重金属的盐、含氟化合物、醌和多元酚、抗代谢剂、杂环硫醇等。
1、试验原理通过对新鲜土壤与尿素溶液在37℃培养2h后测定氨释放量,估计脲酶的活性(Tabatabai,1994)。
2、试验仪器50mL容量瓶;培养箱或恒温水浴;蒸馏定氮仪。
3、试验试剂(所用试剂均为分析纯)A、甲苯(C6H5CH3);B、缓冲液:三(羟甲基)氨基甲烷[c(C2H8O3N3)=0.05mol·L-1,pH9.0]:称取 6.1g 三(羟甲基)氨基甲烷溶入700mL蒸馏水中,用c(H2SO4)=0.2mol·L-1的硫酸溶液调pH 至9.0,再用蒸馏水定容至1000mL;尿素溶液{c[CO(NH2)2]=0.2 mol·L-1}:称取1.2g尿素溶入约80mL缓冲液中,后用该缓冲液定容至100mL。
尿素溶液要当天配制,并在4℃下保存备用;氯化钾硫酸银混合溶液[c(KCl)=2.5mol·L-1]-[ρ(Ag2SO4)=100mg·L-1]:先将100mg Ag2SO4溶于700mL蒸馏水中,再加入188g的KCl(分析纯)使之溶解,在定容至1000mL;氧化镁(MgO):于高温电炉中,将氧化镁在600℃-700℃温度下灼烧2h,再放置于干燥器中冷却,贮于瓶中;混合指示剂:溶解0.099g的溴甲酚绿和0.066g甲基红于100mL的乙醇(95%)中;硼酸指示剂溶液[ρ(H3BO3)=20g·L-1]:溶解20g硼酸于950mL的热蒸馏水中,冷却,加入20mL的混合指示剂,充分混匀后,小心滴加氢氧化钠溶液[c(NaOH)=0.1mol·L-1],直至溶液呈红紫色(pH约4.5),稀释成1L;硫酸标准溶液[c(1/2H2SO4)=0.005mol·L-1]。

土壤脲酶测定一、实验目的1.了解土壤中脲酶的活性及其对氮素转化的重要作用;2.通过脲酶测定,评估土壤中氮素的转化和利用效率;3.为制定合理的施肥和作物管理措施提供依据。
二、实验原理脲酶是一种能够催化尿素分解的酶,在土壤中起着至关重要的作用。
它能够将尿素分解成氨和二氧化碳,释放出的氨可以被植物吸收利用。
因此,脲酶的活性可以反映土壤中氮素转化的能力。
本实验采用靛酚比色法测定脲酶活性。
该方法基于脲酶催化尿素分解产生的氨与靛酚反应生成靛酚蓝,其颜色深浅与脲酶活性呈正比。
通过比色法可以测定样品中脲酶的相对活性。
三、实验步骤1.样品采集与处理:选取具有代表性的土壤样品,将其风干、磨碎并过筛。
称取适量样品于试管中,加入适量的磷酸盐缓冲液,充分搅拌均匀。
2.实验溶液配制:配制尿素溶液(100mmol/L)和靛酚溶液(0.05mol/L)。
3.对照试验:取一支试管,加入等体积的磷酸盐缓冲液和尿素溶液,充分混合后放置在30℃恒温箱中30分钟。
然后加入靛酚溶液并充分混合,放置10分钟。
最后加入适量碳酸钠溶液,使溶液呈碱性,终止反应。
以靛酚蓝为标准品,在625nm波长下测定吸光度。
4.样品试验:取适量样品于试管中,加入等体积的磷酸盐缓冲液和尿素溶液,充分混合后放置在30℃恒温箱中30分钟。
然后按照对照试验的步骤加入靛酚溶液并测定吸光度。
5.数据记录与处理:记录对照试验和样品试验的吸光度值,计算脲酶活性。
四、结果分析1.对照试验与样品试验吸光度值的差异反映了样品中脲酶的活性。
对照试验中,由于没有脲酶的作用,尿素分解较慢,因此靛酚与氨的反应较慢,吸光度值较低。
而在样品试验中,由于样品中存在脲酶,脲酶催化尿素分解加速,导致靛酚与氨的反应加快,吸光度值较高。
2.通过比较对照试验和样品试验的吸光度值,可以计算出样品的脲酶活性。
具体计算方法为:脲酶活性(mg/g·h)= [(样品吸光度-对照吸光度)/(对照吸光度×时间×样品质量)]×100%。

土壤脲酶活性的比色法测定是一种常用的方法,它可以测量土壤中脲酶的存在和活性。
这种方法通常使用一种叫做脲酶试剂盒的工具,该试剂盒中包含了所需的试剂和比色剂。
具体的测试步骤如下:
取一定量的土壤样品,并加入适量的水,搅拌均匀。
将混合物加入试剂盒中,加入脲酶试剂。
按照试剂盒中的说明,在一定的时间内进行反应。
比较样品的颜色和标准对照物的颜色,并记录下来。
根据脲酶试剂盒的不同,颜色的变化可能会有所不同。
一般来说,脲酶的存在和活性越高,样品的颜色就会越深。
通过对样品颜色的比较,就可以知道土壤中脲酶的存在和活性水平。
请注意,这种方法只能测量土壤中脲酶的活性水平,并不能测量脲酶的种类和数量。
土壤脲酶活性的比色法测定是一种常用的测量土壤中脲酶存在和活性的方法。
它使用脲酶试剂盒,包含所需试剂和比色剂。
测试步骤包括取样、加水搅拌、加入试剂盒、反应并比较颜色。
结果表明,脲酶存在和活性越高,样品颜色越深。
注意,这种方法只能测量脲酶活性水平,不能测量脲酶种类和数量。

土壤与环境微生物研究法/李振高,骆永明,滕应编著.一北京:科学出版社,2008过氧化氢酶(398-399)脲酶(404-405)磷酸酶(412-413)关松荫/土壤酶及其研究法农业出版社 1986年七月第一版蔗糖酶274-276土壤脲酶(urease)活性的测定方法:靛酚比色法(一)方法原理土壤中脲酶活性的测定是以尿素为基质,酶促水解生成的氨与酚类化合物起反应生成蓝色的靛酚,颜色深度与氨含量相关,因而用于脲酶活性的测定。
(二)试剂1)甲苯2)10%尿素:称取10g尿素,加蒸馏水90ml。
3)柠檬酸盐缓冲液(PH6.7):取184g柠檬酸溶于300ml蒸馏水中,另取147.5g KOH 溶于蒸馏水,再将二种溶液合并,用1N NaOH将pH调节至6.7,用水稀释至1L。
4)苯酚钠溶液(1.35mol/L):62.5克苯酚溶于少量乙醇,加2毫升甲醇和18.5毫升丙酮,用乙醇稀释至100毫升(A 液),存于冰箱中;27克NaOH溶于100毫升水(B液),存于冰箱中。
将A、B溶液保存在冰箱中。
使用前将两种溶液各20ml混合,用蒸馏水稀释至100ml。
5)次氯酸钠溶液:用水稀释试剂,至活性氯的浓度为0.9%,溶液稳定。
6)氮的标准溶液:精确称取0.4717克硫酸铵溶于水并稀释至1000mL,得到1mL含有0.1mg 氮的标准液(100ppm)。
(三)测定步骤(1)标准曲线绘制吸取配置好的氮溶液10mL,定容至100mL,即为10ppm,吸取0、1、2、3、4、5、10、15、20 mL移至50mL容量瓶,加水至20mL,再加入4mL苯酚钠,仔细混合,加入3mL次氯酸钠,充分摇荡,放置20分钟,用水稀释至刻度。
即为0、0.2ppm、0.4ppm、0.6ppm、0.8ppm、1ppm、2ppm、3ppm、4ppm的标准曲线。
将着色液在紫外分光光度计上于578nm处进行比色测定,以标准溶液浓度为横坐标,以光密度值为纵坐标绘制曲线图。

土壤脲酶的测定方法(改良靛酚蓝比色法)一、原理以尿素为底物,经培养后根据脲酶酶促产物--氨(忽略硝化过程造成的氨氮损失)在碱性介质中与苯酚、次氯酸钠作用生成蓝色的靛酚。
该生成物数量与氨浓度成正比。
后即称为靛酚蓝比色法,其结果精确性较高,重现性较好,在脲酶活性测定中的应用最为广泛。
二、试剂1)甲苯1ml/ps注:甲苯易挥发,要在通风条件好的地方操作。
2)5%尿素:称取5g尿素,用水溶至100ml。
10ml/ps3)柠檬酸盐缓冲液(PH6.7):184g柠檬酸和147.5g氢氧化钾(KOH)溶于蒸馏水。
将两溶液合并,用1mol/LNaOH将PH调至6.7,用水稀释定容至1000ml。
20ml/ps注:柠檬酸和氢氧化钾混合时大量放热,需小心缓慢混合,冷却后定容。
4)苯酚钠溶液(1.35mol/L):62.5g苯酚溶于少量乙醇,加2ml甲醇和18.5ml丙酮,用乙醇稀释至100ml(A液),存于冰箱中;27gNaOH溶于100ml水(B液)。
将A、B溶液保存在冰箱中。
使用前将A液、B液各20ml混合,用蒸馏水稀释至100ml。
4ml/ps注:实际配比为:125g苯酚+4ml甲醇+37ml丙酮+25ml乙醇,混合溶解为A液。
54g氢氧化钠溶解为B液,冷却后备用。
A+B,定容至1000ml即得苯酚钠溶液。
苯酚有毒,常温下凝固,不宜称取,需小心。
5)次氯酸钠溶液:用水稀释试剂,至活性氯的浓度为0.9%,溶液稳定。
3ml/ps注:一般次氯酸钠溶液瓶上标注为活性≥5.5%,163.64ml次氯酸钠定容至1000ml。
6)氮的标准溶液:精确称取0.4717g硫酸铵溶于水并稀释至500ml,得到1ml含有0.2mg 氮的标准液;再将此液稀释10倍(吸取5ml标准液定容至100ml)制成氮的工作液(0.01mg/ml)。
二、器材50ml三角瓶,50ml容量瓶,漏斗,25ml试管,定量滤纸,振荡器,分光光度器四、操作步骤1)称取5g过1mm筛的风干土样于50ml三角瓶中,加1ml甲苯,振荡均匀,盖好;注:实际称取2g土。

靛酚蓝比色法测定土壤脲酶的活性一、实验目的:1. 测定土壤脲酶活性的意义。
2. 掌握测定土壤脲酶活性的原理和方法。
二、实验原理靛酚蓝比色法的基本原理是:被测物浸提剂中的NH4+,在强碱性介质中与次氯酸盐和苯酚反应,生成水溶性染料靛酚蓝,其深浅与溶液中的NH4+-N含量呈正比,线性范围为0.05~0.5mg/l之间。
靛酚蓝反应原理如下: NH3 + OCl——NH2 Cl +OH-三、实验试剂1) 10%尿素:称取10g尿素,用蒸馏水溶至100ml。
2)柠檬酸盐缓冲液(PH=6.7):184克柠檬酸和147.5克氢氧化钾溶于蒸馏水。
将两溶液合并,用1mol/LNaOH将PH调至6.7,用水稀释至1000毫升。
3)苯酚钠溶液(1.35mol/L):62.5克苯酚溶于少量无水乙醇,加2毫升甲醇和18.5毫升丙酮,用无水乙醇稀释至100毫升(A),存于冰箱中;27克NaOH溶于100毫升水(B)。
将AB溶液保存在冰箱中。
使用前将2溶液各20毫升混合,用蒸馏水稀释至100毫升。
4)次氯酸钠溶液:用水稀释试剂至活性氯的浓度为0.9%,溶液稳定。
5)氮的标准溶液(0.1mg/ml):精确称取0.4717克硫酸铵溶于水并稀释至1000ml,得到1ml含有0.1mg氮的标准液。
四、实验过程1.标准曲线的测定吸取10ml氮的标准溶液定容至100ml,摇匀。
从其中分别吸取0,1.00,3.00,5.00,7.00,10.00ml移至50ml比色管中,加水至20ml,再加入4ml苯酚钠,充分混合。
加入3ml次氯酸钠,充分摇荡,放置20分钟,用水稀释至刻度。
将显色液在可见分光光度计上于578nm处,以1cm比色皿进行比色测定,以试剂空白为参比。
以标准溶液氮含量为横坐标,以吸光度值为纵坐标绘制标准曲线。
2.土样中脲酶活性的测定分别称取2g过1mm筛的风干土样于3个100ml锥形瓶中,向其中加入1ml甲苯,以使土样全部湿润为宜。
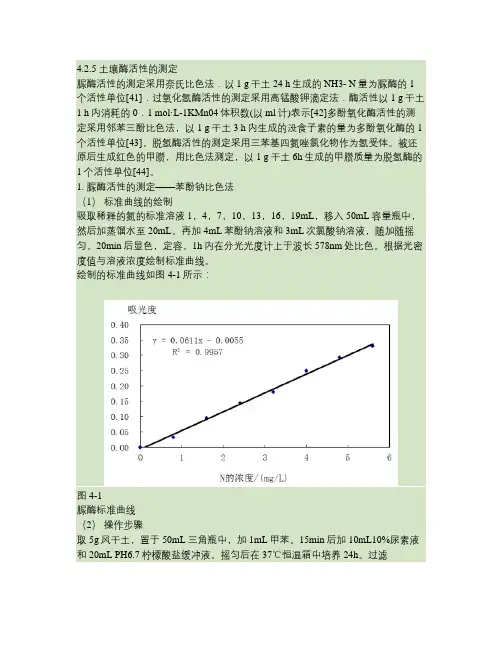
4.2.5 土壤酶活性的测定脲酶活性的测定采用奈氏比色法.以1 g干土24 h生成的NH3- N量为脲酶的1个活性单位[41].过氧化氢酶活性的测定采用高锰酸钾滴定法.酶活性以1 g干土1 h内消耗的0.1 mol·L-1KMn04体积数(以ml计)表示[42]多酚氧化酶活性的测定采用邻苯三酚比色法,以1 g干土3 h内生成的没食子素的量为多酚氧化酶的1个活性单位[43],脱氢酶活性的测定采用三苯基四氮唑氯化物作为氢受体。
被还原后生成红色的甲臜,用比色法测定,以1 g干土6h生成的甲臜质量为脱氢酶的1个活性单位[44]。
1. 脲酶活性的测定——苯酚钠比色法(1)标准曲线的绘制吸取稀释的氮的标准溶液1,4,7,10,13,16,19mL,移入50mL容量瓶中,然后加蒸馏水至20mL。
再加4mL苯酚钠溶液和3mL次氯酸钠溶液,随加随摇匀。
20min后显色,定容。
1h内在分光光度计上于波长578nm处比色。
根据光密度值与溶液浓度绘制标准曲线。
绘制的标准曲线如图4-1所示:图4-1脲酶标准曲线(2)操作步骤取5g风干土,置于50mL三角瓶中,加1mL甲苯。
15min后加10mL10%尿素液和20mL PH6.7柠檬酸盐缓冲液。
摇匀后在37℃恒温箱中培养24h。
过滤后取3mL滤液注入50mL容量瓶中,然后按绘制标准曲线显色方法进行比色测定。
脲酶活性以24h后1g土壤中NH3-N的毫克数表示。
2. 过氧化氢酶活性的测定——高锰酸钾滴定法(1)操作步骤取5g土壤样品于100mL三角瓶中(用不加入土样的作空白对照),加0.5mL甲苯,摇匀,于4℃冰箱中放置30min。
取出,立刻加入25mL冰箱储存的3%H2O2水溶液,充分混匀后,再置于4℃冰箱中放置1h。
取出,迅速加入冰箱储存的2mol/L H2SO425mL,摇匀,过滤。
取1mL滤液,用0.05mol/L的KMnO4滴定。
(2)计算根据对照和样品的滴定差,求出相当于分解的H2O2的量所消耗的KMnO4。

土壤脲酶(urease)活性的测定方法:靛酚比色法(一)方法原理土壤中脲酶活性的测定是以尿素为基质,酶促水解生成的氨与酚类化合物起反应生成蓝色的靛酚,颜色深度与氨含量相关,因而用于脲酶活性的测定。
(二)试剂1)甲苯2)10%尿素:称取10g尿素,用水溶至100mL。
3)柠檬酸盐缓冲液(PH6.7):184克和147.5克氢氧化钾溶于蒸馏水。
将两溶液合并,用1mol/LNaOH将PH调至6.7,用水稀释至1000毫升。
4)苯酚钠溶液(1.35mol/L):62.5克苯酚溶于少量乙醇,加2毫升甲醇和18.5毫升丙酮,用乙醇稀释至100毫升(A),存于冰箱中;27克NaOH溶于100毫升水(B)。
将A、B溶液保存在冰箱中。
使用前将2溶液各20毫升混合,用蒸馏水稀释至100毫升。
5)次氯酸钠溶液:用水稀释试剂,至活性氯的浓度为0.9%,溶液稳定。
6)氮的标准溶液:精确称取0.4717克硫酸铵溶于水并稀释至1000mL,得到1mL含有0.1mg氮的标准液。
(三)测定步骤(1)标准曲线绘制吸取配置好的氮溶液10mL,定容至100mL,即稀释了10倍,吸取1,3,5,7,9,11,13mL移至50mL容量瓶,加水至20mL,再加入4mL苯酚钠,仔细混合,加入3mL次氯酸钠,充分摇荡,放置20分钟,用水稀释至刻度。
将着色液在紫外分光光度计上于578nm处进行比色测定,以标准溶液浓度为横坐标,以光密度值为纵坐标绘制曲线图。
(2)土壤中脲酶活性的测定称取10 g土壤置于100mL容量瓶中。
用2mL甲苯处理15分钟。
往瓶中加入10mL 10%尿素溶液和20mL柠檬酸缓冲液(pH6.7)。
仔细混合后,将瓶放在37℃恒温箱中,放置3 h。
与此同时,进行以水代替基质,及无土壤的基质对照测定。
培养结束后,用热至38℃的水稀释至刻度。
摇匀,将悬液过滤。
吸取1mL 滤液于50mL容量瓶中,用蒸馏水加至10mL。
然后按标准曲线绘制的操作加入苯酚钠等试剂,显色,比色,最后根据标准曲线求出氨态氮含量。

一、实验目的1. 了解土壤脲酶的作用及其在土壤氮素循环中的重要性。
2. 掌握土壤脲酶活性的测定方法。
3. 分析不同土壤类型、不同施肥处理对土壤脲酶活性的影响。
二、实验原理土壤脲酶是一种水解酶,能够将土壤中的尿素分解为氨和二氧化碳。
土壤脲酶活性反映了土壤中氮素转化和循环的能力。
本实验采用苯酚钠滴定法测定土壤脲酶活性,通过计算生成的氨的量来反映土壤脲酶活性。
三、实验材料1. 土壤样品:采集不同土壤类型、不同施肥处理的土壤样品。
2. 试剂:苯酚钠、氢氧化钠、硼酸、盐酸、硫酸铜、硫酸锌、尿素、蒸馏水等。
3. 仪器:分析天平、滴定管、锥形瓶、移液管、烧杯、试管等。
四、实验步骤1. 土壤样品处理:将采集的土壤样品风干、磨细、过筛(筛孔直径为2mm),备用。
2. 土壤脲酶活性的测定:(1)配制苯酚钠溶液:称取苯酚钠0.1g,溶解于100ml蒸馏水中,配制成0.1mol/L苯酚钠溶液。
(2)配制0.5mol/L氢氧化钠溶液。
(3)配制硼酸溶液:称取硼酸0.5g,溶解于100ml蒸馏水中,配制成0.5mol/L硼酸溶液。
(4)配制硫酸铜溶液:称取硫酸铜0.5g,溶解于100ml蒸馏水中,配制成0.5mol/L硫酸铜溶液。
(5)配制硫酸锌溶液:称取硫酸锌0.5g,溶解于100ml蒸馏水中,配制成0.5mol/L硫酸锌溶液。
(6)配制0.5mol/L盐酸溶液。
(7)配制尿素溶液:称取尿素0.5g,溶解于100ml蒸馏水中,配制成0.5mol/L 尿素溶液。
(8)取10g土壤样品,加入100ml蒸馏水,充分振荡,使土壤中的脲酶与尿素充分接触。
(9)取5ml土壤悬浊液,加入5ml苯酚钠溶液,混匀。
(10)加入5ml氢氧化钠溶液,混匀。
(11)在60℃水浴中加热30分钟。
(12)加入5ml硼酸溶液,混匀。
(13)加入5ml硫酸铜溶液,混匀。
(14)加入5ml硫酸锌溶液,混匀。
(15)加入5ml盐酸溶液,混匀。
(16)静置30分钟,使沉淀完全。
一、脲酶测定(苯酚钠-次氯酸钠比色法)脲酶是对尿素转化起关键作用的酶,它的酶促反应产物是可供植物利用的氮源,它的活性可以用来表示土壤供氮能力。
1、试剂配制:(1)pH6.7柠檬酸盐溶液:取368g柠檬酸溶于600mL蒸馏水中,另取295g氢氧化钾溶于水,再将两种溶液合并,用1N氢氧化钠将pH调至6.7,并用水稀释至2L。
(2)苯酚钠溶液:称取62.5g苯酚溶于少量乙醇中,加2mL甲醇和18.5mL丙酮,后用乙醇稀释至100mL(A液),保存再冰箱中。
称取27g氢氧化钠溶于100mL水中(B液),保存于冰箱中。
使用前,取A、B两液各20mL混和,并用蒸馏水稀释至100mL备用。
(3)次氯酸钠溶液:用水稀释制剂至活性氯的浓度为0.9%,溶液稳定。
(4)10%尿素溶液:10g尿素溶于100mL水中。
(5)N的标准溶液:精确称取0.4717g硫酸铵溶于水稀释至1L,则得1mL含0.1mgN 的标液,再将此液稀释10倍制成氮工作液(0.01mg/mL)。
标准曲线绘制:分别取0、0.5、1.5、2.5、3.5、4.5、5.5、6.5mL氮工作液置于25mL刻度试管中,加蒸馏水至10mL,再加2mL苯酚钠溶液和1.5mL次氯酸钠溶液,随加随摇匀,20min 后显色,定容25mL。
1h内再分光光度计上于578nm处比色。
1020304050607000.20.40.62、操作步骤(1)称取2.5g土置于25mL 刻度试管中, 加0.5mL 甲苯处理,加塞塞紧轻摇15min;往瓶中加入2.5mL10%尿素液和5mL 的柠檬酸盐缓冲液(pH6.7),仔细混匀。
在37℃恒温箱中培养3h。
(当脲酶活性为3~80微克NH3-N 时,本法能获得可靠的结果。
若脲酶活性小于3微克,培养时间需增至24h )。
(2)然后用热至38℃的蒸馏水稀释至刻度(甲苯应浮在刻度以上),摇荡,将悬液过滤。
对每一土样,设置用水代替基质的对照。
对整个实验,进行无土壤基质的对照,以检验实验的纯度。
一、实验目的1. 了解土脲酶的概念和作用;2. 掌握土脲酶的测定方法;3. 分析土脲酶在土壤环境中的分布和影响因素。
二、实验原理土脲酶是一种水解脲的酶,能将土壤中的尿素分解成氨和二氧化碳,从而释放出氮素。
土脲酶的活性是土壤氮素循环的重要指标,对土壤肥力、作物生长及环境质量具有重要意义。
本实验采用酚酞比色法测定土脲酶活性。
在碱性条件下,脲酶将尿素分解成氨,氨与酚酞指示剂发生反应,生成红色络合物,通过测定红色络合物的吸光度,可以计算出氨的浓度,进而推算出土脲酶的活性。
三、实验材料与仪器1. 实验材料:土壤样品、尿素、酚酞指示剂、氢氧化钠、硫酸、无水碳酸钠、硫酸钾、蒸馏水等;2. 实验仪器:分光光度计、电子天平、锥形瓶、移液管、烧杯、漏斗、玻璃棒、容量瓶等。
四、实验步骤1. 土壤样品的制备:取一定量的土壤样品,加入适量的蒸馏水,充分振荡,过滤,收集滤液;2. 标准曲线的制作:配制一系列不同浓度的氨标准溶液,分别加入酚酞指示剂,用氢氧化钠溶液滴定至终点,记录滴定数据,绘制标准曲线;3. 土脲酶活性的测定:a. 将土壤样品与适量的尿素溶液混合,加入酚酞指示剂,在一定的温度下反应一定时间;b. 反应结束后,用氢氧化钠溶液滴定至终点,记录滴定数据;c. 根据标准曲线,计算氨的浓度,进而推算出土脲酶的活性。
五、实验结果与分析1. 标准曲线的制作:绘制标准曲线,线性范围为0.1-1.0mg/L;2. 土脲酶活性的测定:根据实验数据,计算出不同土壤样品的土脲酶活性,并进行分析。
(此处省略实验数据及分析)六、实验结论1. 土脲酶在土壤环境中具有重要作用,其活性受土壤类型、温度、水分、有机质等因素的影响;2. 本实验采用酚酞比色法测定土脲酶活性,操作简便,结果准确;3. 通过对土壤样品的测定,可以了解土壤中土脲酶的分布及影响因素,为土壤改良和作物生长提供依据。
七、实验注意事项1. 实验过程中要严格控制温度、时间等因素,确保实验结果的准确性;2. 使用移液管、滴定管等精密仪器时,要注意操作规范,避免误差;3. 实验过程中要妥善处理废弃物,确保实验安全。
土壤酶活性的测定方法及部分样品配制详细请参考《土壤微生物分析方法手册》,《土壤酶及其研究法》土壤样品采集与制备土壤样品取样后混匀,用于土壤酶活性测定的土壤磨细过2mm筛后,置于4℃冰箱内保存备测。
1.土壤酶活性的测定方法1.1.脲酶采用靛酚蓝比色法方法原理:本法基于以尿素为基质,酶促水解生成的氨与酚类化合物起反应生成蓝色的靛酚,颜色深度与氨含量相关,用于尿酶活性的测定。
操作步骤:取10g风干土,置于100ml三角瓶中,加2ml甲苯,15min后加10ml 10%尿素液和20ml pH6.7柠檬酸盐缓冲液。
摇匀后在37℃恒温箱中培养3h。
按此操作,进行以水代替基质,及无土壤的基质对照测定,过滤后取0.5ml滤液于50ml比色管中,然后按绘制标准曲线显色方法进行比色测定。
氮的标液:精确称取0.4717g硫酸按溶于水并稀释至1000ml,则得1ml含0.1mg氮的标准液。
绘制标准曲线时,可将此液稀释10倍供用。
pH6.7柠檬酸盐缓冲液:用368g柠檬酸溶于600ml水,另取295g氢氧化钾溶于水,再将二种溶液混合,然后用1M的氢氧化钠调节pH到6.7,定容到2L。
苯酚溶液:称取苯酚(C6H5OH)10g和硝基铁氰化钠[Na2Fe(CN)5NO2H2O]100mg稀释至1L。
此试剂不稳定,须贮于棕色瓶中,在4℃冰箱中保存。
次氯酸钠碱性溶液:称取氢氧化钠(化学纯)10g、磷酸氢二钠(Na2HPO4·7H2O, 化学纯)7.06g、磷酸钠(Na3PO4·12H2O, 化学纯)31.8g 和52.5g·L-1次氯酸钠(NaOCl,化学纯,即含5%有效氯的漂白粉溶液)10mL 溶于水中,稀释至1L,贮于棕色瓶中,在4℃冰箱中保存。
标线绘制:取稀释的标准液0、l、2、4、6、8、10ml,移于50rnl容量瓶中,然后加入蒸馏水至20mL。
再加4mL苯酸钠溶液和4mL次氯酸钠溶液,随加随摇匀。
一、脲酶测定(比色法)脲酶是对尿素转化起关键作用的酶,它的酶促反应产物是可供植物利用的氮源,它的活性可以用来表示土壤供氮能力。
1、试剂配制:(1)pH6。
7柠檬酸盐溶液:取368g柠檬酸溶于600mL蒸馏水中,另取295g氢氧化钾溶于水,再将两种溶液合并,用1N氢氧化钠将pH调至6.7,并用水稀释至2L。
(2)苯酚钠溶液:称取62。
5g苯酚溶于少量乙醇中,加2mL甲醇和18.5mL 丙酮,后用乙醇稀释至100mL(A液),保存再冰箱中。
称取27g氢氧化钠溶于100mL水中(B液),保存于冰箱中。
使用前,取A、B两液各20mL混和,并用蒸馏水稀释至100mL备用。
(3)次氯酸钠溶液:用水稀释制剂至活性氯的浓度为0。
9%,(1。
9g次氯酸钠溶于1L水中)溶液稳定。
(4)10%尿素溶液:10g尿素溶于100mL水中。
(5)N的标准溶液:精确称取0。
4717g硫酸铵溶于水稀释至1L,则得1mL 含0.1mgN的标液,再将此液稀释10倍制成氮工作液(0.01mg/mL)。
2、操作步骤称取5g土置于50mL容量瓶中,加1mL甲苯处理,加塞塞紧轻摇15min;往瓶中加入5mL10%尿素液和10mL的柠檬酸盐缓冲液(pH6.7),仔细混匀。
在37℃恒温箱中培养24h。
然后用热至38℃的蒸馏水稀释至刻度(甲苯应浮在刻度以上),摇荡,将悬液过滤。
取滤液1mL置于50mL容量瓶中,用蒸馏水稀释至10mL,然后加入4mL苯酚钠溶液,并立即加入3mL次氯酸钠溶液,加入每一试剂后,立即将混合物摇匀,20min后,将混合物稀释至刻度,在波长578nm处测定吸光值。
脲酶活性以样品所得的吸光值减去对照样品吸光值之差,根据标准曲线求出氨态氮量。
标准曲线绘制:分别取0、1、3、5、7、9、11、13mL氮工作液置于50mL容量瓶中,加蒸馏水至20mL,再加4mL苯酚钠溶液和3mL次氯酸钠溶液,随加随摇匀,20min后显色,定容。
1h内再分光光度计上于578nm处比色。
土壤脲酶测定(专用)关松荫苯酚-次氯酸钠比色法测定土壤脲酶活性(Sunny-zhao)1 方法原理脲酶存在于大多数细菌、真菌和高等植物内。
它是一种酰胺酶作用是极为专性的,它仅能水解尿素,水解的最终产物是氨、二氧化碳和水。
土壤脲酶活性与土壤的微生物数量、有机物质含量、全氮和速效磷含量呈正相关。
根际土壤脲酶活性较高,中性土壤脲酶活性大于碱性土壤,所以人们常用土壤脲酶活性表征土壤氮素的状况。
土壤中脲酶活性的测定是以尿素为基质经酶促反应后测定生成的氨量,也可以通过测定为水解的尿素量来求得。
本方法以尿素为基质,根据酶促产物氨在强碱性介质与苯酚——次氯酸钠的作用生成蓝色的靛酚,其颜色深浅与溶液中的NH4+-N含量成正比,进而分析脲酶活性。
2 试剂和材料2.1 甲苯分析纯。
2.2 10% 尿素:称取10 g尿素,用水溶至100 ml。
2.3 柠檬酸盐缓冲液(pH 6.7):184 g柠檬酸和147.5 g氢氧化钾溶于适量蒸馏水中,用水稀释至950 ml,用1 mol/L NaOH将pH调至6.7,最后用水定容到1000 ml。
2.4 苯酚钠溶液(1.35 mol/L):62.5 g苯酚溶于少量无水乙醇,加2 ml甲醇和18.5 ml丙酮,用无水乙醇稀释至100 ml(A溶液),存于冰箱;27 g NaOH溶于100 ml水(B液)。
将A、B保存于冰箱中。
使用前将A、B液各20 ml混合,用蒸馏水稀释至100 ml。
2.5 次氯酸钠溶液:用水稀释试剂,至活性氯的浓度为0.9%。
(根据分析纯原有活性氯含量而定)2.6 氮的标准溶液:精确称取0.4717 g硫酸铵溶于水并稀释至1000 ml,得到1 ml 含有0.1 mg的氮的标准液。
3 主要仪器恒温培养箱,可见分光光度计。
4 分析步骤4.1 标准曲线的测定将标准溶液稀释10倍(吸取10 ml标准液定容至100 ml)制成氮的工作液(0.01 mg/ml)。
从其中分别吸收0,1.00,3.00,5.00,7.00,9.00,11.00,13.00 ml移至50 ml容量瓶,加水至20 ml,再加入4 ml苯酚钠溶液,充分混合。