靶向药靶点介绍
- 格式:xls
- 大小:5.81 MB
- 文档页数:27


靶向治疗肿瘤药物的可能靶点位置癌症的常规治疗手段包括外科手术、化学治疗和放射治疗。
化学治疗也被人们成为药物治疗,在癌症治疗中一直发挥着重要作用,但是其治疗效果却受到其剂量依赖性毒性的影响,目前药物治疗的效果已经进入平台期。
分子靶向治疗指以癌症相关分子作为靶点,将药物、抗体等有效成分靶向定位于癌细胞及相关成分,从而达到治疗癌症的目的。
分子靶向治疗具有定向、定位的优势,乐意减少用药剂量,提高治疗效果,减少毒副作用,正成为全世界癌症治疗的研究热点。
在分子靶向治疗研究过程中,靶点分子的确具有重要的意义,可以为癌症的分子靶向治疗提供理论和实践依据。
根据靶点分子和癌细胞的位置关系,可分为癌细胞本身靶点分子和癌细胞相关分子两大类:前者是指靶点分子位于癌细胞上;后者是指那些不在癌细胞上,但却与癌细胞状态有密切关系的靶点分子。
1 癌细胞本身靶点分子根据靶点分子解剖位置可将癌细胞本身靶点分为癌细胞靶点分子、癌细胞质内靶点分子、癌细胞核内靶点分子。
1.1 癌细胞膜靶点分子细胞膜是细胞同外界进行物质能量交换的门户,同时也是药物作用于细胞时首先接触到的部位,细胞膜外表面因此成为选取靶点分子的理想位置。
1.1.1 细胞膜受体靶点分子表皮生长因子受体家族(epidermal growth factor receptor EGFR)包括erbB1(EGFR),erbB2(HER-2)、erbB3(HER-3)和erbB4(HER-4)4类,由胞外区、跨膜区、胞内区3部分组成;胞外区是配体结合区,胞内区有ATP结合位点和酪氨酸激酶区。
EGFR与配体结合后的活化可激活许多下游信号转导通路,参与癌细胞的增殖、粘附、侵袭、转移、凋亡和肿瘤血管生成等。
研究发现,很多癌细胞高表达EGFR,如头颈部癌、卵巢癌、宫颈癌、膀胱癌和食管癌等[1]。
目前,针对EGFR胞外区的抗体药物研究比较深入,部分药物已经市场化,如赫赛汀、西妥昔单抗、泰欣生等。


靶向药物治疗的靶点检测与选择方法摘要:靶向药物治疗是一种利用药物直接干预肿瘤细胞特定分子信号通路的治疗方法。
靶点检测与选择是靶向药物治疗的关键环节,它有助于确定患者特定疾病的靶点,并为个体化治疗提供指导。
本文将介绍靶向药物治疗的靶点检测与选择方法,包括肿瘤组织检测、基因检测和蛋白质检测,并探讨其应用前景和挑战。
1. 引言靶向药物治疗是一种与传统治疗方式不同的治疗手段。
与广谱化疗或放疗相比,靶向药物治疗通过选择性地干预癌细胞的特定靶点,降低了对正常细胞的毒性作用,提高了治疗效果。
靶点检测与选择是靶向药物治疗的关键环节,它有助于确定患者特定疾病的靶点,并为个体化治疗提供指导。
2. 肿瘤组织检测肿瘤组织检测是靶向药物治疗中常用的一种方法。
通过对患者的肿瘤组织进行检测,可以确定患者特定疾病的分子表达情况,从而选择合适的靶向药物。
肿瘤组织检测方法包括免疫组织化学染色、原位杂交和基于DNA测序的方法等。
这些方法可以检测患者的基因突变、蛋白质异常表达等信息,为靶向治疗提供依据。
3. 基因检测基因检测是靶向药物治疗中常用的一种方法。
通过对患者基因组的检测,可以确定患者是否存在特定基因变异,从而判断是否适合接受靶向药物治疗。
基因检测方法包括多态性标记分析、聚合酶链式反应、DNA芯片技术和基于下一代测序的方法等。
这些方法可以准确地检测患者的基因突变、基因扩增、基因缺失等异常情况,为选择合适的靶向药物提供指导。
4. 蛋白质检测蛋白质检测是靶向药物治疗中常用的一种方法。
通过对患者蛋白质组的检测,可以确定患者特定疾病的蛋白质表达情况,从而选择合适的靶向药物。
蛋白质检测方法包括免疫组织化学染色、酶联免疫吸附试验、质谱分析和蛋白质芯片技术等。
这些方法可以检测患者的蛋白质异常表达、蛋白质修饰等信息,为个体化治疗提供依据。
5. 应用前景和挑战靶向药物治疗的靶点检测与选择方法为个体化治疗提供了有力支持,但仍存在一些挑战。
首先,技术手段的不断进步仍然是推动靶点检测与选择发展的关键。

靶向药物治疗的分子靶点选择与删除靶向药物治疗是一种通过选择性地干预癌症细胞中的特定分子靶点,从而抑制或抢夺其生长和繁殖能力的治疗方法。
在靶向治疗过程中,选择合适的分子靶点对于疗效的提高至关重要,而删除不适合的分子靶点则可以避免药物对正常细胞造成的不良作用。
本文将重点讨论靶向药物治疗的分子靶点选择与删除的关键因素及方法。
分子靶点选择是靶向药物研发的首要任务。
在选择分子靶点时,首先需要确保该靶点在肿瘤细胞中高度表达,并且在正常细胞中表达较低或不存在。
这种差异表达是靶向药物的基础,因为只有在使用药物时,才能对高度表达该靶点的癌细胞产生明显的治疗效果,而对正常细胞造成的毒副作用较小。
因此,通过分析肿瘤细胞与正常细胞的基因表达谱和蛋白质组学数据,可以筛选出潜在的靶点。
此外,靶点选择还需要考虑其在癌细胞增殖、转移和耐药等生物学过程中的重要作用。
一般来说,参与多个关键生物学过程的靶点更具有治疗潜力。
在这方面,各种细胞信号通路上的关键蛋白质往往是研究的热点。
细胞信号通路参与调控细胞的生长、分化、凋亡等基本生理过程,而异常活化的信号通路常常与癌症的发生和发展密切相关。
在分子靶点选择的基础上,还需要进行有效的分子靶点删除。
不适合的分子靶点可能会导致药物对正常细胞的毒副作用,甚至加速肿瘤细胞的发展。
确定删除分子靶点的方法有多种。
一种常见的方法是使用基因编辑技术对目标基因进行靶向敲除。
这可以通过使用CRISPR/Cas9等工具,将细胞的自我修复机制引导到目标基因上,从而引发目标基因的敲除。
此外,还可以使用RNA干扰技术(RNAi)来抑制目标基因的表达,从而达到删除靶点的目的。
除了以上的分子方法外,还可以利用药物分子筛选技术进行靶点删除。
通过构建库存有大量化合物的化学结构库,可以通过这些化合物与特定的目标蛋白质相互作用,从而发现潜在的药物分子。
通过筛选这些化合物,可以找到对应于特定靶点的药物分子,最终达到删除该靶点的论据。
作者简介邱⽴新,就职于复旦⼤学附属肿瘤医院肿瘤内科。
主要从事胃癌、肠癌等恶性肿瘤的化疗、靶向治疗、免疫治疗和研究。
创办了肿瘤科普公众号“邱⽴新医⽣(qiulixinyisheng)”。
在International Journal of Cancer、European Journal of Cancer等发表SCI论⽂65篇,累计影响因⼦约300 分,其中第⼀或并列第⼀作者SCI论⽂40篇,累计影响影⼦约180分。
副主编《赢在论⽂*术篇》、参编《实⽤循证医学⽅法学》。
负责国家⾃然科学基⾦、中国临床肿瘤学科学基⾦等。
获得教育部科技进步⼆等奖、上海市医学科技进步奖三等奖、上海医学院⾸届青年学者论坛⼆等奖等。
实,PIK3CA突变在许多不同类型的实体肿瘤中均存在,其中,发现概率较⾼的主要有:肺癌、结直肠癌和乳腺癌。
各癌种突变情况肺癌在⾮⼩细胞肺癌中,不同病理类型的PIK3CA突变频率为不尽相同,约为:鳞癌3.9%、腺癌2.7%。
有意思的是,PIK3CA突变与EGFR突变、KRAS突变可能同时存在。
并且,有部分研究表明,PIK3CA突变可能与患者服⽤EGFR-TKIs后的⽆进展⽣存期(PFS)降低和总⽣存期(OS)缩短具有相关性。
最新的研究显⽰,PIK3CA在NSCLC的原发灶和其转移灶均呈过表达,主要是扩增和突变的形式,并随着AKT活性的增强,呈现共表达的特点。
总的来说,PIK3CA基因突变可能预测患者预后,但仍需要更多的研究数据来加以佐证。
结直肠癌PIK3CA基因在结直肠癌中的突变率,约15-20%,且往往与KRAS、NRAS、BRAF发⽣交叉突变。
既往发表的荟萃分析研究结果显⽰PIK3CA突变的患者相对于野⽣型的患者化疗客观有效率(ORR)明显降低,并且有较差PFS及OS的趋势。
PIK3CA突变的CRC患者使⽤阿司匹林者能够显著延长总⽣存时间,⽽PIK3CA 野⽣型者,则⽆受益。
乳腺癌PIK3CA基因突变在乳腺癌中发⽣率约为30%,在ER+/HER2-乳腺癌中,PI3K/AKT通路常被异常激活,该通路中的PIK3CA,PIK3R1等基因存在⾼频突变。

肿瘤靶向药靶点治疗及不良反应总结肿瘤靶向药是一种能够特异性地靶向肿瘤细胞并抑制其增殖、侵袭和转移的药物。
与传统化疗药物相比,肿瘤靶向药具有更高的选择性、更好的耐受性和更低的毒副作用。
本文将对常见的肿瘤靶向药的靶点、治疗及不良反应进行总结。
一、抗EGFR(表皮生长因子受体)靶向药物:EGFR是一种过度表达于多种肿瘤细胞表面的膜蛋白,抑制EGFR可以阻止癌细胞的增殖和侵袭。
常见的抗EGFR靶向药物包括鲁西单抗、曲妥珠单抗。
不良反应方面,常见的包括皮疹、腹泻、疲劳等。
二、抗HER2(人类表皮生长因子受体2)靶向药物:HER2是乳腺癌和胃癌等肿瘤中过度表达的靶标,抑制HER2可以阻止癌细胞的增殖。
常见的抗HER2靶向药物包括曲妥珠单抗、帕妥珠单抗。
不良反应方面,常见的包括心脏毒性、恶心和呕吐等。
三、多酪氨酸激酶(BRAF)抑制剂:BRAF是一个在恶性黑色素瘤等肿瘤中突变的基因,抑制BRAF可以阻止癌细胞的增殖。
常见的BRAF抑制剂包括达沙替尼、维美替尼。
不良反应方面,常见的包括皮肤病变、发热和疲劳等。
四、ALK(酪氨酸激酶)抑制剂:ALK基因突变与非小细胞肺癌相关,抑制ALK可以阻止肿瘤细胞的生长。
常见的ALK抑制剂包括克唑替尼、阿法替尼。
不良反应方面,常见的包括肝功能异常、恶心和疲劳等。
五、PD-1(程序化细胞死亡蛋白1)抑制剂:PD-1是一种负调控肿瘤相关免疫反应的膜蛋白,抑制PD-1可以增强机体抗肿瘤免疫能力。
常见的PD-1抑制剂包括伊普伐木单抗、润达单抗。
不良反应方面,常见的包括乏力、皮疹、恶心等。
六、PARP(多精胺ADP核糖聚合酶)抑制剂:PARP在DNA损伤修复中起重要作用,抑制PARP可以阻止肿瘤细胞的DNA修复能力。
常见的PARP抑制剂包括奥拉帕尼布、利普帕尼布。
不良反应方面,常见的包括恶心、呕吐、疲劳等。
需要注意的是,不同的肿瘤靶向药对于不同的肿瘤类型存在差异,具体使用时需要根据患者的肿瘤类型、基因突变状态和身体状况进行选择。

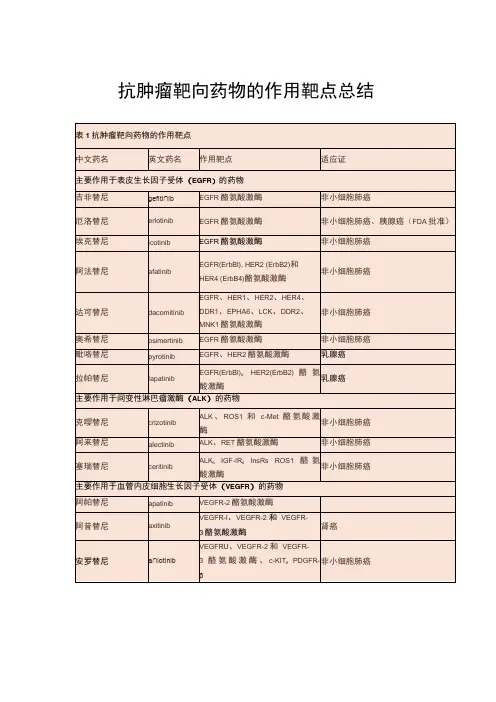
肿瘤靶向药物靶点汇总肿瘤靶向药物是一类可以选择性地作用于肿瘤细胞特定靶点的药物。
这些靶点可以是肿瘤细胞上表达的特定分子、受体和酶。
通过作用于这些靶点,肿瘤靶向药物可以抑制肿瘤细胞的增殖,诱导其凋亡,阻断其侵袭和转移能力,从而达到治疗肿瘤的目的。
以下是肿瘤靶向药物常用的靶点的汇总:1.表皮生长因子受体(EGFR):EGFR是一种受体酪氨酸激酶,它在许多肿瘤细胞上高表达。
EGFR靶向药物包括西妥昔单抗、埃洛替尼等,可以抑制EGFR信号通路的活化,阻断肿瘤细胞的增殖和生存,适用于EGFR突变阳性的肿瘤,如非小细胞肺癌。
2.奥曲肽受体:奥曲肽受体是一种在神经内分泌肿瘤中高表达的受体。
奥曲肽受体靶向药物奥曲肽可以结合奥曲肽受体,抑制肿瘤细胞的增殖和释放,适用于胰腺神经内分泌肿瘤等。
3.CD20:CD20是B细胞表面的一种膜糖蛋白,也是一种B细胞淋巴瘤的标志物。
CD20靶向药物包括利妥昔单抗等,可以选择性地杀伤CD20阳性的B细胞,适用于非霍奇金淋巴瘤等。
4.血管内皮生长因子受体(VEGFR):VEGFR是一种与血管新生有关的受体酪氨酸激酶。
VEGFR靶向药物包括贝伐珠单抗、舒尼替尼等,可以抑制肿瘤细胞与血管内皮细胞的相互作用,阻断肿瘤的血供,适用于肾细胞癌、转移性结直肠癌等。
5.基因重排:一些肿瘤具有特定基因重排,这些基因重排产生了新的融合基因,参与肿瘤的发生和发展。
针对这些融合基因的靶向药物可以抑制这些基因的活性,如克唑替尼可以抑制ALK融合基因的活性,适用于ALK融合基因阳性的非小细胞肺癌。
6.细胞周期调节蛋白:肿瘤细胞的增殖过程离不开细胞周期调节蛋白的活性调节。
针对细胞周期调节蛋白的靶向药物可以干扰肿瘤细胞的细胞周期,如帕利珠单抗可以抑制CDK4/6蛋白的活性,适用于乳腺癌等。
7.PARP酶:PARP酶在DNA损伤修复过程中起重要作用。
针对PARP酶的靶向药物可以阻断DNA修复机制,导致肿瘤细胞死亡,适用于BRCA突变的卵巢癌等。


最热门抗肿瘤靶点及小分子靶向药物全景报告抗肿瘤靶点是指对肿瘤生长、转移等过程具有重要调控作用的蛋白分子或通路。
小分子靶向药物是一类能够专一靶向抗肿瘤靶点并抑制其活性的化学物质。
随着抗肿瘤研究的不断深入,越来越多的抗肿瘤靶点及小分子靶向药物被发现并应用于临床。
以下将介绍一些当前最热门的抗肿瘤靶点及小分子靶向药物:1.EGFR(表皮生长因子受体):EGFR是一种跨膜酪氨酸激酶受体,参与肿瘤细胞的生长和分化等过程。
一些小分子靶向药物如吉非替尼和厄洛替尼等通过抑制EGFR的酪氨酸激酶活性,抑制肿瘤细胞生长。
2.HER2(人表皮生长因子受体2):HER2是一种细胞表面受体,参与调节细胞增殖和存活等过程。
一些小分子靶向药物如曲妥珠单抗和拉普替尼等能够靶向结合HER2,抑制其信号传导,减少肿瘤细胞的增殖。
3.ALK(酪氨酸激酶受体):ALK是一种重排基因,其突变被发现与多种肿瘤的发生和发展相关。
小分子靶向药物如克唑替尼和艾尔莎替尼能够抑制ALK的活性,阻断肿瘤细胞的生长和转移。
4.BRAF(B型RAF激酶):BRAF是一种信号转导分子,突变导致了多种恶性黑色素瘤的发生。
例如,维米非尼和达替尼等小分子靶向药物能够抑制BRAF的活性,减少肿瘤细胞的增殖和转移。
5.PD-1(程序性死亡受体1)和PD-L1(程序性死亡配体1):PD-1和PD-L1参与抑制免疫系统对肿瘤的攻击,突变导致肿瘤逃避免疫监视。
一些免疫检查点抑制剂如伊普替尼和纳武利尼等能够靶向PD-1或PD-L1,恢复免疫系统的抗肿瘤活性。
除了上述靶点外,还有许多其他热门的抗肿瘤靶点及小分子靶向药物,如PI3K、FLT3、VEGFR等。
这些靶点及药物的发现和应用为肿瘤治疗提供了新的进展和希望。
需要注意的是,虽然靶向药物在抗肿瘤治疗中具有重要作用,但并非适用于所有患者。
个体化治疗是当前的研究热点,通过检测患者的肿瘤基因和蛋白表达水平来选择最合适的靶向药物,以提高治疗效果和减少不良反应。
依伏卡塞作用靶点-概述说明以及解释1.引言1.1 概述概述部分应该对主题进行简要介绍,说明为什么研究依伏卡塞的作用靶点是重要的。
以下是可能的一些内容:概述:依伏卡塞(Ivacaftor)是一种被广泛应用于囊性纤维化(Cystic Fibrosis,CF)患者治疗的药物。
这种罕见的遗传性疾病主要影响到患者的呼吸系统、消化系统和生殖系统。
依伏卡塞是一种新型的治疗CF的药物,其作用机制与传统疗法不同,其在改善患者症状和延缓病情进展方面取得了显著的成果。
然而,要更好地理解依伏卡塞的作用方式,我们需要深入了解其作用的靶点。
正确认识依伏卡塞的作用靶点对于更好地使用这种药物来治疗CF患者至关重要。
因为依伏卡塞的作用靶点与CF的发病机制密切相关,了解这些靶点可以帮助我们更好地了解该疾病的病理生理学。
随着对依伏卡塞机制的深入研究,我们能够更好地发现新的治疗方法,并且开发更有效的药物来改善患者的生活质量。
在本文中,我们将对依伏卡塞的作用机制进行详细探讨,并针对依伏卡塞的作用靶点展开讨论。
我们将介绍已有的研究成果,并探索目前对该领域的研究进行展望。
通过对依伏卡塞作用靶点的深入了解,我们可以为未来的疾病研究和新药开发提供有力的依据。
文章结构:本文将按照以下结构进行展开:首先,我们将简要介绍依伏卡塞的作用机制,重点描述其在调节离子通道功能方面的作用。
接下来,我们将重点关注依伏卡塞的作用靶点,包括离子通道和蛋白质通道等方面。
通过对这些靶点的介绍,我们可以更全面地了解依伏卡塞对CF病情的影响。
最后,我们将总结已有的研究成果,并展望未来的研究方向,以期为进一步开发治疗CF的药物提供新的思路和方向。
目的:本文的目的在于深入探讨依伏卡塞的作用靶点,以提升对其作用机制的理解。
通过对依伏卡塞作用靶点的介绍,我们可以为进一步研究和开发更有效的药物治疗手段提供科学依据。
同时,我们也希望能够引起更多研究者的关注,推动相关研究领域的进一步发展。
肿瘤的靶向治疗名词解释近年来,肿瘤的靶向治疗在肿瘤治疗领域中得到了广泛的关注和应用。
随着技术的不断进步和研究的深入,靶向治疗正在成为治疗肿瘤的重要手段之一。
本文将对肿瘤的靶向治疗相关的名词进行解释,以便读者更好地了解和理解这一领域。
1. 肿瘤靶点肿瘤靶点是指在肿瘤细胞或其周围环境中存在的分子、蛋白质或结构等,它们在肿瘤的发生发展过程中起到关键的作用。
肿瘤靶点的特点是在正常组织中表达量低或不表达,但在肿瘤细胞中大量表达。
通过针对这些靶点进行干预,可以达到治疗肿瘤的目的。
2. 靶向药物靶向药物是专为靶向肿瘤靶点而设计的药物。
与传统的化疗药物不同,靶向药物可以更精准地干预肿瘤细胞,减少对正常细胞的损伤。
靶向药物有多种类型,包括小分子靶向药物和单克隆抗体等。
小分子靶向药物是指分子量较小的化合物,可以通过口服或注射等途径给药;而单克隆抗体是由人工合成的抗体,可以通过静脉注射等途径给药。
3. 靶向治疗的机制靶向治疗的机制多种多样,常见的机制包括抑制信号传导、阻断血管供应和改变免疫应答等。
抑制信号传导是指通过干扰肿瘤细胞内的信号转导通路来阻止肿瘤细胞增殖和生存。
常见的靶向信号通路包括EGFR信号通路和VEGF信号通路等。
阻断血管供应是指通过抑制肿瘤细胞周围的血管生长和新生血管的形成来阻断肿瘤的营养供应。
改变免疫应答是指通过调节免疫系统的功能来增强对肿瘤细胞的攻击能力。
4. 靶向治疗的优势与传统的化疗相比,靶向治疗具有很多优势。
首先,靶向治疗可以更精确地干预肿瘤细胞,减少对正常细胞的损伤和副作用。
其次,靶向治疗可以提高治疗的效果和预后,因为它能够直接作用于肿瘤的关键环节,避免了肿瘤细胞对化疗药物产生的耐药性。
此外,靶向治疗还可以带来更好的生活质量,因为它少有毒副作用,患者可以更好地耐受治疗。
5. 靶向治疗的局限性虽然靶向治疗在肿瘤治疗中取得了很大的成功,但它也存在一些局限性。
首先,由于肿瘤的异质性和复杂性,靶向治疗并不适用于所有类型的肿瘤。
药物作用的靶点药物作用的靶点是指药物通过特定的分子靶点,影响或调节靶点的功能,从而产生治疗效果。
药物作用的靶点可以是酶、激素受体、离子通道或细胞表面受体等。
下面我们以几种常见的药物为例,介绍其作用的靶点。
首先是抗生素。
抗生素的作用机制主要是通过靶向细菌特定的靶点,干扰细菌的生命活动。
例如,青霉素类抗生素通过与细菌的细胞壁合成酶结合,阻断细胞壁的合成,导致细菌死亡。
氨基糖苷类抗生素则是通过结合细菌的核糖体,阻碍蛋白质的合成,从而达到杀菌的效果。
其次是抗癌药物。
抗癌药物的作用靶点多样,通常是指癌细胞中特定的分子或细胞结构。
比如,激酶抑制剂通过抑制肿瘤相关激酶的活性,阻断了一系列细胞信号途径的传导,抑制癌细胞的增殖和生存。
另外,抗癌药物还可以靶向癌细胞表面的受体,如HER2受体和EGFR受体,通过阻断其信号传导通路,减少癌细胞生长和扩散。
再者是心血管药物。
例如钙离子通道阻滞剂是一类常见的药物,它的作用靶点是心肌细胞中的钙离子通道。
通过阻塞钙离子通道,减少钙离子的内流,抑制心肌细胞的收缩力和抗心律失常的作用。
另一类常见的药物是ACE抑制剂,其作用靶点是血管紧张素转换酶(ACE)。
通过抑制ACE的活性,可以减少血管紧张素Ⅱ的生成,从而扩张血管、降低血压,起到抗高血压和保护心脏的作用。
最后是抗精神病药物。
抗精神病药物的作用靶点多样,常见的包括多巴胺受体和5-HT受体等。
多巴胺受体拮抗剂通过抑制多巴胺的作用,减少多巴胺神经递质的功能,从而改善精神病症状。
5-HT受体拮抗剂则是通过阻断5-HT神经递质的作用,调节5-HT通路的功能,对抗精神病症状。
总的来说,药物的作用靶点是药物发挥治疗效果的重要基础。
不同类型的药物有不同的作用靶点,通过作用于特定的靶点,调节分子或细胞的功能,从而产生特定的药理效应。
药物的研发和设计往往以靶点为基础,针对特定的靶点进行定向治疗,提高药物疗效,减少不良反应。
靶向药物和分子靶点的研究和设计随着生物技术的发展和进步,靶向药物和分子靶点的研究和设计在医学领域中变得越来越重要。
靶向药物是一种治疗特定疾病的药物,它们通过选择性地作用于分子靶点来发挥疗效,而不会对其他的分子造成影响。
这种药物疗效高、副作用小,常常被用于治疗癌症、心血管疾病以及许多其他慢性疾病。
本文将介绍一些靶向药物和分子靶点的研究和设计。
靶向药物针对的是病原体或者病理生理学分子/通路。
这些靶向药物可以通过多个不同的方式发挥作用,包括阻断信号传导通路、调节蛋白质功能、干扰细胞周期等等。
例如,EGFR靶向药物(埃洛替尼)针对的是表皮生长因子受体,它可以通过抑制受体的活性来阻断肿瘤细胞的生长和扩散。
还有蛋白酶体抑制剂(Bortezomib),它可以通过抑制细胞质插入蛋白在细胞中的降解,从而导致有贡献的蛋白质的降解和细胞凋亡。
分子靶点研究的主要目的是发现新的分子靶点,同时通过小分子药物来选择性地作用于这些靶点,从而达到治疗疾病的目的。
靶标分子来自各种生物分子中,如蛋白质、核酸和多肽等,可以进行结构和功能分析,以了解其在细胞中的作用和与其他分子之间的相互作用。
这个过程通常被称为分子建模,通过计算机模拟和分析,可以对候选分子进行预测,从而最终确定具有特定功能的药物。
现在,化学合成和生物分子工程技术仍在不断发展,靶向药物和分子靶点的研究和设计也不断更新,研究人员不断地寻找新的治疗疾病的方法。
在这个过程中,一些技术也变得越来越重要。
例如,基因组学技术和计算机模拟技术可以用于识别适用于治疗从头痛到癌症的不同分子靶点,特别是与癌症或其他疾病有关的分子靶点。
这些技术可以模拟一个细胞中的分子互动,以评估少量的分子作为潜在药物的适用性。
同时,一些方法也被用于快速筛选候选分子,例如高通量筛选(HTS)和计算机辅助药物设计(CADD)等。
最近,深度学习技术也正逐步在靶向药物和分子靶点的研究和设计中发挥重要作用。
深度学习技术已在各个领域得到广泛应用,如图像和语音识别等。