第十五章 质谱法(一)
- 格式:ppt
- 大小:1.86 MB
- 文档页数:28


第十五章质谱法 - 经典习题1.某未知物经测定为仅含C、H、O的有机化合物,其IR光谱显示在3100-3700cm-1之间无吸收,其质谱如图15-1,试推断其结构。
图15-1 未知物的质谱图解:(1)分子离子峰(m/z 136)较强,说明此分子离子结构稳定,可能具有苯环或共轭系统。
(2)查Beynon表136栏下,含C、H、O的只有下列四个分子式:a.C9H12O(U=4)b.C8H8O2(U=5)c.C7H4O3(U=6)d.C5H12O4(U=0)(3)m/z 105为基峰,提示可能为苯甲酰离子(C6H5CO+)峰(见教材附录十二),m/z 77、 m/z 51、m/z 39等芳烃特征峰的出现也进一步证实了苯环的存在。
(4)m/z 56.5、m/z 33.8两个亚稳离子峰的出现表明存在下列开裂过程:(5)根据上述解析推断,证明未知化合物含有苯甲酰基C6H5CO(U=5),这样即可排除分子式中的C9H12O(U=4)、C7H4O3(U=6,H原子不足)及C5H12O4(U=0),唯一可能的分子式为C8H8O2(U=5)。
(6)由分子式C8H8O2扣去苯甲酰基C6H5CO,剩余的碎片为CH3O,则可能的剩余结构为-CH2-OH或CH3O-。
(7)将苯甲酰基C6H5CO与剩余结构单元相连接,得到以下两种可能结构:由于该样品的IR光谱在3100~3700cm-1之间无吸收,提示结构中应无-OH,因此该化合物的结构为A。
(8)验证质谱中各峰的归属:验证结果说明所提出的结构式是合理的。
2.已知某未知物的分子式为C9H18O,IR光谱显示在~1715cm-1处有强吸收,在~2820cm-1、~2720cm-1处无吸收,其质谱如图15-2所示,试推断其结构。
图15-2 未知物C9H18O的质谱图解:(1)由分子式C9H18O求得化合物的不饱和度U=1,且含有一个O原子,可能为一个羰基,故未知物可能是羰基化合物。

2020年药学基础综合考研大纲(科目代码:717)Ⅰ.考试性质药学基础综合是我校为招收药学(全日制)研究生而设置的具有选拔性质的自命题考试科目,旨在科学、公平、有效地测试考生是否掌握相关学科的基础知识和基本技能,评价的标准是高等学校药学专业优秀本科毕业生能达到的及格或及格以上水平,确保硕士研究生的招生质量。
Ⅱ.考查目标药学基础综合考试范围为有机化学和分析化学。
要求考生系统掌握以上学科的基本理论、基本知识和基本技能,并且能够运用所学的基本理论、基本知识和基本技能综合分析、判断和解决有关理论问题和实际问题。
Ⅲ.考试形式和试卷结构一、试卷满分及考试时间本试卷满分为300分,考试时间为180分钟。
二、答题方式答题方式为闭卷、笔试。
三、试卷内容结构1.有机化学,占50%;2.分析化学,占50%。
四、试卷题型结构试题结构一般可包括以下内容,每套试题可有变化:1.选择题;2.命名题/填空;3.完成反应式;4.鉴别题;5.合成与反应机理题;6.判断题;7.问答题;8.论述题;9.计算题Ⅳ.考查内容一、有机化学第一章绪论1.1有机化合物和有机化学1.2有机化学与医学的关系1.3有机分子结构与共价键1.4有机反应类型及条件1.5有机化合物的分类与结构表示方法1.6研究有机化合物的一般步骤第二章链烃2.1链烃的结构2.2链烃的命名2.3链烃的物理性质2.4链烃的化学性质:烷烃的化学性质;烯烃的化学性质;炔烃的化学性质;共轭二烯烃的化学性质。
第三章环烃3.1脂环烃:脂环烃的分类和命名;脂环烃的结构与稳定性;脂环烃的构象;脂环烃的物理性质;脂环烃的化学性质。
3.2芳香烃:芳香烃的分类和命名;苯的结构;苯及其同系物的物理性质;苯的亲电取代反应及其反应机理;苯环上的亲电取代反应的定位效应;烷基苯侧链的反应;稠环芳香烃;非苯型芳香烃和休克尔规则;致癌稠环芳烃。
第四章立体化学4.1基本概念4.2含有一个手性碳原子的立体异构体4.3含有两个手性碳原子的立体异构体4.4无手性碳原子的立体异构体4.5有机化学反应中的立体选择性4.6立体异构体与生物活性的关系第五章卤代烃5.1卤代烃的分类和命名5.2卤代烃的物理性质5.3卤代烃的化学性质:卤代烷烃的亲核取代反应及其机理;卤代烷烃的消除反应及其机理;卤代烷烃消除反应与取代反应的竞争性;卤代烯烃的亲核取代反应;卤代芳烃的亲核取代反应;Grignard试剂的制备。


第十五章思考题1.色谱法具有同时能进行分离和分析的特点而区别于其它方法,特别对复杂样品和多组份混合物的分离,色谱法的优势更为明显。
2.按固定相外形不同色谱法是如何分类的?是按色谱柱分类:①平面色谱法:薄层色谱法、纸色谱法②柱色谱法:填充柱法、毛细管柱色谱法3.什么是气相色谱法和液相色谱法?气体为流动相的色谱称为气相色谱。
液体为流动相的色谱称为液相色谱。
4.保留时间(tr)、死时间(t0)及调整保留时间(t’r)的关系是怎样的?t’r = tr - t05.从色谱流出曲线可以得到哪些信息?①根据色谱峰的个数可以判断样品中所含组分的最少个数;②根据色谱峰的保留值可以进行定性分析;③根据色谱峰的面积或峰高可以进行定量分析;④色谱峰的保留值及其区域宽度是评价色谱柱分离效能的依据;⑤色谱峰两峰间的距离是评价固定相(或流动相)选择是否合适的依据。
6.分配系数在色谱分析中的意义是什么?①K值大的组分,在柱内移动的速度慢,滞留在固定相中的时间长,后流出柱子;②分配系数是色谱分离的依据;③柱温是影响分配系数的一个重要参数。
7.什么是选择因子?它表征的意义是什么?是A,B两组分的调整保留时间的比值α= t’r(B)/t’r(A)>1意义:表示两组分在给定柱子上的选择性,值越大说明柱子的选择性越好。
8.什么是分配比(即容量因子)?它表征的意义是什么?是指在一定温度和压力下,组分在两相分配达到平衡时,分配在固定相和流动相的质量比。
K=ms/mm意义:是衡量色谱柱对被分离组分保留能力的重要参数;9. 理论塔板数是衡量柱效的指标,色谱柱的柱效随理论塔板数的增加而增加,随板高的增大而减小。
10.板高(理论塔板高度H/cm)、柱效(理论塔板数n)及柱长(L/cm)三者的关系(公式)?H=L / n11.利用色谱图如何计算理论塔板数和有效理论塔板数(公式)?12.同一色谱柱对不同物质的柱效能是否一样?同一色谱柱对不同物质的柱效能是不一样的13.塔板理论对色谱理论的主要贡献是怎样的?(1)塔板理论推导出的计算柱效率的公式用来评价色谱柱是成功的;(2)塔板理论指出理论塔板高度H 对色谱峰区域宽度的影响有重要意义。



质谱基本原理质谱(Mass Spectrometry,MS)是一种用于分析化合物分子结构和确定化合物分子量的重要分析技术。
它通过将化合物分子转化为离子,然后根据离子的质量和电荷比进行分析,从而得到化合物的质谱图谱。
质谱技术在化学、生物、药学等领域具有广泛的应用,是一种非常重要的分析手段。
质谱的基本原理可以简单地概括为离子化、分离、检测和数据处理四个步骤。
首先,样品中的化合物分子被转化为离子,这一过程通常通过电离源完成。
常用的电离源包括电子轰击电离源、化学电离源和电喷雾电离源等。
不同的电离源适用于不同类型的化合物,选择合适的电离源对于获得准确的质谱数据至关重要。
接下来,离子经过质谱仪中的分析部分,根据其质荷比(m/z)进行分离。
质谱仪通常包括离子源、质量分析器和检测器。
质量分析器的种类有多种,包括飞行时间质谱仪、四级杆质谱仪和离子阱质谱仪等。
这些质谱仪能够根据离子的质荷比进行高效分离,从而得到高质量的质谱数据。
在检测部分,分离后的离子被检测器检测到,并转化为电信号。
这些信号随后被转化为质谱图谱,显示出离子的质荷比和相对丰度。
通过分析质谱图谱,可以得到化合物的分子量、结构信息以及相对丰度等重要数据。
最后,得到的质谱数据需要进行处理和解释。
数据处理包括质谱图谱的峰识别、质谱数据的校正和质谱图谱的解释等步骤。
这些步骤需要借助专业的质谱数据处理软件进行,以确保得到准确可靠的结果。
总的来说,质谱的基本原理是将化合物分子转化为离子,然后根据离子的质量和电荷比进行分析,最终得到化合物的质谱数据。
质谱技术在化学、生物、药学等领域具有广泛的应用,对于研究化合物的结构和性质具有重要意义。
随着质谱技术的不断发展,相信它将在更多领域展现出强大的应用潜力。

第十五章质谱法 - 经典习题1.某未知物经测定为仅含C、H、O的有机化合物,其IR光谱显示在3100-3700cm-1之间无吸收,其质谱如图15-1,试推断其结构。
图15-1 未知物的质谱图解:(1)分子离子峰(m/z 136)较强,说明此分子离子结构稳定,可能具有苯环或共轭系统。
(2)查Beynon表136栏下,含C、H、O的只有下列四个分子式:a.C9H12O(U=4)b.C8H8O2(U=5)c.C7H4O3(U=6)d.C5H12O4(U=0)(3)m/z 105为基峰,提示可能为苯甲酰离子(C6H5CO+)峰(见教材附录十二),m/z 77、 m/z 51、m/z 39等芳烃特征峰的出现也进一步证实了苯环的存在。
(4)m/z 56.5、m/z 33.8两个亚稳离子峰的出现表明存在下列开裂过程:(5)根据上述解析推断,证明未知化合物含有苯甲酰基C6H5CO(U=5),这样即可排除分子式中的C9H12O(U=4)、C7H4O3(U=6,H原子不足)及C5H12O4(U=0),唯一可能的分子式为C8H8O2(U=5)。
(6)由分子式C8H8O2扣去苯甲酰基C6H5CO,剩余的碎片为CH3O,则可能的剩余结构为-CH2-OH或CH3O-。
(7)将苯甲酰基C6H5CO与剩余结构单元相连接,得到以下两种可能结构:由于该样品的IR光谱在3100~3700cm-1之间无吸收,提示结构中应无-OH,因此该化合物的结构为A。
(8)验证质谱中各峰的归属:验证结果说明所提出的结构式是合理的。
2.已知某未知物的分子式为C9H18O,IR光谱显示在~1715cm-1处有强吸收,在~2820cm-1、~2720cm-1处无吸收,其质谱如图15-2所示,试推断其结构。
图15-2 未知物C9H18O的质谱图解:(1)由分子式C9H18O求得化合物的不饱和度U=1,且含有一个O原子,可能为一个羰基,故未知物可能是羰基化合物。

2019华中科技大学硕士研究生入学考试《药学综合(一)》考试大纲(科目代码:755)一、考试性质药学综合是报考我校药学专业硕士研究生的一门综合基础课程,由有机化学、分析化学和药理学三门课程组成。
旨在考察学生对药学基础课程基本概念、理论以及各方面知识的掌握程度,为进一步学习药学相关课程打下基础。
二、考试形式与试卷结构1、答卷方式:闭卷、笔试2、答题时间:180分钟3、题型比例:单选题50%简答题30%论述题20%三、考查要点有机化学部分本课程理论部分着重介绍有机化学的基本结构理论、各类化合物的结构、命名、性质和合成等方面的知识,强调学生灵活运用有机基本理论来解释、分析实验现象、结果的能力。
通过本课程的学习,要求学生:(1)掌握各类有机化合物的命名法、有机化合物的异构现象(碳链、位置及官能团异构、构象、顺反及对映异构);(2)应用价键理论和共振论的基本概念,理解典型有机化合物的基本结构;(3)掌握立体化学的基本知识和基本理论;(4)能运用电子效应(诱导与共轭)理论,理解结构与性质的关系,解释某些有机反应的问题;(5)初步掌握碳正离子、碳负离子、碳游离基、碳烯等活性中间体及其在有机反应中的作用;(6)掌握重要亲核取代、亲电取代、亲电加成、亲核加成和游离基反应的历程,并能初步运用以解释相应的化学反应。
(7)掌握各类有机化合物的基本性质与重要有机化学反应:取代、加成、消除、氧化、酯化、酰化、脱羧、偶联等反应,以及它们在有机合成上的初步运用。
第一章绪论1、有机化合物的分类和构造式的表达;2、有机酸碱的概念。
重点内容:有机酸碱理论。
第二章烷烃和环烷烃1、烷烃和环烷烃的分类、命名、构造异构;2、烷烃的结构与构象分析;3、烷烃的化学反应:氧化、热裂解和卤代反应;卤代反应机理、反应进程与能量关系、过渡态理论对理解有机反应机理的促进;4、环烷烃的结构与化学性质:活泼性(开环及开环方向)与环大小的关系;5、环己烷及取代环己烷的构象(船式和椅式、a键和e键)。
第十五章 质 谱 法思考题与习题1.简述质谱仪的组成部分及其作用,并说明质谱仪主要性能指标的意义。
质谱仪,其基本组成是相同的。
都包括进样系统、离子源、质量分析器、检测器和真空系统。
进样系统:把被分析的物质,即样品送进离子源。
离子源:将欲分析样品电离,得到带有样品信息的离子。
质量分析器:将离子源产生的离子按m/z 顺序别离开来。
检测器:用以测量、记录离子流强度而得出质增图。
真空系统:保证离子源中灯丝的正常工作,保证离子在离子源和分析器正常运行,消减不必要的离子碰撞,散射效应,复合反应和离子-分子反应,减小本底与记忆效应,衡量一台质谱仪性能好坏的指标包括灵敏度,分辨率,质量范围,质量稳定性等。
灵敏度表示在一定的样品〔如八氟萘或六氯苯〕,在一定的分辨率下,产生一定信噪比的分子离子峰所需的样品量。
质谱仪的分辨率表示质谱仪把相邻两个质量分开的能力 质量范围是质谱仪所能测定的离子质荷比的范围。
质量稳定性主要是指仪器在工作时质量稳定的情况, 质量精度是指质量测定的精确程度。
2.在质谱图中,离子的稳定性与其相对丰度有何关系?由于键断裂的位置不同,同一分子离子可产生不同质荷比的碎片离子,而其相对丰度与键断裂的难易以及化合物的结构密切相关,离子的稳定性越高,其相对丰度越大。
因此,碎片离子的峰位(m/z)及相对丰度可提供化合物的结构信息。
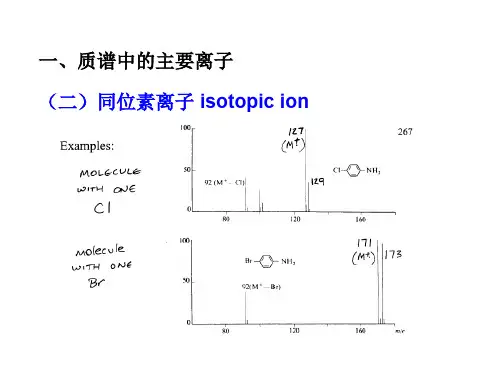
3、指出含有一个碳原子和一个氯原子的化合物,可能的同位素组合有哪几种?它们将提供哪些分子离子峰?可能的同位素组合有C 12Cl 35、C 13Cl 35、C 12Cl 37、C 13Cl 37;提供的分子离子峰为M 、M +1、M +2、M +3。
4.某化合物的分子离子峰的m/z 值为201,由此可得出什么结论?由于多数分子易失去一个电子而带一个电荷,分子离子的质荷比是质量数被1除,即m/1。
因此,分子离子峰的质荷比值就是它的分子量。
该化合物的分子离子峰的m/z 值为201,由此可得出其分子量为201。
第十二章原子吸收分光光度法一、填空题1、外层电子;第一激发态;共振吸收线;共振线;2、32S1/2;32P1/2,32P3/2;3、光源、原子化器、单色器和检测系统;4、共振线;5、电离干扰、物理干扰、光学干扰和化学干扰。
6、主量子数n、角量子数l、自旋量子数n、内量子数j。
7、频率、半宽度、强度。
二、选择题AAB AAB三、简答题1、主要有Doppler线宽、Lorentz线宽、Holtsmark线宽和自然宽度。
在通常的原子吸收分光光度法条件下,吸收线线宽主要由Doppler变宽和Lorentz变宽控制,当局外元素浓度很小时,吸收线线宽主要由Doppler变宽控制。
2、特点:灵敏度高。
选择性好。
精密度高。
测量范围广。
局限性:标准曲线的线性范围窄。
测一种元素要使用一种元素灯,使用不方便。
3、(1)锐线光源、(2)发射线最大发射波长和吸收线的最大吸收波长必须重叠。
第十三章红外分光光度法第十四章核磁共振波谱法一、填空题1、ν照 = ν进△m=+ 12、一级;高级;△ν/J > 103、化学位移,偶合常数4、局部抗磁屏蔽;磁各相异性5、自旋-自旋偶合;偶合常数6、27、38、无线电波、核自旋能级分裂、1/29、7.1710、中心位置,峰裂距11、屏蔽效应,各向异性效应,氢键12、213、氢分布; 质子类型; 核间关系二、选择题ACCDD DBACB CD三、简答题1、所谓磁全同质子是指这些质子化学位移、与组外任何一核的偶合强弱相同,它们在核磁共振谱上不产生分裂 ,例如:2、烯烃处于C=C 双链的负屏蔽区,δ增大。
炔烃处于C ≡C 地正屏蔽区,δ减小3、(1) 12个氢处于完全相同的化学环境,只产生一个尖峰;(2)屏蔽强烈,共振频率最小,吸收峰在磁场强度高场,与有机化合物中的质子峰不重迭;(3)化学惰性;易溶于有机溶剂;沸点低,易回收。
四、解谱题1、 CH3COCH2COOCH2CH32、3、C 6H 5-C(CH 3)=CH-COOH4、 偶合系统为: AMX3系统 可能结构为:CH3–CHCH-COOH5、 CH H 3CCH 36、CH 3CH 2I7、 C C C H H H H H H O (1)(2)(3)(4)(5)(6)C O HH 3C O第十五章质谱一、填空题1、奇数、偶数;2、偶数;3、奇数;偶数;4、分子离子、碎片离子、重排离子、同位素离子、亚稳离子;5、峰弱、峰钝、质核比一般不是整数;6、峰强比;Cl、Br、S;7、均裂、异裂、半均裂;8、M+2、M+4、M+6;M:(M+2):(M+4):(M+6)≈27:27:9:1;二、简答题略;三、选择题ABDAC ACB四、解析题1、为3,3-二甲基-丁醇-22、解:m/z 69相当于M-29(C2H5质量),m/z 69是奇数,故m/z 98->m/z 69 是单纯开裂;m/z(偶数)相当于M-28(C2H4质量),系由McLafferty重排产生。
分析化学教材(系列一)目 录第一章 绪论第二章 误差和分析数据处理 第三章 滴定分析法概论 第四章 酸碱滴定法 第五章 配位滴定法 第六章 氧化还原滴定法 第七章 沉淀滴定法和重量分析法 第八章 电位法和永停滴定法 第九章 光谱分析法概论 第十章 紫外可见分光光度法 第十一章 荧光分析法 第十二章 红外吸收光谱法 第十三章 原子吸收分光光度法第十四章核磁共振波谱法第十五章 质谱法 第十六章 色谱分析法概论 第十七章 气相色谱法 第十八章 高效液相色谱法 第十九章 平面色谱法 第二十章 毛细管电泳法 第二十一章 色谱联用分析法 附录一 元素的相对原子质量(2005) 附录二 常用化合物的相对分子质量 附录三 中华人民共和国法定计量单位 附录四 国际制(SI )单位与cgs 单位换算及常用物理化学常数附录五常用酸、碱在水中的离解常数(25℃)附录六配位滴定有关常数附录七常用电极电位附录八难溶化合物的溶度积常数(25℃,I=0)附录九标准缓冲溶液的pH(0—95℃)附录十主要基团的红外特征吸收峰附录十一质子化学位移表附录十二质谱中常见的中性碎片与碎片离子附录十三气相色谱法用表参考文献英文索引中文索引目录第三版前言第二版前言第一版前言第1章绪论第2章误差和分析数据处理第3章重量分析法第4章滴定分析法概论第5章酸碱滴定法第6章络合滴定法第7章沉淀滴定法第8章氧化还原滴定法第9章取样与样品预处理方法附录附录Ⅰ中华人民共和国法定计量单位附录Ⅱ分析化学中常用的物理化学常数及物理量附录Ⅲ国际相对原子质量表附录Ⅳ常用相对分子质量表附录Ⅴ酸、碱在水中的离解常数附录Ⅵ常用标准缓冲溶液的pH(0~60℃)附录Ⅶ络合滴定有关常数附录Ⅷ标准电极电位及条件电位表附录Ⅸ难溶化合物的溶度积(Ksp) 符号表第1章概论1.1 定量分析概述1.1.1 分析化学的任务和作用1.1.2 定量分析过程1.1.3 定量分析方法1.2 滴定分析法概述1.2.1 滴定分析法对反应的要求和滴定方式1.2.2 基准物质和标准溶液1.2.3 滴定分析中的体积测量1.2.4 滴定分析的计算思考题习题第2章误差与分析数据处理2.1 有关误差的一些基本概念2.1.1 误差的表征——准确度与精密度2.1.2 误差的表示——误差与偏差2.1.3 误差的分类——系统误差与随机误差2.2 随机误差的分布2.2.1 频率分布2.2.2 正态分布2.2.3 随机误差的区间概率2.3 有限数据的统计处理2.3.1 数据的集中趋势和分散程度的表示——对μ和σ2.3.2 总体均值的置信区间——对μ的区别间估计2.3.3 显著性检验2.3.4 异常值的检验2.4 测定方法的选择与测定准确度的提高2.5 有效数字思考题习题第3章酸碱平衡与酸碱滴定法3.1 酸碱反应3.1.2 酸碱反应的平衡常数3.1.3 活度与浓度,平衡常数的几种形式3.2 酸度对弱酸(碱)形态分布的影响3.2.1 一元弱酸溶液中各种形态的分布3.2.2 多元酸溶液中各种形态的分布3.2.3 浓度对数图3.3 酸碱溶液的H+浓度计算3.3.1 水溶液中酸碱平衡处理的方法3.3.2 一元弱酸(碱)溶液pH的计算3.3.3 两性物质溶液pH的计算3.3.4 多元弱酸溶液pH的计算3.3.5 一元弱酸及其共轭碱(HA+A)混合溶液pH的计算3.3.6 强酸(碱)溶液pH的计算3.3.7 混合酸和混合碱溶液pH的计算3.4 酸碱缓冲溶液3.4.1 缓冲容量和缓冲范围3.4.2 缓冲溶液的选择3.4.3 标准缓冲溶液3.5 酸碱指示剂3.5.1 酸碱指示剂的作用原理3.5.2 影响指示剂变色间隔的因素3.5.3 混合指示剂3.6 酸碱滴定曲线和指示剂的选择3.6.1 强碱滴定强酸或强酸滴定强碱3.6.2 一元弱酸(碱)的滴定3.6.3 滴定一元弱(弱碱)及其与强酸(强碱)混合物的总结3.6.4 多元酸和多元碱的滴定3.7 终点误差3.7.1 代数法计算终点误差图及其应用3.7.2 终点误差公式和终点误差图及其应用3.8 酸碱滴定法的应用3.8.1 酸碱标准溶液的配制与标定……第4章络合滴定法第5章氧化还原滴定法第6章沉淀重量与沉淀滴定法第7章分光光度法第8章分析化学中常用的分离方法第9章其他常用仪器分析方法附录目录编写说明第1章绪论第1节分析化学的任务与作用第2节分析化学方法的分类第3节试样分析的基本程序第4节分析化学的发展与趋势第2章误差和分析数据的处理第1节误差第2节测量值的准确度和精密度第3节有效数字及其运算法则第4节分析数据的统计处理与分析结果的表示方法第5节相关与回归思考与练习第3章重量分析法第1节挥发法第2节萃取法第3节沉淀法思考与练习第4章滴定分析法概论第1节滴定反应类型与滴定方式第2节基准物质与标准溶液第3节滴定分析的计算思考与练习第5章酸碱滴定法第1节水溶液中的酸碱平衡第2节基本原理第3节滴定终点误差第4节应用与示例第5节非水滴定法思考与练习第6章沉淀滴定法第1节基本原理第2节应用与示例思考与练习第7章配位滴定法第1节配位平衡第2节基本原理第3节滴定条件的选择第4节应用与示例思考与练习第8章氧化还原滴定法第9章电位法和永停滴定法参考资料附录目录符号缩写或简称第一篇概述第1章分析化学的目的及其对社会的重要性1.1 分析化学的目的:对社会的基本重要性1.2 分析化学的目的:作为问题解决者的分析化学家1.3 非常规实验实应用分析化学的目的参考文献第2章分析过程2.1 概述2.2 全分析过程2.3 工作特性2.4 分析化学中的误差参考文献第3章质量保证和质量控制3.1 分析化学的质量和目标3.2 分析方法3.3 如何保证准确度3.4 质是保证和质是控制受规章限制的方面3.5 结论参考文献第二篇化学分析第4章化学分析的基本原理第5章色谱法第6章动力学与催化第7章化学分析的方法及其应用第三篇物理分析第8章元素分析第9章化合物和分子特效分析第10章微束流和表面分析第11章结构分析第四篇基于计算机的分析化学(COBAC)第12章化学计理学第13章计算机软硬件及分析仪器接口第五篇全分析系统第14章联用技术第15章微分析系统第16章过程分析化学VI. 附录汉英索引英汉索引目录总序出版说明第二版前言第一版前言符号表绪论0.1 分析化学的任务与作用0.2 分析方法的分类0.3 发展中的分析化学1 分析质量保证1.1 分析化学中关于误差的一些基本概念 1.2 有效数字及其运算规则1.3 分析数据的统计处理1.4 提高分析结果准确度的方法小结习题分析化学前沿领域简介——化学计量学2 化学分析法2.1 滴定分析概述2.2 滴定分析的基本理论2.3 确定滴定终点的方法2.4 滴定条件选择2.5 滴定分析的应用2.6 重理分析法小结习题化学大师Liebig3 分离分析方法3.1 分析试样的制备和分解3.2 沉淀分离法3.3 溶齐萃取分离法3.4 离子交换分离法3.5 挥发和蒸馏分离法3.6 气相色谱法3.7 高效液相色谱法3.8 色谱分离技术发展简介3.9 膜分离法3.10 激光分离法3.11 复杂试样分析实例3.12 分离技术的发展趋势小结习题科学家及其思维方法简介——色谱学家马丁4 原子光谱分析法4.1 原子吸收分光光度法4.2 原子发射光谱分析法小结习题著名化学家本生对分析化学的贡献5 分子光谱分析法5.1 紫外-可见分光光度法5.2 红外光谱法5.3 分子发光分析法小结习题光分析化学前沿简介——光化学传感器6 核磁共振谱法6.1 基本原理6.2 核磁共振谱仪6.3 化学位移6.4 自旋偶合与自旋裂分6.5 核磁共振谱图解析6.6 13C核磁共振谱小结习题生物分子的革命性分析方法7 质谱法7.1 基本原理7.2 质谱仪7.3 离子的主要类型7.4 有机化合物质谱7.5 质谱图解析7.6 飞行时间质谱简介7.7 UV、IR、NMR和MS四谱综合解析小结习题科学展望——2000年诺贝尔化学奖简介8 电化学分析法8.1 电位分析法8.2 极谱法和伏安法8.3 库仑分析法8.4 电分析化学新进展小结习题2003年诺贝尔化学奖得主阿格雷和麦金农参考文献附录后记目录第1篇分析化学基础第1章分析化学导言1.1 分析化学的定义、任务和作用1.2 分析化学的特点和分类1.3 分析化学的发展趋势1.4 学习分析化学课程的方法思考题第2章试样的采集、制备与分解2.1 试样的采集2.2 固体物料试样的制备2.3 试样的分解思考题第3章定量分析中的误差及数据处理3.1 误差的基本概念3.2 误差的传递3.3 有效数字的表示与运算规则3.4 随机误差的正态分布3.5 少量数据的统计处理3.6 数据的评价——显著性检验、异常值的取舍3.7 回归分析3.8 提高分析结果准确度的方法思考题习题第2篇化学分析法第4章化学分析法概述4.1 化学分析法概述4.2 滴定分析法概述4.3 标准溶液与基准物4.4 化学分析法的计算思考题习题第5章酸碱滴定法第6章配位滴定法第7章氧化还原滴定法第8章沉淀滴定法第9章重量分析法第3篇仪器分析法第10章仪器分析法概述第11章紫外可见吸收光谱法第12章原子吸收光谱法第13章电位分析法第14章气相色谱法第4篇复杂物质分析第15章定量分析中的分离及富集方法第16章复杂物质分析示例附录参考文献目录第1章绪论第1节分析化学的任务和作用第2节分析化学的分类一、化学分析与仪器分析二、定性分析、定量分析和结构分析三、无机分析和有机分析四、常量分析、半微量分析和微量分析五、例行分析和仲裁分析第3节试样分析的基本程序一、取样二、分析试液的制备三、分析测定四、分析结果的计算与评价第4节分析化学的发展与趋势第2章误差和分析数据的处理第1节概述第2节定量分析误差一、系统误差和偶然误差二、绝对误差和相对误差三、准确度与精密度四、提高分析准确度的方法第3节有效数字及其运算法则一、有效数字二、有效数字的运算法则三、有效数字的运算法则在分析化学中的应用第4节分析数据的统计处理与分析结果的表示方法一、偶然误差的正态分布二、实验数据的统计处理三、可疑值的取舍四、分析数据处理与报告第3章重量分析法第1节概述第2节挥发法一、定义二、操作过程三、应用第3节萃取法一、定义及分类二、操作过程三、应用第4节沉淀法一、沉淀重量法二、沉淀的溶解度及影响因素三、沉淀的纯度及其影响因素四、沉淀的类型与沉淀条件五、沉淀法中的计算第5节应用一、药物含量测定二、药物纯度检查第4章滴定分析法概论第1节概述第2节滴定方式一、直接滴定法二、反滴定法三、置换滴定法四、间接滴定法第3节基准物质和标准溶液一、基准物质二、标准溶液三、标准溶液浓度的表示第4节滴定分析中的计算一、计算依据二、计算示例第5章酸碱滴定法第1节概述第2节水溶液中的酸碱平衡一、酸碱质子理论二、溶液中酸碱组分的分布三、酸碱溶液中H+浓度的计算第3节酸碱指示剂一、酸碱指示剂的变色原理二、酸碱指示剂的理论变色点和变色范围三、影响指示剂变色范围的因素四、混合指示剂第4节酸碱滴定法的基本原理……第6章沉淀滴定法第7章配位滴定法第8章氧化还原滴定法第9章电位分析法第10章紫外-可见分光光度法第11章荧光分析法第12章红外分光光度法第13章原子吸收分光光度法第14章经典液相色谱法第15章气相色谱法第16章高效液相色谱法第17章其他分析方法实验部分参考文献附录《分析化学》教学基本要求目录第一章绪论第一节分析化学的任务和作用第二节分析方法的分类一、定性分析、定量分析和结构分析二、无机分析和有机分析三、常量、半微量、微量、超微量分析四、化学分析和仪器分析五、例行分析、仲裁分析和快速分析第三节分析化学的发展趋势一、分析理论与其他学科相互渗透二、分析技术的发展趋势本章小结思考题与习题第二章定量分析误差和分析数据的处理第一节定量分析误差的种类和来源一、系统误差二、随机误差第二节准确度与精密度一、准确度与误差二、精密度与偏差三、准确度与精密度的关系第三节随机误差的正态分布一、频率分布二、正态分布三、随机误差的区间概率第四节有限测定数据的统计处理一、置信度与μ的置信区间二、可疑测定值的取舍三、显著性检验第五节提高分析结果准确度的方法一、选择适当的分析方法二、减小测量的相对误差三、检验和消除系统误差四、减小随机误差第六节有效数字及其运算规则一、有效数字的意义和位数二、数字修约规则三、有效数字的运算规则本章小结思考题与习题第三章滴定分析法概论第一节滴定分析法的分类及滴定方式一、滴定分析法的分类二、滴定分析法对化学反应的要求三、滴定方式第二节滴定分析的标准溶液一、标准溶液浓度的表示方法二、化学试剂的规格与基准物质三、标准溶液的配制第三节滴定分析的有关计算一、滴定分析计算的理论依据二、滴定分析计算示例本章小结思考题与习题第四章酸碱滴定法第一节酸碱反应及其平衡常数一、酸碱反应及其实质二、酸碱反应的平衡常数以及共轭酸碱对Ka与Kb的关系第二节酸碱溶液中各型体的分布系数与分布曲线一、一元弱酸(碱)溶液中各型体的分布系数与分布曲线二、多元酸(碱)溶液中各型体的分布系数与分布曲线第三节酸碱溶液pH的计算一、质子等衡式(质子条件式)二、酸碱溶液pH的计算第四节酸碱指示剂一、酸碱指示剂的作用原理二、影响酸碱指示剂变色范围的因素三、混合酸碱指示剂第五节酸碱滴定原理及指示剂选择一、强碱与强酸的滴定二、强碱(酸)滴定一元弱酸(碱)三、多元酸(碱)的滴定四、酸碱滴定中CO2的影响第六节酸碱滴定法的应用一、酸(碱)标准溶液的配制及标定二、酸碱滴定法应用实例本章小结思考题与习题第五章配位滴定法第一节概述第二节 EDTA及其配合物一、乙二胺四乙酸(EDTA)的结构与性质二、EDTA在水溶液中各存在型体的分布系数三、EDTA与金属离子形成螯合物的特点第三节 EDTA与金属离子的配位平衡一、配合物的稳定常数二、溶液中各级配合物浓度的计算第四节影响配位平衡的主要因素一、酸效应及酸效应系数二、配位效应及配位效应系数三、配合物的条件稳定常数第五节配位滴定原理一、配位滴定曲线二、影响配位滴定突跃范围的主要因素三、准确滴定金属离子的判据四、配位滴定中适宜pH范围第六节金属指示剂一、金属指示剂的作用原理二、金属指示剂应具备的条件三、金属指示剂的选择四、金属指示剂的封闭、僵化和氧化变质现象五、常用的金属指示剂第七节提高配位滴定选择性的方法一、控制溶液酸度二、利用掩蔽和解蔽作用三、采用其他配位剂四、分离干扰离子第八节配位滴定法的应用一、EDTA标准溶液的配制、标定二、各种配位滴定方式三、配位滴定法应用实例本章小结思考题与习题第六章氧化还原滴定法第一节氧化还原反应的特点一、标准电极电势和条件电极电势二、氧化还原反应进行的方向三、氧化还原反应进行的程度四、氧化还原反应速率第二节氧化还原滴定原理一、氧化还原滴定曲线二、化学计量点时溶液电势的计算三、影响氧化还原滴定突跃范围的因素第三节氧化还原滴定的指示剂一、自身指示剂二、特殊指示剂三、氧化还原指示剂第四节常见氧化还原滴定法及其应用一、高锰酸钾法二、重铬酸钾法三、碘量法本章小结思考题与习题第七章沉淀滴定法第一节沉淀滴定法基本原理第二节银量法一、莫尔法二、佛尔哈德法三、法扬司法第三节沉淀滴定法的应用一、标准溶液的配制与标定二、应用示例本章小结思考题与习题第八章分析化学中的常用分离方法第一节沉淀分离法一、无机沉淀剂分离二、有机沉淀剂分离三、共沉淀分离第二节液?液萃取分离法一、萃取分离法的基本原理二、萃取体系的分类和萃取条件的选择三、萃取分离技术四、溶剂萃取在分析化学中的应用第三节离子交换分离法一、离子交换剂的种类和性质二、离子交换树脂的亲和力三、离子交换分离操作技术四、离子交换分离法的应用第四节常规色谱法一、柱色谱法二、纸色谱法三、薄层色谱法本章小结思考题与习题第九章电势分析法第一节电势分析法基本原理一、直接电势法二、电势滴定法三、电池电动势的测量第二节参比电极和指示电极一、参比电极二、指示电极第三节直接电势法及应用一、溶液pH值的测定二、离子活度(浓度)的测定三、直接电势法的应用第四节电势滴定法一、电势滴定法的原理二、电势滴定终点的确定三、电势滴定法的应用本章小结思考题与习题第十章吸光光度分析法第一节吸光光度法的基础知识一、光的基本性质二、光的互补作用与溶液的颜色三、光的吸收曲线第二节光的吸收定律一、朗伯?比耳定律二、朗伯?比耳定律的推导三、吸光度与透光度四、吸光系数、摩尔吸光系数及桑德尔灵敏度第三节显色反应及影响因素一、吸光光度法对显色反应的要求二、影响显色反应的主要因素三、显色剂第四节吸光光度分析法及仪器一、吸光光度分析的类型二、吸光光度分析的定量分析方法三、分光光度计的构造四、分光光度计的类型第五节吸光光度法测量误差及测量条件的选择一、吸光光度法的测量误差二、测量条件的选择第六节吸光光度法的应用一、示差吸光光度法二、多组分的分析三、配合物组成的测定本章小结思考题与习题第十一章原子吸收分光光度法第一节基本原理一、共振发射线与吸收线二、基态原子与激发态原子的关系三、原子吸收线的宽度四、原子吸收的测量五、灵敏度和检出限第二节原子吸收分光光度计一、光源二、原子化器三、分光系统四、检测系统五、读数装置六、原子吸收分光光度计的类型第三节仪器测量条件的选择一、分析线的选择二、灯电流的选择三、原子化条件的选择四、燃烧器高度的选择五、进样量六、单色器狭缝宽度与光谱通带的选择第四节定量分析方法一、标准工作曲线法二、标准加入法第五节干扰及消除方法一、光谱干扰二、化学干扰、物理干扰及电离干扰第六节原子吸收分光光度法的应用一、测定生物样品中的化学元素二、有机物分析本章小结思考题与习题第十二章气相色谱分析法第一节色谱法概述一、色谱法原理介绍二、色谱法的分类第二节气相色谱法的特点及基本原理一、气相色谱法的特点二、气相色谱法的基本原理第三节气相色谱的实验技术一、色谱系统二、实验技术要点三、程序升温和衍生物制备第四节气相色谱法的应用一、定性分析二、定量分析三、气相色谱分析误差产生的原因第五节气相色谱法的新进展一、顶空气相色谱二、气相色谱?质谱联用技术三、气相色谱?红外光谱联用技术本章小结思考题与习题第十三章高效液相色谱法第一节高效液相色谱法的技术参数一、速率理论二、柱外效应三、分离度四、系统适应性实验第二节高效液相色谱法的色谱系统一、高压泵二、梯度洗脱装置三、进样器四、色谱柱五、检测器六、数据处理系统和结果处理第三节高效液相色谱法的分离方式一、吸附色谱法二、分配色谱法三、离子色谱法四、尺寸排阻色谱法五、亲和色谱法第四节样品预处理与色谱柱的保护一、样品预处理二、色谱柱的保护第五节液相色谱分析技术的新进展一、液相色谱?质谱联用技术概述二、超临界流体色谱法概述三、高效毛细管液相色谱法概述本章小结思考题与习题第十四章现代仪器分析简介第一节光分析法导论一、电磁波的辐射能特性二、光分析法的分类第二节原子发射光谱法一、基本原理二、原子发射光谱仪三、应用第三节原子荧光光谱法一、基本原理二、原子荧光光谱仪三、应用第四节分子荧光和磷光分析法一、荧光和磷光的产生二、荧光和磷光强度的影响因素三、荧光/磷光分析仪器四、荧光/磷光分析法应用第五节红外分光光度法一、分子的红外吸收二、红外光谱解析程序第六节核磁共振波谱法一、基本原理二、1HNMR谱的解析三、13CNMR谱的特点与解析第七节流动注射分析本章小结思考题与习题第十五章样品分析的一般过程第一节试样采集和制备一、试样的采集二、试样的制备第二节试样的分解与处理一、无机试样的分解处理二、有机试样的分解处理三、试样分解处理方法的选择四、干扰组分的处理第三节测定方法的选择一、测定的具体要求二、被测组分的性质三、被测组分的含量四、共存组分的影响五、实验室条件第四节分析结果的计算和数据评价一、分析结果的计算及表示方法二、分析结果的报告与评价本章小结思考题与习题附录附录一相对原子质量表(2001年国际原子量)附录二化合物的相对分子质量表附录三弱酸在水中的离解常数(25℃)附录四弱碱在水中的离解常数(25℃)附录五常用浓酸浓碱的密度和浓度附录六几种常用缓冲溶液的配制附录七常用标准缓冲溶液不同温度下的pH值附录八金属离子与EDTA配合物的lgKf(25℃)附录九标准电极电势表(25℃)附录十部分氧化还原电对的条件电极电势(25℃)附录十一难溶化合物的溶度积常数(25℃)参考文献目录绪论0.1 分析化学的任务和作用0.2 分析方法的分类0.2.1 无机分析和有机分析0.2.2 化学分析和仪器分析0.2.3 常量分析、半微量分析和微量分析。