ctd所需要资料
- 格式:doc
- 大小:64.00 KB
- 文档页数:11


CTD申报资料注册分类:化药六类 CTD资料*********CTD格式申报资料一、目录 3.2.P.1 剂型及产品组成3.2.P.2 产品开发3.2.P.2.1 处方组成3.2.P.2.1.1 原料药3.2.P.2.1.2 辅料3.2.P.2.2 制剂研究3.2.P.2.2.1 处方开发过程3.2.P.2.2.2 制剂相关特性 3.2.P.2.3 生产工艺的开发3.2P.2.3.1 小试工艺筛选3.2P.2.3.2 中试生产工艺筛选3.2P.2.3.3 生产工艺总结3.2P.2.3.4 关键工艺参数控制3.2P.2.3.5 生产工艺变化汇总3.2P.2.3.6 批分析汇总3.2.P.2.4 包装材料/容器3.2.P.2.5 相容性3.2.P.3 生产3.2.P.3.1 生产商3.2.P.3.2 批处方3.2.P.3.3 生产工艺和工艺控制 3.2.P.3.4 关键步骤和中间体的控制3.2.P.3.5 工艺验证和评价 3.2.P.4 原辅料的控制3.2.P.5 制剂的质量控制3.2.P.5.1 质量标准第 1 页共 36 页注册分类:化药六类 CTD资料 3.2.P.5.2 分析方法3.2.P.5.3 分析方法的验证3.2.P.5.4 批检验报告3.2.P.5.5 杂质分析3.2.P.5.6 质量标准制定依据3.2.P.6 对照品3.2.P.7 稳定性3.2.P.7.1 稳定性总结3.2.P.7.2 上市后的稳定性研究方案及承诺3.2.P.7.3 稳定性数据二、申报资料正文3.2.P.1 剂型及产品组成(1)本品为淡黄色或类白色片,规格为50mg,单位剂量产品的处方组成,各成分在处方中的作用以及执行的标准见表3.2.P.1。
表3.2.P.1 产品组成成分用量百分重量作用执行标准60 69.40 填充剂中国药典2010年版微晶纤维素26 30.08 填充剂中国药典2010年版淀粉0.52 适量黏合剂中国药典2010年版第 2 页共 36 页注册分类:化药六类 CTD资料********* 50 35.71 活性成分中国药典2010年版2.5 1.79 二氧化硅助流剂中国药典2010年版(2)本品无专用溶剂。


化学药品各号申报资料的一般要求申报资料的一般要求为便于梳理与理解,在同一号资料中分为以下三种情形:A:新药报临B:新药报生产C:仿制药1号资料:A:包括通用名、商品名、化学名、英文名、汉语拼音,并注明其化学结构式、分子量、分子式等(见药审中心要求)。
如果是新剂型新命名、应附上药典委员会命名的复函B:同AC:同A外,需提供:国家标准(注:不允许申请商品名)2号资料:A:1、药品生产企业:“三证”(GMP与生产许可证的单位名称和生产地址一致)新药证书申请人:有效的营业执照、事业单位法人证书及其变更登记证明2、专利查询报告、不侵权保证书3、特殊药品:SFDA安监司的立项批件4、制剂用原料药的合法来源(一套)①直接向原料生产厂家购买:a、原料厂三证(三证与原料的批准证明文件的单位名称、地址必须一致)1、生产企业:营业执照、税务登记证、组织机构代码证、生产许可证(QS 证)(还需要产品第三方检测报告、出厂检测报告,产品执行标准等) 。
2、贸易型企业:营业执照、流通许可证(同时也需要提供所销售产品生产厂家的营业执照、生产许可证等)b、原料的批准证明文件(《药品注册批件》、《药品注册证》、统一换发文号的文件等)c、原料的质量标准及原料药出厂检验报告d、购货发票(赠送的,提供相关证明(赠送证明))e、购销合同或供货协议复印件f、自检报告书(全检)②向原料经销单位购买的:除需提供上述文件外,还需提供经销商与原料厂的供货协议新增:申报生产时,原料药如系通过赠送途径获得而未能提供该原料药合法来源证明和供货协议的,不批准③原料与制剂同时注册申请:原料和制剂厂不一致的,应提供原料和制剂厂之间的供货协议或合作开发协议(申报相同剂型的原料药来源不能是相同的原料药申请人)×A厂胶囊原料甲×B厂胶囊只能一对一,因此时的原料甲还未批准上市④使用进口原料的:略5、商标查询单或商标注册证(可推迟至报生产时提供)6、直接接触药品的包装材料和容器的包材证或受理通知单(2005版药典已将胶囊归为包材)7、委托试验:应提供委托合同,并附该机构合法登记证明、必要的资质证明。



CTD申报资料模版1. 介绍本文档提供了CTD申报资料的模版,帮助申请人编写CTD 申报资料。
CTD,即Common Technical Document,是国际上通用的药品注册申报文档格式。
CTD申报资料是药品注册申请的核心文档,用于向药品监管机构提交药品的安全性、有效性和质量等相关信息。
2. CTD申报资料的结构与内容CTD申报资料包含5个模块,分别是:质量部分(Quality)、非临床部分(Nonclinical)、临床部分(Clinical)、申请人概述部分(Applicant’s Overview)和审核员概述部分(Module 5)。
2.1 质量部分质量部分包括了药品的质量控制和生产工艺方面的信息,主要内容包括:•药品的质量规范(Specifications)•药品的制造工艺(Manufacturing Process)•药品的成分(Composition)•药品的稳定性研究(Stability Studies)•药品的包装和标签(Packaging and labeling)2.2 非临床部分非临床部分包含了药物的非临床研究数据,主要内容包括:•药物的药理学和毒理学研究(Pharmacology and Toxicology Studies)•药物代谢与药物动力学研究(Metabolism and Pharmacokinetics Studies)2.3 临床部分临床部分包含了药物的临床试验数据,主要内容包括:•临床试验设计(Clinical Trial Design)•临床试验结果(Clinical Trial Results)•药物在人群中的疗效(Efficacy)•药物的安全性(Safety)2.4 申请人概述部分申请人概述部分是申请人对药物的总结和解释,主要内容包括:•药物的概述和用途(Overview and Uses of the Drug)•为什么该药物是安全和有效的(Why the Drug is Safe and Effective)•药物的剂量和给药途径(Dosage andAdministration)•药物的不良反应(Adverse Reactions)2.5 审核员概述部分审核员概述部分是药品审评机构对申请资料的总结和评价,主要内容包括:•药物的总结和评价(Summary and Assessment of the Drug)•对申请人的要求和建议(Recommendations for the Applicant)•对药物的批准或拒绝的意见(Opinion on Approval or Rejection of the Drug)3. 编写CTD申报资料的注意事项在编写CTD申报资料时,需要注意以下几点:•按照CTD的结构和内容编写,确保包含了所有必要的信息。
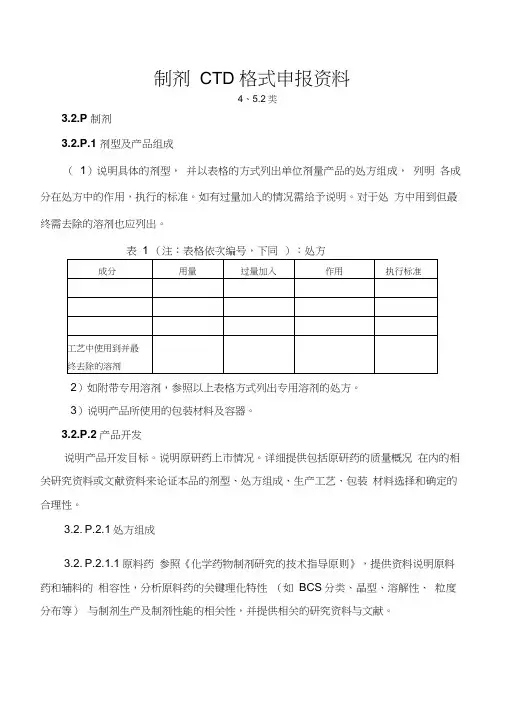
制剂CTD 格式申报资料4、5.2类3.2.P 制剂3.2.P.1 剂型及产品组成(1)说明具体的剂型,并以表格的方式列出单位剂量产品的处方组成,列明各成分在处方中的作用,执行的标准。
如有过量加入的情况需给予说明。
对于处方中用到但最终需去除的溶剂也应列出。
表1 (注:表格依次编号,下同):处方2)如附带专用溶剂,参照以上表格方式列出专用溶剂的处方。
3)说明产品所使用的包装材料及容器。
3.2.P.2 产品开发说明产品开发目标。
说明原研药上市情况。
详细提供包括原研药的质量概况在内的相关研究资料或文献资料来论证本品的剂型、处方组成、生产工艺、包装材料选择和确定的合理性。
3.2. P.2.1处方组成3.2. P.2.1.1原料药参照《化学药物制剂研究的技术指导原则》,提供资料说明原料药和辅料的相容性,分析原料药的关键理化特性(如BCS分类、晶型、溶解性、粒度分布等)与制剂生产及制剂性能的相关性,并提供相关的研究资料与文献。
3.2. P.2.1.2辅料说明辅料是否适合所用的给药途径结合辅料在处方中的作用分析辅料的哪些性质会影响制剂特性,提供相关的研究资料与文献。
3.2. P.2.2 制剂研究3.2. P.2.2.1处方开发过程参照《化学药物制剂研究的技术指导原则》,提供处方的研究开发过程和确定依据,包括文献信息(如对照药品的处方信息)、研究信息(包括处方设计,处方筛选和优化、处方确定等研究内容)、辅料种类和用量选择的依据、分析辅料用量是否在常规用量范围内,以及自制样品与原研药的质量特性对比研究结果(需说明原研药的来源、批次和有效期,自研样品批次,对比项目、采用方法),并重点说明在药品开发阶段中处方组成的主要变更、原因以及支持变化的验证研究。
如生产中存在过量投料的问题,应提供过量投料的必要性和合理性的相关研究资料。
3.2. P.2.2.2制剂相关特性对与制剂性能相关的理化性质,如pH、离子强度、溶出度、再分散性、复溶、粒径分布、聚合、多晶型、流变学等进行分析。

制剂CTD格式申报资料4、5.2类3.2.P 制剂3.2.P.1 剂型及产品组成(1)说明具体的剂型,并以表格的方式列出单位剂量产品的处方组成,列明各成分在处方中的作用,执行的标准。
如有过量加入的情况需给予说明。
对于处方中用到但最终需去除的溶剂也应列出。
表1(注:表格依次编号,下同):处方(2)如附带专用溶剂,参照以上表格方式列出专用溶剂的处方。
(3)说明产品所使用的包装材料及容器。
3.2.P.2 产品开发说明产品开发目标。
说明原研药上市情况。
详细提供包括原研药的质量概况在内的相关研究资料或文献资料来论证本品的剂型、处方组成、生产工艺、包装材料选择和确定的合理性。
3.2.P.2.1处方组成3.2.P.2.1.1原料药参照《化学药物制剂研究的技术指导原则》,提供资料说明原料药和辅料的相容性,分析原料药的关键理化特性(如BCS分类、晶型、溶解性、粒度分布等)与制剂生产及制剂性能的相关性,并提供相关的研究资料与文献。
3.2.P.2.1.2辅料说明辅料是否适合所用的给药途径结合辅料在处方中的作用分析辅料的哪些性质会影响制剂特性,提供相关的研究资料与文献。
3.2.P.2.2 制剂研究3.2.P.2.2.1处方开发过程参照《化学药物制剂研究的技术指导原则》,提供处方的研究开发过程和确定依据,包括文献信息(如对照药品的处方信息)、研究信息(包括处方设计,处方筛选和优化、处方确定等研究内容)、辅料种类和用量选择的依据、分析辅料用量是否在常规用量范围内,以及自制样品与原研药的质量特性对比研究结果(需说明原研药的来源、批次和有效期,自研样品批次,对比项目、采用方法),并重点说明在药品开发阶段中处方组成的主要变更、原因以及支持变化的验证研究。
如生产中存在过量投料的问题,应提供过量投料的必要性和合理性的相关研究资料。
3.2.P.2.2.2制剂相关特性对与制剂性能相关的理化性质,如pH、离子强度、溶出度、再分散性、复溶、粒径分布、聚合、多晶型、流变学等进行分析。

CTD申报资料模版1. 引言本文档旨在为CTD(药物临床试验数据)申报提供一个标准化的资料模板,以便帮助申请人整理和准备相关文件。
本模板按照国家药监局的要求进行编写,并参考了相关指南和标准。
2. 资料清单下面是CTD申报资料的清单:1.申请表2.药物研究概况3.临床研究计划4.药物化学和药学附件5.其他相关附件3. 申请表在申请表中,需要填写以下信息:•申请人信息:包括申请人姓名、单位、联系方式等。
•药物信息:包括药物名称、剂型、规格、批号等。
•申报内容:包括申报的研究阶段、测试目标、研究计划等。
•相关声明:包括研究过程中的伦理和合规问题的声明。
4. 药物研究概况药物研究概况需要提供以下信息:•药物研究的背景和目的•相关研究基础和先行研究•临床试验方案的设计和方法•参与者招募和纳入标准•数据收集和统计分析方法•预期研究结果5. 临床研究计划临床研究计划需要提供以下信息:•研究设计与方法:包括研究类型、研究中心、样本大小、随机化方案等。
•研究过程的伦理和合规问题:包括伦理委员会审查、知情同意和机密保护等问题。
•数据收集和管理:包括数据收集时间点、数据管理计划等。
•统计分析计划:包括主要的统计分析方法和假设检验等。
6. 药物化学和药学附件药物化学和药学附件需要提供以下信息:•药物的化学结构和化学性质•药物的制备方法和工艺•药物的质量标准和分析方法(如鉴别、含量测定等)•药物的稳定性研究和储存条件7. 其他相关附件除了上述资料,申请人还需要提供其他相关附件,如:•急救方案和不良事件报告•临床试验结果和分析报告•相关专家和机构的鉴定或推荐信•其他与申报相关的文件8. 结论本文档提供了一个CTD申报资料的模版,帮助申请人整理和准备相关文件。
申请人应根据具体情况进行调整和补充,以确保申报资料的完整和准确。
努力准备好CTD申报资料,将有助于快速获得批准,并推动药物研究的进展。
注意:本文所提供的模版仅供参考,申请人需要根据实际需求和相关法规进行适当的调整和修改。

CTD格式申报资料撰写要求(原料药)一、目录3.2.S 原料药3.2.S.1 基本信息3.2.S.1.1 药品名称3.2.S.1.2 结构3.2.S.1.3 理化性质3.2.S.2 生产信息3.2.S.2.1生产商3.2.S.2.2生产工艺和过程控制3.2.S.2.3物料控制3.2.S.2.4关键步骤和中间体的控制3.2.S.2.5工艺验证和评价3.2.S.2.6生产工艺的开发3.2.S.3 特性鉴定3.2.S.3.1结构和理化性质3.2.S.3.2杂质3.2.S.4 原料药的质量控制3.2.S.4.1质量标准3.2.S.4.2分析方法3.2.S.4.3分析方法的验证3.2.S.4.4批检验报告3.2.S.4.5质量标准制定依据3.2.S.5对照品3.2.S.6包装材料和容器3.2.S.7稳定性3.2.S.7.1稳定性总结3.2.S.7.2上市后稳定性承诺和稳定性方案3.2.S.7.3稳定性数据二、申报资料正文及撰写要求3.2.S.1 基本信息3.2.S.1.1药品名称提供原料药的中英文通用名、化学名,化学文摘(CAS)号以及其它名称(包括国外药典收载的名称)。
3.2.S.1.2 结构提供原料药的结构式、分子式、分子量,如有立体结构和多晶型现象应特别说明。
3.2.S.1.3 理化性质提供原料药的物理和化学性质(一般来源于药典和默克索引等),具体包括如下信息:性状(如外观,颜色,物理状态);熔点或沸点;比旋度,溶解性,溶液pH, 分配系数,解离常数,将用于制剂生产的物理形态(如多晶型、溶剂化物、或水合物),粒度等。
3.2.S.2 生产信息3.2.S.2.1生产商生产商的名称(一定要写全称)、地址、电话、传真以及生产场所的地址、电话、传真等。
3.2.S.2.2 生产工艺和过程控制(1)工艺流程图:按合成步骤提供工艺流程图,标明工艺参数和所用溶剂。
如为化学合成的原料药,还应提供其化学反应式,其中应包括起始原料、中间体、所用反应试剂的分子式、分子量、化学结构式。
*********C T D格式申报资料一、目录剂型及产品组成产品开发处方组成原料药辅料制剂研究处方开发过程制剂相关特性生产工艺的开发包装材料/容器相容性生产生产商批处方生产工艺和工艺控制关键步骤和中间体的控制工艺验证和评价原辅料的控制制剂的质量控制质量标准分析方法分析方法的验证批检验报告杂质分析质量标准制定依据对照品稳定性 稳定性总结上市后的稳定性研究方案及承诺 稳定性数据二、申报资料正文剂型及产品组成(1)本品为淡黄色或类白色片,规格为50mg ,单位剂量产品的处方组成,各(2)本品无专用溶剂。
(3)本品采用PVC 铝塑包装,外加聚酯/铝/聚乙烯复合膜袋。
产品开发*********是德国拜耳开发上市的首个口服苷酶抑制剂,1990年首先在德国上市。
于1998年进入我国,商品名为“*********”。
我公司以“*********”为对照药品,研制了*********片,规格为50mg ,按照国家药品注册分类,属于化学药第6类已有国家标准品种。
处方组成 原料药*********化学名称为: 化学结构式为: 分子式: 分子量:*********为白色或类白色无定形粉末,在水中极易溶,在甲醇中溶解,在乙醇中极成 分 用量 百分重量作用 执行标准 微晶纤维素淀粉6026适量填充剂 填充剂 黏合剂中国药典2010年版 中国药典2010年版 中国药典2010年版********* 二氧化硅50活性成分 助流剂中国药典2010年版 中国药典2010年版微溶解,在乙腈和丙酮中不溶。
本品应密封、避光、在阴凉处保存。
辅料“*********”处方中所用的辅料为:微晶纤维素、淀粉、硬脂酸镁、二氧化硅。
本品处方参照“*********”,除加入粘合剂羟丙甲基纤维素外,其他辅料均与上市对照药“*********”一致,辅料相容性试验结果显示羟丙甲基纤维素对活性成分无明显影响。
制剂研究处方开发过程为尽量保证研制品与上市药品安全、有效性一致,我们对上市样品进行了全面的考察及评价,并全面考察原料的性质。
医药CRO化学药品各号申报资料的一般要求申报资料的一般要求为便于梳理与理解,在同一号资料中分为以下三种情形:A:新药报临B:新药报生产C:仿制药1号资料:A:包括通用名、商品名、化学名、英文名、汉语拼音,并注明其化学结构式、分子量、分子式等(见药审中心要求)。
如果是新剂型新命名、应附上药典委员会命名的复函B:同AC:同A外,需提供:国家标准(注:不允许申请商品名)2号资料:A:1、药品生产企业:“三证”(GMP与生产许可证的单位名称和生产地址一致)新药证书申请人:有效的营业执照、事业单位法人证书及其变更登记证明2、专利查询报告、不侵权保证书3、特殊药品:SFDA安监司的立项批件4、制剂用原料药的合法来源(一套)①直接向原料生产厂家购买:a、原料厂三证(三证与原料的批准证明文件的单位名称、地址必须一致)1、生产企业:营业执照、税务登记证、组织机构代码证、生产许可证(QS 证)(还需要产品第三方检测报告、出厂检测报告,产品执行标准等) 。
2、贸易型企业:营业执照、流通许可证(同时也需要提供所销售产品生产厂家的营业执照、生产许可证等)b、原料的批准证明文件(《药品注册批件》、《药品注册证》、统一换发文号的文件等)c、原料的质量标准及原料药出厂检验报告d、购货发票(赠送的,提供相关证明(赠送证明))e、购销合同或供货协议复印件f、自检报告书(全检)②向原料经销单位购买的:除需提供上述文件外,还需提供经销商与原料厂的供货协议新增:申报生产时,原料药如系通过赠送途径获得而未能提供该原料药合法来源证明和供货协议的,不批准③原料与制剂同时注册申请:原料和制剂厂不一致的,应提供原料和制剂厂之间的供货协议或合作开发协议(申报相同剂型的原料药来源不能是相同的原料药申请人)×A厂胶囊原料甲×B厂胶囊只能一对一,因此时的原料甲还未批准上市④使用进口原料的:略5、商标查询单或商标注册证(可推迟至报生产时提供)6、直接接触药品的包装材料和容器的包材证或受理通知单(2005版药典已将胶囊归为包材)7、委托试验:应提供委托合同,并附该机构合法登记证明、必要的资质证明。
医药CRO化学药品各号申报资料的一般要求申报资料的一般要求为便于梳理与理解,在同一号资料中分为以下三种情形:A:新药报临B:新药报生产C:仿制药1号资料:A:包括通用名、商品名、化学名、英文名、汉语拼音,并注明其化学结构式、分子量、分子式等(见药审中心要求)。
如果是新剂型新命名、应附上药典委员会命名的复函B:同AC:同A外,需提供:国家标准(注:不允许申请商品名)2号资料:A:1、药品生产企业:“三证”(GMP与生产许可证的单位名称和生产地址一致)新药证书申请人:有效的营业执照、事业单位法人证书及其变更登记证明2、专利查询报告、不侵权保证书3、特殊药品:SFDA安监司的立项批件4、制剂用原料药的合法来源(一套)①直接向原料生产厂家购买:a、原料厂三证(三证与原料的批准证明文件的单位名称、地址必须一致)1、生产企业:营业执照、税务登记证、组织机构代码证、生产许可证(QS 证)(还需要产品第三方检测报告、出厂检测报告,产品执行标准等) 。
2、贸易型企业:营业执照、流通许可证(同时也需要提供所销售产品生产厂家的营业执照、生产许可证等)b、原料的批准证明文件(《药品注册批件》、《药品注册证》、统一换发文号的文件等)c、原料的质量标准及原料药出厂检验报告d、购货发票(赠送的,提供相关证明(赠送证明))e、购销合同或供货协议复印件f、自检报告书(全检)②向原料经销单位购买的:除需提供上述文件外,还需提供经销商与原料厂的供货协议新增:申报生产时,原料药如系通过赠送途径获得而未能提供该原料药合法来源证明和供货协议的,不批准③原料与制剂同时注册申请:原料和制剂厂不一致的,应提供原料和制剂厂之间的供货协议或合作开发协议(申报相同剂型的原料药来源不能是相同的原料药申请人)×A厂胶囊原料甲×B厂胶囊只能一对一,因此时的原料甲还未批准上市④使用进口原料的:略5、商标查询单或商标注册证(可推迟至报生产时提供)6、直接接触药品的包装材料和容器的包材证或受理通知单(2005版药典已将胶囊归为包材)7、委托试验:应提供委托合同,并附该机构合法登记证明、必要的资质证明。
医药CRO化学药品各号申报资料的一般要求申报资料的一般要求为便于梳理与理解,在同一号资料中分为以下三种情形:A:新药报临B:新药报生产C:仿制药1号资料:A:包括通用名、商品名、化学名、英文名、汉语拼音,并注明其化学结构式、分子量、分子式等(见药审中心要求)。
如果是新剂型新命名、应附上药典委员会命名的复函B:同AC:同A外,需提供:国家标准(注:不允许申请商品名)2号资料:A:1、药品生产企业:“三证”(GMP与生产许可证的单位名称和生产地址一致)新药证书申请人:有效的营业执照、事业单位法人证书及其变更登记证明2、专利查询报告、不侵权保证书3、特殊药品:SFDA安监司的立项批件4、制剂用原料药的合法来源(一套)①直接向原料生产厂家购买:a、原料厂三证(三证与原料的批准证明文件的单位名称、地址必须一致)1、生产企业:营业执照、税务登记证、组织机构代码证、生产许可证(QS 证)(还需要产品第三方检测报告、出厂检测报告,产品执行标准等) 。
2、贸易型企业:营业执照、流通许可证(同时也需要提供所销售产品生产厂家的营业执照、生产许可证等)b、原料的批准证明文件(《药品注册批件》、《药品注册证》、统一换发文号的文件等)c、原料的质量标准及原料药出厂检验报告d、购货发票(赠送的,提供相关证明(赠送证明))e、购销合同或供货协议复印件f、自检报告书(全检)②向原料经销单位购买的:除需提供上述文件外,还需提供经销商与原料厂的供货协议新增:申报生产时,原料药如系通过赠送途径获得而未能提供该原料药合法来源证明和供货协议的,不批准③原料与制剂同时注册申请:原料和制剂厂不一致的,应提供原料和制剂厂之间的供货协议或合作开发协议(申报相同剂型的原料药来源不能是相同的原料药申请人)×A厂胶囊原料甲×B厂胶囊只能一对一,因此时的原料甲还未批准上市④使用进口原料的:略5、商标查询单或商标注册证(可推迟至报生产时提供)6、直接接触药品的包装材料和容器的包材证或受理通知单(2005版药典已将胶囊归为包材)7、委托试验:应提供委托合同,并附该机构合法登记证明、必要的资质证明。
8、相关证明性文件的变更证明文件9、申请申报OTC的证明文件等10、需由非法定代表人签名的,应当由法定代表人授权的负责人签名,并提供委托签字授权书原件B:同A,还提供:1、临床批件2、临床试验用药的质量标准3、中检所出具的制备标准品的原材料受理单(原料)4、新开办企业、新建车间或新增剂型,在取得载明相应生产范围的《生产许可证》后方可申报生产C:同A,但无商品名、商标的查询单3号资料:A:分为以下六部分撰写(具体内容照“化学药品申报资料撰写格式与内容技术指导原则:立题目的与依据撰写格式和内容”,特别注意陈述规格、剂型的依据)1、品种基本情况2、立题背景(“国外上市”不是立题的依据)3、品种的特点4、国内外有关该品种的知识产权等情况5、综合分析(现行审评强调此内容)6、参考文献新增要求:制剂研究合理性和临床使用必需性的综述,对于改剂型的申请,不接受“增加临床使用选择”的理由。
B:同AC:同A,特别阐述清楚规格问题(仿制全部规格还是部分仿制?是否增加新规格)★规格依据(常见的):1) 现行说明书上的表述2) 说明书临床使用依据(不低于最小量,不大于最大量)3) 同品种其他厂家有相同的规格上市新增规格的依据4) 国外有此规格上市的文献资料(如说明书原文及译文)新增:“虽有同品种已上市规格,但该规格已不符合临床需要的”不批准新增要求:说明已上市同品种的新药保护期、过渡期、监测期等情况,总之,对各类注册申请的立题依据各有侧重点。
4号资料:A:分以下五部分来撰写(具体内容照“化学药品申报资料撰写格式与内容技术指导原则:对主要研究结果的总结及评价撰写格式和内容”)1、品种基本情况2、药学主要研究结果及评价3、药理毒理主要研究结果及评价4、临床主要研究结果及评价5、综合分析及评价6、申请人对主要研究结果进行的总结;从安全性、有效性、质量可控性等方面对所申报品种进行综合评价B:同A增加了:临床研究的结果、稳定性考察(长期)的结果(全部研究是否紧扣立题目的),还应说明临床批件号和批准时间,其中要明确该药临床批件上是否有遗留试验。
如果有,应表明是否完成,结果是什么?这些内容分别在几号申报资料中。
同时还应说明:在临床期间,工艺是否有变化,质量标准是否有修改完善及数据积累的结果。
C:同A(有临床研究的就同B)5号资料:A:1、包括按有关规定起草的药品说明书2、说明书各项内容的起草说明(准确拟定“适应症”,忌把他人说明书上的适应症照抄在自己申报的说明书上)3、相关文献(国外说明书应全文翻译)B:同A,注意说明书中各项应紧扣各项研究的数据与结果(结合临床研究与文献资料,准确描述“适应症、用法用量、不良反应、注意事项等”)C:参考A,必须提供被仿(指用于平行研究的)产品的最新的说明书复印件,可以与被仿品的说明书一致。
6号资料:A:可无B:按24号令规定设计的word版样稿(不要求彩稿,也不是上市件)C:同B,可加上已注册的商标7号资料:A:资料格式与内容照药审中心要求(化学药品申报资料撰写格式与内容技术指导原则:药学研究资料综述撰写格式和内容),包括:合成工艺、剂型选择、处方筛选、结构确证、质量研究和质量标准制定、稳定性研究、国内外文献资料的综述。
B:如果在临床阶段,药学某些方面作了修改(最好不要在临床试验中做生产工艺、处方等调整,否则与临床样品缺乏一致性。
除非做完工艺、处方修改后再生产上临床的样品),本号资料需重新提供,增加修改的内容。
C:同A8号资料:A:详见相关的技术指导原则提示:原料包括:1、工艺流程和化学反应式(多条合成路线的比较、取舍的原因)2、起始原料和有机溶媒等(对起始原料,国家局有严格监督管理,同行们要引起高度重视!)3、反应条件(温度、压力、时间、催化剂等)4、操作步骤5、精制方法6、主要理化常数及阶段性的数据积累及文献资料7、对环保的影响及其评价(对三废的处理)新增:工艺验证资料(报生产时提交)请关注过渡期品种集中审评《化学药品技术标准不予批准》中“三”的相关内容。
制剂包括:1、处方依据(多个处方取舍必须有处方筛选的过程)2、剂型选择理由3、规格依据4、工艺流程(文字+流程图)5、工艺参数的确立依据(包括工艺条件)6、相关图谱★常见的工艺参数1) 药物粉碎的具体方法,粒度要求2) 药物与辅料的混合方法,采用的设备、混合时间3) 片剂湿法制粒时黏合剂的加入量及加入方法4) 湿颗粒的干燥温度及时间5) 片剂压片压力6) 包衣操作温度、包衣液雾化压力、喷液方式及速度、干燥温度及时间7) 注射剂的灭菌温度及时间、冻干曲线……7、原辅料的作用及其辅料用量的依据辅料的型号必须交待原辅料供应商的全检报告及进厂自检报告(全检)均需附上明确表示,如何控制原辅料的质量?7、工艺验证应包括起始物料、处方筛选、生产工艺、设备等验证资料(药审中心网上已有部分“验证”的技术指导文章可供参考)1)无菌/灭菌的工艺验证2)注明投料量和收得率3)工艺过程中可能产生或引入的杂质或其他中间产物4)影响因素试验:光照、高温、高湿(省去某项应说明原因)工艺研究资料要明确:小试规模研究的处方、工艺、步骤、参数是什么?中试放大研究的规模、批次,关注处方、工艺、步骤、参数是否有调整,并拟定出工艺操作程序与参数变化的允许范围B:与原来不同,本号资料涉及报生产,而且要接受生产现场检查的严格检查,是最主要的申报资料!!需要提交大生产规模的研究情况(尤其需紧扣“药品注册现场检查要点及判定原则”的要求),在中试基础上又进行的研究情况,关注放大过程中的各步骤和参数的变化。
即要求提供完整的规模化生产工艺,同时要说明临床研究期间生产工艺的研究资料;说明临床研究样品的生产情况和检验情况。
总之,这一环节申报的工艺是后期生产现场检查所依据的内容,至关重要!!C:同A,注意相关研究项,应与被仿制品(一批)平行对比研究,以此说明与上市产品的“等同性”(一般不可能有相同性)。
尤其是“影响因素”试验应与被仿品(一批)平行试验最能说明自己的结果具体试验请参考《仿制化学药品研究技术指导原则》9号资料:A:详见“技术指导原则”(化学药物原料药制备和结构确证研究的技术指导原则),委托研究的,注意签定委托合同,报告书及图谱上盖章,试验单位的资质证明、委托人(一般是申请人)要特别注意真实性问题,因《办法》第13条明确是申请人对全部资料的真实性负责。
B:无补充内容,可不提供C:同A(仿原料时)10号资料:A:详见“技术指导原则”(化学药物杂质研究的技术指导原则、化学药物残留溶剂研究的技术指导原则)等;包括:理化性质、纯度检查、溶出度、微生物检查、无菌检查、含量测定的方法学验证及阶段性的数据积累结果等、标准品来源、图谱。
提示:注重细节,例如:“过滤”用什么材质与型号,依据是什么?均应有试验的过程与结果。
B:无修改内容,可不提供;若有修改完善之处,逐一阐述,注意前后的衔接性C:同A,附上国家标准,各项研究必须与被仿品平行研究。
当某药品同时有进口标准和国家药品标准时,最好要参考进口标准(正常程序见不到全文)的测定项目与其指标要求,充实自己的研究,最后拟定出注册申请的标准。
11号资料:A:详见“技术指导原则”(化学药物质量标准建立的规范化过程技术指导原则要求):1、质量标准应当符合《中国药典》现行版的格式,并使用其术语和计量单位2、所使用试药、试液、缓冲液、滴定液等,应当采用现行版《中国药典》收载的品种及浓度,有不同的,应详细说明3、提供的标准品或对照品应另附资料说明:来源、理化常数、纯度、含量及其测定方法和数据注:各项起草说明所依据的试验数据至少应加上中试三批样品的结果及临床用样品的结果,或者应加上做验证的多批样品的数据。
起草说明还应包括,在执行此标准时,需注意的环节,否则,以后现场核查时,口头上再解释可能不被核查专家接受。
B:无修改内容,药审中心要求仍需再提交,目的是方便审评!有修改内容,更需在此逐一简述这一环节,也是生产现场检查的核心!!C:参考A,需要明确说明,在研究过程中对标准是否有提高?理由与依据什么?12号资料:A:指申报样品的自检报告书(1~3批)B:三批B的三批样品生产必须符合GMP条件C:三批(因临床结束后,直接将后续的临床等方面的资料报药审中心,不再做生产现场考核抽样等,故一步到位;三批,在临床结束报生产时,附上药检所的三批复核报告书复印件)C的三批样品必须是GMP车间里的生产规模的样品申请人要注意药检所报告的结果与自检的结果是否接近,若相差较大在寄出复核报告书前查明原因,否则在审评时会遭遇不必要的麻烦!强调:上临床的样品一定是工艺、处方确定的样品,且是中试规模的产品,否则没有一致性,尤其是固体制剂。