钝化金属阳极极化曲线的测定(精)
- 格式:ppt
- 大小:2.91 MB
- 文档页数:9

实验一:恒电位法测定阳极极化曲线一.实验目的1. 熟悉恒电位仪测定极化曲线的方法;2. 了解金属钝化现象及活化钝化转变过程二.基本原理极化曲线测量是金属电化学腐蚀和保护中一种重要的研究手段。
测量腐蚀体系的极化曲线,实际就是测量在外加电流作用下,金属在腐蚀介质中的电极电位与外加电流密度之间的关系。
某些金属在特定介质中存在钝化现象,表面生成一层具有保护作用的钝化膜,其阳极极化曲线如图所示:图1-1. 具有活化钝化转变的阳极极化曲线图中Ⅰ区为活化区,Ⅱ区为钝化过渡区,Ⅲ区为钝化区,此时金属表面生成一层具有保护性的钝化膜,Ⅳ区为过钝化区,钝化膜破裂,极化电流增大。
图中a 点所对应的电流密度为维钝电流密度,b 点所对应的电流密度为致钝电流密度。
为了判定金属在电解质溶液中采用阳极保护的可能性,选择阳极保护的三个主要技术参数——致钝电流密度、维钝电流密度和钝化电位,必须测定阳极极化曲线。
三.实验仪器及用品恒电位仪,极化池,参比电极,辅助电极,工作电极,天平,量筒,水浴锅,温度计,搅拌棒,碳酸氢铵,氨水,无水酒精棉,水砂纸,四.实验步骤1. 配制实验溶液100毫升去离子水在水浴中加热至40度左右,放入22.9克碳酸氢铵,用玻璃棒搅拌至完全溶解,再加入9毫升氨水;2. 测定阳极极化曲线用水砂纸打磨工作电极至光亮,用无水酒精棉擦干待用;按照仪器要求连线,盐桥尖端与研究电极齐高,经教师确认无误方可开始实验;极化速度100mv/分钟。
实验完毕后拆线,整理实验台。
lgiab五.实验报告要求1.姓名、学号、班级2.试验目的:根据自己的理解简述3.实验原理:根据自己的理解简述,请勿抄书或实验讲义4.仪器药品及实验步骤:简述5.实验数据在表中列出实验数据6.数据处理作E-lgi曲线图,在图中标明致钝电流密度、维钝电流密度及钝化电位区间,并附表列出。
7.结果分析要求对所得的试验结果进行讨论分析,得出最终结论,文中引用参考文献处用上角标[1]的格式标明,并在试验报告后列出所引用的文献。

金属极化曲线测定及机理分析一、实验目的1. 了解测定金属极化曲线的意义和方法。
2. 了解自腐蚀电势、自腐蚀电流和钝化电势、钝化电流等概念以及它们的测定方法。
3. 了解电化学保护的概念、种类及其意义。
4. 了解CHI电化学工作站基本工作原理,掌握其使用方法。
二、基本原理将一种金属(电极)浸在电解液中,在金属与溶液之间就会形成电位,这种电位称为该金属在该溶液中的电极电位。
当有外加电流通过此电极(电解)时,其电极电位会发生变化,这种现象称为电极的极化。
如果电极为阳极,则电极电位将向正方向偏移,称为阳极极化;对于阴极,电极电位将向负方向偏移,称为阴极极化。
令:(16.1)图16.1 典型的阴、阳极极化曲线对于可逆电极,即为平衡电极电位; 对于不可逆电极,为系统达到稳态时的电极电位,即稳态电极电位,或称自腐蚀电位。
习惯上将电极电流密度为i 时对应的电极电位与平衡电极电位之差定义为在该电流密度时的过电位,用符号表示。
并规定阴、阳极的过电位均为正。
根据上述定义,可以分别写出阴、阳极的过电位计算公式为:过电位是一个很重要的电化学参量。
例如在金属电沉积中,析出金属的过电位越小,消耗的电能也就越少。
在电解提纯工艺中,往往借助改变析出金属的过电位,来改变金属的析出顺序,从而获得所需的金属,达到提纯的目的。
如前所述,过电位的大小与流经电极的电流密度有关,电极电位(或过电位)与电流密度的关系曲线称为极化曲线。
图16.1是一种典型的极化曲线。
随着电流密度的增加,电极电位将越来越偏离平衡电位,亦即过电位将越来越大。
极化曲线还常用半对数座标表示,如图16.2 所示。
考察图16.2 可知,当电流密度较大时,过电位与电流密度的对数成线性关系,即:式(16.4),式(16.5) 均称为塔菲尔(Tafel)公式。
图16.2 半对数极化曲线示意图事实上,对于任一电极总是同时存在着两个共轭反应(也可存在两对或两对以上的反应),一是还原反应:(16.6)与之相对应的共轭反应是氧化反应:(16.7)式中o为氧化态;R 为还氧态。


实验2:金属Zn阳极极化曲线的测量一、实验目的1.掌握阳极极化曲线测试的基本原理和方法;2.测定Zn电极在1M KOH溶液和1M ZnCl2溶液中的阳极极化曲线;3.通过实验理解金属电极钝化与活化过程。
二、实验原理线性电位扫描法是指控制电极电位在一定的电位范围内,以一定的速度均匀连续的变化,同时记录下各电位下反应的电流密度,从而得到电位-电流密度曲线,即稳态电流密度与电位之间的函数关系:i= f(ψ)。
特别适用于测量电极表面状态有特殊变化的极化曲线。
如下:如阳极钝化行为的阳极极化曲线。
阳极极化:金属作为阳极时在一定的外电势下发生的阳极溶解过程叫做阳极极化,金属的钝化现象:阳极的溶解速度随电位变正而逐渐增大。
这是正常的阳极溶出。
但当阳极电位正到某一数值时,其溶解速度达到一最大值。
此后阳极溶解速度随着电位变正,反而大幅度的降低,这种现象称为金属的钝化现象。
线性电位扫描法不但可以测定阴极极化曲线,也可以测定阳极极化曲线,特别适用于测定电极表面状态有特殊变化的极化曲线,如测定具有阳极钝化行为的阳极极化曲线,用线性电位扫描法测得的阳极极化曲线,如下图所示•AB段-----称为活性溶解区;此时金属进行正常的阳极溶解,阳极电流随电位改变服Tafel 公式的半对数关系。
•BC段-----称为钝化过渡区;此时是由于金属开始发生钝化,随着电极电位的正移,金属的溶解速度反而减小了。
•CD段-----称为钝化稳定区;在该区域中金属的溶解速度基本上不随电位二改变;•DE段-----称为过度钝化区;此时金属溶解速度重新随电位的正移而增大,为氧的析出或者高价金属离子的生成。
从阳极极化曲线上可以得到下列参数:c点对应的电位---临界钝化电位;c点对应的电流—临界钝化电流密度;而这些参数恒电流法是测不出来的。
影响金属钝化的因素很多,包括溶液的组成、金属的组成和结构以及外界条件。
三、仪器与试剂CHI电化学工作站、锌电极、Hg/HgO电极、甘汞电极、铂电极、三口电解槽、1M KOH溶液250ml、1M ZnCl2溶液250ml金属Zn是中性锌锰电池、碱性锌锰电池和锌-空气电池等的负极材料,其电化学行为受到广泛的研究。


点蚀研究方法--钝化曲线的测量1.金属的钝化原理在以金属作阳极的电解池中,通过电流时,通常会发生阳极的电化学溶解过程:M →M n++ne 。
当阳极的极化不太大时,溶解速度随着阳极电极电位(电极电位)的增大而增大,这是金属正常的阳极溶解。
但是在某些化学介质中,当阳极电极电位超过某一正值后,阳极的溶解速度随着阳极电极电位的增大反而大幅度地降低,这种现象称为金属的钝化。
研究金属的钝化过程,需要测定钝化曲线,通常用恒电位法。
将被研究金属例如铁、镍、铬等或其合金置于硫酸或硫酸盐溶液中即为研究电极,它与辅助电极(铂电极)组成一个电解池,同时它又与参比电极(硫酸亚汞电极)组成原电池。
以镍作阳极为例,其基本测量线路如图,这个测量回路实际上分为两部分,一是研究电极和辅助电极形成的极化回路,由mA 表测量极化电流的大小;二是参比电极与研究电极形成的电位测量回路。
图中WE 表示研究电极,CE 表示辅助电极,RE 表示参比电极。
参比电极与研究电极组成原电池,可确定研究电极的电位;辅助电极与研究电极组成电解池,使研究电极处于极化状态。
通过恒电位仪研究电极给定一个恒定电位后,测量与之对应准稳态电流值I 。
以通过研究电极的电流密度i 的对数lgi 对超电位作图,即得到金属的钝化曲线。
超电位η即为电速密度为i 时的阳极电极电位E(i)与i=0时的阳极电极电位之差:()(0)i ηϕϕ=-图是Fe 在1.0mol/L H 2SO 4溶液中的阴极极化和阳极极化曲线图。
AR 为阴极极化曲线,当对电极进行阴极极化时,阳极反应被抑制,阴极反应加速,电化学过程以H 2析出为主。
AB 为阳极极化曲线,当对电极进行阳极极化时,阴极反应被抑制,阳极反应加速,电化学图1.恒电位法测定金属钝化曲线 图2.阴极极化和阳极极化曲线图过程以Fe溶解为主。
在一定的极化电位范围内,阳极极化和阴极极化过程以活化极化为主,因此,电极的超电位与电流之间的关系均符合Tafel方程。

金属钝化是一种保护金属表面的方法,通过形成一层非活性的氧化膜来降低金属的化学活性,从而延长其使用寿命。
这一过程可以通过阳极极化曲线来进行研究和表征。
1. 介绍金属钝化的概念金属钝化是一种重要的表面处理技术,它可以提高金属材料的耐腐蚀性和机械性能。
在金属表面形成的氧化膜可以有效地防止金属与外界介质(如空气、水)发生化学反应,从而起到保护作用。
这一过程常常通过阳极极化曲线进行分析和研究。
2. 金属钝化过程的典型阳极极化曲线通常,金属钝化过程的阳极极化曲线呈现出三个典型区域:主动状态区、传质控制区和钝化区。
在主动状态区,金属处于活跃状态,电流密度随阳极电位的升高而增大;在传质控制区,金属表面开始形成氧化膜,电流密度逐渐减小;金属进入钝化区,在这一区域内,电流密度几乎不变,金属表面形成的稳定氧化膜起到了保护作用。
3. 讨论金属钝化过程中的关键因素金属钝化过程受到多种因素的影响,例如金属种类、表面处理方式、介质性质等。
在阳极极化曲线上,这些因素会导致曲线形状发生变化,反映出金属钝化过程的不同特点和表现。
4. 金属钝化在工程实践中的应用金属钝化技术在航空航天、汽车、船舶等领域有着广泛的应用。
通过对金属钝化过程的深入研究,可以更好地设计和选择适合的金属材料,并优化工艺参数,从而提高产品的耐用性和可靠性。
总结与展望金属钝化过程的典型阳极极化曲线是研究金属材料表面特性的重要手段,通过对这一曲线的深入理解,可以丰富我们对金属钝化机制的认识,为相关工程应用提供科学依据。
未来,随着材料科学和工程技术的不断发展,金属钝化技术必将得到进一步完善和应用推广。
个人观点金属钝化作为保护金属材料的一种有效方法,其研究对于提高材料的抗腐蚀性和机械性能具有重要意义。
阳极极化曲线作为研究金属钝化过程的重要工具,可以为我们揭示金属表面特性的变化规律,为工程实践提供强有力的支持。
在未来的研究中,我将继续关注金属钝化领域的最新进展,为推动该领域的发展贡献自己的力量。

实验十三阳极极化曲线的测定一、实验目的1.掌握用恒电位法测定金属极化曲线的原理和方法。
2.了解极化曲线的意义和应用。
二、实验原理1.阳极极化曲线为了探索电极过程的机理及影响电极过程的各种因素,必须对电极过程进行研究,在该研究过程中极化曲线的测定是重要的方法之一。
在研究可逆电池的电动势和电池反应时, 电极上几乎没有电流通过,每个电极或电池反应都是在无限接近于平衡条件下进行的,因此电极反应是可逆的。
当有电流通过电池时,则电极的平衡状态被破坏,此时电极反应处于不可逆状态,随着电极上电流密度的增加,电极反应的不可逆程度也随之增大。
在有电流通过电极时,由于电极反应的不可逆而使电极电位偏离平衡值的现象称为电极的极化。
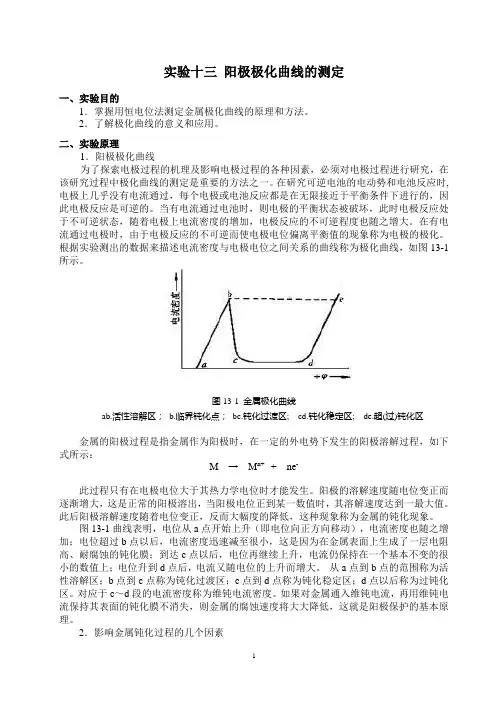
根据实验测出的数据来描述电流密度与电极电位之间关系的曲线称为极化曲线,如图13-1所示。
图13-1 金属极化曲线ab.活性溶解区;b.临界钝化点;bc.钝化过渡区; cd.钝化稳定区; de.超(过)钝化区金属的阳极过程是指金属作为阳极时,在一定的外电势下发生的阳极溶解过程,如下式所示:M →M n+ + ne-此过程只有在电极电位大于其热力学电位时才能发生。
阳极的溶解速度随电位变正而逐渐增大,这是正常的阳极溶出,当阳极电位正到某一数值时,其溶解速度达到一最大值。
此后阳极溶解速度随着电位变正,反而大幅度的降低,这种现象称为金属的钝化现象。
图13-1曲线表明,电位从a点开始上升(即电位向正方向移动),电流密度也随之增加;电位超过b点以后,电流密度迅速减至很小,这是因为在金属表面上生成了一层电阻高、耐腐蚀的钝化膜;到达c点以后,电位再继续上升,电流仍保持在一个基本不变的很小的数值上;电位升到d点后,电流又随电位的上升而增大。
从a点到b点的范围称为活性溶解区;b点到c点称为钝化过渡区;c点到d点称为钝化稳定区;d点以后称为过钝化区。
对应于c~d段的电流密度称为维钝电流密度。
如果对金属通入维钝电流,再用维钝电流保持其表面的钝化膜不消失,则金属的腐蚀速度将大大降低,这就是阳极保护的基本原理。

物理化学实验报告镍等金属钝化曲线的测定及腐蚀行为评价学院:班级:学号:姓名:指导教师:一、实验目的(1)掌握用线性电位扫描法测定镍在硫酸溶液中的阳极极化曲线和钝化行为。
(2)了解金属钝化行为的原理和测量方法。
(3)测定C1-浓度对Ni钝化的影响。
二、实验原理(一)金属的钝化金属处于阳极过程时会发生电化学溶解,其反应式为:M →Mn+ + ne-在金属的阳极溶解过程中,其电极电势必须大于其热力学电势,电极过程才能发生。
这种电极电势偏离其热力学电势的行为称为极化。
当阳极极化不大时,阳极过程的速率(即溶解电流密度)随着电势变正而逐渐增大,这是金属的正常溶解。
但当电极电势正到某一数值时,其溶解速率达到最大,而后,阳极溶解速率随着电势变正,反而大幅度降低,这种现象称为金属的钝化。
金属钝化一般可分为:化学钝化和电化学钝化。
金属之所以由活化状态转变为钝化状态,目前对此问题有着不同看法:(1)氧化膜理论:在钝化状态下,溶解速度的剧烈下降,是由于在金属表面上形成了具有保护性的致密氧化物膜的缘故。
(2)吸附理论:这是由于表面吸附了氧,形成氧吸附层或含氧化物吸附层,因而抑制了腐蚀的进行。
(3)连续模型理论:开始是氧的吸附,随后金属从基底迁移至氧吸附膜中,然后发展为无定形的金属-氧基结构。
各种金属在不同介质或相同介质中的钝化原因不尽相同,因此很难简单地用单一理论予以概括。
(二)影响金属钝化过程的几个因素(1)溶液的组成溶液中存在的H+、卤素离子以及某些具有氧化性的阴离子对金属钝化现象起着显著的影响。
在中性溶液中,金属一般是比较容易钝化的,而在酸性或某些碱性溶液中要困难得多。
(2)金属的化学组成和结构各种纯金属的钝化能力均不相同,以Fe、Ni、Cr种金属为例,易钝化的顺序Cr>Ni>Fe。
(3)外界因素当温度升高或加剧搅拌,都可以推迟或防止钝化过程的发生。
这显然是与离子的扩散有关。
在进行测量前,对研究电极活化处理的方式及其程度也将影响金属的钝化过程。

图2.1金属极化曲线ab 活性溶解区b 临界钝化点bc 过渡钝化区cd 稳定钝化区de 过(超)钝化区实验一钝化金属阳极极化曲线的测定一实验目的1、掌握用恒电流和恒电位法测定金属极化曲线的原理和方法。
2、通过阳极极化曲线的测定,判定实施阳极保护的可能性,初步选取阳极保护的技术参数。
3、掌握恒电位仪的使用方法。
二实验原理阳极电位和电流的关系曲线叫做阳极极化曲线。
为了判定金属在电解质溶液中采取阳极保护的可能性,选择阳极保护的三个主要技术参数——致钝电流密度、维钝电流密度和钝化区的电位范围,需要测定阳极极化曲线。
阳极极化曲线可以用恒电位法和恒电流发测定。
图2.1是一条典型的阳极极化曲线。
曲线abcde是恒电位法测得的阳极极化曲线。
当电位从a 逐渐向正向移动到b 点时,电流也随之增加到b 点,当电位过b 点以后,电流反而急剧减小,这是因为在金属表面上生成一层高电阻耐腐蚀的钝化膜,钝化开始发生。
人为控制电位的增高,电流逐渐衰减到c 。
在c 点之后,电位若继续增高,由于金属完全进入了钝态,电流维持在一个基本不变得很小的值——维钝电流。
当使电位增高到d 点以后,金属进入了过钝化状态,电流又重新增大。
从a 点到b 点的范围叫活性溶解区,从b 点到c 点叫钝化过渡区,从c 点到d 点叫钝化稳定区,过d 点以后叫过钝化区。
对应于b 点的电流密度叫致钝电流密度,对应于cd 段的电流密度叫维钝电流密度。
若把金属作为阳极,通以致钝电流使之钝化,再用维钝电流去保护其表面的钝化膜,可使金属的腐蚀速度大大降低,这就是阳极保护原理。
用恒电流法测不出上述曲线的bcde 段。
在金属受到阳极极化时其表面发生了复杂的变化,电极电位成为电流密度的多值函数,因此当电流增加到b 点时,电位即由b 点跃增到很正的e 点,金属进入了过钝化状态,反映不出金属进入钝化区的情况。
由此可见只有用行电位法才能测出完整的阳极极化曲线。
本实验采用恒电位仪逐点恒定阳极电位,同时测定对应的电流值,并在半对数坐标纸上绘成φ-lgi 曲线,即为恒电位阳极极化曲线。
阳极极化曲线的测定实验报告阳极极化曲线的测定实验报告引言:阳极极化曲线是用于研究金属在电化学腐蚀过程中的行为的重要工具。
通过测定金属在不同电位下的电流密度,可以得到阳极极化曲线,从而了解金属的腐蚀行为及其抗腐蚀性能。
本实验旨在通过测定铁的阳极极化曲线,探究其腐蚀行为及其抗腐蚀性能。
实验方法:1. 准备工作:将实验所需的试样铁片进行清洗和抛光,确保表面光洁无杂质。
2. 搭建电化学腐蚀实验装置:将试样铁片作为阳极,配备铂丝作为对电极,以及参比电极。
将试样铁片浸入含有适量电解液的电解池中。
3. 测定阳极极化曲线:通过改变电位,测定不同电位下的电流密度,记录数据并绘制阳极极化曲线。
实验结果:通过实验测定,得到了铁的阳极极化曲线,如图1所示。
曲线呈现出三个明显的区域:主动腐蚀区、穿孔区和过氧化物区。
在主动腐蚀区,随着电位的增加,电流密度逐渐增大,但增速较慢。
这是由于铁表面的氧化膜逐渐变厚,形成一层保护膜,阻止了进一步的氧化反应。
在穿孔区,电流密度急剧增大,表明铁开始发生局部腐蚀。
这是由于氧化膜中存在缺陷,使得金属表面暴露在电解液中,导致局部腐蚀的发生。
在过氧化物区,电流密度逐渐减小,说明铁的腐蚀速率降低。
这是由于过氧化物的生成,形成了一层致密的氧化膜,有效地抑制了进一步的腐蚀反应。
讨论与分析:通过实验测定的阳极极化曲线,我们可以对铁的腐蚀行为及其抗腐蚀性能进行一定的分析与评价。
首先,从主动腐蚀区的曲线斜率可以得到铁的腐蚀速率。
曲线斜率越大,说明腐蚀速率越快。
通过对比不同金属的阳极极化曲线,可以评估铁的腐蚀性能与其他金属的相对抗腐蚀性能。
其次,在穿孔区的曲线上,可以观察到局部腐蚀的发生。
穿孔区的位置与腐蚀环境有关,不同腐蚀环境下金属的穿孔区位置不同。
通过观察穿孔区的位置,可以评估铁在不同腐蚀环境中的腐蚀抗性。
最后,在过氧化物区的曲线上,可以观察到铁的腐蚀速率减缓。
过氧化物的生成可以形成一层致密的氧化膜,有效地抑制了进一步的腐蚀反应。
极化曲线的测定极化曲线的测定物理化学实验教案【⽬的要求】1. 掌握稳态恒电位法测定⾦属极化曲线的基本原理和测试⽅法。
2. 了解极化曲线的意义和应⽤。
3. 掌握恒电位仪的使⽤⽅法。
【实验原理】1. 极化现象与极化曲线为了探索电极过程机理及影响电极过程的各种因素,必须对电极过程进⾏研究,其中极化曲线的测定是重要⽅法之⼀。
我们知道在研究可逆电池的电动势和电池反应时,电极上⼏乎没有电流通过,每个电极反应都是在接近于平衡状态下进⾏的,因此电极反应是可逆的。
但当有电流明显地通过电池时,电极的平衡状态被破坏,电极电势偏离平衡值,图2-19-1 极化曲线电极反应处于不可逆状态,⽽且随着电极上电流密A-B:活性溶解区;B:临界钝化点B-C:度的增加,电极反应的不可逆程度也随之增⼤。
由过渡钝化区;C-D:稳定钝化区D-E:于电流通过电极⽽导致电极电势偏离平衡值的现超(过)钝化区象称为电极的极化,描述电流密度与电极电势之间关系的曲线称作极化曲线,如图2-19-1所⽰。
⾦属的阳极过程是指⾦属作为阳极时在⼀定的外电势下发⽣的阳极溶解过程,如下式所⽰:M?Mn++ne此过程只有在电极电势正于其热⼒学电势时才能发⽣。
阳极的溶解速度随电位变正⽽逐渐增⼤,这是正常的阳极溶出,但当阳极电势正到某⼀数值时,其溶解速度达到最⼤值,此后阳极溶解速度随电势变正反⽽⼤幅度降低,这种现象称为⾦属的钝化现象。
图2-19-1中曲线表明,从A点开始,随着电位向正⽅向移动,电流密度也随之增加,电势超过B点后,电流密度随电势增加迅速减⾄最⼩,这是因为在⾦属表⾯⽣产了⼀层电阻⾼,耐腐蚀的钝化膜。
B点对应的电势称为临界钝化电势,对应的电流称为临界钝化电流。
电势到达C点以后,1物理化学实验教案随着电势的继续增加,电流却保持在⼀个基本不变的很⼩的数值上,该电流称为维钝电流,直到电势升到D点,电流才有随着电势的上升⽽增⼤,表⽰阳极⼜发⽣了氧化过程,可能是⾼价⾦属离⼦产⽣也可能是⽔分⼦放电析出氧⽓,DE段称为过钝化区。
镍电极在硫酸溶液中极化(钝化)曲线的测定1.实验目的1.1了解金属钝化的原因和钝化行为的测定方法;1.2了解金属钝化行为的原理;1.3掌握用CHI660来测定镍电极在硫酸体系中不同KCl浓度时的阳极钝化曲线。
2.实验原理:2.1 金属的阳极与钝化过程:金属的阳极过程是指金属作为阳极发生电化学溶解的过程。
M → M n++ n e-在金属的阳极溶解过程中,其电极电势必须高于其热力学电势,电极过程才能发生。
这种电极电势偏离其热力学的现象称为极化。
当阳极极化不大时,极化的速率随着电势变正而逐渐增大,这就是金属的正常溶解。
当电极电势正到某一数值时,其溶解速率随着电势变正,反而大幅度地降低,这种现象称为金属钝化。
金属钝化一般可分为两种。
若把铁浸入浓硝酸(d>1.25)中,一开始铁溶解在酸中并放出NO,这时铁处于活化状态.经过一段时间后,铁几乎停止了溶解,此时的铁即使放在硝酸银溶液中也不能转换出银,这种现象称为化学钝化。
另一种钝化称为电化学钝化,即用阳极极化的方法使金属发生钝化。
金属处于钝化状态时,其溶解速率较小,一般为10-6~10-8 A/cm2。
金属之所以会由活化状态转变为钝化状态,至今还存在着不同的观点。
有人认为金属钝化是由于金属表面形成了一层保护性的致密氧化膜,因而阻止了金属的进一步溶解,称为氧化物理论;另一种观点则认为金属钝化是由于金属表面吸附了氧,形成了氧吸附层或氧化物吸附层,因而拟制了腐蚀的进行,称为表面吸附理论;第三种观点认为,开始是氧的吸附,随后金属从基底迁移至氧吸附膜中,然后发展为无定形的金属-氧基结构而使金属溶解速率降低,被称为连续模型理论。
2.2 研究金属钝化的方法:该实验是通过用恒电位法测定金属钝化曲线。
也就是说通过恒电位仪对研究电极给定一个恒定电位(即给定电位)后,测量与之对应的准稳态电流值(I),以阳极电位E给定与开路电位E开路之差,即过电位η对通过电极的电流密度j对数l舀作图,得如图1所示金属Ni钝化曲线示意图。
华南师范大学实验报告学生姓名学号专业年级、班级课程名称电化学实验实验项目金属Zn阳极极化曲线的测量实验类型✉验证✉设计✉综合实验时间实验指导老师实验评分一、实验目的1、掌握阳极极化曲线测试的基本原理和方法;2、测定Zn电极在1M NaOH溶液和1M ZnCl2溶液中的阳极极化曲线;3、通过实验理解金属电极钝化与活化过程。
二、实验原理金属Zn是中性锌锰电池、碱性锌锰电池和锌-空气电池等的负极材料,其电化学行为受到广泛的研究。
本实验应用线性电位扫描法测量金属Zn电极在1M KOH和1M ZnCl2中阳极极化曲线。
三、仪器与试剂CHI电化学工作站、锌电极、Hg/HgO电极、甘汞电极、铂电极、三口电解槽、1M KOH溶液250ml、1M ZnCl2溶液250ml四、实验步骤采用CHI 电化学工作站中的线性电位扫描法分别测量锌在下面2种溶液中的极化曲线:(1) 1M ZnCl2溶液中常温和450C的阳极极化曲线,电位扫描范围:开路电压测量值~ -0. 5V;(2)1M KOH溶液中常温和450C的阳极极化曲线,电位扫描范围:开路电压测量值~ -1. 0V;扫描速度0. 005V /S。
1.接好线路。
2. 1M ZnCl2溶液中常温和450C的阳极极化曲线(1)将待测锌电极的一面用金相砂纸打磨,除去氧化膜,用去离子水冲洗干净,再用滤纸吸干,放进电解池中。
电解池中的辅助电极为铂电极,参比电极为甘汞电极,电解池中注入1M ZnCl2溶液。
(2) 启动工作站,运行CHI 测试软件。
测量并记录开路电压值。
在Setup 菜单中点击"Technique"选项。
在弹出菜单中选择"Linear Sweep Voltammetry" 测试方法,然后点击OK按钮。
(3) 在Setup 菜单中点击"Parameters"选项。
在弹出菜单中输入测试条件:Init E为开路电压测量值,Final E为-0.5V,Scan Rate为0. 005V / s,Sample Interval 为0.001 V,Quiet Time为2s,Sensitivity为1e-6,选择Auto-sensitivity。