蛋白质检验原始记录表格格式
- 格式:docx
- 大小:558.12 KB
- 文档页数:2
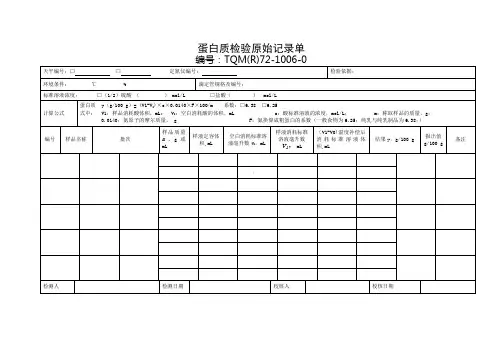

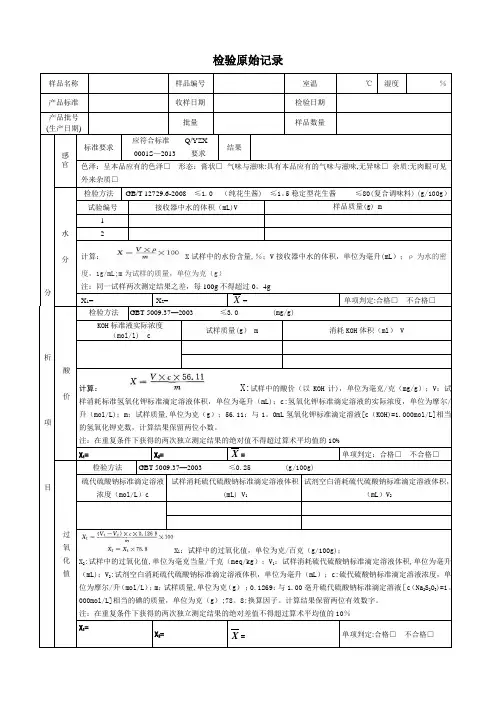
样品名称样品编号室温℃湿度%产品标准收样日期检验日期产品批号(生产日期)批量样品数量分析项目感官标准要求应符合标准Q/YZX0001S—2013 要求结果色泽:呈本品应有的色泽□形态:膏状□气味与滋味:具有本品应有的气味与滋味,无异味□杂质:无肉眼可见外来杂质□水分检验方法GB/T 12729.6-2008 ≤1.0 (纯花生酱) ≤1。
5稳定型花生酱≤80(复合调味料) (g/100g)试验编号接收器中水的体积(mL)V 样品质量(g) m12计算: X试样中的水份含量,%;V接收器中水的体积,单位为毫升(mL);ρ为水的密度,1g/mL;m为试样的质量,单位为克(g)注:同一试样两次测定结果之差,每100g不得超过0。
4gX1= X2= X= 单项判定:合格□不合格□酸价检验方法GBT 5009.37—2003 ≤3.0 (mg/g)KOH标准液实际浓度(mol/l) c试样质量(g) m 消耗KOH体积(ml) V计算:X:试样中的酸价(以KOH计),单位为毫克/克(mg/g);V:试样消耗标准氢氧化钾标准滴定溶液体积,单位为毫升(mL);c:氢氧化钾标准滴定溶液的实际浓度,单位为摩尔/升(mol/L);m:试样质量,单位为克(g);56.11:与1。
0mL氢氧化钾标准滴定溶液[c(KOH)=1.000mol/L]相当的氢氧化钾克数,计算结果保留两位小数。
注:在重复条件下获得的两次独立测定结果的绝对值不得超过算术平均值的10%X1= X2= X= 单项判定:合格□不合格□过氧化值检验方法GBT 5009.37—2003 ≤0.25 (g/100g)硫代硫酸钠标准滴定溶液浓度(mol/L)c试样消耗硫代硫酸钠标准滴定溶液体积(mL) V1试剂空白消耗硫代硫酸钠标准滴定溶液体积,(mL)V2X1:试样中的过氧化值,单位为克/百克(g/100g);X2:试样中的过氧化值,单位为毫克当量/千克(meq/kg);V1:试样消耗硫代硫酸钠标准滴定溶液体积,单位为毫升(mL);V2:试剂空白消耗硫代硫酸钠标准滴定溶液体积,单位为毫升(mL);c:硫代硫酸钠标准滴定溶液浓度,单位为摩尔/升(mol/L);m:试样质量,单位为克(g);0.1269:与1.00亳升硫代硫酸钠标准滴定溶液[c(Na2S2O3)=1。

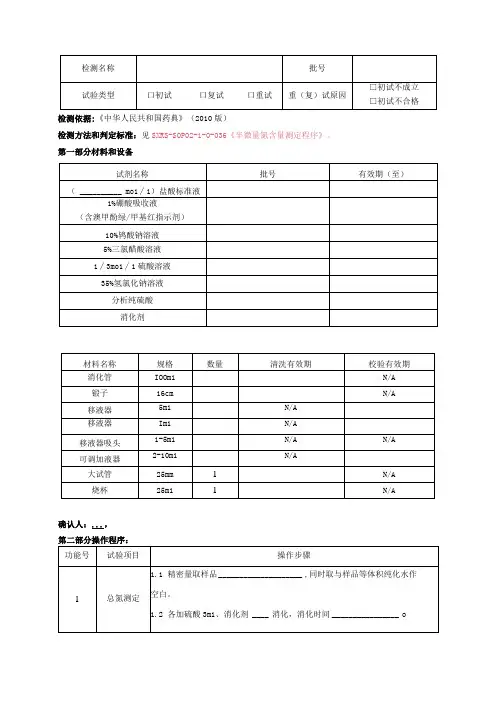

蛋白质原始记录表
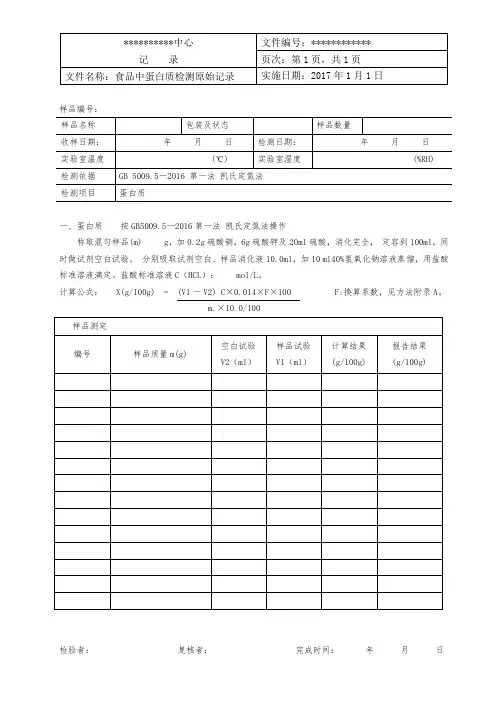
蛋白质原始检验记录
产品名称
检测方法:
称取0.0995g±0.1005g样品于100ml容量瓶,用纯化水定容,溶解,精密量取1.0ml供试品溶液于10ml具塞刻度管,加5ml碱性铜,摇匀,室温放置10分钟,快速加入0.5ml酚试剂,摇匀,室温放置30分钟。
用分光光度计检测。
检测温度:20℃。
计算公式:平均值=(检测值A+检测值B+检测值C)÷3 蛋白含量=吸光度/稀释倍数(100)/标准曲线斜率(0.2023)/称样量批号检验号日期称样量g 检测值蛋白含量备注检测人:复核人:批号检验号日期称样量g 检测值蛋白含量备注检测人:复核人:。
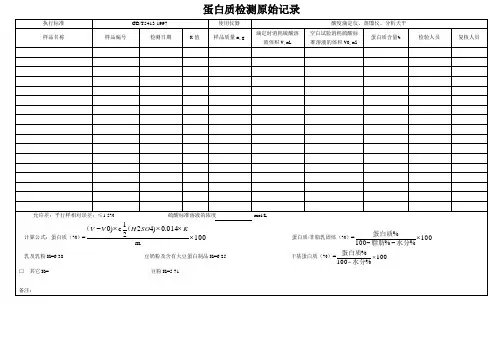


HY4-04-055
烟台浩洋农业科技有限公司
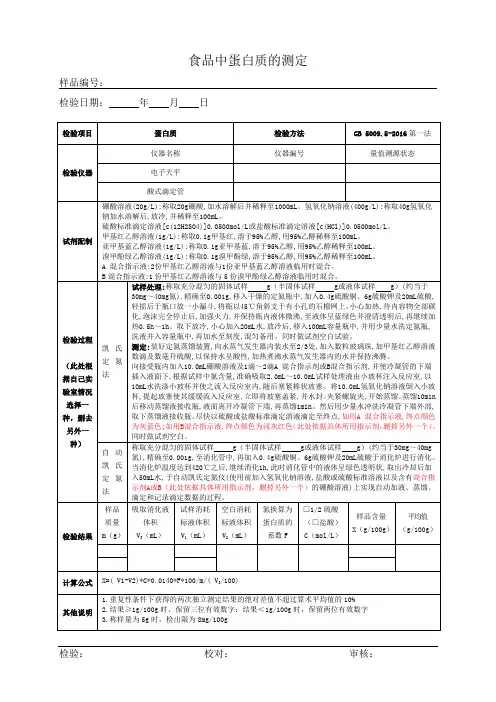
蛋白质测定记录
样品编号:
样品名称:检测项目:
样品状态:检测依据、方法:
检测日期:实验室环境:室温℃,相对湿度% 标准滴定溶液、编号:滴定管名称、编号:
配制日期:标准滴定溶液浓度:
主要检测仪器□分析天平,量程0-210g,精度0.1mg。
□凯氏定氮仪
□滴定管,量程0-50ml,精度0.02ml。
样品前处理方法
□称取试样m,放入凯氏烧瓶中,加入6g硫酸钾(或硫酸钠)、0.4g硫酸铜、12mL浓硫酸和2粒玻璃珠充分混匀,加热消化至蓝色透明,定容。
取试液蒸馏、定氮。
滴定
数据
空白消耗标准液V0= mL
样品分号取样量
m
定容体
积V1
测定用
体积V2
试样消耗标准液体积
V
计算结果
X
平均值
X
相对偏
差
报告值
X
g mL mL mL g/100g g/100g % g/100g
1 2
计算公式
()
()
100
1000
/
100
/
1
2
0⨯
⨯
⨯
⨯
⨯
⨯
-
=F
V
V
m
M
c
V
V
g
g
X
X——试样中被测物质含量,以计;
c——标准溶液浓度;
M =0.014g/mol,与标准溶液相当的、以克表示氮的质量;
F——氮换算为蛋白质的平均系数:F= .审核:检验:。
蛋白质含量测定1.考马斯亮兰微量法:(1) 取10ml浓度为0.1mg/ml的标准蛋白。
(2) 取17支试管,分别编号后按表上剂量依次加入标准蛋白(或未知蛋白)、去离子水和考马斯亮兰染料。
每支试管加完后,立即在漩涡混合器上混合。
(3) 加完染料5-20min内,用UNIC7202B可见分光光度计,塑料常量可见比色杯,在595nm处测量吸光度A595值。
空白对照为1号试管。
(4) 数据处理:标准蛋白浓度(mg/ml)为横坐标,A595为纵坐标,进行直线拟合,得到标准曲线。
根据测得的未知样品的A595,查表即可求得未知样品的蛋白质含量。
考马斯亮兰微量法实验数据表2.紫外吸收法:(1) 取15ml浓度为1.0mg/ml的标准蛋白。
(2) 取14支试管,分别编号后按表上剂量依次加入标准蛋白(或未知蛋白)、去离子水, 每支试管加完后,立即在漩涡混合器上混合。
(3) 使用SPECORD200紫外可见分光光度计,微量塑料紫外比色皿,在280nm处测量吸光度A280。
空白对照为1号试管。
(4) 用标准蛋白浓度(mg/ml)为横坐标,用A280为纵坐标,进行直线拟合,得到标准曲线。
根据测得的未知样品的A280,查表即可求得未知样品的蛋白质含量。
紫外吸收法实验数据表做出标准曲线得到未知蛋白浓度,计算出该蛋白质的百分吸光度值A1%1cm= (280nm)注意事项:1.标准曲线上每个实验点要做两个平行实验,最后取平均值作图,若差别太大.需要重做。
2.配的标准蛋白浓度为1.0mg/ml.取1.0ml浓度为1.0mg/ml的标准蛋白,加入9.0ml去离子水。
配成考马斯亮蓝法中的标准蛋白(0.1mg/ml)。
3.每组取标准蛋白-15ml备用。
取考马斯亮蓝溶液60ml备用。
未知蛋白取6ml备用。
4.比较两种方法测定的未知蛋白数值,並进行讨论。