2009年高考四川理综化学试题和参考答案
- 格式:doc
- 大小:259.50 KB
- 文档页数:6
2009年普通高等学校招生全国统一考试(四川卷)理科综合测试试题第Ⅰ卷本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Al 27 S 32 K39 Mn 55一、选择题(本题包括13小题。
每小题只有一个....选项符合题意)1.下列关于哺乳动物体内三大营养物质代谢的叙述,不正确...的是A. 用15N标记的苯丙氨酸饲喂小鼠后,在其体内检测不到15N标记的酪氨酸B. 当体内脂肪的分解速度加快时,意味着糖类的供应不足C. 肝细胞中内质网的功能出现障碍,脂蛋白的合成受阻D. 肝糖元和肌糖元去路的差异,与所在细胞功能密切相关2.下列关于几种微生物的营养代谢和生长繁殖的描述,正确的是A.根瘤菌通过生物固氮,制造了含氮养料和含碳有机物B.接种到培养基上的青霉菌,进入对数期能大量积累有毒素C.培养液中溶氧量的变化,会影响酵母菌的生长繁殖和代谢途径D.用32P标记的噬菌体感染细菌,在新形成的噬菌体中都能检测到32PCO浓度升高引起的温室效应,可能改变土壤水分状况和矿质元素含量。
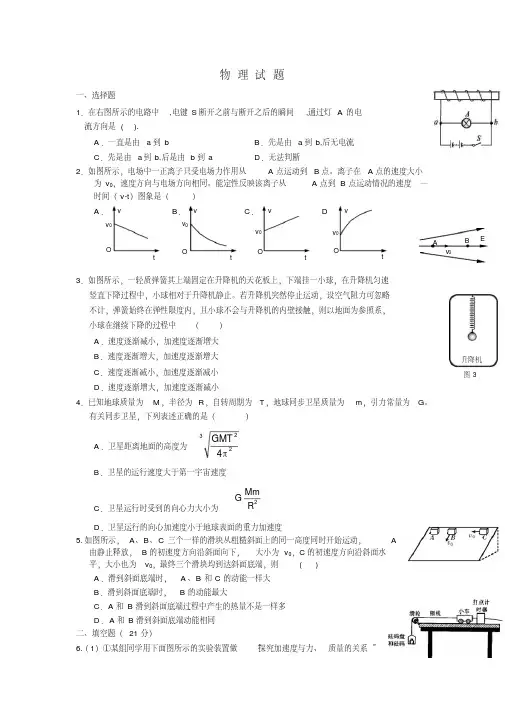
为探究3.大气中2有关生态因子的变化对植物的影响,有人用同一环境中生长的两种植物,在温度、光照和水的是分等适宜条件下做了模拟试验,测得数据如表。
下列相关分析,不正确*蒸腾比率:植物消耗1摩尔水,通过光合作用固定的2CO浓度升高和施磷肥都能促进两种植物的光合作用,施磷肥的效果更明显A.2CO浓度下,施磷肥对石楠光合作用的促进作用都大于欧洲蕨B.两种2C.由试验结果可推测,干旱对欧洲蕨光合作用的影响大于石楠CO浓度都高于355 μmol·mol-1D.两种植物光合作用的最适24.下列关于高等动物神经调节和体液调节的叙述,正确的是A. 寒冷环境中肾上腺素分泌量增加,将引起骨骼肌不自主战粟B. 刺激大脑皮层中央前回的底部,可以引起上肢的运动C. 垂体通过下丘脑分泌的相关激素调控甲状腺、性腺等内分泌腺的活动D. 神经元受刺激产生的兴奋,沿轴突传递给下一个细胞只能是单向的5.病原体对不同免疫状态小鼠的感染进程如图所示。

2009年普通高等学校招生全国统一考试试卷答案(全国2)理科综合(化学部分)本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
第Ⅰ卷1至5页,第Ⅱ卷6至14页。
考试结束后,将本试卷和答题卡一并交回。
注意事项:1. 答卷前,考生务必将自己的姓名,准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上指定位置。
2. 选择题每小题选出答案后,用2B 铅笔将答题卡上,对应题目的答案标号涂写,如需改动,用橡皮擦干净后,再选涂其它答案标号,答在试题卷上无效。
3. 非选择题用0.5毫米的黑色墨水签字笔答在答题卡上每题对应的答题区域内,答在试题卷上无效。
4. 考试结束,请将本试题卷和答题卡一并上交。
第Ⅰ卷 (选择题)本卷共21小题,每小题6分,共126分。
以下数据可供解题时参考: 相对原子质量(原子量):H – 1 C – 12 N – 14 O - 16第Ⅰ卷 (选择题)本卷共21小题,每小题6分,共126分。
以下数据可供解题时参考: 相对原子质量(原子量):H – 1 C – 12 N – 14 O - 16一、 选择题(本题共13小题。
在每小题给出的四个选项中,只有一项是符合题目要求的。
)6. 物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N 2O ,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是 A. 1:4 B.1:5 C. 2:3 D.2:5 答案A【解析】设2m o lZ n 参与反应7.下列关于溶液和胶体的叙述,正确的是 A. 溶液是电中性的,胶体是带电的 B. 通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 C. 溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 D. 一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有 答案D 【解析】胶体本身是不带电,只是其表面积较大,吸附了溶液中的离子而带了电荷,故A 项错;溶液中的溶质,要看能否电离,若是非电解质,则不导电,也即不会移动,B 项错;溶液中溶质粒子没有规律,C 项错;丁达尔效应可以用来区分溶液和胶体,D 项正确。

2009年全国高考理综试题答案(四川卷)第1卷包括21小题,每小题6分,共126分。
一、选择题:选对的给6分,选错或未选的给0分。
1.A 2.C 3.C 4.D 5.B 6.A 7.B8.D 9.B 10.D 11.C 12.B 13.C二、选择题:每小题全部选对得6分,选对但不全的得3分,有选错的得0分。
14.D 15.A 16.B 17.C 18.C 19.D20.AD 21.AB第II卷包括10小题,共174分。
22.(17分)解:(1)①设计的电路如图。
(只要电路能正常工作且电流表测量的是通过ab的电流,电路设计就算正确。
)(3分)23.(16分)解:(1)设起重机允许输出的最大功率为P0,重物达到最大速度时,拉力F0等于重力。
P0=F0m①P0=mg②代入数据,有:P0=5.1×104W ③说明:①式2分,②③式各1分。
(2)匀加速运动结束时,起重机达到允许输出的最大功率,设此时重物受到的拉力为F,速度为v1,匀加速运动经历时间为t1,有:P0=Fv1 ④F-mg=ma⑤V1=at1 ⑥由③④⑤⑥,代入数据,得:t1=5 s ⑦t=2 s时,重物处于匀加速运动阶段,设此时速度为v2,输出功率为P,则=at ⑧P=F⑨由⑤⑧⑨,代入数据,得:P=2.04×104W ⑩说明④⑤⑥⑦⑧⑨式各2分,⑦⑩式各1分。
24.(19分)解:(1)小滑块运动到位置时速度为v1,由动能定理有:25.(20分)解:(1)设弹簧的弹力做功为W,有:27.(15分)28.(14分)29.(15分)(1)为了防止亚铁化合物被氧化30.(22分)Ⅰ.(12分)(1)胰蛋白酶(1分)(2)胰岛B (1分)胰岛B细胞分泌的胰岛素是唯一降血糖的激素(3分)(3)基因的选择性表达(胰岛素基因的表达)(2分)(4)能(1分)细胞核含有该物种所特有的全套遗传物质(细胞核的全能性)(2分)Ⅱ(10分)(1)19:30(或E点(2分)(2)B点(或10:00)C点(或12:00)(2分)(3)C点(或12:00)(1分)(4)①a.样本量太小。

2009年普通高等学校招生全国统一考试理综(四川卷,解析版)第Ⅰ卷本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Al 27 S 32 K39 Mn 55一、选择题(本题包括13小题。
每小题只有一个....选项符合题意)1.下列关于哺乳动物体内三大营养物质代谢的叙述,不正确...的是A. 用15N标记的苯丙氨酸饲喂小鼠后,在其体内检测不到15N标记的酪氨酸B. 当体内脂肪的分解速度加快时,意味着糖类的供应不足C. 肝细胞中内质网的功能出现障碍,脂蛋白的合成受阻D. 肝糖元和肌糖元去路的差异,与所在细胞功能密切相关答案:A.解析:本题考察了三大营养物质代谢的相关问题。
A选项中15N标记的苯丙氨酸饲喂小鼠后,通过氨基酸的代谢,在其体内仍可能检测到15N标记的酪氨酸,A错误;B中当糖类的供应不足时,只有加快脂肪的分解速度来提供生物体生长代谢所需的能量,B正确;C中内质网是脂质的合成和蛋白质加工的场所;D中肌糖元不能转化是因为肌细胞代谢旺盛,当肌糖原转化成葡萄糖后直接被细胞代谢利用,不能进入到血液中成为血糖。
2.下列关于几种微生物的营养代谢和生长繁殖的描述,正确的是A.根瘤菌通过生物固氮,制造了含氮养料和含碳有机物B.接种到培养基上的青霉菌,进入对数期能大量积累有毒素C.培养液中溶氧量的变化,会影响酵母菌的生长繁殖和代谢途径D.用32P标记的噬菌体感染细菌,在新形成的噬菌体中都能检测到32P2. 答案:C.解析:本题考察了几种微生物的营养代谢和生长繁殖的问题。
A中根瘤菌通过生物固氮不能制造含碳有机物;B中接种到培养基上的青霉菌,进入稳定期能大量积累有毒素;C中酵母菌是兼性厌氧型生物,故溶氧量的变化,会影响酵母菌的生长繁殖和代谢途径,C正确;D中用32P 标记的噬菌体感染细菌,在新形成的噬菌体中只有两个噬菌体能检测到32P3.大气中2CO浓度升高引起的温室效应,可能改变土壤水分状况和矿质元素含量。



2009年普通高等学校招生全国统一考试(四川卷)理科综合测试试题第Ⅰ卷本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Al 27 S 32 K 39 Mn 55一、选择题(本题包括13小题。
每小题只有一个....选项符合题意) 1.下列关于哺乳动物体内三大营养物质代谢的叙述,不正确...的是 A. 用15N 标记的苯丙氨酸饲喂小鼠后,在其体内检测不到15N 标记的酪氨酸B. 当体内脂肪的分解速度加快时,意味着糖类的供应不足C. 肝细胞中内质网的功能出现障碍,脂蛋白的合成受阻D. 肝糖元和肌糖元去路的差异,与所在细胞功能密切相关2.下列关于几种微生物的营养代谢和生长繁殖的描述,正确的是A. 根瘤菌通过生物固氮,制造了含氮养料和含碳有机物B. 接种到培养基上的青霉菌,进入对数期能大量积累有毒素C. 培养液中溶氧量的变化,会影响酵母菌的生长繁殖和代谢途径D. 用32P 标记的噬菌体感染细菌,在新形成的噬菌体中都能检测到32P3.大气中CO 2浓度升高引起的温室效应,可能改变土壤水分状况和矿质元素含量。
为探究有关生态因子的变化对植物的影响,有人用同一环境中生长的两种植物,在温度、光照和水分等适宜条件下做了模拟试验,测得数据如表。
下列相关分析,不正确的是*蒸腾比率:植物消耗1摩尔水,通过光合作用固定的CO 3微摩尔数。
A. CO 2浓度升高和施磷肥都能促进两种植物的光合作用,施磷肥的效果更明显B. 两种CO 2浓度下,施磷肥对石楠光合作用的促进作用都大于欧洲蕨C. 由试验结果可推测,干旱对欧洲蕨光合作用的影响大于石楠D. 两种植物光合作用的最适CO 2浓度都高于355 μmol ·mol -14.下列关于高等动物神经调节和体液调节的叙述,正确的是A. 寒冷环境中肾上腺素分泌量增加,将引起骨骼肌不自主战粟B. 刺激大脑皮层中央前回的底部,可以引起上肢的运动C. 垂体通过下丘脑分泌的相关激素调控甲状腺、性腺等内分泌腺的活动D. 神经元受刺激产生的兴奋,沿轴突传递给下一个细胞只能是单向的5.病原体对不同免疫状态小鼠的感染进程如图所示。
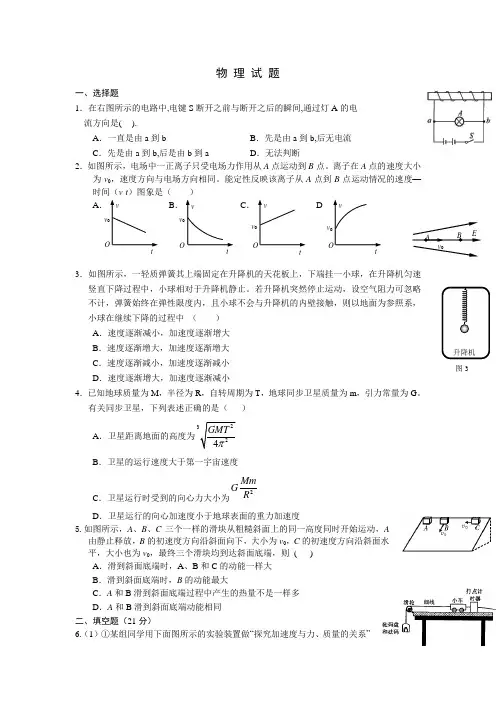
物 理 试 题一、选择题1.在右图所示的电路中,电键S 断开之前与断开之后的瞬间,通过灯A 的电 流方向是( ).A .一直是由a 到bB .先是由a 到b,后无电流C .先是由a 到b,后是由b 到aD .无法判断2.如图所示,电场中一正离子只受电场力作用从A 点运动到B 点。
离子在A 点的速度大小为v 0,速度方向与电场方向相同。
能定性反映该离子从A 点到B 点运动情况的速度—时间(v -t )图象是( )A .B .C . D3.如图所示,一轻质弹簧其上端固定在升降机的天花板上,下端挂一小球,在升降机匀速竖直下降过程中,小球相对于升降机静止。
若升降机突然停止运动,设空气阻力可忽略不计,弹簧始终在弹性限度内,且小球不会与升降机的内壁接触,则以地面为参照系,小球在继续下降的过程中 () A .速度逐渐减小,加速度逐渐增大 B .速度逐渐增大,加速度逐渐增大 C .速度逐渐减小,加速度逐渐减小 D .速度逐渐增大,加速度逐渐减小4.已知地球质量为M ,半径为R ,自转周期为T ,地球同步卫星质量为m ,引力常量为G 。
有关同步卫星,下列表述正确的是( )A .卫星距离地面的高度为B .卫星的运行速度大于第一宇宙速度C .卫星运行时受到的向心力大小为2Mm GRD .卫星运行的向心加速度小于地球表面的重力加速度5.如图所示,A 、B 、C 三个一样的滑块从粗糙斜面上的同一高度同时开始运动,A 由静止释放,B 的初速度方向沿斜面向下,大小为v 0,C 的初速度方向沿斜面水平,大小也为v 0,最终三个滑块均到达斜面底端,则 ( ) A .滑到斜面底端时,A 、B 和C 的动能一样大B .滑到斜面底端时,B 的动能最大C .A 和B 滑到斜面底端过程中产生的热量不是一样多D .A 和B 滑到斜面底端动能相同 二、填空题(21分)6.(1)①某组同学用下面图所示的实验装置做“探究加速度与力、质量的关系”v v v v EABv 0图3的实验.在探究加速度与力的关系过程中应保持 不变,用砝码和盘的重力作为小车所受外力,利用纸带算出小车的加速度,改变所挂钩码的数量,多次重复测量,进而研究加速度和力的关系.这种研究方法是 法.②在验证牛顿第二定律的实验中,得出若干组F 和a 的数据。

2009年普通高等学校招生全国统一考试(四川卷)理科综合测试试题第Ⅰ卷本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Al 27 S 32 K 39 Mn 55一、选择题(本题包括13小题。
每小题只有一个....选项符合题意)1.下列关于哺乳动物体内三大营养物质代谢的叙述,不正确...的是.A. 用15N标记的苯丙氨酸饲喂小鼠后,在其体内检测不到15N标记的酪氨酸B. 当体内脂肪的分解速度加快时,意味着糖类的供应不足C. 肝细胞中内质网的功能出现障碍,脂蛋白的合成受阻D. 肝糖元和肌糖元去路的差异,与所在细胞功能密切相关2.下列关于几种微生物的营养代谢和生长繁殖的描述,正确的是A.根瘤菌通过生物固氮,制造了含氮养料和含碳有机物B.接种到培养基上的青霉菌,进入对数期能大量积累有毒素C.培养液中溶氧量的变化,会影响酵母菌的生长繁殖和代谢途径D.用32P标记的噬菌体感染细菌,在新形成的噬菌体中都能检测到32P3.大气中CO浓度升高引起的温室效应,可能改变土壤水分状况和矿质元素含量。
为探究有2关生态因子的变化对植物的影响,有人用同一环境中生长的两种植物,在温度、光照和水分的是等适宜条件下做了模拟试验,测得数据如表。
下列相关分析,不正确CO微摩尔数。
2A.CO浓度升高和施磷肥都能促进两种植物的光合作用,施磷肥的效果更明显2B.两种CO浓度下,施磷肥对石楠光合作用的促进作用都大于欧洲蕨2C.由试验结果可推测,干旱对欧洲蕨光合作用的影响大于石楠D.两种植物光合作用的最适CO浓度都高于355 μmol·mol-124.下列关于高等动物神经调节和体液调节的叙述,正确的是A. 寒冷环境中肾上腺素分泌量增加,将引起骨骼肌不自主战粟B. 刺激大脑皮层中央前回的底部,可以引起上肢的运动C. 垂体通过下丘脑分泌的相关激素调控甲状腺、性腺等内分泌腺的活动D. 神经元受刺激产生的兴奋,沿轴突传递给下一个细胞只能是单向的5.病原体对不同免疫状态小鼠的感染进程如图所示。

09年高考全国理综卷II(化学部分)真题完全解析2009年普通高等学校招生全国统一考试理科综合(全国II )化学部分相对原子质量(原子量):H – 1 C – 12 N – 14 O - 166. 物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N 2O ,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是A. 1:4B.1:5C. 2:3D.2:5【答案】A【解析】设2m o l Z n 参与反应,因Z n 无剩余,则最终生成了2m o l Z n (N O 3)2,显然含有4m 7. 下列关于溶液和胶体的叙述,正确的是A.溶液是电中性的,胶体是带电的 B. 通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 D. 一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有【答案】D 【解析】胶体本身是不带电,只是其表面积较大,吸附了溶液中的离子而带了电荷,故A 项错;溶液中的溶质,要看能否电离,若是非电解质,则不导电,也即不会移动,B 项错;布朗运动本身即是无规律的运动,C 项错;丁达尔效应可以用来区分溶液和胶体,D 项正确。
8.下列叙述中正确的是 A. 向含有CaCO 3沉淀的水中通入CO 2 至沉淀恰好溶解,再向溶液中加入NaHCO 3 饱和溶液,又有CaCO 3沉淀生成B. 向Na 2 CO 3溶液中逐滴加入等物质的量的稀盐酸,生成的CO 2与原Na 2 CO 3的物质的量之比为1:2.C.等质量的NaHCO 3和Na 2 CO 3分别与足量盐酸反应,在同温同压下,生成的CO 2体积相同 D. 向Na 2 CO 3饱和溶液中通入CO 2,有NaHCO 3结晶析出【答案】D 【解析】CaCO 3与CO 2反应生成Ca(HCO 3)2,再加入NaHCO 3是没有现象的,A 项错;向Na 2CO 3溶液中逐滴加入等物质的量的稀盐酸,仅生成NaHCO 3,无CO 2气体放出,B 项错;等质量的NaHCO 3和Na 2CO 3,其中NaHCO 3的物质的量多,与足量HCl 反应时,放出的CO 2多,C 项错;D 项,发生的反应为:Na 2CO 3 + CO 2 + H 2O =2NaHCO 3↓,由于NaHCO 3的溶解性较小,故有结晶析出,正确。
2009年全国高考理综化学试题及答案-四川卷2009年普通高等学校招生全国统一考试(四川卷)理科综合测试试题第Ⅰ卷本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Al 27 S 32 K39 Mn 55一、选择题(本题包括13小题。
每小题只有一个....选项符合题意)6.开发新材料是现代科技发展的方向之一。
下列有关材料的说法正确的是 A. 氮化硅陶瓷是新型无机非金属材料 B. C 60属于原子晶体,用于制造纳米材料C. 纤维素乙酸酯属于天然高分子材料D. 单晶硅常用于制造光导纤维A.无色溶液:2Ca+、、H +、Cl -、3HSO -B.能使pH 试纸呈红色的溶液:Na +、NH +4、I -、3NO -C.FeCl 2溶液:K +、、Na +、、24SO -、、2AlO -D.()Kw c H +=0.1 mol/L 的溶液:Na +、K +、23SiO -、3NO - 9.25 ℃,101 k Pa 时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol ,辛烷的燃烧热为5518 kJ/mol 。
下列热化学方程式书写正确的是A.2H +(aq) +24SO -(aq)+2Ba +(aq)+2OH -(aq)=BaSO 4(s)+2H 2O(1);?H=-57.3 kJ/molB.KOH(aq)+12H 2 SO 4(aq)= 12K 2SO 4(aq)+H 2O(I); ?H=-57.3kJ/molC.C 8H 18(I)+252O 2 (g)=8CO 2 (g)+ 9H 2O; ?H=-5518 kJ/mol D.2C 8H 18(g)+25O 2 (g)=16CO 2 (g)+18H 2O(1); ?H=-5518 kJ/mol10.X 、Y 、Z 、M 是元素周期表中前20号元素,其原子序数依次增大,且X 、Y 、Z 相邻。
2009年普通高等学校招生全国统一考试(四川卷)理科综合测试试题第Ⅰ卷本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Al 27 S 32 K 39 Mn 55 一、选择题(本题包括13小题。
每小题只有一个....选项符合题意)1.下列关于哺乳动物体内三大营养物质代谢的叙述,不正确...的是.w.w.k.s.5.u.c.o.mA. 用15N标记的苯丙氨酸饲喂小鼠后,在其体内检测不到15N标记的酪氨酸B. 当体内脂肪的分解速度加快时,意味着糖类的供应不足C. 肝细胞中内质网的功能出现障碍,脂蛋白的合成受阻D. 肝糖元和肌糖元去路的差异,与所在细胞功能密切相关答案:A.解析:本题考察了三大营养物质代谢的相关问题。
A选项中15N标记的苯丙氨酸饲喂小鼠后,通过氨基酸的代谢,在其体内仍可能检测到15N标记的酪氨酸,A错误;B中当糖类的供应不足时,只有加快脂肪的分解速度来提供生物体生长代谢所需的能量,B正确;C中内质网是脂质的合成和蛋白质加工的场所;D中肌糖元不能转化是因为肌细胞代谢旺盛,当肌糖原转化成葡萄糖后直接被细胞代谢利用,不能进入到血液中成为血糖。
2.下列关于几种微生物的营养代谢和生长繁殖的描述,正确的是A.根瘤菌通过生物固氮,制造了含氮养料和含碳有机物B.接种到培养基上的青霉菌,进入对数期能大量积累有毒素C.培养液中溶氧量的变化,会影响酵母菌的生长繁殖和代谢途径D.用32P标记的噬菌体感染细菌,在新形成的噬菌体中都能检测到32P2. 答案:C.解析:本题考察了几种微生物的营养代谢和生长繁殖的问题。
A中根瘤菌通过生物固氮不能制造含碳有机物;B中接种到培养基上的青霉菌,进入稳定期能大量积累有毒素;C中酵母菌是兼性厌氧型生物,故溶氧量的变化,会影响酵母菌的生长繁殖和代谢途径,C正确;D中用32P标记的噬菌体感染细菌,在新形成的噬菌体中只有两个噬菌体能检测到32PCO浓度升高引起的温室效应,可能改变土壤水分状况和矿质元素含量。
2009年高考试题——理综(四川卷及答案2009年普通高等学校招生全国统一考试(四川卷)理科综合测试试题第Ⅰ卷本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Al 27 S 32 K 39 Mn 55一、选择题(本题包括13小题。
每小题只有一...个.选项符合题意)1.下列关于哺乳动物体内三大营养物质代谢的叙述,不正确...的是A. 用15N标记的苯丙氨酸饲喂小鼠后,在其体内检测不到15N标记的酪氨酸B. 当体内脂肪的分解速度加快时,意味着糖类的供应不足C. 肝细胞中内质网的功能出现障碍,脂蛋白的合成受阻D. 肝糖元和肌糖元去路的差异,与所在细胞功能密切相关2.下列关于几种微生物的营养代谢和生长繁殖的描述,正确的是A.根瘤菌通过生物固氮,制造了含氮养料和含碳有机物B.接种到培养基上的青霉菌,进入对数期能大量积累有毒素C.培养液中溶氧量的变化,会影响酵母菌的生长繁殖和代谢途径D.用32P标记的噬菌体感染细菌,在新形成的噬菌体中都能检测到32P3.大气中CO浓度升高引起的温室效应,可能改变2土壤水分状况和矿质元素含量。
为探究有关生态因子的变化对植物的影响,有人用同一环境中生长的两种植物,在温度、光照和水分等适宜条件下做了模拟试验,测得数据如表。
下列相关分析,不正确...的是*蒸腾比率:植物消耗1摩尔水,通过光合作用固定的CO微摩尔数。
2A.CO浓度升高和施磷肥都能促进两种植物的光2合作用,施磷肥的效果更明显B.两种CO浓度下,施磷肥对石楠光合作用的促2进作用都大于欧洲蕨C.由试验结果可推测,干旱对欧洲蕨光合作用的影响大于石楠D.两种植物光合作用的最适CO浓度都高于3552μmol·mol-14.下列关于高等动物神经调节和体液调节的叙述,正确的是A.寒冷环境中肾上腺素分泌量增加,将引起骨骼肌不自主战粟B.刺激大脑皮层中央前回的底部,可以引起上肢的运动C.垂体通过下丘脑分泌的相关激素调控甲状腺、性腺等内分泌腺的活动D.神经元受刺激产生的兴奋,沿轴突传递给下一个细胞只能是单向的5.病原体对不同免疫状态小鼠的感染进程如图所示。
2009年普通高等学校招生全国统一考试(四川卷)理科综合测试试题第Ⅰ卷本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Al 27 S 32 K39 Mn 55一、选择题(本题包括13小题。
每小题只有一个....选项符合题意)1.下列关于哺乳动物体内三大营养物质代谢的叙述,不正确...的是A. 用15N标记的苯丙氨酸饲喂小鼠后,在其体内检测不到15N标记的酪氨酸B. 当体内脂肪的分解速度加快时,意味着糖类的供应不足C. 肝细胞中内质网的功能出现障碍,脂蛋白的合成受阻D. 肝糖元和肌糖元去路的差异,与所在细胞功能密切相关2.下列关于几种微生物的营养代谢和生长繁殖的描述,正确的是A.根瘤菌通过生物固氮,制造了含氮养料和含碳有机物B.接种到培养基上的青霉菌,进入对数期能大量积累有毒素C.培养液中溶氧量的变化,会影响酵母菌的生长繁殖和代谢途径D.用32P标记的噬菌体感染细菌,在新形成的噬菌体中都能检测到32PCO浓度升高引起的温室效应,可能改变土壤水分状况和矿质元素含量。
为探究3.大气中2有关生态因子的变化对植物的影响,有人用同一环境中生长的两种植物,在温度、光照和水的是分等适宜条件下做了模拟试验,测得数据如表。
下列相关分析,不正确*蒸腾比率:植物消耗1摩尔水,通过光合作用固定的2CO浓度升高和施磷肥都能促进两种植物的光合作用,施磷肥的效果更明显A.2CO浓度下,施磷肥对石楠光合作用的促进作用都大于欧洲蕨B.两种2C.由试验结果可推测,干旱对欧洲蕨光合作用的影响大于石楠CO浓度都高于355 μmol·mol-1D.两种植物光合作用的最适24.下列关于高等动物神经调节和体液调节的叙述,正确的是A. 寒冷环境中肾上腺素分泌量增加,将引起骨骼肌不自主战粟B. 刺激大脑皮层中央前回的底部,可以引起上肢的运动C. 垂体通过下丘脑分泌的相关激素调控甲状腺、性腺等内分泌腺的活动D. 神经元受刺激产生的兴奋,沿轴突传递给下一个细胞只能是单向的5.病原体对不同免疫状态小鼠的感染进程如图所示。
2009年高考理综全国I 卷化学试题和参考答案第I 卷一、选择题(本题共13小题。
在每小题给出的四个选项中,只有一项是符合题目要求的) 6.下列各组离子,在溶液中能大量共存、加入NaOH 溶液后加热既有气体放出又有沉淀生成的一组是A.Ba 2+、3N O -、4N H +、Cl - B. 2C a +、3H C O -、4N H +、2A lO - C.K +、Ba 2+、Cl -、3H SO - D. 2M g + 、4N H +、24SO -、K +7. 将15ml.2mol•.1L -23N a C O 溶液逐滴加入到40 ml.0.5mol•.1L -n M C l 盐溶液中,恰好将溶液中的n M+离子完全沉淀为碳酸盐,则n M C l 中n 值是A. 4B. 3C. 2D. 1 8.下列表示溶液中发生反应的化学方程式错误..的是 A.22222223AL NaOH H O NaALO H ++=+↑B.4242222K M nO H C O O K K O H K M nO C O H O ++=+↑+C 22224(2M nO H C l M nC l C l H O ∆+=+↑+浓)D.22742424324324267()3()7K Cr O FeSO H SO Cr SO Fe SO K SO H O ++=+++ 9. 现有乙酸和两种链状单烯烃混合物,其中氧的质量分数为a,则碳的质量分数是A.(1)7a - B.34a C.6(1)7a - D.12(1)13a -10. 用0.1 mol•.1L -的盐酸滴定0.10 mol•.1L -的氨水,滴定过程中不可能...出现的结果是 A.4()c N H +>()c C l -,()c O H - >()c H +B. 4()c N H +=()c C l -,()c O H - =()c H +C.()c C l - >4()c N H +,()c O H - >()c H +D. ()c C l - >4()c N H +,()c H +>()c O H -11. 为了检验某含有3N aH C O 杂质的23N a C O 样品的纯度,现将1w 克样品加热,其质量变为2w g,,则该样品的纯度(质量分数)是A.211845331w w w - B.12184()31w w w -C.211734231w w w - D.2111158431w w w -12. 有关下图所示化合物的说法不正确的是A.既可以与Br 2的CCl 4溶液发生加成反应,又可以在光照下与Br 2发生取代反应B.1mol 该化合物最多可以与3molNaOH 反应C.既可以催化加氢,又可以使酸性KmnO 4溶液褪色D.既可以与Fecl 3溶液发生显色反应,又可以与NaHCO 3溶液反应放出CO 2气体 13.下图表示反应X(g)4Y(g)+Z(g),0H ∆<,在某温度时X 的浓度随时间变化的曲线:下列有关该反应的描述正确的是A.第6m in 后,反应就终止了B.X 的平衡转化率为85%C.若升高温度,X 的平衡转化率将大于85%D.若降低温度,v 正和v 逆将以同样倍数减少 参考答案:6.D7.B8.B9.C 10.C 11.A 12.D 13.B 第Ⅱ卷(共176分) 27.(15分)(注意:在试题卷上作答无效.........) 浓H 2SO 4和木炭在加热时发生反应的化学方程式是2 H2SO4 (浓) + C CO2↑+ 2 H2O + 2SO2↑请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并检出反应产物的装置。
2009年高考四川理综化学试题和参考答案第Ⅰ卷本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Al 27S 32 K 39 Mn 55 一、选择题(本题包括13小题。
每小题只有一个....选项符合题意) 6.开发新材料是现代科技发展的方向之一。
下列有关材料的说法正确的是 A .氮化硅陶瓷是新型无机非金属材料 B .C 60属于原子晶体,用于制造纳米材料 C .纤维素乙酸酯属于天然高分子材料 D .单晶硅常用于制造光导纤维8.在下列给定条件的溶液中,一定能大量共存的离子组是 A.无色溶液:Ca 2+、、H +、Cl -1、HSO -3B.能使pH 试纸呈红色的溶液:Na +、NH +4、I -、NO -3C.FeCl 2溶液:K +、、Na +、、SO 2-4、、AlO -1D.()Kw c H +=0.1 mol/L 的溶液:Na +、K +、SiO 2-3、NO -39.25 ℃,101 k Pa 时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol ,辛烷的燃 烧热为5518 kJ/mol 。
下列热化学方程式书写正确的是A.2H +(aq)+SO 2-4+SO 2-4(aq)+Ba 2+(aq)+2OH -(aq)=BaSO 4(s)+2H 2O(1);∆H=-57.3 kJ/molB.KOH(aq)+12H 2 SO 4(aq)= 12K 2SO 4(aq)+H 2O(l); ∆H=-57.3kJ/mol C.C 8H 18(1)+ 252O 2(g)=8CO 2(g); ∆H=-5518 kJ/molD.2C 8H 18(g)+25O 2(g)=16CO 2(g)+18H 2O(1); ∆H=-5518 kJ/mol10.X 、Y 、Z 、M 是元素周期表中前20号元素,其原子序数依次增大,且X 、Y 、Z 相邻。
X 的核电荷数是Y 是核外电子数的一半,Y 与M 可形成化合物M 2Y 。
下列说法正确的是A .还原性:X 的氧化物>Y 的氧化物>Z 的氢化物B .简单离子的半径:M 的离子>Z 的离子>Y 的离子>X 的离子C .YX 2、M 2Y 都是含有极性键的极性分子D .Z 元素的最高价氧化物的水化物的化学式为HZO 411.向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。
向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。
再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。
则下列关系不正确的是A.100011.2bcV= B.125Vcp m=+ C.n=m+17Vc D.51739p m12.关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是A.c(NH+4):③>①B.水电离出的c(H+):②>①C.①和②等体积混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O)D. ①和③等体积混合后的溶液:c(NH+4)>c(Cl-)>c(OH-)>c(H+)13.在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g)nY(g),△H=Q kJ/mol。
反应达到平衡时,Y的物质的量浓度与温度、气下列说法正确的是A.m>nB.Q<0C.温度不变,压强增大,Y的质量分数减少D.体积不变,温度升高,平衡向逆反应方向移动参考答案:6.A 7.B 8.D 9.B 10.D 11.C 12.B 13.C第Ⅱ卷26.(16分)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。
某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化的含量请填写下列空白:(1)移取10.00 m密度为ρ g/mL的过氧化氢溶液至250mL ___________(填仪器名称)中,加水衡释至刻度,摇匀。
移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
口MnO4-+口H2O+口H+===口Mn2++口H2O++口;(3) 滴定时,将高锰酸钾标准溶液注入______________________(填“酸式”或“碱式”)滴定管中。
滴定到达终点的现象是___________________________________________ ______________________________________________________________。
(4)复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为______________________________________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质该化学举小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。
(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾演粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。
)请将他们的实验方法和实验现象填入下表:参考答案:I.(1)容量瓶(2)2 5 6 2 8 502(3)酸式滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色(4)17 200 cV(5)偏高II.27.(15分)已知A-O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去)。
A、B、H分别是由短周期元素组成的单质。
B与冷水缓慢反应,与沸水迅速反应,放出氢气。
D 是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱。
C 为淡黄色固体化合物,O 能与G 的水溶液反应生成蓝色沉淀。
请回答下列问题:(1) 组成B 单质的元素位于周期表第______________周期,第_______________族。
化合物C 的电子式为__________________________________。
(2) J 的沸点比硒化氢(H 2Se )的沸点高,其原因是_________________。
(3) 写出I 与H 在点燃条件下反应生成A 和J 的化学方程式:________________。
(4) 写出D 与足量的N 反应生成E 和F 的化学方程式:_____________________。
(5) 上图中,在同一反应里一种物质作氧化剂,又作还原剂,这样的反应共有_______个。
参考答案:(1)三;II A(2)水分子之间存在氢键且比硒化氢的分子间作用力强 (3)4NH 3+3O 2点燃2N 2+6H 2O(4)Mg 3N 2+8HNO 3===3Mg(NO 3)2+2NH 4NO 3 (5)2 28.(14分)四川汶川盛产品质优良的甜樱桃。
甜樱桃中含有一种羟基酸(用A 表示),A 的碳链结构无支链,化学式为C 4H 6O 5;1.34 g A 与足量的碳酸氢钠溶液反应,生成标准状况下的气体0.448 L 。
A 在一定条件下可发生如下转化:ABC D E其中,B 、C 、D 、E 分别代表一种直链有机物,它们的碳原子数相等。
E 的化学式为C 4H 6O 6(转化过程中生成的其它产物略去)。
已知:稀盐酸足量的NaOH 溶液 Br 2加热催化剂A的合成方法如下:其中,F、G、M分别代表一种有机物。
请回答下列问题:(1)A的结构简式是_____________________。
(2)C生成D的化学方程式是。
(3)A与乙醇之间发生分子间脱水瓜,可能生成的有机物共有种。
(4)F的结构简式是。
(5)写出G与水反应生成A和M的化学方程式:。
参考答案:(3)729.(15分)新型锂离子电池在新能源的开发中占有重要地位。
可用作节能环保电动汽车的动力电池。
磷酸亚铁锂(LiFePO4)是新型锂离子电池的首选电极材料,它的制备方法如下:方法一:将碳酸锂、乙酸亚铁[(CH3COO)2Fe]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其它产物均以气体逸出。
方法二:将一定浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷酸亚铁锂沉淀。
沉淀经过滤、洗涤、干燥,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂。
在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子选移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下:请回答下列问题:(1)上述两种方法制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行。
其原因是。
(2)在方法一所发生的反应中,除生成磷酸亚铁锂、乙酸外,还有、、(填化学式)生成。
(3)在方法二中,阳极生成磷酸亚铁锂的电极反应式为。
(4)写出M与足量氧化钠溶液反应的化学方程式:。
(5)已知该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为。
参考答案:(1)为了防止亚铁化合物被氧化(2)CO2H2O NH3(3)Fe+H2PO4-+Li+-2e-====LiFePO4+2H+(4)(5)FePO4+Li++e-====LiFePO4。