蛋白酶提取、活力测定实验总结
- 格式:doc
- 大小:26.50 KB
- 文档页数:3

蛋白酶活力测定实验报告
实验目的:
通过测定蛋白酶的活力,了解其功能和活性。
实验原理:
蛋白酶是一类能够水解蛋白质的酶,可以将蛋白质分解为多肽和氨基酸。
蛋白酶活力是指单位时间内酶水解蛋白质的能力,通常以单位时间内水解的底物的量来表示。
本实验使用的方法是酶促反应测定法。
首先,将待测蛋白酶与底物混合,反应一定时间后,停止反应并添加淀粉溶液产生反应终止剂,最后用碘化钾溶液滴定反应产物。
实验步骤:
1. 预备试剂:制备蛋白酶和底物的工作液,制备淀粉溶液和反应终止剂,制备碘化钾溶液。
2. 实验装置:准备滴定装置和试管架。
3. 设置实验条件:保持温度恒定,控制pH值。
4. 实验操作:在试管中加入待测蛋白酶和底物工作液,反应一定时间后,加入淀粉溶液和反应终止剂,最后用碘化钾溶液滴定。
5. 记录数据:记录滴定所需碘化钾的体积,计算出酶活力。
实验结果:
根据实验数据,计算出蛋白酶的活力,通常以单位时间内水解的底物的量来表示。
实验讨论:
分析实验结果,比较不同条件下蛋白酶的活力差异,并讨论影响蛋白酶活力的因素。
实验结论:
通过分析实验结果,得出结论,总结蛋白酶活力与其他因素之间的关系,并提出可能的应用前景。
实验总结:
总结实验过程,评价实验结果及数据,提出改进意见,并对今后可能的研究方向进行展望。
参考文献:
列出所参考的文献。

蛋白酶的制备及活力的测定目的要求1.学习胰蛋白酶的纯化及其结晶的基本方法。
2.了解酶的活性与比活性的概念。
实验原理胰蛋白酶是以无活性的酶原形式存在于动物胰脏中,在Ca2+的存在下,被肠激酶或有活性的胰蛋白酶自身激活,从肽链N端赖氨酸和异亮氨酸残基之间的肽键断开,失去一段六肽,分子构象发生一定改变后转变为有活性的胰蛋白酶。
胰蛋白酶原的分子量约为24000,其等电点约为pH8.9,胰蛋白酶的分子量与其酶原接近(23300),其等电点约为pH10.8,最适pH7.6~8.0,在pH=3时最稳定,低于此pH时,胰蛋白酶易变性,在pH>5时易自溶。
Ca2+离子对胰蛋白酶有稳定作用。
重金属离子,有机磷化合物和反应物都能抑制胰蛋白酶的活性,胰脏、卵清和豆类植物的种子中都存在着蛋白酶抑制剂。
最近发现在一些植物的块基(如土豆、白薯、芋头等)中也存在有胰蛋白酶抑制剂。
胰蛋白酶能催化蛋白质的水解,对于由碱性氨基酸(精氨酸、赖氨酸)的羧基与其他氨基酸的氨基所形成的键具有高度的专一性。
此外还能催化由碱性氨基酸和羧基形成的酰胺键或酯键,其高度专一性仍表现为对碱性氨基酸一端的选择。
胰蛋白酶对这些键的敏感性次序为:酯键> 酰胺键> 肽键。
因此可利用含有这些键的酰胺或酯类化合物作为底物来测定胰蛋白酶的活力。
目前常用苯甲酰-L-精氨酸-对硝基苯胺(简称BAPA)和苯甲酰-L-精氨酸-β-萘酰胺(简称BANA)测定酰胺酶活力。
用苯甲酰-L-精氨酸乙酯(简称BAEE)和对甲苯磺酰-L-精氨酸甲酯(简称TAME)测定酯酶活力。
本实验以BAEE为底物,用紫外吸收法测定胰蛋白酶活力。
酶活力单位的规定常因底物及测定方法而异。
从动物胰脏中提取胰蛋白酶时,一般是用稀酸溶液将胰腺细胞中含有的酶原提取出来,然后再根据等电点沉淀的原理,调节pH以沉淀除去大量的酸性杂蛋白以及非蛋白杂质,再以硫酸铵分级盐析将胰蛋白酶原等(包括大量的酸性杂蛋白以及非蛋白杂质,再以硫酸铵分级盐析将胰蛋白酶原等(包括大量糜蛋白酶原和弹性蛋白酶原)沉淀析出。

一、实验目的1. 掌握蛋白酶活力的测定原理和方法。
2. 学习酶促反应动力学的基本知识。
3. 了解蛋白酶在不同条件下的活性变化。
二、实验原理蛋白酶是一种催化蛋白质水解的酶,其活性可通过测定在一定条件下水解底物产生氨的速率来表示。
本实验采用紫外分光光度法测定蛋白酶活力,通过测定反应体系中氨的生成速率,间接反映蛋白酶的活力。
三、实验材料与试剂1. 实验材料:- 酪蛋白:1g- 胰蛋白酶:适量- 磷酸氢二钠溶液(0.1mol/L)- 磷酸二氢钠溶液(0.1mol/L)- 氢氧化钠溶液(0.1mol/L)- 蒸馏水- 紫外分光光度计2. 试剂:- Folin试剂:1.25g钼酸铵溶于50ml水中,加入25ml硫酸,混匀,用蒸馏水定容至100ml- 草酸溶液:7.5g草酸溶于100ml水中- 硫酸铜溶液:5g硫酸铜溶于50ml水中,用蒸馏水定容至100ml- 酶标液:1mg/mL四、实验步骤1. 准备反应体系:取0.5g酪蛋白,加入5ml磷酸氢二钠溶液(0.1mol/L)和5ml 磷酸二氢钠溶液(0.1mol/L),混匀后加入适量的胰蛋白酶,使酶与底物比例约为1:100。
2. 预热反应体系:将反应体系放入水浴锅中,恒温40℃。
3. 启动反应:每隔一定时间(如30秒)取样,立即加入0.5ml氢氧化钠溶液(0.1mol/L)终止反应。
4. 测定氨含量:将终止反应后的样品加入0.5ml Folin试剂,混匀后加入0.5ml 硫酸铜溶液,再加入0.5ml草酸溶液,混匀后放入紫外分光光度计中,于波长620nm处测定吸光度。
5. 计算蛋白酶活力:根据标准曲线计算样品中氨的浓度,进而计算蛋白酶活力。
五、实验结果与分析1. 标准曲线绘制:以不同浓度的氨溶液为标准品,绘制标准曲线。
2. 蛋白酶活力计算:根据样品的吸光度值,从标准曲线中查找对应的氨浓度,计算蛋白酶活力。
3. 分析不同条件对蛋白酶活性的影响:通过改变温度、pH值、底物浓度等条件,观察蛋白酶活性的变化。

一、实验目的1. 了解胃蛋白酶的化学性质和生理功能。
2. 掌握从胃黏膜中提取胃蛋白酶的方法。
3. 学习实验操作技巧,提高实验技能。
二、实验原理胃蛋白酶是一种消化酶,主要存在于胃液中,能将蛋白质分解成肽和氨基酸。
本实验通过从新鲜猪胃黏膜中提取胃蛋白酶,探讨其提取方法及活性。
三、实验材料与仪器1. 实验材料:新鲜猪胃黏膜、生理盐水、蒸馏水、氢氧化钠、硫酸铵、乙酸、酚酞指示剂、标准蛋白质溶液、考马斯亮蓝G-250染料、酶标仪、离心机、冰箱、烧杯、玻璃棒、移液管、滴定管、电子天平等。
2. 实验试剂:胃蛋白酶提取液、胃蛋白酶活性测定液、胃蛋白酶标准曲线、缓冲液等。
四、实验步骤1. 胃蛋白酶提取液的制备(1)将新鲜猪胃黏膜洗净,去除脂肪和杂质。
(2)将胃黏膜剪成小块,放入烧杯中,加入适量的生理盐水,用玻璃棒搅拌。
(3)将搅拌后的胃黏膜液过滤,收集滤液。
(4)向滤液中加入氢氧化钠溶液,调节pH至7.0。
(5)将溶液在室温下静置30分钟。
(6)加入硫酸铵溶液,使蛋白质盐析,沉淀蛋白质。
(7)将沉淀物用蒸馏水洗涤,直至无色。
(8)将洗涤后的沉淀物溶于适量的乙酸溶液中,制成胃蛋白酶提取液。
2. 胃蛋白酶活性测定(1)配制标准蛋白质溶液,用考马斯亮蓝G-250染料进行比色,绘制标准曲线。
(2)取一定量的胃蛋白酶提取液,加入适量的缓冲液,使pH值调至7.0。
(3)取标准蛋白质溶液和胃蛋白酶提取液,分别加入适量的胃蛋白酶活性测定液。
(4)将混合液置于37℃水浴中保温15分钟。
(5)取出混合液,加入适量的酚酞指示剂,用NaOH溶液滴定至终点。
(6)根据滴定结果,计算胃蛋白酶活性。
五、实验结果与分析1. 胃蛋白酶提取液的制备通过实验,成功从新鲜猪胃黏膜中提取出胃蛋白酶,提取液呈淡黄色。
2. 胃蛋白酶活性测定根据实验结果,绘制出胃蛋白酶标准曲线。
在实验条件下,胃蛋白酶活性为(XX±XX)U/mg。
六、实验结论1. 本实验成功从新鲜猪胃黏膜中提取出胃蛋白酶,提取方法简单可行。
实验四、蛋白酶活力的测定1.实验目的掌握用Folin-酚法测定蛋白酶活力的方法,与Azocasein(偶氮酪蛋白)法作为比较。
2.实验原理蛋白酶在一定的温度和pH下,水解酪素底物产生含有酚基的氨基酸(如酪氨酸、色氨酸),在碱性条件下,将福林试剂还原,生成钼蓝和钨蓝,其颜色的深浅与酚基氨基酸含量成正比,通过在660nm测定其吸光度,可得到酶解产生的酚基氨基酸的量,计算出蛋白酶活力,以此代表蛋白酶的总酶活力。
酶活单位定义:在37℃、相应的pH条件下,在1min内水解酪蛋白底物,产生相当于1µg酚类化合物(由酪氨酸等同物表示)的酶量,为1个酶活单位。
3.主要仪器和试剂试剂:0.1mg/mL L-酪氨酸标准贮备溶液、0.55mol/LNa2CO3、福林试剂、Casein溶液、TCA 溶液仪器设备:恒温水浴锅、分光光度计、pH计,分析天平、秒表。
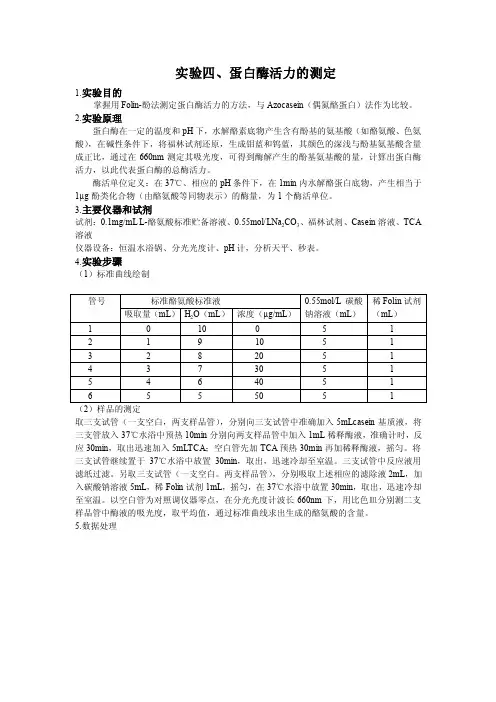
4.实验步骤(1)标准曲线绘制取三支试管(一支空白,两支样品管),分别向三支试管中准确加入5mLcasein基质液,将三支管放入37℃水浴中预热10min分别向两支样品管中加入1mL稀释酶液,准确计时,反应30min,取出迅速加入5mLTCA;空白管先加TCA预热30min再加稀释酶液,摇匀。
将三支试管继续置于37℃水浴中放置30min,取出,迅速冷却至室温。
三支试管中反应液用滤纸过滤。
另取三支试管(一支空白。
两支样品管),分别吸取上述相应的滤除液2mL,加入碳酸钠溶液5mL,稀Folin试剂1mL,摇匀,在37℃水浴中放置30min,取出,迅速冷却至室温。
以空白管为对照调仪器零点,在分光光度计波长660nm下,用比色皿分别测二支样品管中酶液的吸光度,取平均值,通过标准曲线求出生成的酪氨酸的含量。
5.数据处理。

一、实验目的1. 了解蛋白酶比活力的概念及测定方法。
2. 掌握利用比色法测定蛋白酶比活力的原理和操作步骤。
3. 通过实验,了解蛋白酶在不同条件下的活性变化,为实际应用提供参考。
二、实验原理蛋白酶比活力是指单位质量的蛋白质所具有的酶活性。
在实验中,通过测定蛋白酶在一定条件下对底物(如酪蛋白)的水解程度,可以计算出蛋白酶的比活力。
本实验采用比色法,通过测定底物水解产生的产物(如酪氨酸)的吸光度变化,间接反映蛋白酶的活性。
三、实验材料与仪器1. 实验材料:- 蛋白酶样品- 酪蛋白- 0.02mol/L pH7.5磷酸盐缓冲液- 0.1mol/L Folin-酚试剂- 0.4mol/L三氯乙酸- 0.05mol/L氢氧化钠溶液- 2.5mol/L硼砂缓冲溶液(pH10.5)- 680nm比色计2. 实验仪器:- 磁力搅拌器- 移液器- 电子天平- 恒温水浴锅- 10mL具塞试管- 50mL容量瓶- 试管架四、实验步骤1. 准备实验试剂:- 配制0.1mol/L Folin-酚试剂:将钨酸钠、钼酸钠、磷酸、盐酸、硫酸锂、液溴等试剂按比例混合,微火回流加热10小时,加入碳酸钠和蒸馏水,定容至1000mL。
- 配制0.4mol/L三氯乙酸溶液:称取三氯乙酸16.34g,用水溶解并定容至500mL。
- 配制0.05mol/L氢氧化钠溶液:按GB601配制。
- 配制2.5mol/L硼砂缓冲溶液(pH10.5):称取硼酸钠19.08g,加水溶解并定容至1000mL,称取氢氧化钠4.0g,加水溶解并定容至1000mL,取甲液500mL乙液400mL混合,用水稀释至1000mL。
2. 实验操作:- 将酪蛋白溶解于0.02mol/L pH7.5磷酸盐缓冲液中,配制成2%酪蛋白溶液。
- 将蛋白酶样品用0.02mol/L pH7.5磷酸盐缓冲液稀释至适宜浓度。
- 取10mL具塞试管,加入2%酪蛋白溶液1mL,然后加入蛋白酶溶液1mL,置于37℃恒温水浴锅中反应30分钟。

蛋白酶比活力实验报告蛋白酶比活力实验报告引言:蛋白酶是一类能够水解蛋白质的酶,广泛存在于生物体内。
通过测定蛋白酶的比活力,可以评估其催化反应的速率和效率。
本实验旨在通过比较不同条件下蛋白酶的活力,探究影响蛋白酶活性的因素。
实验方法:1. 实验材料准备:- 蛋白酶溶液:从动物组织中提取的蛋白酶溶液,浓度为10 mg/mL。
- 底物溶液:使用明胶作为蛋白酶的底物,浓度为1%。
- 缓冲液:pH值为7.4的磷酸盐缓冲液。
- 试管:用于混合反应液的透明试管。
- 恒温水浴:用于控制反应温度的设备。
2. 实验步骤:- 步骤一:在不同温度下测定蛋白酶的活力。
- 将5 mL蛋白酶溶液和5 mL底物溶液混合,并放置于恒温水浴中,分别设置不同温度条件(如25℃、37℃、50℃)。
- 在反应开始后的1分钟、2分钟、3分钟等时间点,取出一定量的反应液,立即停止反应。
- 使用布拉德福法测定反应液中未被水解的底物浓度,计算蛋白酶的比活力。
- 步骤二:在不同pH条件下测定蛋白酶的活力。
- 在不同pH值的缓冲液中,重复上述步骤一的实验操作。
- 测定不同pH条件下蛋白酶的比活力,并比较其差异。
实验结果:1. 温度对蛋白酶活力的影响:- 在25℃、37℃和50℃下进行实验,测得蛋白酶的比活力分别为0.05 U/mg、0.1 U/mg和0.02 U/mg。
- 结果显示,蛋白酶的活力随着温度的升高而增加,但当温度过高时(如50℃),蛋白酶的活力反而下降。
2. pH值对蛋白酶活力的影响:- 在pH为7.4、8.0和9.0的缓冲液中进行实验,测得蛋白酶的比活力分别为0.08 U/mg、0.06 U/mg和0.04 U/mg。
- 结果显示,蛋白酶的活力在中性条件下(pH 7.4)最高,而在酸性和碱性条件下,蛋白酶的活力均降低。
讨论与结论:通过本实验,我们可以得出以下结论:1. 温度对蛋白酶活力有显著影响,适宜的温度可以提高蛋白酶的催化效率,但过高的温度会导致酶的变性,从而降低活力。

酶活力测定实验报告一、实验目的酶活力测定实验的主要目的是了解酶的活性及其影响因素,掌握测定酶活力的基本方法和原理,以及学会使用相关仪器和试剂进行实验操作。
二、实验原理酶是生物体内具有催化作用的蛋白质或核酸。
酶活力是指酶催化一定化学反应的能力,通常用在一定条件下酶催化反应的速度来表示。
本实验采用分光光度法测定酶活力,其原理是基于酶催化反应所产生的产物在特定波长下具有光吸收特性,通过测定反应体系在该波长下吸光度的变化,可以计算出酶催化反应的速度,从而反映酶的活力。
以过氧化氢酶为例,过氧化氢酶能够催化过氧化氢分解为水和氧气。
在本实验中,通过加入一定量的过氧化氢溶液,使其与过氧化氢酶反应,然后使用高锰酸钾溶液滴定剩余的过氧化氢,根据高锰酸钾溶液的用量计算出过氧化氢酶的活力。
三、实验材料与仪器1、实验材料新鲜的猪肝或土豆等富含过氧化氢酶的组织。
过氧化氢溶液(3%)。
高锰酸钾溶液(002 mol/L)。
磷酸缓冲液(pH 70)。
2、实验仪器研钵。
离心机。
移液器。
分光光度计。
恒温水浴锅。
试管、量筒、容量瓶等玻璃仪器。
四、实验步骤1、酶液的制备称取新鲜的猪肝或土豆组织_____g,置于研钵中,加入适量的磷酸缓冲液(pH 70),研磨成匀浆。
将匀浆转移至离心管中,以_____rpm 的转速离心_____min,取上清液即为粗酶液。
2、酶活力的测定取_____支试管,分别标记为 1、2、3。
在 1 号试管中加入_____mL 磷酸缓冲液(pH 70)作为空白对照,在 2、3 号试管中分别加入_____mL 粗酶液。
向 1、2、3 号试管中分别加入_____mL 过氧化氢溶液(3%),立即摇匀,并同时开始计时。
在反应进行_____min 后,迅速向 1、2、3 号试管中分别加入_____mL 浓度为 2 mol/L 的硫酸溶液终止反应。
用移液器吸取_____mL 反应液,加入到另一支装有_____mL 高锰酸钾溶液(002 mol/L)的试管中,摇匀。

发酵实验总结生物技术1002 1610100311 刘小波摘要:1、实验目的:通过本次实验,学习用选择平板从自然界中分离胞外蛋白酶产生菌的方法,学习并掌握细菌菌株的药瓶液体发酵技术,了解碱性蛋白酶活力测定的原理,掌握碱性蛋白酶活力测定的方法。
2、实验方法:从玉米黄顶菊混种土壤中筛选蛋白酶,之后经液体发酵扩大培养,挑选出活力较强的菌落,通过碱性蛋白酶活力测定的方法测出蛋白酶活力的大小。
3、实验结果:实验原理:1、能够产生胞外蛋白酶的菌株在平板上生长后,其菌落周围可形成明显的蛋白水解圈。
水解圈与菌落直径的比值常被作为判断该菌株蛋白酶产生能力的筛选依据。
2、蛋白酶在一定条件下不仅能够水解蛋白质中的肽键,也能够水解酰胺键和酯键,因此可以利用蛋白质或人工合成的酰胺及酯类化合物作为底物来测定蛋白酶的活力。
本实验选用酪蛋白为底物,测定微生物蛋白酶水解肽键的活力。
酪蛋白经蛋白酶作用后,降解成相对分子质量较小的肽和氨基酸,在反应混合物中加入三氯醋酸溶液,相对分子质量较大的蛋白质和肽就沉淀下来,先对分子质量较小的仍留在溶液中,溶解于三氯醋酸溶液中的肽的数量正比于酶的数量和反应时间。
在280nm 波长下测定溶液吸光度的增加,就可以计算酶的活力。
实验材料:玉米黄顶菊混种土样、酪蛋白、牛肉膏、磷酸氢二钠、氯化钠、琼脂、蒸馏水、0.02mol/l磷酸盐缓冲液(ph7.5)、1%酪蛋白溶液、5%三氯醋酸(TCA)溶液、烧杯、试管、容量瓶、量筒、玻璃棒、移液枪、电子秤、高温高压灭菌锅、恒温培养箱、离心机、水浴锅、紫外线分光光度计等。
实验方法:蛋白酶的筛选:1、准确称取玉米黄顶菊混种土样10g,放入装有90mL无菌水的250mL三角瓶中,用手震荡20min,使微生物细胞分散,静置20~30s,即成10-1稀释液;再用1mL无菌吸管,吸取10-1稀释液1mL,移入装有9mL无菌水的试管中,吹吸3次,让菌液混合均匀,即成10-2稀释液;再换一支无菌吸管,吸取10-2稀释液1mL,移入装有9mL无菌水的试管中,也吹吸3次,成10-3稀释液;以此类推,连续稀释,制成10-4、10-5、10-6、10-7、10-8一系列稀释菌液。

菠萝蛋白酶的提取、初步分离纯化及活性测定12食安2班陈志廉摘要本文阐述了通过运用高速离心法提取粗酶,盐析分离提纯,透析除杂等方法提取出了菠萝蛋白酶并将其初步分离纯化且测定了各个步骤的酶活性的过程。
关键词菠萝蛋白酶纯化酶活性前言菠萝蛋白酶(Bromelain,EC3.4.22.3)简称菠萝酶,是从凤梨属植物菠萝中提取的一组复合的半胱氨酸巯基蛋白水解酶,1891年Mercaro于菠萝的汁中首先发现。
在食品工业中菠萝蛋白酶作为一种食品添加剂,能分解蛋白质、肽、酯和酰胺等,可用于肉质嫩化、水解蛋白、啤酒澄清、干酪生产等。
菠萝蛋白酶来可以用来增加豆饼和豆粉的PDI值和NSI值,从而生产出可溶性蛋白制品及含豆粉的早餐、谷类食物和饮料。
其它还有生产脱水豆类、婴儿食品和人造黄油;澄清苹果汁;制造软糖;为病人提供可消化的食品;给日常食品添味等。
在医药上它可以治疗水肿及多种炎症,并有助消化,健胃消食等功能。
菠萝蛋白酶属于糖蛋白,是由巯基蛋白酶和非蛋白酶组分构成的复杂复合物,因含有一个不稳定的游离巯基,所以菠萝蛋白酶极易被氧化而使其酶活下降。
本文主要验证了从新鲜菠萝皮中提取菠萝蛋白酶并将之纯化的方法,以求改进工艺等。
1实验材料与仪器1.1实验材料与试剂新鲜菠萝、0.1mo1/L pH7.8磷酸缓冲液(PBS)、0.01mo1/L pH7.8磷酸缓冲液(PBS)、1%酪蛋白、激活剂、10%三氯乙酸(TCA)、牛血清白蛋白、考马斯亮蓝G2501.2实验仪器722型可见光分光光度计:上海舜宇恒平科学仪器有限公司;752型光栅分光光度计:北京光学仪器厂;TDL-60B台式离心机:上海安宁科学仪器厂;D5M离心机:长沙湘智离心机仪器有限公司;DK-8D电热恒温水浴锅:上海森信实验仪器有限公司;可控硅恒温水浴锅:上海锦屏仪器仪表有限公司;AMPUT电子天平:深圳安普特科技有限公司;BS110S分析天平北京赛多利斯天平有限公司;DS-1型高速组织捣碎机:上海标本模型厂;HZS-H型水浴振荡器:哈尔滨市东联电子技术开发有限公司2实验方法2.1菠萝蛋白酶的粗酶提取称取菠萝皮材料30g,将菠萝皮在清水中洗净,沥干,切成小段后置于超高速搅拌机中,加入约60mL预冷的0.1mo1/L pH7.8PBS,持续搅拌10~15min至粉碎,搅拌完成后用4层纱布过滤,得到滤液后,用冷冻离心机于4°C3000rpm 离心6min,弃沉淀,即得到菠萝蛋白酶粗提液,测定粗提液的体积、蛋白质含量和酶活性。

一、实验目的1. 学习和掌握蛋白酶活性检测的基本原理和方法。
2. 了解蛋白酶的特性和作用。
3. 通过实验,学会使用相关仪器和操作技能。
二、实验原理蛋白酶是一种能够水解蛋白质的酶,其活性是指在一定条件下,蛋白酶催化蛋白质水解的能力。
蛋白酶活性检测通常采用紫外分光光度法,通过测定反应体系中蛋白质的降解程度来评估蛋白酶的活性。
三、实验材料与仪器1. 实验材料:(1)蛋白酶样品(2)底物:酪蛋白(3)缓冲液:磷酸盐缓冲液(pH 7.0)(4)其他试剂:硫酸铜、碘化钾、氢氧化钠等2. 实验仪器:(1)紫外分光光度计(2)恒温水浴锅(3)电子天平(4)移液器(5)试管(6)烧杯四、实验步骤1. 准备实验试剂和仪器。
2. 配制底物溶液:称取一定量的酪蛋白,加入适量磷酸盐缓冲液,溶解后备用。
3. 设置实验组:(1)取若干个试管,分别加入不同浓度的蛋白酶样品。
(2)在每个试管中加入相同体积的底物溶液。
(3)将试管放入恒温水浴锅中,设定温度为37℃,反应一定时间。
4. 设置对照组:(1)取若干个试管,分别加入相同体积的蛋白酶样品和底物溶液。
(2)将试管放入恒温水浴锅中,设定温度为37℃,反应一定时间。
5. 测定反应体系中蛋白质的降解程度:(1)取一定体积的反应体系,加入硫酸铜和碘化钾溶液。
(2)用紫外分光光度计测定反应体系的吸光度。
(3)根据吸光度计算蛋白质的降解程度。
6. 数据处理和分析:(1)绘制蛋白酶活性与酶浓度、反应时间的关系曲线。
(2)分析蛋白酶的特性和作用。
五、实验结果与分析1. 实验结果:(1)不同浓度的蛋白酶样品对底物溶液的降解程度不同。
(2)随着反应时间的延长,蛋白质的降解程度逐渐增加。
2. 分析:(1)蛋白酶的活性与酶浓度呈正相关,即酶浓度越高,活性越强。
(2)在一定反应时间内,蛋白酶活性随着反应时间的延长而增加,但当反应时间过长时,活性逐渐降低,可能是因为蛋白酶自身发生降解。
六、实验结论1. 通过本实验,掌握了蛋白酶活性检测的基本原理和方法。
蛋白酶的提取制备和活力测定一、目的要求:1、了解蛋白酶活性测定原理,并掌握测定技术;2、通过实验加深对酶活力和比活力含义的理解二、原理:采用酶活力单位数/毫克蛋白质样品表示酶的比活力。
用Folin酚试剂法测定酶活力,凯氏定氮法测定蛋白质含量。
蛋白酶活力单位定为每分钟内分解出1ug酪氨酸与Folin酚试剂作用呈兰色,其兰色深浅与酪氨酸量成正比,所以首先要作出兰色程度(用光密度值表示)与酪氨酸深度关系的标准曲线,然后再将酶和底物反应的产物(tyr)与Folin酚试剂作用,在分光光度计上测出光密度(OD值),从标准曲线上查出相当于多少微克的酪氨酸,再计算出酶活力单位数。
蛋白质量用克氏定氮法进行测定。
三、器材高速组织捣碎机;解剖刀、镊子、剪刀;量筒、吸量管、漏斗、玻棒三角烧瓶、离心管、离心机;恒温水浴、托盘天平;比色器、分光光度计、冰箱四、试剂1.25M H2SO4;固体(NH4)2SO4;Folin酚试剂;标准酪氨酸溶液:取预先在105℃烘至恒重的酪氨酸,称取100mg,以0.2M HCL溶液,定容至100 mL,再加水稀释10倍,得到100ug/ mL的酪氨酸溶液。
酪蛋白溶液称取酪蛋白2克,置150 mL三角烧杯中,加入0.2M磷酸氢钠61 mL,在水浴上搅拌使溶解,再加入39 mL 0.2M 磷酸二氢钠,得到Ph=7的酪蛋白液,倾出上清夜备用。
0.4M三氯醋酸溶液(TCA);0.4MNa2CO3溶液 ;酚酞指示剂;标准氢氧化钠溶液五、操作1、蛋白酶的制备提取:活杀黑鱼内脏若干克,用组织捣碎机,捣碎0.5min然后混悬于两倍体积的冰冷1.25M H2SO4液中,放入冰箱内,2h后,离心(3000 t.pm min)、过滤,合并上清液,即为粗蛋白酶提取液,留样测定蛋白质和酶活力。
2、蛋白酶的活力测定Ty r标准曲线的制作:取6支中试管,按下表加入酪氨酸和蒸馏水,得到一系列不同浓度的酪氨酸溶液。
混合均匀,按表依次加入试剂、保温,然后在分光光度计上比色测定650nm 处的光密度值。
实验:蛋白酶的活力测定一、实验目的1、学习蛋白酶活力的测定方法。
2、深入了解酶的活力和比活力的概念。
二、实验原理1、酶活力的大小,是以该酶在适宜的温度和pH下,酶催化一定时间后,反应底物的减少量或者反应产物的增加量来表示。
2、本实验蛋白酶的活力大小是以分解出的酪氨酸的量来表示,其单位为:每分钟内分解出1微克酪氨酸的酶量称为1单位。
3、本实验采用福林-酚与蛋白质水解出的酪氨酸生成兰色物,从兰色的深浅程度可以求知酪氨酸的多少,从而确定酶活力的大小。
4、在测酶活力前,先用福林-酚与用已知的不同浓度的酪氨酸作用,作出兰色深浅程度(用光密度表示)与酪氨酸浓度关系的标准曲线。
5、将酶与底物反应产生的产物与福林-酚试剂作用后测光密度,从标准曲线上查出相当于多少微克的酪氨酸,就可以计算出酶的单位了。
三、实验材料、仪器和试剂1.实验材料1398中性蛋白酶粗酶粉(上海新型发酵厂)、滤纸2.仪器(1)试管(1.5*15cm*24) (2)移液管(3)电热恒温水浴(4)721型分光光度计3.试剂(1)福林-酚试剂B(2)标准酪氨酸溶液称取50毫克酪氨酸(预先在105摄氏度烘至恒重),加0.2MHCL溶液后定容至100ml,在加水稀释5倍得到100微克/毫升的酪氨酸溶液。
(3)酪蛋白溶液称取酪蛋白2克,置150ml三角烧瓶中,加入0.2M磷酸氢二钠61ml,在水浴上搅拌使溶解,再加入39ml0.2M磷酸二氢钠,得到pH7的酪蛋白液,倾出上清液备用。
(4)0.4M三氯醋酸溶液(TCA)(5)0.4M碳酸钠溶液四、操作步骤1、酪氨酸标准曲线制作:按下列次序加入试剂,混合均匀,保温,然后在分光光度计上进行比色,测出650nm处的光密度值。
以酪氨酸浓度为横坐标,光密度值为纵坐标,作出标准曲线。
管号 1 2 3 4 5 62、蛋白酶活力测定 (1)浸出酶液称取0.5克酶粉加入40ml 水,在室温下放置1小时并时加搅动。
将酶浸出液过滤,取滤液1ml 用水稀释至20ml ,即为稀释1600倍的酶液。
测定蛋白酶活力实验一、实验目的1.加深了解酶活力的概念。
2.学习掌握测定蛋白酶活力的方法。
二、实验原理酶活力指酶催化某一特定反应的能力。
其大小可用在一定条件下酶催化反应进行一定时间后,反应体系中底物的减少量或产物的生成量来表示。
酶活力单位是表示酶活力大小的重要指标。
本实验规定酶活力单位(U)为一定条件下每分钟分解1μg 酪氨酸所需的酶量。
实验选用枯草杆菌蛋白酶水解酪蛋白产生酪氨酸的反应体系。
产物酪氨酸在碱性条件下与Folin-酚试剂反应生成蓝色化合物,该蓝色化合物在680nm 处有最大光吸收,其吸光值与酪氨酸含量呈正比。
因此通过测定一定条件下产物酪氨酸的含量变化,可计算出蛋白酶的活力。
三、仪器和试剂仪器:恒温水浴锅、分光光度计、试管及试管架、干燥滤纸、玻璃漏斗。
原料枯草杆菌蛋白酶:称取1g 枯草杆菌蛋白酶粉,用少量0.02mol/L,pH7.5磷酸缓冲液溶解并定容至100mL,震荡15分钟,使充分溶解,干纱布过滤,取滤液冰箱备用。
使用时视酶活力高低用缓冲液适当稀释。
试剂1. Folin-酚试剂:在2L 磨口回流瓶中加入钨酸钠(Na2WoO4 . 2H2O)100g,钼酸钠(Na2WoO4 . 2H2O)25g,蒸馏水700mL,85%磷酸50mL 以及浓盐酸100mL,充分混匀后,微火回流加热10小时。
再加入硫酸锂150g,蒸馏水50mL 和液溴数滴,摇匀后开口继续煮沸15min,以驱赶过剩的溴。
冷却后加蒸馏水定容至1000mL,过滤,溶液呈黄绿色,置于棕色试剂瓶中暗处贮藏。
使用前用标准NaOH 溶液、酚酞为指示剂标定酸度(约为2mol/L),然后加水稀释至1mol/L,即可使用。
2. 0.2mol/L 盐酸溶液3. 0.04mol/L 氢氧化钠溶液4. 0.55mol/L 碳酸钠溶液5. 10%三氯乙酸溶液6. 0.02mol/LpH7.5磷酸缓冲液:称取磷酸氢二钠(Na2HPO4 . 12H2O)7.16g,用水定容至100mL(A 液);称取磷酸二氢钠(Na2HPO4.12H2O)3.12g,用水定容至100mL(B 液)。
发酵实验总结
生物技术1002 1610100311 刘小波
摘要:
1、实验目的:通过本次实验,学习用选择平板从自然界中分离胞外蛋白酶产生菌的方法,学习并掌握细菌菌株的药瓶液体发酵技术,了解碱性蛋白酶活力测定的原理,掌握碱性蛋白酶活力测定的方法。
2、实验方法:从玉米黄顶菊混种土壤中筛选蛋白酶,之后经液体发酵扩大培养,挑选出活力较强的菌落,通过碱性蛋白酶活力测定的方法测出蛋白酶活力的大小。
3、实验结果:
实验原理:
1、能够产生胞外蛋白酶的菌株在平板上生长后,其菌落周围可形成明显的蛋白水解圈。
水解圈与菌落直径的比值常被作为判断该菌株蛋白酶产生能力的筛选依据。
2、蛋白酶在一定条件下不仅能够水解蛋白质中的肽键,也能够水解酰胺键和酯键,因此可以利用蛋白质或人工合成的酰胺及酯类化合物作为底物来测定蛋白酶的活力。
本实验选用酪蛋白为底物,测定微生物蛋白酶水解肽键的活力。
酪蛋白经蛋白酶作用后,降解成相对分子质量较小的肽和氨基酸,在反应混合物中加入三氯醋酸溶液,相对分子质量较大的蛋白质和肽就沉淀下来,先对分子质量较小的仍留在溶液中,溶解于三氯醋酸溶液中的肽的数量正比于酶的数量和反应时间。
在280nm 波长下测定溶液吸光度的增加,就可以计算酶的活力。
实验材料:
玉米黄顶菊混种土样、酪蛋白、牛肉膏、磷酸氢二钠、氯化钠、琼脂、蒸馏水、0.02mol/l磷酸盐缓冲液(ph7.5)、1%酪蛋白溶液、5%三氯醋酸(TCA)溶液、烧杯、试管、容量瓶、量筒、玻璃棒、移液枪、电子秤、高温高压灭菌锅、恒温培养箱、离心机、水浴锅、紫外线分光光度计等。
实验方法:
蛋白酶的筛选:
1、准确称取玉米黄顶菊混种土样10g,放入装有90mL无菌水的250mL三角瓶中,用手震荡20min,使微生物细胞分散,静置20~30s,即成10-1稀释液;再用1mL无菌吸管,吸取10-1稀释液1mL,移入装有9mL无菌水的试管中,吹吸3次,让菌液混合均匀,即成10-2稀释液;再换一支无菌吸管,吸取10-2稀释液1mL,移入装有9mL无菌水的试管中,也吹吸3次,成10-3稀释液;以此类推,连续稀释,制成10-4、10-5、10-6、10-7、10-8一系列稀释菌液。
2、配酪素培养基(加琼脂),高压灭菌,倒平板,编号1、2、3。
另外配不加琼脂的液体培养基,
编号1、2、3。
3、取1的融入土壤的水1mL涂平板,置于恒温箱,于37℃或以上培养2~3天,挑选有水解圈(透明圈)的菌落。
4、液体发酵:挑去水解圈菌落,接种到液体培养基,恒温箱37℃培养2~3天,得酶原液。
注:酪素培养基成分:蛋白10g牛肉膏3g 磷酸氢二钠2g氯化钠5g琼脂15g 蒸馏水1000mL pH7.4
制法:将除指示剂外的各成分混合,加热溶解(但酪蛋白不溶解),校正pH。
加入指示剂,分装烧瓶,121℃高压灭菌15min。
用时加热溶化琼脂,冷至37℃,倾注平板。
蛋白酶活力测定:
1、将5%TCA溶液和1%酪蛋白溶液在37℃下保温。
2、取四支15ml具塞试管,分别标记A B C D,在A B 试管中各吸入0.20ml酶液,在C D试管中各吸入0.40ml酶液,分别用0.2mol/l磷酸盐缓冲液定容至2.00ml。
在B D试管中各吸入6.00ml 5%三氯醋酸溶液,上述四支试管都置于37℃水浴中恒温。
3、在各试管中吸入2.00ml 1%酪蛋白溶液,在37℃保温10min后,再向A C试管中吸入6.00ml 5%三氯醋酸溶液。
4、将试管从水浴中取出,在室温下放置1h,5000rpm离心10min,保留滤出液。
5、在280nm波长下,分别以B D滤液为空白,测定A C滤液的吸光值。
结果分析:
建议感想:
经过本次历时一周多的发酵实验,我产生了很多的感悟想法。
首先,这是我们上学这么年来第一次自己设计实验,自己动手配制实验药品,感觉自己收获最多的一次实验;第二,在查阅文献资料设计实验的过程中,自己第一次认真查阅并理解每一步骤的意义及其重要性,思考实验的可行性;第三、在实验过程中,自己独立操作了好多实验仪器,以前的专业技能训练内容终于派上了用场,弱弱的高兴自豪了一把;第四,在自主操作实验的过程中,每次离开实验室时,主动收拾用过的仪器,打扫实验室卫生,有种以实验室为家的感觉,这种感觉对我来说挺好,因为我以后打算工作的第一步以药厂实验员起步;最后,通过自己动手查阅文献、资料,自主设计操作实验流程,为以后科研查阅文献、资料、实验奠定了一定的基础。
至于建议,我认为:首先,咱们学校应该从大一开始就开展这样的实验,培养同学们自主查阅文献资料、动手做实验的能力,使同学们以后实验过程中形成正确的实验观;其次同学们在某些仪器的使用方法上仍然有些不足,在专业技能训练过程中应注重培养同学们实践动手操作能力,增加同学们使用重要仪器的机会;最后,同学们在实际操作过程中,仍有很多不规范操作,所以我认为
我们以后应该增加实验课程,培养同学实践动手能力,为以后科研奠定一定的基础。