粗化溶液分析
- 格式:doc
- 大小:34.00 KB
- 文档页数:3


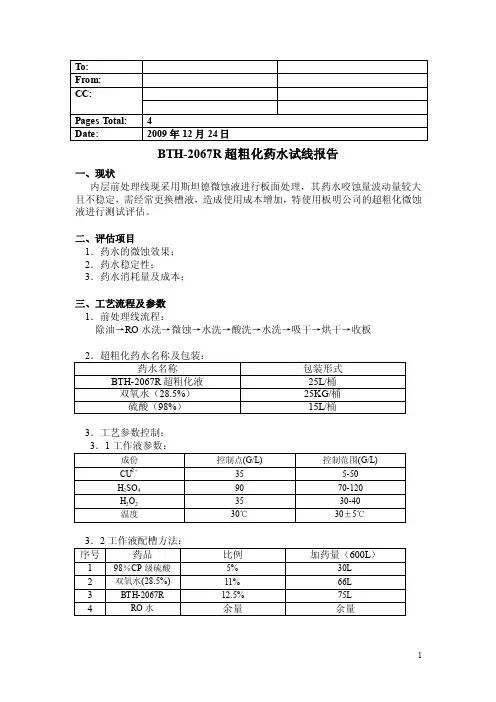
BTH-2067R超粗化药水试线报告一、现状内层前处理线现采用斯坦德微蚀液进行板面处理,其药水咬蚀量波动量较大且不稳定,需经常更换槽液,造成使用成本增加,特使用板明公司的超粗化微蚀液进行测试评估。
二、评估项目1.药水的微蚀效果;2.药水稳定性;3.药水消耗量及成本;三、工艺流程及参数1.前处理线流程:除油→RO水洗→微蚀→水洗→酸洗→水洗→吸干→烘干→收板3.工艺参数控制:3.4补充液参数:3.5添加设定:3.5.1自动添加每次加药量通过机台控制界面中加药时间设定,一经设定,不得随意调整。
补加流量:500ml/5PNL(按每PNL板平均尺寸0.2m2计算)3.5.2手动添加通常每做板1000 ft2补加50--60 升补充液.三、开缸准备1.机台的清洗用清水循环洗30分钟用5%硫酸循环洗2小时用RO循环洗二次,每次30分钟检查上下喷淋管、喷嘴,并清堵用RO水冲洗缸体各部位及缸底,除尽缸底的垃圾等沉积物,排尽洗缸水更换过滤芯安装拆下的输送轮检查后开缸2.检查及准备项目检查喷嘴、喷压、传输速度、各添加泵的性能微蚀速率测定用铜箔的准备、确定自动添加泵的添加流量的测量微蚀缸体积及各补充缸体积刻度确认实际温度与表显温度的校正;药水准备:硫酸、双氧水、BTH-2067化验室试剂准备及化验方法四、开缸五、评估项目测试 5.1药水的微蚀效果经过超粗化微蚀后的铜箔色泽呈淡红色,其粗糙度相对较大,结合力会增强。
微蚀后效果图:没有微蚀的铜表面 微蚀量(μm ):0.95 微蚀量(μm ):1.20 微蚀量(μm ):1.50超粗化微蚀后SEM 图:5.2药水稳定性测试 5.2.1开缸药水分析:硫酸:97.38 g/L 双氧水:32.94 g/L 微蚀量:1.51um(速度2.5m/min,温度30℃)5.2.3咬蚀量变化趋势图见下:数据.xls5.2.4小结从上述分析测试中可以看出,板明超粗化药水组份较稳定,微蚀量波动较小。

合金表面粗化处理方法
1. 机械研磨,通过机械研磨可以在合金表面形成微小的凹凸结构,从而增加表面粗糙度。
这种方法适用于对表面粗糙度要求不高
的情况,操作简单,成本较低。
2. 酸蚀处理,酸蚀是一种常用的合金表面粗化方法,通过在酸
性溶液中处理合金表面,可以在表面形成微观的坑洞和凹凸结构,
从而增加表面粗糙度。
常用的酸蚀剂包括氢氟酸、硝酸等。
3. 硅微米球喷射,将硅微米球以一定的速度喷射到合金表面,
可以在表面形成微小的凹凸结构,从而实现表面粗化处理。
这种方
法适用于对表面粗糙度和均匀性要求较高的场合。
4. 激光处理,激光可以在合金表面产生微小的熔化和凝固,形
成微观的凹凸结构,从而实现表面粗化处理。
激光处理可以实现对
合金表面的局部粗化,适用于对表面粗糙度和形貌要求较高的情况。
5. 化学氧化,通过在特定的化学溶液中进行氧化处理,可以在
合金表面形成氧化膜,从而增加表面粗糙度。
这种方法可以同时实
现对合金表面的防腐蚀和粗化处理。
综上所述,合金表面粗化处理方法有多种,可以根据具体的要求和条件选择合适的方法进行处理。
在实际应用中,需要综合考虑工艺成本、粗糙度要求、表面形貌等因素,选择最适合的表面粗化处理方法。
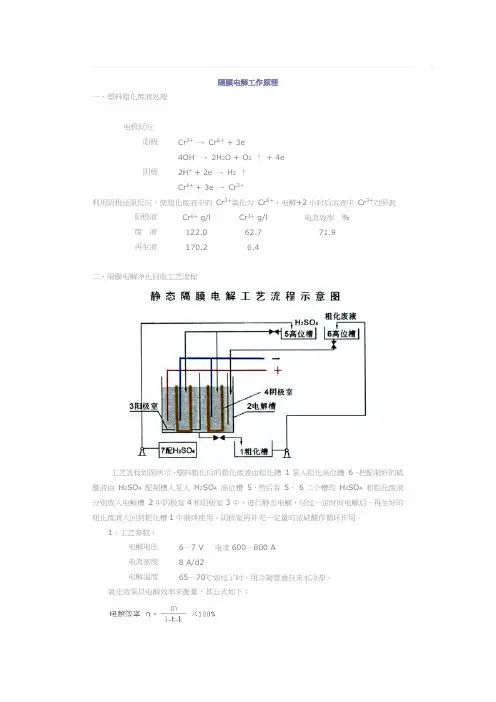
隔膜电解工作原理一、塑料粗化废液处理电极反应阳极Cr3+→Cr6+ + 3e4OH-→2H2O + O2↑+ 4e阴极2H+ + 2e →H2↑Cr6+ + 3e →Cr3+利用阴极还原反应,使粗化废液中的Cr3+氧化为Cr6+,电解+2小时后溶液中Cr3+对照表阳极液Cr6+ g/l Cr3+ g/l 电流效率%废液122.0 62.7 71.9再生液170.2 6.4二、隔膜电解净化回收工艺流程工艺流程如图所示,塑料粗化后的粗化废液由粗化糟1泵入粗化高位糟6。
把配制好的硫酸液由H2SO4配制槽人泵入H2SO4高位槽5,然后将5、6二个槽的H2SO4和粗化废液分别放入电解槽2中阴极室4和阳极室3中,进行静态电解,经过一定时间电解后,再生好的粗化废液入回到粗化槽1中继续使用,阴极室再补充一定量的浓硫酸作循环作用。
1、工艺参数:电解电压6-7 V 电流600-800 A电流密度8 A/d2电解温度65-70℃如过了时,用冷凝管通自来水冷却。
氧化效果以电解效率来衡量,其公式如下:式中:m= 实际Cr3+氧化成Cr6+的量(克)I= 通过的电流强度(安培)t= 通过电流的时间(小时)k= 电化当量(克/ 安培小时)2、使用说明:(1)阳极室粗化液总含铬量在200-250 g/l 左右,浓度过高则适当用水稀释,以免电解过程中析出铬矸,影响电解的正常进行。
(2)阴极中放入浓度为15% 左右的H2SO4溶液或根据不同浓度适当配置。
(3)在一槽处理好后,打开槽底阀门,把溶液放出并立即加入废溶液得第二次使用,否则阴极液就要流入阳极室。
阴阳二极室溶液应保持水平线,以免两种溶液流出流进,影响电解效益。
在第二次处理时,阳极室放入粗化废液至原来标准,阴极室只需补充占浓度为70%的硫酸到原来位置。
(4)一般使用时,电压开到7-6 V ,半小时后,电流升高,电压下降,此时为电解正常,如出现相反现象则应检查导电杆与极板之间接触是否良好。


PCB超粗化药水原理引言PCB(Printed Circuit Board,印刷电路板)超粗化药水是一种用于电子制造过程中的化学药水,用于去除印刷电路板上的铜材料,以便形成电路图案。
本文将详细解释与PCB超粗化药水原理相关的基本原理。
PCB制造过程在了解PCB超粗化药水原理之前,先了解一下PCB的制造过程。
PCB制造通常包括以下几个步骤:1.设计:根据电路设计要求,使用电子设计自动化(EDA)软件绘制电路图。
2.制版:将电路图转换为印刷电路板上的图案,并制作成印版。
3.印刷:将印版放置在铜箔覆盖的基板上,通过印刷工艺将图案印刷到基板上。
4.蚀刻:使用化学药水去除未被图案覆盖的铜箔,形成电路图案。
5.焊接:将元件焊接到电路板上。
6.测试:对焊接完成的电路板进行测试,确保其功能正常。
本文将重点关注第4步蚀刻过程中的PCB超粗化药水原理。
PCB超粗化药水的作用在PCB制造过程中,印刷电路板上的铜箔需要根据电路图案进行蚀刻,以形成电路连接。
而PCB超粗化药水的作用就是去除未被图案覆盖的铜箔,从而形成电路图案。
PCB超粗化药水的原理PCB超粗化药水的原理主要基于化学反应和电化学原理。
化学反应原理PCB超粗化药水中的主要成分是一种强氧化剂,通常是含有氯离子的溴化铵(NH4Br)或氯化铵(NH4Cl)。
这些强氧化剂可以与铜表面的氧化铜(Cu2O)反应,将其还原为铜离子(Cu2+),从而使铜箔被溶解。
化学反应的反应方程式如下:Cu2O + 2Br- + H2O -> 2Cu2+ + 2OH- + Br2其中,Cu2O代表氧化铜,Br-代表溴离子,H2O代表水分子,Cu2+代表铜离子,OH-代表氢氧根离子,Br2代表溴。
电化学原理除了化学反应,电化学原理也起到了重要的作用。
在PCB制造过程中,印刷电路板通常被作为阳极,在电解质溶液中形成电解池。
当加上适当的电压时,电解质溶液中的阳离子(如Cu2+)会向阳极(印刷电路板)迁移,而阴离子(如Br-)会向阴极(通常是不锈钢板)迁移。

玻璃粗化工艺-概述说明以及解释1.引言1.1 概述玻璃粗化工艺是指通过一系列的加工步骤,将玻璃表面进行处理,使其表面变得粗糙、有纹理,从而具有更好的触感和防滑性能。
在日常生活中,我们可以在很多地方看到应用了玻璃粗化工艺的产品,比如手机屏幕、餐桌、地板等。
这些产品经过粗化处理后,不仅更加美观,而且也更加安全和舒适。
玻璃粗化工艺的原理主要是通过物理或化学方法,改变玻璃表面的结构和形态,从而实现表面的粗化。
物理方法主要包括喷砂、研磨、打磨等,通过机械力或能量将玻璃表面进行切削或磨损。
化学方法则是利用一些酸碱等化学物质对玻璃表面进行蚀刻或溶解,以达到粗化的效果。
不同的方法适用于不同的玻璃材料和粗化要求,可以根据实际情况进行选择。
玻璃粗化工艺在很多领域都有广泛的应用。
在建筑领域,粗化处理后的玻璃可以用于装饰墙面、窗户、楼梯扶手等,增加其触感和装饰效果。
在电子领域,粗化处理后的玻璃可用于制造触摸屏、显示屏等产品,提高操作的舒适性和精准度。
此外,在工业制造过程中,粗化处理后的玻璃还可以用于防滑地板、玻璃器皿等,提高使用安全性。
目前,玻璃粗化工艺的发展已经取得了很大的进展。
随着科技的不断进步,新的粗化方法和设备不断涌现,使得玻璃粗化工艺更加高效、精准和环保。
同时,随着人们对产品质量和安全性要求的提高,玻璃粗化工艺在各个领域的应用也越来越广泛。
总而言之,玻璃粗化工艺是一项重要的表面处理技术,通过改变玻璃表面的结构和形态,使其具有更好的触感和防滑性能。
它在建筑、电子和工业等领域有广泛的应用,并且随着科技的发展,将会有更多的创新和进步。
文章结构部分的内容应该介绍整篇文章的结构,说明每个章节的主要内容和目的。
以下是文章结构部分的一种编写方式:【1.2 文章结构】本文主要分为引言、正文和结论三个部分。
引言部分首先概述了玻璃粗化工艺的背景和意义,说明了该工艺在实际应用中的重要性。
然后介绍了本文的目的,即对玻璃粗化工艺进行全面的研究和探讨。


铜超粗化配方和原理铜超粗化配方和原理,听起来是不是有点儿高大上?别急,我来给你聊聊这事儿。
铜是咱们生活中常见的金属,反正你家如果有电线插座、锅具啥的,都少不了它。
但你知道吗,有时候这铜不是直接就能用的,得经过一番“加工”和“改造”,才行。
这时候,超粗化处理就派上用场了。
“超粗化”是啥意思?其实就简单说就是把铜表面弄得很粗糙,让它更适合后面的工艺操作。
听着是不是有点不可思议?别着急,慢慢听我跟你细细道来。
铜这东西嘛,如果表面太光滑,有时候就不好跟其他材料结合,特别是在电子元器件、传感器之类的地方。
你想想,要是把一张超级光滑的铜片和一块塑料或者其他金属粘到一起,粘得住吗?不太可能吧。
所以,铜表面需要一种特别的处理——超粗化。
超粗化处理基本上就是通过一些化学和物理的方法,让铜的表面形成一种粗糙的、像小颗粒一样的结构。
嗯,听起来可能有点复杂,但其实就是通过一些化学液体把铜表面“磨”成颗粒状,反正就是让它不再光滑,而是变得像沙纸一样。
这样一来,其他材料就能牢牢地“咬住”铜表面了。
记得上次我看一篇技术文章,里面说这种粗化处理能提高铜的附着力和抗腐蚀性,简直是给铜穿上一层“防护服”,谁也不敢小看它。
铜超粗化是怎么做到的呢?其实很简单,有时候我们通过溶液加上一些特殊的化学物质,给铜表面“洗澡”。
这些物质会溶解掉铜表面的一些成分,然后产生一系列反应,形成微小的颗粒状结构。
这一过程,你可以想象成给铜表面做了一次彻底的大扫除,所有的污垢、油脂和杂质都被去掉,剩下的就是粗糙的质感了。
说起来,这种粗化处理不仅仅是让铜表面看起来有点“野”,它还能够提高铜的硬度和强度。
就像你想让一个人变得更有力量,不光是要锻炼,还得有好的装备。
铜也是,超粗化处理让它的“装备”更强,抗压能力更好,寿命更长。
对于一些需要耐用材料的地方,铜超粗化真的是个好帮手。
至于配方,别以为这只是简单的化学方程式。
这里头还挺讲究的。
不同的配方决定了粗化的效果,比如粗化的颗粒多大,粗化的深度有多少,甚至是粗化后铜的色泽也会有所不同。

不同塑料表面的粗化方法(周生电镀导师)塑料在进行化学镀镍前需要经过一系列复杂的前处理,目的是保证结合力。
前处理需要粗化表面并调整表面电荷以利于后续钯的吸附,为化学镀镍创造条件。
好的前处理是成功的一半。
前处理涉及多种表面处理化学品。
WETTER 920是一种液体材料,专门用于塑料电镀的铬酸粗化溶液中,添加WETTER 920在塑料表面可产生更加均匀的腐蚀,特别在裂缝中,深孔和连接处,它也可以帮助清洗表面的铬酸和减低铬酸对以后工序的坏影响。
聚碳酸酯膨润剂PM-912是一种溶剂混合物,在腐蚀前对特种聚碳酸酯树脂进行表面膨胀,以促进后续的化学镀层与基体之间的结合力。
粗化则有铬酸和高锰酸钾两种选择,当然后续都需要还原。
一旦微观粗糙表面产生就可以进行电荷调整和钯活化了,加速之后镀碱性化学镍,再镀酸性光亮化学镍,即可实现塑料件的电镀。
周生导师之@(Q):(3)(8)(0)(6)(8)(5)(5)(0)(9)。
●操作方法WETTER 920可以按以下浓度添加到铬酸粗化溶液中它的用量可以控制在每升铬酸溶液2-15毫升,当第一次添加WETTER 920时粗化溶液的表面将出现一种轻微的气泡,特别是当使用空气搅拌时更显清楚,WETTER 920的补充应维持一种少量的气泡,通常的需求可以按照每天每一百公升30-40毫升的条件补充,可以根据塑料件表面腐蚀均匀性来决定是否需要进行较大数量的补充。
PC-602消泡剂可消除粗化槽中气泡,在开缸时加入,其消耗极少,按带出量计微量补加。
通常的需求可以按照每添加WETTER 920 1000毫升的量,添加PC-602粗化消泡剂5-10毫升。
周生导师之(W)(X):(1)(3)(6)(5)(7)(2)(0)(1)(4)(7)(0)●槽液维护PM WETTER 920必须维持在一种足够的浓度来保证塑料工件表面的均匀腐蚀,可以根据顾客的需要提供有效的分析方法。
(我们$声$明):(建&群的都是假冒)(二手转卖我们配方的不完整)(请#认#准#文#中Q和WX)(广&告&-长*期*有*效)我们的配方平台帮助了很多中小企业提高产品技术水平,也有不少个人因此创业成功,帮助国内企业抢占国外知名企业市场,提升国产占有率是我们长期追求的目标。
铝件粗化处理方案铝件的粗化处理是一种常见的表面处理方法,通过增加铝件表面的粗糙度,可以提高其附着力和耐磨性,使其更适合用于各种工业应用和装饰用途。
下面给出一种常见的铝件粗化处理方案。
首先,选择合适的粗化剂。
常见的铝件粗化剂有酸性粗化剂、碱性粗化剂和电解粗化剂。
根据具体的铝件和要求,选择适合的粗化剂。
其次,准备工作。
将铝件洗净,去除表面的污垢和油脂,保持表面干燥。
同时,需要根据具体要求,将铝件进行去氧化处理以去除表面的氧化层,以便粗化剂更好地与铝表面反应。
然后,进行粗化处理。
将铝件放入粗化剂溶液中,浸泡一段时间。
粗化剂的配方和浸泡时间可以根据具体要求和试验结果进行调整。
在浸泡的过程中,需要定期翻动铝件,以保证均匀表面粗化。
在浸泡结束后,将铝件取出,用水冲洗干净,去除粗化剂残留。
然后,可选择进行中和处理来中和粗化剂对铝件表面的酸碱影响,以防止后续处理过程中对铝件的腐蚀影响。
最后,对粗化处理后的铝件进行清洗和干燥。
清洗的目的是去除铝件表面的杂质,以保证后续处理的效果。
清洗可以采用水洗或有机溶剂洗涤,根据具体情况选择合适的清洗方法。
清洗后,将铝件风干或烘干,以保证表面干燥,防止水分对后续处理的干扰。
这种粗化处理方案适用于大部分铝件,通过增加铝件表面的粗糙度,可以提高其表面附着力,使其更适合用于喷涂、电镀和粘接等工艺。
同时,粗化处理还可以提高铝件的耐磨性和抗腐蚀性,延长其使用寿命。
然而,需要注意的是,粗化处理会改变铝件的表面光洁度,对一些有特殊要求的铝件可能会造成影响,因此在选择粗化处理时需要根据具体要求进行评估。
粗化液处理机:塑料电镀前处理,粗化工序相当重要,含有铬酐的粗化液使用相当普遍,粗化液中铬酐含量几乎达到饱和。
随生产进行,粗化液中的六价铬不断的被还原为三价铬,当三价铬累积到一定程度时,粗化液则报废,报废的粗化液中含有大量六价铬,三价铬,硫酸。
造成水处理困难。
生产费用增加。
为解决此项难题,我公司塑料电镀生产线的粗化工位均配备粗化液处理机。
在生产中不间断的处理产生的三价铬,使粗化液中的三价铬稳定在工艺参数内。
避免三价铬积累,使粗化效果稳定,粗化液使用不存在报废,只需按分析补加铬酐,硫酸即可。
粗化液处理机处理原理:主要是利用电解方法处理溶液中的三价铬。
在粗化液中,阳极(铅)反应为:1、Pb-2e=Pb2+2、Cr3+-3e=Cr6+3、4OH--4e=O2↑+2H2O在阳极上铅溶解只是通电一瞬间产生,在电压升高后,析氧产生的过氧化铅覆盖表面即停止。
此时阳极表面主要为2,3反应。
控制阳极的电流密度,使阳极上主要发生反应2.粗化液处理机的组成:1、粗化液处理槽,与粗化槽材质相同。
体积为粗化槽的1/8.2、阳极及阳极杠:采用铅锡碾压阳极。
极杠为铜杠外敷绿勾胶。
阳极板数量使阳极电流密度达到最佳。
3、阴极及阴极杠:采用材质与阳极、阳极杠相同。
阴极板面积为阳极板面积一半。
阴极置于素烧陶瓷筒内,筒内加入硫酸溶液。
处理机配硫酸液储槽,储槽为碳钢板,内衬耐酸橡胶。
硫酸溶液通过循环泵打入陶瓷筒下部,陶瓷筒上部开口接管回流至储槽。
4、粗化处理机选用整流器:一般为0.3-0.4A/L。
此通电量可以满足一般粗化液生产中平衡三价铬的需求。
5、粗化液处理槽与粗化槽通过PVDF循环泵及管连接,循环泵抽粗化槽的溶液打入粗化液处理槽,经处理后进处理槽溢流盒溢流管,回流至粗化槽另一端。
粗化液处理槽放置在高位。
并配有通风。
化学中的溶液过程及分析方法众所周知,溶液是由溶剂和溶质组成的,其中溶剂为多数,溶质为少数。
溶液在化学中占有至关重要的地位,不仅仅在化学实验中会用到,而且在生活中也扮演着重要的角色。
这篇文章将会介绍化学中的溶液过程及其分析方法。
一、溶液的形成溶液是由溶剂和溶质组成的,溶质可以溶解在溶剂中形成一个均匀的混合物。
当溶剂和溶质分子处于热运动状态时,溶质分子将会与溶剂分子相互作用,从而使溶质分子逐渐分散在溶剂中,形成溶解的过程。
在化学上,溶解是一个热力学过程,主要是由温度、压力和溶剂/溶质的属性决定的。
继续用水作为例子,当晶体状的NaCl与水发生反应时,Na+和Cl-离子将会离开晶体逐渐分散在水溶液中,形成氯化钠水溶液。
在这个过程中,Na+和Cl-离子将会离开晶体形成一组孤对电荷,被溶剂包围,这个包裹离子的现象被称为水合。
二、溶液的浓度在任何溶液的实验中,浓度是一个重要的指标。
浓度的定义是单位体积的溶液中所含的物质的质量或物质的数量。
以下是几种常见的浓度单位:1) 质量浓度:按质量计算的溶质含量,通常用g/L或mg/mL表示。
2) 摩尔浓度:按物质的量计算的溶质含量,通常用mol/L表示。
3) 体积浓度:按体积计算的溶质含量,通常用mL/L表示。
三、溶液中离子的分析溶液的浓度的测量是分析化学中的核心内容之一。
在溶液中,离子的浓度和所含元素的化学状态与质量相关。
因此,离子分析是溶液分析的一个重要部分。
常用的离子分析技术有以下几种:1) 酸碱中和滴定法:测定酸或碱组分的浓度。
2) 氧化还原滴定法:测定溶液中的还原剂或氧化剂的含量。
3) 沉淀法:根据不溶性物质的数量测定分析物液中溶解的离子,也可以用于分离需要的分析物。
4) 阴离子交换法:用特殊的树脂捕获离子,从而可以在实验室中分离这些离子。
该方法常用于测定汞、银等离子。
5) p降法:使用pH计或指示剂测定溶液的pH值,从而测定分析物伴随的离子。
四、结语总之,溶液是化学中的基本概念,很多化学实验都与溶液有关。
表面粗化工艺表面粗化工艺是一种常见的表面处理方法,通过改变材料表面的形貌和结构,从而提高材料的使用性能。
表面粗化工艺广泛应用于各个领域,如机械制造、电子工业、航空航天等。
本文将从表面粗化的原理、方法和应用领域等方面进行介绍。
表面粗化是通过改变材料表面的形貌和结构,增加表面的粗糙度,从而提高材料的摩擦性能、附着力、抗疲劳性和耐腐蚀性等。
表面粗化的原理主要包括机械力作用、化学作用和热力学作用等。
其中,机械力作用是最常见的一种表面粗化方法,通过切削、研磨、冲击等方式,改变材料表面的形貌和结构,使其变得更加粗糙。
表面粗化的方法有很多种,常见的有砂轮研磨、喷砂、酸洗、电化学抛光、电火花加工等。
砂轮研磨是一种常见的机械力粗化方法,通过砂轮对材料表面进行研磨,使其表面产生微小的凸起和凹陷,从而增加表面的粗糙度。
喷砂是一种常见的物理力粗化方法,通过高速喷射砂粒对材料表面进行冲击,使其表面产生微小的凸起和凹陷,从而增加表面的粗糙度。
酸洗是一种常见的化学力粗化方法,通过在酸性溶液中浸泡材料,使其表面与酸发生化学反应,从而改变表面的形貌和结构,增加表面的粗糙度。
电化学抛光是一种常见的电化学力粗化方法,通过在电解液中加入适量的电解质,使材料表面产生氧化还原反应,从而改变表面的形貌和结构,增加表面的粗糙度。
电火花加工是一种常见的热力学粗化方法,通过在材料表面放电,使其表面产生微小的熔融和蒸发,从而改变表面的形貌和结构,增加表面的粗糙度。
表面粗化工艺在各个领域中都有广泛的应用。
在机械制造领域,表面粗化可以提高零件的摩擦性能和附着力,从而提高零件的工作效率和使用寿命。
在电子工业领域,表面粗化可以提高半导体器件的散热性能和耐腐蚀性,从而提高器件的可靠性和稳定性。
在航空航天领域,表面粗化可以提高航空器材的抗疲劳性和耐腐蚀性,从而提高航空器材的飞行安全性和使用寿命。
此外,表面粗化还可以应用于建筑材料、汽车制造、医疗器械等领域,提高材料的使用性能。
粗化镀液分析方法
用移液管吸10毫升镀液于250毫升容量瓶中,加水至刻度,摇匀。
(A) 铬酐(CrO3)含量之分析
1) 取已稀释试液5毫升。
2) 加100毫升纯水。
3) 加1毫升氟化氢铵(Ammonium Bifluoride, 15 g/L )。
4) 加20毫升1:1 HCl溶液。
5) 加10毫升10%碘化钾(KI)溶液。
6) 用0.1N Na2S2O3溶液滴定至浅黄色。
7) 加2毫升淀粉(Starch)指示剂。
8) 继续滴定由蓝色至绿色为终点。
铬酐( g/L ) = 所用0.1N Na2S2O3的毫升数(a) x 16.67
(B) 三价铬含量之分析
1) 取已稀释试液5毫升。
2) 加100毫升纯水。
3) 加0.2克过氧化钠( Na2O2 )。
4) 加热至沸腾,并保持20-30分钟, 冷却。
5) 重复以上A部份步骤3-8。
Cr2O3 ( g/L ) = [ 所用0.1N Na2S2O3的毫升数- (a) ] x 12.67
Cr3+ ( g/L ) = [ 所用0.1N Na2S2O3的毫升数- (a) ] x 8.67
(C) 硫酸含量之分析
1) 取已稀释试液5毫升。
2) 加100毫升纯水。
3) 加5 滴甲基红指示剂
4) 用0.1 N 氢氧化钠溶液滴由红色变橙黄色为终点.
硫酸( g/L ) = ( 0.1 N 氢氧化钠滴定数–铬酐( 克/升) x 0.02 ) x 24.5。
粗化溶液分析
粗化溶液,其成分含量范围一般为[1] : H2SO4 330~405 g/ L ,CrO3 400~430 g/ L ;或H2SO4 600 g/ L ,CrO3 250~350 g/ L。
笔者通过分析试验,研究出一种高铬酸型粗化溶液分析方法,自塑料电镀生产线建立以来,对粗化槽液维护、调整及控制起到非常好的效果。
2 分析方法/2.1 H2SO4 含量分析/2.1.1 方法原理
在分析试样中加入的Pb (NO3 ) 2 溶液与CrO2 -4 和SO2 -4 反应,生成PbCrO4 沉淀和PbSO4 沉淀,析出定量的H+ ,用NaOH标准溶液滴定分离后的试样溶液,通过计算得出粗化溶液中H2SO4 含量。
2.1.2 试剂/w(Pb(NO3) 2) = 20 %的Pb (NO3) 2 溶液, c (NaOH) =1 mol/ L的NaOH 标准溶液, w(甲基橙) = 1 %的甲基橙指示剂。
/2.1.3 分析步骤
取1 mL 粗化溶液于250 mL 烧杯中,在不断振荡下缓缓滴加温热( < 45 ℃) 的Pb(NO3) 2 溶液,直至上层清液黄色完全消失且呈无色为止。
用两层滤纸过滤于300 mL三角烧杯中,用温水洗涤沉淀数次,滤液冷却至室温加入1滴甲基橙指示剂,用NaOH 标准溶液滴定至溶液由红色变为橙色为终点。
2.1.4 计算/ρ(H2SO4 ) / ( g/ L) = c ×V ×5016/ V0 - ρ( CrO3 ) ×1.0112
式中: c —NaOH 标准溶液的物质的量的浓度/ (mol/L) ;/V —滴定时消耗NaOH标准溶液的体积/ mL ;/V0 —滴定时所取粗化液的体积/ mL ;/ρ—粗化液中CrO3 的质量浓度/ (g/ L) ;/1.0112 —CrO3 换算成H2SO4 的换算因数。
/2.1.5 此方法与传统方法(重量法) 比较
/此分析方法简单、快捷、准确度高,解决了传统方法耗用时间长、含量高时准确度差的问题,对槽液维护、控制、调整起着重要作用,在实际生产中取得极佳效果。
/2.2 CrO3 、Cr2O3 含量分析/粗化溶液中CrO3 、Cr2O3 含量分析方法同镀铬溶液中CrO3 、Cr2O3 含量分析方法。
此分析方法同样适用于高硫酸型粗化溶液[1] 。
/3 结语/此方法实用、
柠檬酸钠分析
7(NaH2PO2 ·H2O-15)
n:为取样的ml数。
.求K值:
取25ml 0.1N KMnO4于250ml锥形瓶,加6N硫酸10ml;MnSO41g;KI 2g。
用0.1N Na2S2O3滴至淡黄色,加淀粉指示剂3ml,继续滴至蓝色消失为终点,记下读数V1。
K=25V1 V1为Na2S2O3滴定ml数。
2.4.2.求T值:
标准化学镍溶液配制(1L):
硫酸镍30g/L 氯化铵35g/L
次钠15g/L T=38-40℃
柠钠40g/L PH=8.0-8.3(用NH3 H2O调)
按照化学镀液中柠檬酸钠的测定方法求得:
T=0.008/(25-KV)
W:为每升标准液中含柠钠的克数。
n:为取样液ml数。
2.4.
3.柠檬酸钠的测定:
取样液2ml置于100ml的容量瓶中并稀释至刻度。
吸取此稀释液10ml于250ml锥形瓶中,加50ml纯水,加12N H2SO4 10ml,MnSO4 1g,加热至70℃,在不断搅拌下加入25ml 0.1N的KMnO4液,保温15min。
流水冷却后加入2g KI,用0.1N Na2S2O3滴至淡黄色、加淀粉指示剂2-3 ml,继续滴至蓝色消失1min为终点,记下读数ml数。
柠檬酸钠(Na3Cit·g/L)=5000T·〔25-(KV)〕-0.6
体积(L)体积(L)成份成份工艺范围工艺范围操作条件操作条件体积(L)成份工艺范围操作条件
温度℃温度℃PHPH 过滤机转数过滤机转数温度℃PH 过滤机转数
A线3800A线3800 B线(I)1800 (II)1800B线(I)1800 (II)1800☆NiSO4·6H2O 硫酸镍☆NiSO4·6H2O 硫酸镍28-31g/L28-31g/L 38±238±2
8.0-8.58.0-8.5 4转/小时以上4转/小时以上A线3800 B线(I)1800 (II)1800 ☆NiSO4·6H2O 硫酸镍28-31g/L 38±2 8.0-8.5 4转/小时以上
Na3Cit·2H2O 柠钠Na3Cit·2H2O 柠钠35-55L35-55L
Na3Cit·2H2O 柠钠35-55L
☆NaH2PO2·H2O 次钠☆NaH2PO2·H2O 次钠13-16g/L13-16g/L
☆NaH2PO2·H2O 次钠13-16g/L
NH4Cl 氯化铵NH4Cl 氯化铵30-35g/L30-35g/L NH4Cl 氯化铵30-35g/L
NH3 H2O 氨水NH3 H2O 氨水镀液的1/50(V)
处理时间:参照相关产品作业指示
☆--表示过程特性
硫酸铜镀液分析方法
(1)硫酸铜(CuSO4·5H2O)含量之分析
移液管取镀液2毫升,加100毫升纯水,加热至40—50℃ ,加10毫升1:1的氨水,加5滴PAN指示剂,用0.1N EDTA溶液滴定,由深蓝色变绿色为终点。
硫酸铜(g/L)=0.1N EDTA V1×12.49
在分析时发现大量棕色沉淀物产生,采用下面方法解析
取镀液2毫升,加纯水100毫升,加入2克NH4Cl,加入10毫升缓冲液并加热至50℃, 静置一会,此时瓶中液体分为两层,上层为淡紫蓝色,下层为棕色沉淀物,将液体过滤,用纯水冲浇滤纸三次,然后将已过滤液体到如三角锥形瓶中加热至50—60℃,加入5滴PAN指示剂,用0.1NETDA溶液滴定,由深蓝色变绿色为终点。
硫酸铜(g/L)=所有0.1EDTA之毫升数V1×12.49×1.04
1.04是用以补偿因沉淀及过滤所损失的硫酸铜
(2)硫酸含量之分析
用溶液管取样本2毫升加100毫升纯水,加3滴甲基橙指示剂,用1N NaOH溶液滴定,有红色变黄色为终点。
硫酸(g/L)=1N NaOHV1×13.3
(3)氯离子含量分析
用移液管取样本25ml加纯水100ml,加热至50℃, 加3ml 1:1硝酸,,加入2滴0.1N硝酸银,使溶液产生浑浊,用0.01N硝酸汞Hg(NO3)2溶液滴定,由浑浊至清澈为终点
氯离子(PPM)=0.01N Hg(NO3)2 V1×14.2。