电化学复习
复习要求: 1、原电池、电解池的形成条件及比较; 2、原电池原理及应用,金属的腐蚀与防护; 3、理解电解原理、电解规律及电解原理的应用; 4、池的判断、电极判断及电极反应式的书写; 5、电化学计算的方法和技巧。 知识概括: 1、一个反应:氧化还原反应 2、两个转化:化学能和电能的相互转化 3、三个条件:原电池、电解池的形成条件 4、四个池子:原电池、电解池、电镀池、精炼池
3)不活泼金属的含氧酸盐(含氟化物) (CuSO4、 AgNO3)
4)活泼金属的无氧酸盐(除氟化物) (NaCl、 KBr)
——电解电解质和水
85.每一年,我都更加相信生命的浪费是在于:我们没有献出爱,我们没有使用力量,我们表现出自私的谨慎,不去冒险,避开痛苦,也失去了快乐。――[约翰·B·塔布] 86.微笑,昂首阔步,作深呼吸,嘴里哼着歌儿。倘使你不会唱歌,吹吹口哨或用鼻子哼一哼也可。如此一来,你想让自己烦恼都不可能。――[戴尔·卡内基]
负极:——Zn Zn + 2OH- - 2e- = Zn(OH)2
正极:——MnO2 2MnO2+2H2O+2e-=2MnOOH+2OH-
电解质: KOH
条件 过程 特点 联系
电离
电解
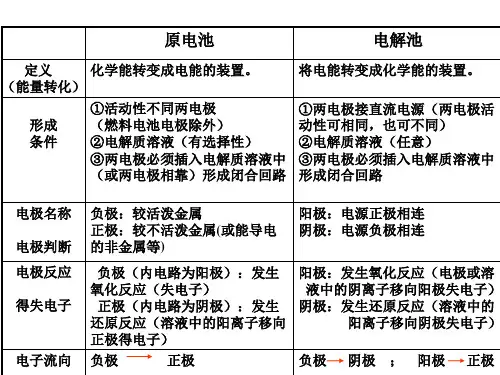
装置 构成条件 电极名称、确定 电极反应 电子移动方向 能量转变 应用举例
原电池
电解池
金属导电和电解质导电的比较 金属导电 电解质导电
例:铂电极电解1LCu(NO3)2和KNO3混合溶 液,通电一段时间,两极均产生11.2L(S.T.P) 气体。 求电解后溶液的pH 值。
阳极 4OH--4e=2H2O+O2↑ 阴极 Cu2++2e=Cu 2H++2e=H2↑ n(Cu2+)×2+0.5×2=0.5×4 n(Cu2+)=0.5mol