任务一-间歇操作釜式反应器设计
- 格式:doc
- 大小:205.50 KB
- 文档页数:18



反应工程课程设计反应釜设计任务书一、设计题目:5×103T/Y乙酸乙酯反应釜设计1、用间歇反应器进行乙酸和乙醇的酯化反应,年生产量为5000吨,2、反应式为()()()()3253252CH COOH A C H OH B CH COOC H R H O S +=+3、原料中反应组分的质量比为:::1:2:1.35A B S =4、反应液的密度为31020/kg m ,并假设在反应过程中不变 5、每批装料、卸料及清洗等辅助操作时间为1小时678二、摘要摘要:本选题为年产量为5×103T 的间歇釜式反应器的设计。
通过物料衡算、热量衡算,反应器体积为319.77m 、换热量为62.8710KJ 。
设备设计结果表明,反应器的特征尺寸为高2973.3mm ,直径3000mm ,还对塔体等进行了辅助设备设计,换热则是通过夹套与内冷管共同作用完成。
搅拌器的形式为圆盘桨式搅拌器,搅拌轴直径80mm ,搅拌轴长度3601mm 。
在此基础上绘制了设备条件图。
本设计为间歇釜式反应器的工业设计提供较为详尽的数据与图纸。
关键字:间歇釜式反应器; 物料衡算; 热量衡算; 壁厚设计;Abstract: The batch reactor for five million T a year is to be designed. Through the material, heat balance reactor volume, heat transfer. Equipment design results show that the characteristic dimensions for high reactor is 2973.3 mm, diameter is 3000mm, height is 3180mm , the auxiliary equipment also is to be designed , heat is finished through the clip with the common cold tube inside. The mixer for disk paddle type mixer, stirring shaft diameter and length of stirring shaft is 3601mm , diameter is 80mm. Based on the condition of equipment drawing. This design for batch reactor industrial design provides a detailed data and drawings. Key words : batch reactor, Material, Heat balance, Thick wall design,目录第一章反应釜物料衡算 (1)1.1 反应釜反应时间、反应体积的确定 (1)第二章反应釜公称直径、公称压力的确定 (2)2.1 反应釜公称直径的确定 (2)2.2 反应釜PN的确定 (2)第三章反应釜体设计 (3)3.1 反应釜筒体壁厚的确定 (3)3.1.1 设计参数的确定 (3)3.2 筒体壁厚设计 (4)3.3 釜体封头设计 (4)3.3.1 封头的选型 (4)3.3.2 封头壁厚设计 (4)3.3 筒体长度H设计 (5)3.4 反应釜的压力校核 (6)3.4.1 釜体的水压试验 (6)3.4.2 液压试验的强度校核 (6)3.5 釜体的气压试验 (7)3.5.1 气压试验压力的确定 (7)第四章反应釜夹套的设计 (8)4.1 夹套公称直径、公称压力的确定 (8)4.1.1 夹套DN的确定 (8)4.1.2 夹套PN的确定 (8)4.2 夹套筒体的设计 (8)4.2.1 夹套筒体壁厚的设计 (8)4.2.2 夹套筒体长度H的确定 (8)4.3 夹套封头的设计 (9)4.3.1 封头的选型 (9)4.3.2 椭圆型封头结构尺寸的确定 (9)4.4 夹套的液压试验 (9)4.4.1 液压试验压力的确定 (9)4.4.2 液压试验的强度校核 (10)第五章外压壁厚的设计 (10)5.1 圆筒的临界压力计算 (10)5.2 外压封头壁厚设计 (11)第六章热量衡算 (11)6.1 热量衡算基本数据 (11)6.2 原料带入的热量Q1的计算 (12)6.3 反应热的计算 (13)6.4 夹套给热量的计算 (14)6.5 内冷管移热量的计算 (14)第七章反应釜附件的选型及尺寸设计 (15)7.1 釜体法兰连接结构的设计 (15)7.2 密封面形式的选型 (15)7.3 工艺接管的设计 (15)7.3.1 原料液进口管 (15)7.3.2 物料出口管 (16)7.3.3 催化剂进口设计 (16)7.3.4 温度计接口 (16)7.3.5 视镜 (17)第八章搅拌装置设计 (17)8.1 凸缘法兰选择 (17)8.2 临界转速的计算 (17)8.3 搅拌装置的选型与尺寸设计 (19)8.3.1 搅拌轴直径的初步计算 (19)8.3.2 搅拌轴临界转速校核计算 (20)8.4 搅拌轴的结构及尺寸设计 (20)8.4.1 搅拌轴长度的设计 (20)8.4.2 搅拌桨的尺寸设计 (21)第九章支座 (21)结论 (21)设计结果一览表 (22)参考文献 (23)第一章 反应釜物料衡算1.1 反应釜反应时间、反应体积的确定原料处理量0Q ,根据乙酸乙酯的产量,每小时的一算用量为:500020.77/Kmol h=原料1BO SO AO AO c c b c c K ⎛⎫=-++ ⎪⎝⎭11c K =-得反应时间[1]212 1Af Af XAAO A Ab X adXtk c a bX cX++ ==++⎰10.23.908a=()10.217.591 5.153.908 3.908 2.92b⎛⎫=-++=-⎪⨯⎝⎭110.65752.92c=-=查到反应釜的2800DN mm=2.2 反应釜PN的确定[2]由lg s Bp A t C =-+得一下数据在100℃下,各物质的饱和蒸汽压为下列图表()()()()3253252CH COOH A C H OH B CH COOC H R H O S +=+3.1.1 设计参数的确定设计压力p :()1.05~1.1W p P =,取1.1 1.10.350.385W p P Mpa ==⨯= 液体静压忽略不计 计算压力c p :0.385c L p p p P Mpa=+==设计温度t :110t =℃焊缝系数Φ:1φ=(双面对接焊,100%无损探伤)[3]许用应力[]t σ:根据材料001910Cr Ni ,设计温度为110℃,该材料的[]118tMpaσ=[4]钢板负偏差1C :10.6C mm=腐蚀裕量2C :22C mm=(双面腐蚀)3.2 筒体壁厚设计C n S 制造较难,中、低压小设备不宜采用;蝶形封头的深度可通过过渡半径加以调节,但由于蝶形封头母线曲率不连续,存在局部应力,故受力不如椭圆形封头;保准椭圆形封头制造比较简单,受力状况比蝶形封头好,故该反应釜采用椭圆形封头。






理想间歇操作釜式反应器的计算王丽婷 13化工二班 1303022011间歇釜式反应器的特征特点:1、由于剧烈搅拌,反应器内物料浓度达到分子尺度上的均匀,且反应器内浓度处处相等,因而排除了物质传递对反应的影响;2、具有足够强的传热条件,温度始终相等,无需考虑器内的热量传递问题;3、物料同时加入并同时停止反应,所有物料具有相同的反应时间。
优点:操作灵活,适用于小批量、多品种、反应时间较长的产品生产,精细化工产品、制药、染料、涂料生产。
缺点:装料、卸料等辅助操作时间长,产品质量不稳定。
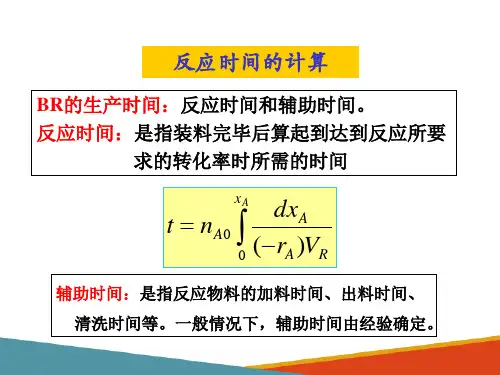
一、基础方程式单位时间进入反应器的物料A 的量-单位时间流出反应器的物料A 的量-单位时间内反应掉的物料A 的量=单位时间内在反应器内物料A 的积累量 )_1(0A A A X n n =RA A A V r dx n dt )(_0= 二、反应时间的计算n A0 ----在t=0时反应器中物料A 的摩尔数n A ----在 t 时反应器中物料A 的摩尔数-r A ----组分 A 在操作条件下的反应速率(消失速率)A x ----在 t 时反应器中物料A 的转化率上式是间歇反应器计算的基本方程式,表达了在一定操作条件下为达到所需求的转化率A x 所需要的反应时间t ,适用于任何间歇反应过程,均相或多相,等温或非等温的,可以直接积分求解,也可以用图解法。
如果是非等温过程,反应速度常数随温度变化,而温度又随转化率变化,则需联立解方程恒温、恒容不可逆时间歇操作釜式反应器中物料达到一定出口转化率所需时间t 取决于反应速度,与处理量无关,所以可用于直接放大。
零级反应k r A )(一级反应二级反应当动力学方程解析式相当复杂或不能做数值积分时,可用图解法。

一概述醋酸乙酯生产工艺的现状和特点醋酸乙酯分子式C4H8O2,又名:乙酸乙酯,英文名称:acetic ester;ethyl acetate,简称EA。
醋酸乙酯是醋酸工业重要的下游产品,也是一种重要的绿色有机溶剂,溶解能力及快干性能均属上乘,主要用做涂料(油漆和瓷漆)、油墨和粘合剂配方中的活性溶剂,也可用做制药和有机化学合成的工艺溶剂。
EA可用于制造乙酰胺、乙酰醋酸酯、甲基庚烯酮等,并在香料、油漆、医药、火胶棉、硝化纤维、人造革、染料等行业中广泛应用,还可用作萃取剂和脱水剂,亦可用于食品工业。
还可用于硝酸纤维、乙基纤维、氯化橡胶和乙烯树脂、乙酸纤维素脂、纤维素乙酸丁酯和合成橡胶等的生产过程;也可用于复印机的液体硝基纤维墨水。
在纺织工业中用作清洗剂;在食品工业中作为特殊改性酒精的香味萃取剂;在香料工业中是重要的香料添加剂,可作为调香剂的组份。
同时醋酸乙酯本身也是制造染料、香料和药物的原料。
在高级油墨、油漆及制鞋用胶生产过程中,对醋酸乙酯的质量要求较高。
当前全球醋酸乙酯的市场状况是:欧美等发达国家醋酸乙酯的市场发展比较成熟,产量和消费量的增长都比较缓慢,亚洲尤其是中国成为醋酸乙酯生产和消费增长最为快速的国家和地区。
由于中国国内快速发展的市场,尤其是建筑、汽车等行业的强劲发展,推动国内醋酸乙酯的需求,但是同时,醋酸乙酯生产能力的增长也非常快速,市场未来发展充满了机遇与挑战。
醋酸乙酯消费持续增长的主要原因是它取代了污染空气环境的用于表面涂层和油墨配方的甲乙酮和甲基异丁基酮。
醋酸乙酯作为优良溶剂,正逐步替代一些低档溶剂,发展潜力较大。
受消费拉动,20世纪90年代以来,我国醋酸乙酯生产发展迅速。
“八五”期间,产量年均增长率为%;1995-2000年,年均增长率达到%;2000-2002年,年均增长率高达%。
目前我国有醋酸乙酯生产企业30多家,年产能力为万吨。
其中,万吨级以上规模的企业有14家,年产能力为47万吨。
江西应用技术职业学院教案首页本学期授课次序授课班级15化工01班课题名称任务一间歇操作釜式反应器设计教学目的要求1、掌握理想流动模型及返混对反应的影响2、掌握化学反应速率及反应动力学方程3、掌握均相反应速率表示方式4、掌握均相反应动力学教学重点及难点均相反应速率的表示方式、均相反应动力学教学程序设计次序内容计划时间(min)123456点名、回顾上节课内容反应器流动模型化学反应速率及反应动力学方程均相反应速率均相反应动力学小结5252015205作业:小结:任务一间歇操作釜式反应器设计工作任务:根据化工产品的生产条件和工艺要求进行间歇操作釜式反应器的工艺设计预备知识:一、反应器流动模型(一)理想流动模型1、理想置换流动模型也称为平推流模型或活塞流模型。
指在任一截面的物料如同活塞一样在反应器中移动,垂直于流动方向的任一横截面上所有的物料质点的年龄相同,是一种返混量为零的极限流动模型。
其特点是在定态情况下,沿着物料流动方向物料的参数会发生变化,而垂直于流动方向上的任一截面的所有参数都相同,如浓度、压力、流速等。
2、理想混合流动模型称为全混流模型。
由于强烈搅拌,反应器内物料质点返混无穷大,所有空间位置物料的各种参数完全一致3、返混及其对反应的影响指不同时刻进入反应器的物料之间的混合,是逆向的混合,或者说是不同年龄质点之间的混合。
间歇操作反应器不存在返混。
其带来的最大影响是反应器进口处反应物高浓度去的消失或减低。
a 返混改变了反应器内的浓度分布,是反应器内反应物的浓度下降,反应产物的浓度上升b 返混的结果将产生停留时间分布,并改变反应器内浓度分布。
c 不但对反应过程产生不同程度的影响,更重要的是对反应器的工程放大所产生的问题d 降低返混程度的主要措施是分割,通常有横向分割和纵向分割两种(二)非理想流动实际反应器中流动状况偏离理想流动状况的原因课归纳为下列几个方面a 滞留去的存在也称死区、死角,是指反应器中流体流动极慢导致几乎不流动的区域。
江西应用技术职业学院教案首页任务一间歇操作釜式反应器设计工作任务:根据化工产品的生产条件和工艺要求进行间歇操作釜式反应器的工艺设计预备知识:一、反应器流动模型(一)理想流动模型1、理想置换流动模型也称为平推流模型或活塞流模型。
指在任一截面的物料如同活塞一样在反应器中移动,垂直于流动方向的任一横截面上所有的物料质点的年龄相同,是一种返混量为零的极限流动模型。
其特点是在定态情况下,沿着物料流动方向物料的参数会发生变化,而垂直于流动方向上的任一截面的所有参数都相同,如浓度、压力、流速等。
2、理想混合流动模型称为全混流模型。
由于强烈搅拌,反应器内物料质点返混无穷大,所有空间位置物料的各种参数完全一致3、返混及其对反应的影响指不同时刻进入反应器的物料之间的混合,是逆向的混合,或者说是不同年龄质点之间的混合。
间歇操作反应器不存在返混。
其带来的最大影响是反应器进口处反应物高浓度去的消失或减低。
a 返混改变了反应器内的浓度分布,是反应器内反应物的浓度下降,反应产物的浓度上升b 返混的结果将产生停留时间分布,并改变反应器内浓度分布。
c 不但对反应过程产生不同程度的影响,更重要的是对反应器的工程放大所产生的问题d 降低返混程度的主要措施是分割,通常有横向分割和纵向分割两种(二)非理想流动实际反应器中流动状况偏离理想流动状况的原因课归纳为下列几个方面a 滞留去的存在也称死区、死角,是指反应器中流体流动极慢导致几乎不流动的区域。
b 存在沟流与短路c 循环流d 流体流速分布不均匀e 扩散二、均相反应动力学基础工业反应器中,化学反应过程与质量、热量和动量传递过程同时进行,这种化学反应与物理变化过程的综合称为宏观反应过程。
研究宏观反应过程的动力学称为宏观反应动力学。
排除了一切物理传递过程的影响得到的反应动力学称为化学动力学或本征动力学。
(一)化学反应速率及反应动力学方程1、化学反应速率其定义为:在反应系统中,某一物质在单位时间、单位反应区域内的反应量 反应速度=反应量/(反应区域)(反应时间)其实针对某一种反应物而言,以符号+r i 表示。
可以是反应物,也可以是产物。
2、化学反应动力学方程定量描写反应速率与影响反应速率之间的关系式陈伟化学反应动力学方程,有反应温度、组成、压力、溶剂性质等。
但大多数为浓度和温度,所以其动力学方程一般可写为+r i =f (c ,T )恒温条件下,可写为 +r i =kf (C A,,C B ..........) 非恒温,(二)均相反应速率及反应动力学 1、均相反应速率均相反应是指在均一的液相或气相中进行的化学反应。
均相反应速率的定义指在均相反应系统中某一物质在单位时间、单位反应混合物总体积的反应量,反应速率单位以Kmol/(m3•h)(1) 用组分传化率表示-rA=n A0dx A /Vd τ (2) 用浓度表示(3) 对于多组分单一反应体系,各个组分的反应速率受化学计量关系的约束,存在一定比列关系。
对于单一不可逆反应 各组分的变化量符合下列关系2、均相反应动力学(1)均相反应应满足的两个必要条件 a 反应系统可以成为均相b 预混和速率>>反应速率预混和指物料在反应前能否达到分子尺度的均匀混和。
实现装置:机械搅拌和高速流体造成的射流混和(2)均相反应的特点:反应过程不存在相界面,过程总速度由化学反应本身决定。
(3)速率方程在均相反应系统中只进行如下不可逆化学反应: 其动力学方程一般都可表示成: aA bB rR sS +−−→+sn n r n n b n n a n n S S R R B B A A 0000-=-=-=-aA bB rR sS+−−→+12i i A Br k c c αα±=于气相反应,由于分压与浓度成正比,也常常使用分压来表示:其中一般说来,可以用任一与浓度相当的参数来表达反应的速率,但动力学方程式中各参数的因次单位必须一致。
(4)反应分子数与反应级数 A 、基本概念I 单一反应与复杂反应单一反应:指只用一个化学反应式和一个动力学方程式便能代表的反应 复杂反应:有几个反应同时进行,要用几个动力学方程式才能加以描述。
常见的复杂反应有:连串反应、平行反应、平行-连串反应等 II 基元反应与非基元反应基元反应:如果反应物分子在碰撞中一步直接转化为产物分子,则称该反应为基元反应。
非基元反应:若反应物分子要经过若干步,即经由几个基元反应才能转化成为产物分子的反应,则称为非基元反应III 单分子、双分子、三分子反应单分子、双分子、三分子反应,是针对基元反应而言的。
参加反应的分子数是一个,称之为单分子反应;反应是由两个分子碰撞接触的,称为双分子反应。
IV 反应级数是指动力学方程式中浓度项的指数。
它是由实验确定的常数。
可以是分数,也可以是负数B 、理解反应级数时应特别注意:I 反应级数不同于反应的分子数,前者是在动力学意义上讲的,后者是在计量化学意义上讲的。
对基元反应,反应级数 …即等于化学反应式的计量系数值,而对非基元反应,应通过实验来确定。
II 反应级数高低并不单独决定反应速率的快慢,反应级数只反映反应速率对浓度的敏感()111AA A AB dn r kC C V d αβτ-=-=121()A A p A Bdn r k p p V d αατ-=-=12()()A Ap nk k k RT RT αα+==12,αα程度。
级数愈高,浓度对反应速率的影响愈大。
(5)反应速率常数k和活化能EA、反应速率常数kk就是当反应物浓度为1时的反应速率,又称反应的比速率。
k值大小直接决定了反应速率的高低和反应进行的难易程度。
不同的反应有不同的反应速率常数,对于同一个反应,速率常数随温度、溶剂、催化剂的变化而变化。
k随温度的变化规律符合阿累尼乌斯关系式:B、活化能E反应活化能是为使反应物分子“激发”所需给予的能量。
活化能的大小是表征化学反应进行难易程度的标志。
活化能高,反应难于进行;活化能低,则容易进行。
但是活化能E不是决定反应难易程度的唯一因素,它与频率因子A0共同决定反应速率。
C、在理解活化能E时,应当注意:I 活化能E不同于反应的热效应,它不表示反应过程中吸收或放出的热量,而只表示使反应分子达到活化态所需的能量,故与反应热效应并无直接的关系。
II 活化能E不能独立预示反应速率的大小,它只表明反应速率对温度的敏感程度。
E愈大,温度对反应速率的影响愈大。
除了个别的反应外,一般反应速率均随温度的上升而加快。
E愈大,反应速率随温度的上升而增加得愈快。
III 对于同一反应,即当活化能E一定时,反应速率对温度的敏感程度随着温度的升高而降低。
江西应用技术职业学院教案首页任务一间歇操作釜式反应器设计工作任务:根据化工产品的生产条件和工艺要求进行间歇操作釜式反应器的工艺设计预备知识:3、均相单一反应的动力学方程对于单一反应过程: 动力学方程表示为: (1)恒温恒容一级不可逆反应I 恒容过程:液相反应和反应前后无物质的量变化的气相反应。
① 一级不可逆反应工业上许多有机化合物的热分解和分子重排反应等都是常见的一级不可逆反应;或有二个反应物参与的反应,若其中某一反应物极大过量,则该反应物浓度在反应过程中无多大变化,可视为定值而并入反应速率常数中。
此时如果反应速率对另一反应物的浓度关系为一级,则该反应仍可按一级反应处理。
一级反应的动力学方程式为 :初始条件 时,上式分离变量积分,在恒温条件下,κ为常数,积分得到: 若着眼于反应物料的利用率,或者着眼于减轻后分离的任务,应用转化率积分表达式较为方便;若要求达到规定的残余浓度,即为了适应后处理工序的要求,例如有害杂质的除去即属此类,应用浓度积分表达式较为方便。
② 恒温恒容二级不可逆反应它有二种情况:一种是对某一反应物为二级且无其它反应物,或者是其它反应物大量存在,因而在反应过程中可视为常值;另一种是对某一反应物为一级,对另一反应物也是一级,而且二反应物初始浓度相等且为等分子反应时,亦就演变成第一种情况。
此时其动力学方程式为 :经变量分离并考虑初始条件 ,恒温时κ为常数,则积分结果为:若用转化率表示:只要知道其反应动力学方程,代入式 ,积分即可求得结果。
从速率方程积分表可得到一些定性的结论:(1)速率方程积分表达式中,左边是反应速率常数k 与反应时间τ的乘积,表示当反应初aA bB rR sS ++−−→++L L12i A B r kc c αα±=L0τ=0A A c c =0k A A c c eτ-=1ln 1Ak x τ=-2()A A A dc r kc d τ-=-=0τ=0A A c c =011A A k c c τ-=001A A A c c c k τ=+01AA A x c k x τ=-0()A A c Ac Adc r τ=--⎰始条件和反应结果不变时,反应速率常数k 以任何倍数增加,将导致反应时间以同样倍数下降。
(2)一级反应所需时间τ仅与转化率XA 有关,而与初始浓度无关。
因此,可用改变初始浓度的办法来鉴别所考察的反应是否属于一级反应。
以或 对τ作图,若是直线,则为一级反应,其斜率为k 。
(3)二级反应达到一定转化率所需反应时间τ与初始浓度有关。
初始浓度提 高,达到同样转化率XA 所需反应时间减小 。
(4)对n 级反应:当n >1时,达到同样转化率,初始浓度提高,反应时间减少;当n <1时,初始浓度提高时要达到同样转化率,反应时间增加。
对 n <1的反应,反应时间达到某个值时,反应转化率可达100%。
而n ≥1的反应,反应转化率达 100%,所需反应时间为无限长。
这表明反应级数n ≥l 的反应,大部分反应时间是用于反应的末期。
高转化率或低残余浓度的要求会使反应所需时间大幅度地增加。
例1-1 解题思路根据题意是恒温恒容一级不可逆均相反应,又要求求反应一定时间后物料的残余浓度,故选择公式解题较简便。
对于多组分单一反应,反应物的反应量与产物的生成量之间有化学计量关系的约束,可以根据它们的化学计量关系推导出它们反应过程中的浓度关系。
运用恒温恒容一级不可逆反应的转化率积分形式解题。
例1-2 解题思路:根据题意为恒温恒容二级不可逆均相反应,运用相应的浓度积分形式解题。
4、复杂反应动力学方程 (1)复杂反应的类型I 可逆反应 在反应物发生化学反应生成产物的同时,产物之间也在发生 化学反应回复成原料。
如:II 平行反应 在系统中反应物除发生化学反应生成一种产物外,该反应物 还能进行另一个化学反应生成另一种产物。
如: 乙烷裂解生成乙烯0ln(/)A A c c ln[1/(1)]A x -100(1)A x n A A nA dx c k x τ-=-⎰0k A A c c e τ-=A B R S R S A B+→++→+同时乙烷也能裂解成碳和氢III 连串反应 反应物发生化学反应生成产物的同时,该产物又能进一步反 应而成另一种产物。